Trên thị trường hiện nay có rất nhiều thuốc gerneric có hoạt chất là Dapagliflozin tuy nhiên lại rất ít thông tin liên quan đến hoạt chất này. Ở bài này HealCentral.org xin được chia sẻ các thông tin như: Cơ chế tác dụng của Dapagliflozin là gì? Dapagliflozin có tác dụng gì? Tác dụng phụ của Dapagliflozin là gì?… Dưới đây là thông tin chi tiết.
Lịch sử nghiên cứu và phát triển
Đái tháo đường hiện nay là một bệnh nội tiết vô cùng phổ biến và quen thuộc ở các nước phát triển cũng như các nước đang phát triển. Kinh tế ngày càng đi lên kéo theo gia tăng tiêu thụ các nguồn thức ăn nhanh, đồ uống có ga cùng với cường độ vận động ngày càng đi xuống góp phần không nhỏ làm gia tăng tỉ lệ đái tháo đường trong dân số, chủ yếu là đái tháo đường type 2. Bệnh gây ra hàng triệu ca tử vong mỗi năm trên toàn thế giới vì các biến chứng nguy hiểm của nó. Bệnh nhân bị đái tháo đường phải điều trị bằng thuốc suốt đời với chi phí không hề nhỏ.
Dapagliflozin là một thuốc ức chế SGLT2 mới do AstraZeneca nghiên cứu và phát triển. Thuốc được dùng trong điều trị đái tháo đường type 2 ở những bệnh nhân mà chế độ ăn kiêng và tập luyện thể thao không đáp ứng đầy đủ. Thuốc được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt dưới tên thương mại Farxiga ngày 8/1/2014. Hiện nay thuốc được tiếp thị bởi AstraZeneca Pharmaceuticals L.P., Wilmington, Del. và Bristol-Meyers Squibb Company, Princeton, N.J.

Dược lực học
Dapagliflozin là chất ức chế kênh đồng vận chuyển natri – glucose 2 (SGLT2) ở thận mạnh và chọn lọc.
Ở những người khỏe mạnh, 99% glucose trong nước tiểu đầu được tái hấp thu tại ống thận. Quá trình tái hấp thu glucose được thực hiện qua trung gian 2 kênh đồng vận chuyển glucose phụ thuộc natri: Kênh đồng vận chuyển natri – glucose 1 (SGLT1) được tìm thấy ở ruột, tim và thận và SGLT2, được tìm thấy chủ yếu tại thận. Khoảng 90% glucose được tái hấp thu ở thận được thực hiện nhờ SGLT2 trên đoạn S1 của ống lượn gần, 10% còn lại được tái hấp thu nhờ SGLT1 ở đoạn S3 phía xa của ống lượn gần.
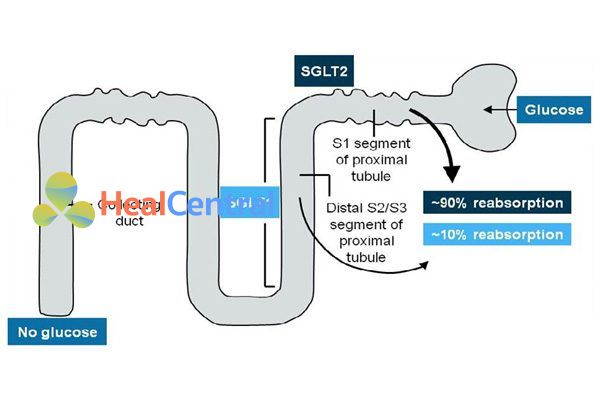
Như vậy, ức chế SGLT2 sẽ gây ra giảm tái hấp thu glucose và tăng đào thải nó qua nước tiểu. Tác dụng của nó không phụ thuộc vào hoạt động của insulin. Sử dụng dapagliflozin trên bệnh nhân đái tháo đường type 2 dẫn đến ức chế tái hấp thu lên tới 40% lượng glucose đã được lọc ở cầu thận.
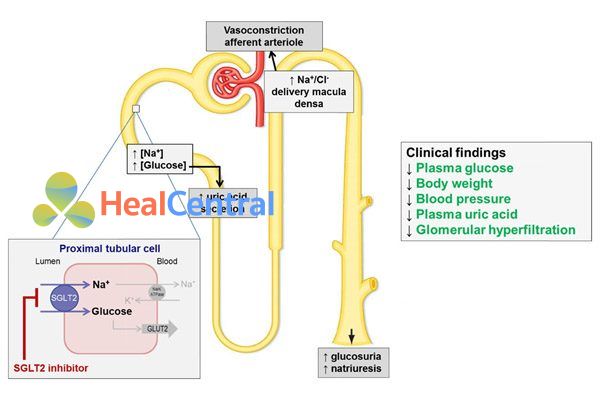
Dapagliflozin cũng có những tác dụng như thuốc lợi tiểu, bao gồm giảm huyết áp, trọng lượng cơ thể, mức lọc cầu thận (GFR) và thể tích huyết tương.
Một số thử nghiệm lâm sàng
Nghiên cứu so sánh dapagliflozin và giả dược trên bệnh nhân đái tháo đường type 2.
Tham khảo: Ferrannini E và các cộng sự, 2010.
Thiết kế nghiên cứu: Nghiên cứu pha 3 ngẫu nhiên, mù đôi, đa trung tâm.
Nhà tài trợ: Bristol-Myers Squibb / AstraZeneca.
Bệnh nhân: 485 bệnh nhân trưởng thành điều trị lần đầu từ 18 đến 77 tuổi bị đái tháo đường type 2 kiểm soát không đầy đủ bằng chế độ ăn uống và tập thể dục, HbA1c từ 7% đến 10%, nồng độ C-peptide khi nhịn ăn từ 1 ng/mL trở lên, và chỉ số khối cơ thể (BMI) không lớn hơn 45 kg/m2. Một đoàn hệ thăm dò bổ sung bao gồm 73 bệnh nhân có HbA1c ban đầu từ 10.1% đến 12%.
Can thiệp: Dapagliflozin 2.5, 5 hoặc 10 mg 1 lần/ngày buổi sáng (đoàn hệ chính), dapagliflozin 2.5, 5 hoặc 10 mg 1 lần/ngày buổi tối (đoàn hệ thăm dò buổi tối) hoặc giả dược 1 lần/ngày buổi sáng hoặc tối trong 24 tuần. Bệnh nhân có HbA1c ban đầu là 10.1% đến 12% được chỉ định ngẫu nhiên dapagliflozin 5 hoặc 10 mg 1 lần/ngày buổi sáng. Điều trị bằng metformin nhãn mở được bắt đầu ở những bệnh nhân có glucose huyết tương lúc đói lớn hơn 270 mg/dL ở tuần 4, 240 mg/dL ở tuần 8 hoặc 200 mg/dL ở tuần 12.
Các kết quả:
Điểm cuối chính: Trong đoàn hệ chính, HbA1c trung bình thay đổi từ đường cơ sở ở tuần 24 là −0.58% với dapagliflozin 2.5 mg, −0.77% với dapagliflozin 5 mg (P < 0.001 so với giả dược), và −0.89% với dapagliflozin 10 mg (P < 0.001 so với giả dược), so với −0.23% ở giả dược. Kết quả trong đoàn hệ thăm dò buổi tối là tương tự, mức giảm từ 2.66% đến 2.88% đã được quan sát trong đoàn hệ có HbA1c cơ bản là 10.1% đến 12%.
Điểm cuối thứ cấp:
- Trong đoàn hệ chính, HbA1c dưới 7% đã đạt được ở 41% bệnh nhân dùng dapagliflozin 2.5 mg, 44% bệnh nhân dùng dapagliflozin 5 mg và 51% bệnh nhân dùng dapagliflozin 10 mg, so với 32% với giả dược. Kết quả trong đoàn hệ thăm dò buổi tối là tương tự.
- Glucose huyết lúc đói đã giảm ngay từ tuần 1. Ở tuần 24, sự giảm glucose huyết lúc đói trên dapagliflozin 5 và 10 mg là lớn hơn so với giả dược: −15.2 mg/dL với dapagliflozin 2.5 mg, −24.1 mg/dL với dapagliflozin 5 mg (P < 0.001 so với giả dược), và −28.8 mg/dL với dapagliflozin 10 mg (P < 0.001 so với giả dược), so với −4.1 mg/dL với giả dược.
- Giảm cân đã quan sát thấy ở tất cả các nhóm dùng dapagliflozin, mặc dù sự khác biệt so với giả dược là không có ý nghĩa thống kê (−2.8 đến −3.3 kg với dapagliflozin so với −2.2 kg so với giả dược).
Hạn chế: Không có đối chứng với thuốc thật. Tỉ lệ bệnh nhân dùng metformin nhãn mở ngoài dapagliflozin không được xác định chính xác.
Dược động học
Hấp thu: Sinh khả dụng (F) tuyệt đối đường uống sau khi uống liều 10 mg là 78%. Thời gian đạt nồng độ đỉnh trong huyết tương (Tmax) là 2 giờ khi nhịn ăn và 3 giờ khi ăn với bữa ăn giàu chất béo. Bữa ăn giàu chất béo cũng làm giảm nồng độ đỉnh trong huyết tương (Cmax) lên tới 50%.
Phân bố: Tỉ lệ liên kết protein huyết tương là 91%.
Chuyển hóa: Trao đổi chất chủ yếu qua trung gian UGT1A9. Chuyển hóa qua trung gian CYP là con đường thanh thải thứ yếu ở người. Thuốc được chuyển hóa rộng rãi, chủ yếu tạo ra dapagliflozin 3-O-glucuronide (chất chuyển hóa không hoạt động).
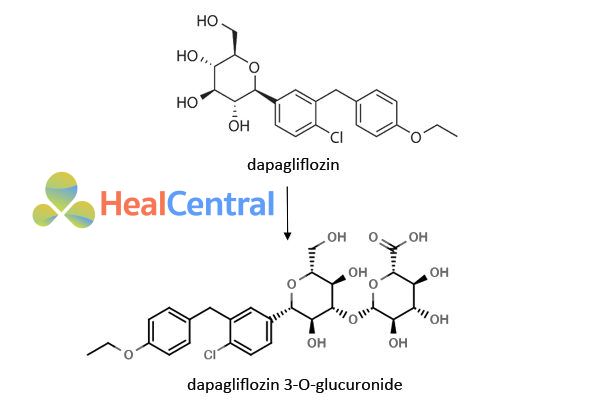
Thải trừ: Thời gian bán huỷ (t1/2) trung bình là 10-17 giờ. Bài xuất qua nước tiểu là chủ yếu (75%, 4% dưới dạng không đổi) và một phần qua phân (21%, 15% dưới dạng không đổi).
Chỉ định và liều dùng
Đái tháo đường type 2:
Bổ sung cho chế độ ăn uống và tập luyện thể dục để cải thiện kiểm soát đường huyết ở bệnh nhân đái tháo đường type 2.
Liều khởi đầu: 5 mg PO 1 lần/ngày.
Bệnh nhân đã dung nạp liều 5 mg/ngày có thể tăng lên 10 mg/ngày ở bệnh nhân cần kiểm soát đường huyết bổ sung.
Chú thích: PO: đường uống.
Chỉnh liều ở bệnh nhân suy thận:
- eGFR ≥ 45mL/min/1.73 m²: Không cần chỉnh liều.
- eGFR 30-45 mL/min/1.73 m²: Không khuyến cáo.
- eGFR < 30 mL/min/1.73 m²: Chống chỉ định.
Chỉnh liều ở bệnh nhân suy gan:
- Nhẹ đến trung bình: Không cần chỉnh liều.
- Nặng: Không được nghiên cứu.
Chú ý: Không dùng trong đái tháo đường type 1 hoặc nhiễm toan ketone do đái tháo đường.
Tác dụng phụ
Rất thường gặp (> 10%):
Suy thận:
- Tổng thể (1.8-6.7%).
- Tuổi từ 65 trở lên (3.1-14%).
- eGFR 30-60 mL/min (8-28.3%).
- Tuổi từ 65 trở lên và eGFR 30-60 mL/min (7-35.1%).
Thường gặp (1-10%):
- Nhiễm nấm sinh dục nữ (6.9-8.4%).
- Nhiễm nấm sinh dục nam (2.7-2.8%).
- Cúm (2.3-2.7%).
- Viêm mũi – họng (6.3-6.6%).
- Nhiễm trùng đường tiết niệu (4.3-5.7%).
- Tăng thể tích nước tiểu (2.9-3.8%).
- Đi tiểu khó chịu (2.1-2.6%).
- Buồn nôn (2.5-2.8%).
- Táo bón (1.9-2.2%).
- Rối loạn mỡ máu (2.1-2.5%).
- Đau lưng (3.1-4.2%).
- Đau cực độ (1.7-2%).
Giảm thể tích tuần hoàn:
- Tổng thể (0.6-1.1%).
- Bệnh nhân dùng lợi tiểu quai (0-9.7%; 1.8-2.5%).
- Bệnh nhân suy thận trung bình, GFR 30-60 mL/min (0.9-1.9%).
- Tuổi từ 65 trở lên (3.1-14%).
- eGFR 30-60 mL/min (0.5-1.7%).
Tác dụng phụ < 1%:
- Quá mẫn cảm (0.3%).
Báo cáo hậu mãi (Postmarketing Reports):
- Phát ban.
- Nhiễm toan ketone.
- Tổn thương thận cấp và suy thận.
- Nhiễm trùng niệu và viêm thận – bể thận.
- Viêm mô hoại tử đáy chậu.
Lưu ý và thận trọng
Có thể xảy ra hạ huyết áp do giảm thể tích nội mạch, đặc biệt ở những bệnh nhân suy thận.
Trước khi bắt đầu điều trị, đánh giá thể tích tuần hoàn và tình trạng giảm thể tích máu ở người cao tuổi, bệnh nhân suy thận, huyết áp tâm thu thấp hoặc ở bệnh nhân dùng thuốc lợi tiểu. Theo dõi cẩn thận các dấu hiệu và triệu chứng trong quá trình điều trị.
Thuốc làm tăng creatinine huyết thanh và giảm eGFR. Những người dễ bị ảnh hưởng là người cao tuổi và bệnh nhân suy giảm chức năng thận. Đánh giá chức năng thận trước khi bắt đầu điều trị và sau đó cần theo dõi định kỳ.
Tổn thương thận cấp tính có thể xảy ra, đặc biệt nếu eGFR < 60 mL/min/1.73 m². Trước khi bắt đầu điều trị, xem xét các yếu tố có thể khiến bệnh nhân bị tổn thương thận cấp bao gồm giảm thể tích máu, suy thận mạn, suy tim sung huyết và một số thuốc (thuốc lợi tiểu, thuốc ức chế men chuyển angiotensin, thuốc chẹn thụ thể angiotensin, thuốc kháng viêm không steroid). Theo dõi các dấu hiệu và triệu chứng của tổn thương thận cấp. Nếu nó xảy ra, ngừng thuốc ngay lập tức và điều trị kịp thời.

Gãy xương được báo cáo ở những bệnh nhân có eGFR từ 30 đến dưới 60 mL/min/1.73 m2, trong thời gian điều trị lên tới 104 tuần.
Nguy cơ hạ đường huyết tăng khi dùng insulin và chất kích thích bài tiết insulin, cần chỉnh liều.
Có thể xảy ra nhiễm nấm cơ quan sinh dục, bệnh nhân có tiền sử nhiễm trùng cơ quan sinh dục và nam giới không được cắt bao quy đầu sẽ dễ mắc bệnh hơn.
Tăng nguy cơ nhiễm trùng tiết niệu, bao gồm nhiễm trùng niệu và viêm thận – bể thận đe dọa tính mạng. Đánh giá các dấu hiệu và triệu chứng của nhiễm trùng tiết niệu và điều trị kịp thời, nếu được chỉ định.
Viêm mô hoại tử vùng đáy chậu (Fournier gangrene) đã được báo cáo với các chất ức chế SGLT2. Các dấu hiệu và triệu chứng bao gồm nhạy cảm, đỏ hoặc sưng bộ phận sinh dục hoặc khu vực từ bộ phận sinh dục đến trực tràng, sốt trên 100.4○F hoặc có cảm giác không khỏe. Nếu nghi ngờ, ngừng thuốc ức chế SGLT2 và bắt đầu điều trị ngay lập tức bằng kháng sinh phổ rộng và phẫu thuật cắt bỏ mô hoại tử nếu cần thiết.
Các trường hợp tử vong do nhiễm toan ketone đã được báo cáo ở những bệnh nhân dùng dapagliflozin. Theo dõi các triệu chứng (ví dụ: khó thở, buồn nôn, nôn, đau bụng, lú lẫn, mệt mỏi bất thường hoặc buồn ngủ), đánh giá và xem xét các yếu tố nguy cơ nhiễm toan ketone của bệnh nhân trước khi bắt đầu điều trị. Bệnh nhân có thể yêu cầu ngừng điều trị tạm thời trong tình huống lâm sàng có thể dẫn đến nhiễm toan ketone.
Tăng LDL-C liên quan đến liều đã được báo cáo.
Các trường hợp mới được chẩn đoán ung thư bàng quang được báo cáo ở 0.17% bệnh nhân được điều trị bằng dapagliflozin và 0.03% bệnh nhân được điều trị bằng giả dược. Các yếu tố nguy cơ của ung thư bàng quang và đái máu (một dấu hiệu tiềm năng của các khối u tồn tại từ trước) đã được cân bằng giữa các nhánh điều trị tạo đường cơ sở và có quá ít trường hợp để xác định liệu sự xuất hiện của các sự kiện này có liên quan đến dapagliflozin không.
Không dùng cho bệnh nhân ung thư bàng quang hoạt động và thận trọng ở bệnh nhân có tiền sử ung thư bàng quang từ trước.
Không có bằng chứng thuyết phục về giảm nguy cơ trên các mạch máu lớn khi điều trị bằng dapagliflozin hoặc bất kỳ thuốc điều trị đái tháo đường nào khác.
Thuốc ức chế SGLT2 làm tăng bài xuất glucose qua nước tiểu và sẽ dẫn đến xét nghiệm glucose niệu dương tính. Cần sử dụng các phương pháp thay thế khác để theo dõi và kiểm soát đường huyết.
Phụ nữ có thai: Dữ liệu trên động vật cho thấy thuốc tác dụng có hại trên thận và không được khuyến cáo trong tam cá nguyệt thứ hai và thứ ba của thai kỳ. Dữ liệu hạn chế ở phụ nữ mang thai không đủ để xác định nguy cơ đối với dị tật bẩm sinh lớn hoặc sảy thai liên quan đến thuốc. Có những rủi ro cho mẹ và thai nhi liên quan đến đái tháo đường được kiểm soát kém trong thai kỳ. Tuy nhiên phụ nữ mang thai thường sẽ được chỉ định insulin, các thuốc đường uống thường không được ưu tiên.
Phụ nữ đang cho con bú: Không có thông tin liên quan đến sự hiện diện của dapagliflozin trong sữa mẹ, ảnh hưởng đến trẻ bú mẹ hoặc sự sản xuất sữa. Thuốc có trong sữa của chuột cho con bú, tuy nhiên, do sự khác biệt đặc trưng về loài trong sinh lý tiết sữa, sự liên quan về mặt lâm sàng của những dữ liệu này không rõ ràng.
Sự trưởng thành thận của con người xảy ra từ khi là thai nhi cho đến 2 năm đầu đời, lúc này sự tiếp xúc với sữa mẹ có thể xảy ra, do đó có thể có nguy cơ với sự phát triển thận của trẻ. Vì có khả năng gây phản ứng phụ nghiêm trọng ở trẻ bú mẹ, phụ nữ không nên dùng thuốc này khi đang cho con bú.
Tương tác thuốc
Dùng cùng các thuốc điều trị đái tháo đường khác (các sulfonylurea, metformin, insulin, nateglinide, repaglinide): Tăng tác dụng của mỗi thuốc do tương tác dược lực học. Xem xét giảm liều.
Dùng cùng letermovir: Tăng nồng độ hoặc tác dụng của dapagliflozin bằng cơ chế chưa xác định. Tăng nguy cơ gặp tác dụng phụ của dapagliflozin. Theo dõi đường huyết thường xuyên.

Chống chỉ định
Quá mẫn cảm với dapagliflozin hoặc bất cứ thành phần nào của thuốc.
Suy thận nặng (eGFR < 30 mL/min/1.73 m²), bệnh thận giai đoạn cuối hoặc bệnh nhân chạy thận nhân tạo.
Tài liệu tham khảo:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4406879/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6116759/
https://www.nejm.org/doi/full/10.1056/NEJMoa1812389
https://www.thelancet.com/journals/landia/article/PIIS2213-8587(19)30180-9/fulltext
https://www.acc.org/latest-in-cardiology/clinical-trials/2018/11/08/23/09/declare-timi-58
https://www.astrazeneca.com/media-centre/press-releases/2019/farxiga-approved-in-the-us-to-reduce-the-risk-of-hospitalisation-for-heart-failure-in-patients-with-type-2-diabetes-21102019.html






Bạn có tài liệu sâu hơn về cơ chế k? Cho mình xin với ạ. Tks bạn
Cái này của công ty Astra Zeneca rồi, sợ không công khai được bạn ạ.