Bài viết Hướng dẫn chính thức: xử trí hội chứng suy hô hấp cấp được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Formal guidelines: management of acute respiratory distress syndrome
Tóm tắt
Mười lăm khuyến nghị và một thuật toán trị liệu liên quan đến việc kiểm soát hội chứng suy hô hấp cấp tính (ARDS, acute respiratory distress syndrome) ở giai đoạn đầu ở người lớn được đề xuất. Phương pháp Khuyến nghị, Đánh giá, Phát triển và Đánh giá (GRADE, Grade of Recommendation, Assessment, Development and Evaluation) đã được áp dụng. Bốn khuyến nghị (thể tích khí lưu thông thấp, giới hạn áp lực cao nguyên, không thông khí dao động và tư thế nằm sấp) có mức độ chứng cứ cao (GRADE 1+ hoặc 1- ); bốn khuyến nghị (áp lực dương cuối thì thở ra [PEEP] cao ở ARDS vừa và nặng, thuốc giãn cơ, thủ thuật huy động và oxygen hóa qua màng ngoài cơ thể [ECMO]) ở mức độ chứng cứ thấp (GRADE 2+ hoặc 2-); bảy khuyến nghị (giám sát, thể tích khí lưu thông đối với bệnh nhân thở máy không ARDS, giới hạn thể tích khí lưu thông khi có áp lực cao nguyên thấp, PEEP > 5 cmH2O, PEEP cao trong trường hợp không có tác động có hại, chế độ áp lực cho phép thông khí tự phát sau giai đoạn cấp tính và nitric oxit) tương ứng với một mức độ bằng chứng không cho phép sử dụng phân loại GRADE và là ý kiến chuyên gia. Cuối cùng, đối với ba khía cạnh của quản lý ARDS (áp lực đẩy, thông khí tự phát sớm và loại bỏ carbon dioxide ngoài cơ thể), các chuyên gia kết luận rằng không có khuyến nghị nào có thể đưa ra với kiến thức hiện tại. Các khuyến nghị và thuật toán trị liệu đã được các chuyên gia phê duyệt với sự đồng thuận mạnh mẽ.
Giới thiệu
Hội chứng suy hô hấp cấp tính (ARDS) là một quá trình viêm trong phổi gây ra phù phổi không tăng áp lực thủy tĩnh – giàu protein. Các vấn đề ngay lập tức là thiếu oxy máu sâu, giảm độ giãn nở phổi và tăng shunt trong phổi và khoảng chết. Các khía cạnh lâm sàng bao gồm tổn thương viêm nghiêm trọng đối với hàng rào phế nang- mao mạch, suy giảm chất hoạt động bề mặt và mất mô phổi có sục khí.
Định nghĩa gần đây nhất về ARDS, định nghĩa của Berlin, được đề xuất bởi một nhóm làm việc dưới sự bảo trợ của Hiệp hội Chăm sóc Chuyên sâu Châu Âu [1]. Nó xác định ARDS bằng sự hiện diện trong vòng 7 ngày kể từ khi bị tổn thương lâm sàng đã biết hoặc các triệu chứng hô hấp mới xuất hiện hoặc xấu đi phối hợp với thiếu oxy cấp tính (PaO2/FiO2 300 mmHg), ở một bệnh nhân thở máy có áp lực dương cuối thì thở ra (PEEP) ít nhất 5 cmH2O và các hình mờ hai bên không được giải thích đầy đủ do suy tim hoặc quá tải thể tích. Định nghĩa Berlin sử dụng tỷ lệ PaO2/FiO2 để phân biệt ARDS nhẹ (200 <PaO2/FiO2 ≤ 300 mmHg), ARDS vừa phải (100 <PaO2/FiO2 ≤ 200 mmHg) và ARDS nặng (PaO2/FiO2 ≤ 100 mmHg) .
Nhiều thông tin về dịch tễ học của ARDS đã tích lũy từ LUNG SAFE, một nghiên cứu quốc tế, đa trung tâm, tiến hành trên 29.000 bệnh nhân tại 50 quốc gia [2]. Trong nghiên cứu này, ARDS chiếm 10% nhập viện vào khoa chăm sóc đặc biệt (ICU, intensive care unit) và 23% bệnh nhân thở máy. Tỷ lệ tử vong tại bệnh viện, tăng theo mức độ nghiêm trọng của ARDS [2], là khoảng 40% và đạt 45% ở những bệnh nhân bị ARDS nặng [2-4]. Các di chứng về thể chất, tâm lý và nhận thức đáng kể, với tác động rõ rệt đến chất lượng cuộc sống, đã được báo cáo tới 5 năm sau ARDS [5].
Một trong những kết quả quan trọng nhất của nghiên cứu LUNG SAFE là ARDS không được xác định bởi bác sĩ lâm sàng chăm sóc chính trong gần 40% trường hợp [2]. Điều này đặc biệt đúng đối với ARDS nhẹ, trong đó chỉ 51% trường hợp được xác định [2]. Khi tất cả các tiêu chí ARDS được đáp ứng, chỉ có 34% bệnh nhân ARDS được xác định, cho thấy có sự chậm trễ trong việc điều trị thích hợp, đặc biệt là thở máy [2]. Đây là lý do chính tại sao các hướng dẫn chính thức này không giới hạn ở những bệnh nhân bị ARDS nặng, nhưng được dùng cho tất cả các bệnh nhân chăm sóc đặc biệt thở máy.
Kết quả từ nghiên cứu LUNG SAFE cho thấy rằng các thiết lập máy thở được sử dụng không hoàn toàn tôn trọng các nguyên tắc của thông khí cơ học bảo vệ [2]. Áp lực cao nguyên được đo chỉ trong 40% bệnh nhân ARDS [2]. Và chỉ hai phần ba số bệnh nhân được ghi nhận áp lực cao nguyên khi được thở máy bảo vệ (thể tích khí lưu thông ≤ 8 mL/kg trọng lượng cơ thể dự đoán [PBW] và áp lực cao nguyên ≤ 30 cmH2O) [2]. Phân tích kết quả LUNG SAFE cũng cho thấy thiếu mối quan hệ giữa PEEP và tỷ lệ PaO2/FiO2 [2]. Ngược lại, có một mối quan hệ nghịch đảo giữa FiO2 và SpO2, cho thấy rằng các bác sĩ lâm sàng đã sử dụng FiO2 để điều trị thiếu oxy máu. Cuối cùng, tư thế nằm sấp sử dụng chỉ trong 8% bệnh nhân nhập viện với ARDS, về cơ bản là điều trị cứu hộ [2].
Việc giảm tỷ lệ tử vong liên quan đến ARDS trong 20 năm qua dường như được giải thích chủ yếu bằng việc giảm tổn thương phổi do máy thở (VILI, ventilator-induced lung injury). VILI về cơ bản có liên quan đến volutrauma, có liên quan mật thiết với “strain” và “stress”. “Stress” phổi tương ứng với áp lực xuyên phổi (áp lực phế nang – áp lực màng phổi), và “strain” phổi liên quan đến sự thay đổi thể tích phổi so với dung tích cặn chức năng (FRC, functional residual capacity) của phổi ARDS ở mức PEEP = 0. Vì vậy, volutrauma tương ứng với “stress” và “strain” quá mức trên phổi bị tổn thương [6-8]. Các nghiên cứu quét CT chất lượng cao và nghiên cứu sinh lý đã cho thấy các tổn thương phổi phân bố không đều, tổn thương hoặc xẹp phổi cùng tồn tại với phế nang có sục khí gần như bình thường [9]. ARDS không phải là một bệnh; đó là một hội chứng được xác định bởi nhiều tiêu chí lâm sàng và sinh lý. Do đó, không có gì đáng ngạc nhiên khi các chiến lược thông khí bảo vệ phổi dựa trên các nguyên tắc sinh lý cơ bản đã được chứng minh là có hiệu quả trong việc cải thiện kết quả. Do đó, giảm thiểu VILI thường nhằm mục đích giảm volutrauma (giảm “stress” và “strain” tổng thể). Áp lực đường thở thấp có lợi ích kép về mặt lý thuyết là giảm thiểu tình trạng quá căng chướng của các khu vực được sục khí và giảm bớt hậu quả tiêu cực trên huyết động.
Các hướng dẫn hiện tại của SRLF đã hơn 20 năm và vì vậy cần phải cập nhật chúng. Mục đích chính của các hướng dẫn chính thức này là tự nguyện giới hạn các chủ đề trong các lĩnh vực được nghiên cứu tốt nhất, để cung cấp cho các học viên những hướng dẫn vững chắc với sự thỏa thuận cao giữa các chuyên gia. Một số khía cạnh rất quan trọng trong quản lý ARDS đã không được giải quyết một cách có chủ ý vì không đủ đánh giá về tác dụng của chúng đối với tiên lượng (nhịp thở, năng lượng cơ học, mục tiêu oxygen hóa, pH, PaCO2 …). Chúng tôi cũng giới hạn các hướng dẫn này cho bệnh nhân người lớn, ở giai đoạn đầu của ARDS (vài ngày đầu tiên) và thở máy xâm lấn.
Phương pháp
Những hướng dẫn này đã được xây dựng bởi một nhóm làm việc chuyên gia được lựa chọn bởi SRLF. Ban tổ chức trước tiên xác định các câu hỏi sẽ được giải quyết và sau đó chỉ định các chuyên gia phụ trách từng câu hỏi. Các câu hỏi được đặt ra theo định dạng Bệnh nhân – Can thiệp – So sánh – Kết cục (PICO, Patient – Intervention – Comparison – Outcome) sau cuộc họp đầu tiên của nhóm chuyên gia. Các tài liệu được phân tích bằng phương pháp Khuyến nghị, Đánh giá, Phát triển và Đánh giá (GRADE). Một mức độ bằng chứng đã được xác định cho mỗi tài liệu tham khảo thư mục được trích dẫn tùy thuộc vào loại nghiên cứu và chất lượng phương pháp luận của nó. Một mức độ tổng thể của bằng chứng đã được xác định cho từng điểm cuối. Sau đó, các chuyên gia đã xây dựng các hướng dẫn phù hợp với phương pháp GRADE (Bảng 1).

Việc xây dựng chứng cứ mức độ cao của cho một khuyến nghị “Mạnh” (nên được thực hiện … GRADE 1+, không nên thực hiện … GRADE 1-). Mức độ chứng cứ vừa phải, thấp hoặc rất thấp dẫn đến việc đưa ra một khuyến nghị tùy chọn của người dùng (có lẽ nên được thực hiện … GRADE 2+, có lẽ không nên thực hiện … GRADE 2-). Khi tài liệu không có hoặc không đủ, câu hỏi có thể là chủ đề của một đề nghị dưới dạng ý kiến chuyên gia (Các chuyên gia gợi ý rằng …). Các khuyến nghị được đề xuất đã được gửi trước và thảo luận tại cuộc họp thứ hai của nhóm chuyên gia. Sau đó, mỗi chuyên gia đã xem xét và đánh giá từng đề xuất sử dụng thang điểm từ 1 (hoàn toàn không đồng ý) đến 9 (hoàn toàn đồng ý). Xếp hạng tập thể được thực hiện bằng phương pháp lưới GRADE. Để phê duyệt một đề xuất liên quan đến một tiêu chí, ít nhất 50% các chuyên gia đã phải đồng ý và dưới 20% không đồng ý. Để có một thỏa thuận “mạnh”, ít nhất 70% các chuyên gia đã phải đồng ý. Trong trường hợp không có thỏa thuận mạnh, các đề xuất đã được cải tổ và đánh giá lại, nhằm đạt được sự đồng thuận (Bảng 2).
Khu vực 1: Đánh giá quản lý ARDS
R1.1 – Các chuyên gia đề xuất rằng hiệu quả và độ an toàn của tất cả các thông số thông khí và điều trị liên quan đến quản lý ARDS nên được đánh giá ít nhất mỗi 24 giờ.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận: Đánh giá hiệu quả và an toàn của các cài đặt và điều trị thông khí cơ học là nền tảng của giai đoạn đầu của việc quản lý bệnh nhân ARDS. Như được thể hiện trong các hướng dẫn chính thức này, các cài đặt của các tham số thông khí, chẳng hạn như PEEP, được dựa trên hiệu quả và dung sai của chúng. Hơn nữa, chỉ định cho một số phương pháp điều trị phụ thuộc vào mức độ nghiêm trọng của ARDS và các phương pháp điều trị này sẽ chỉ được thực hiện khi có đáp ứng không hiệu quả với điều trị đầu tay.
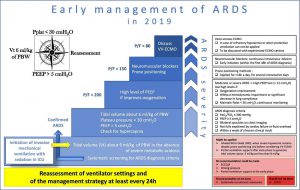
Hình 1 cho thấy các phương pháp điều trị được thực hiện cho bệnh nhân ARDS dựa trên mức độ nghiêm trọng của suy hô hấp. Quyết định bắt đầu một số phương pháp điều trị được đưa ra sau giai đoạn ổn định [10] bao gồm tối ưu hóa thông khí cơ học là bước đầu tiên của quản lý. Đánh giá sớm hiệu quả dựa trên tỷ lệ PaO2/FiO2 là cần thiết để thảo luận về sự liên quan của các chất ngăn chặn thần kinh cơ và tư thế nằm sấp tổn thương (Hình 1).
Sự an toàn của các liệu pháp dùng thuốc và các thủ thuật cũng phải được đánh giá thường xuyên. Những hướng dẫn này cũng giải quyết các vấn đề an toàn chính của phương pháp điều trị. Y văn hỗ trợ cho các thực hành như vậy còn thiếu, và chúng được hướng dẫn bởi ý nghĩa lâm sàng tốt.
Thật vậy, dữ liệu khan hiếm về lợi ích của việc đánh giá thường xuyên các cài đặt thông khí và/hoặc mức độ bệnh ở bệnh nhân ARDS. Một nghiên cứu quan sát đơn trung tâm đã chỉ ra giá trị của việc đánh giá hệ thống các thông số cơ học hô hấp trong ARDS ở giai đoạn ban đầu (chủ yếu trong 48 giờ đầu) [11]. Trong nghiên cứu này, việc đánh giá các cơ chế thụ động của phổi và lồng ngực, về đáp ứng với PEEP và huy động phế nang đã thúc đẩy thay đổi các thông số thông khí ở hầu hết bệnh nhân (41 trên 61 phân tích). Những thay đổi này có liên quan đến sự cải thiện áp lực cao nguyên (- 2 cmH2O trên trung bình), áp lực đẩy (trung bình – 3 cmH2O) và chỉ số oxygen hóa [11].
| Bảng 2. Tóm tắt các hướng dẫn | ||
| Khuyến nghị | Mức độ chứng cứ | |
| Đánh giá xử trí ARDS | ||
| R1.1 | Các chuyên gia khuyên rằng hiệu quả và độ an toàn của tất cả các thông số và phương pháp điều trị thông khí liên quan đến quản lý ARDS nên được đánh giá ít nhất cứ sau 24 giờ | Ý kiến chuyên gia |
| Điều chỉnh thể tích khí lưu thông | ||
| R2.1.1 | Nên sử dụng thể tích khí lưu thông khoảng 6 ml/kg trọng lượng cơ thể dự đoán (PBW) như một phương pháp đầu tiên ở những bệnh nhân mắc ARDS được xác nhận, trong trường hợp không bị nhiễm toan chuyển hóa nặng, bao gồm cả những người mắc ARDS nhẹ, để giảm tỷ lệ tử vong | Grade 1+ |
| R2.1.2 | Các chuyên gia đề xuất một cách tiếp cận tương tự cho tất cả các bệnh nhân thở máy xâm lấn và được dùng thuốc an thần trong ICU, do tỷ lệ thất bại cao để nhận ra ARDS và tầm quan trọng của việc thực hiện bảo vệ phổi nhanh chóng | Ý kiến chuyên gia |
| Áp lực cao nguyên | ||
| R2.2.1 | Khi thể tích khí lưu thông được thiết lập khoảng 6 mL/kg trọng lượng cơ thể dự đoán, áp lực cao nguyên phải được theo dõi liên tục và không được vượt quá 30 cmH2O để giảm tỷ lệ tử vong | Grade 1+ |
| R2.2.2 | Các chuyên gia khuyên rằng không nên tăng thể tích khí lưu thông khi áp lực cao nguyên dưới 30 cmH2O, trừ trường hợp tăng CO2 máu rõ rệt, kéo dài mặc dù giảm khoảng chết dụng cụ và tăng tần số thở | Ý kiến chuyên gia |
| Áp lực đẩy | ||
| R2.3 | Dữ liệu khả dụng không cho phép đưa ra khuyến nghị về cài đặt máy thở chỉ dựa trên giới hạn áp lực đẩy. Giới hạn này có thể được dự kiến như là một bổ sung cho việc giới hạn áp lực cao nguyên trong một số trường hợp đặc biệt | Không khuyến nghị |
| Áp lực dương cuối thì thở ra (PEEP) | ||
| R3.1.1 | PEEP là một thành phần thiết yếu trong việc quản lý ARDS và các chuyên gia đề nghị sử dụng giá trị trên 5 cmH2O ở tất cả các bệnh nhân ARDS | Ý kiến chuyên gia |
| R3.1.2 | PEEP cao có lẽ nên được sử dụng ở những bệnh nhân mắc ARDS vừa hoặc nặng, nhưng không phải ở những bệnh nhân mắc ARDS nhẹ | Grade 2+ |
| R3.1.3 | Các chuyên gia đề nghị dự trữ PEEP cao cho những bệnh nhân cải thiện quá trình oxygen hóa mà không làm suy giảm đáng kể độ giãn nở hệ hô hấp hoặc tình trạng huyết động. Cài đặt PEEP nên được cá nhân hóa | Ý kiến chuyên gia |
| Thông khí dao động tần số cao | ||
| R3.2 | Không nên sử dụng thông khí dao động tần số cao ở bệnh nhân ARDS | Grade 1- |
| Thủ thuật huy động phế nang | ||
| R3.3 | Thủ thuật huy động có lẽ không nên được sử dụng thường quy ở bệnh nhân ARDS | Grade 2- |
| Dùng sớm và ngắn hạn thuốc chẹn thần kinh cơ | ||
| R4.1 | Một thuốc ức chế thần kinh cơ có lẽ nên được xem xét ở những bệnh nhân ARDS có tỷ lệ PaO2/FiO2 <150 mmHg để giảm tỷ lệ tử vong. Thuốc ức chế thần kinh cơ nên được sử dụng bằng cách tiêm truyền liên tục sớm (trong vòng 48 giờ sau khi bắt đầu ARDS), không quá 48 giờ, với ít nhất là đánh giá hàng ngày | Grade 2+ |
| Thông khí tự phát sớm | ||
| R4.2.1 | Dữ liệu hiện có không cho phép đưa ra khuyến nghị về chiến lược thông khí tự phát thường quy trong giai đoạn cấp tính của ARDS | Không khuyến nghị |
| R4.2.2 | Sau giai đoạn cấp tính của ARDS, các chuyên gia khuyên rằng thông khí với chế độ áp lực cho phép thông khí tự phát có thể được sử dụng khi đảm bảo thể tích khí lưu thông tạo ra gần 6 mL/kg PBW và không vượt quá 8 mL/kg PBW | Ý kiến chuyên gia |
| Tư thế nằm sấp | ||
| R5.1 | Tư thế nằm sấp nên được sử dụng ở bệnh nhân ARDS có tỷ lệ PaO2/FiO2 <150 mmHg để giảm tỷ lệ tử vong. Các phiên ít nhất 16 giờ liên tục nên được thực hiện | Grade 1+ |
| Oxygen hóa qua màng ngoài cơ thể tĩnh mạch-tĩnh mạch | ||
| R6.1 | Có thể cân nhắc oxygen hóa qua màng ngoài cơ thể (ECMO) trong trường hợp ARDS nặng với PaO2/FiO2 <80 mmHg và/hoặc khi thở máy trở nên nguy hiểm do tăng áp lực cao nguyên và mặc dù tối ưu hóa quản lý ARDS bao gồm PEEP cao, thuốc chẹn thần kinh cơ, và nằm sấp. Quyết định sử dụng ECMO cần được đánh giá sớm bằng cách liên hệ với trung tâm chuyên gia | Grade 2+ |
| Loại bỏ CO2 ngoài cơ thể lưu lượng thấp | ||
| R6.2 | Dữ liệu hiện có không cho phép đưa ra khuyến nghị liên quan đến việc sử dụng loại bỏ CO2 ngoài cơ thể lưu lượng thấp trong ARDS | Không khuyến nghị |
| Oxit nitric dạng hít | ||
| R7.1 | Các chuyên gia cho rằng oxit nitric dạng hít có thể được sử dụng trong trường hợp ARDS bị thiếu oxy máu nặng, mặc dù đã thực hiện chiến lược thông khí bảo vệ và tư thế nằm sấp và trước khi dự tính sử dụng ECMO tĩnh mạch- tĩnh mạch | Ý kiến chuyên gia |
Thật khó để xác định mức độ thường xuyên để đánh giá các thông số và phương pháp điều trị thông khí trong ARDS. Có vẻ như một quyền tự do ít nhất tương tự như đề xuất cho việc đánh giá các tiêu chí cai máy thở (tức là hàng ngày) là hợp lý [12]. Tuy nhiên, đánh giá thường xuyên hơn có thể là cần thiết và có lợi trong một số trường hợp.
Khu vực 2: Quản lý thể tích khí lưu thông
Điều chỉnh thể tích khí lưu thông R2.1.1 – Nên sử dụng thể tích khí lưu thông khoảng 6 mL/kg trọng lượng cơ thể được dự đoán (PBW) như một phương pháp tiếp cận ở bệnh nhân mắc ARDS được xác nhận, trong trường hợp không có toan chuyển hóa nặng, kể cả những người bị ARDS nhẹ, để giảm tỷ lệ tử vong.
GRADE 1 +, KHUYẾN NGHỊ MẠNH
R2.1.2 – Các chuyên gia đề xuất một cách tiếp cận tương tự cho tất cả các bệnh nhân điều trị thở máy xâm lấn và gây mê trong ICU, do tỷ lệ thất bại cao trong việc nhận ra ARDS và tầm quan trọng của việc thực hiện nhanh chóng việc thông khí bảo vệ phổi.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận:
Để kiểm soát sự gia tăng tiềm tàng của PaCO2 (làm tăng áp lực động mạch phổi), nên sử dụng tần số thở tương đối cao trong khoảng từ 25 đến 30 nhịp thở/phút. Tuy nhiên, tần số quá cao sẽ gây ra nguy cơ siêu bơm phồng động và cũng làm tăng khả năng phơi nhiễm tích lũy mỗi phút đối với nguy cơ bơm phồng tiềm ẩn. Một PaCO2 dưới 50 mmHg thường được chấp nhận. Việc giảm khoảng chết của thiết bị cũng thích hợp và nên sử dụng máy tạo độ ẩm ấm đầu tiên.
PBW nên được tính cho mỗi bệnh nhân khi nhập viện tùy thuộc vào chiều cao và giới tính.
Thể tích khí lưu thông được cung cấp sẽ gây ra sự gia tăng áp lực từ PEEP, do đó cần phải theo dõi áp lực cao nguyên, nên được giữ dưới 30 cmH2O.
Các bác sĩ lâm sàng cần nhận thức được những nguy cơ tiềm ẩn của thể tích khí lưu thông thấp, chẳng hạn như mất đồng bộ và kích hoạt kép. Hướng dẫn về giảm áp lực và thể tích ban hành vào cuối những năm 1980 dựa trên dữ liệu thực nghiệm và lâm sàng [13-16]. Một số thử nghiệm lâm sàng ngẫu nhiên với khá ít đối tượng trong những năm 1990 không tìm thấy lợi ích sống sót của thể tích khí lưu thông thấp [17, 18]. Tất nhiên, việc thiếu sức mạnh (power) có thể giải thích những kết quả tiêu cực này. Cũng lưu ý rằng những thử nghiệm này không nhằm mục đích đạt được sự kiểm soát PaCO2, điều này có thể góp phần vào những ảnh hưởng xấu của nhiễm toan tăng CO2 máu trong các nhóm nghiên cứu sử dụng thể tích khí lưu thông thấp. Mặc dù bằng chứng lâm sàng không dễ cho thấy, tăng CO2 máu có tác dụng phụ không thể nghi ngờ [19], như tăng sức đề kháng của phổi, có thể làm xấu đi tiên lượng. Năm 2000, nghiên cứu ARMA do NHLBI ARDS Network ở Hoa Kỳ thực hiện đã thu được dữ liệu quan trọng so sánh chiến lược bảo vệ phổi bằng cách sử dụng thể tích khí lưu thông thấp, trung bình 6 ml/kg PBW, áp lực cao nguyên giới hạn ở 30 cmH2O và tần số thở lên tới 35 nhịp thở/phút, so với chiến lược không bảo vệ bằng cách sử dụng thể tích khí lưu thông 12 ml/kg PBW [20]. Việc sử dụng PBW được tính tùy thuộc vào giới tính và chiều cao là một sự đổi mới quan trọng trong việc điều chỉnh thể tích khí lưu thông với thể tích phổi dự kiến. Trong nghiên cứu này, tần số hô hấp tăng dẫn đến thông khí thể tích thấp kết hợp với chỉ tăng PaCO2 tối thiểu, kết quả có thể góp phần vào lợi ích của nhánh điều trị này. Giảm 25% nguy cơ tử vong tương đối đã được quan sát, tức là, giảm 30-40% trong tỷ lệ tử vong chung. Nghiên cứu này đã có một tác động rất lớn đến thực hành lâm sàng. Đây không phải là lần đầu tiên sử dụng thể tích thấp thành công, giải thưởng đó thuộc về nghiên cứu hai trung tâm của Amato và cộng sự, nhưng thể tích khí lưu thông thấp được kết hợp với PEEP cao hơn, ý tưởng là giảm áp lực đẩy [21]. Các nghiên cứu khác sử dụng phương pháp tương tự như Amato et al. tìm thấy một sự giảm tương tự về tỷ lệ tử vong [22]. Các phân tích tổng hợp về giảm khí lưu thông thường bao gồm các nghiên cứu khá không đồng nhất [23]. Gần đây nhất bao gồm bảy thử nghiệm ngẫu nhiên ở 1481 bệnh nhân [24] và kết luận rằng tỷ lệ tử vong thấp hơn có liên quan đến thông khí thể tích thấp trong phân tích chính (tỷ lệ nguy hiểm 0,80 [0,66, 0,98]) và tìm thấy mối quan hệ đáng kể giữa giảm thể tích khí lưu thông và tác dụng giảm tử vong. Tuy nhiên, khi các nghiên cứu kết hợp PEEP cao và thể tích thấp bị loại trừ, ảnh hưởng của thể tích khí lưu thông giảm chỉ là một xu hướng không đáng kể (0,87 [0,70, 1,08]). Theo các tác giả, điều này cho thấy, nhưng không chứng cứ rằng việc giảm thể tích khí lưu thông làm giảm đáng kể tỷ lệ tử vong trong ARDS. Trong một nghiên cứu quan sát, 11,558 thông số thông khí có sẵn cho 482 bệnh nhân ARDS được xác định tiền cứu [25]. Các tác giả đã so sánh các bệnh nhân có thể tích 6,5 ml/kg PBW hoặc ít hơn, khi nhập viện, với các bệnh nhân có thể tích > 6,5 ml/kg PBW (68% bệnh nhân), và thấy rằng, sau khi điều chỉnh các yếu tố gây nhiễu đã biết, tăng 1 mL/kg PBW trong cài đặt của thể tích ban đầu có liên quan đến việc tăng 23% nguy cơ tử vong trong chăm sóc đặc biệt (tỷ lệ nguy hiểm, 1,23; khoảng tin cậy 95%, 1,06-1,44; p = 0,008) [25]. Sự gia tăng thứ cấp về thể tích khí lưu thông cũng liên quan đến sự gia tăng nguy cơ tử vong, nhưng nguy cơ tử vong của thể tích khí lưu thông đầu tiên quá cao so với ảnh hưởng của các thể tích sau [25]. Trong nghiên cứu LUNG SAFE [2], thể tích khí lưu thông dường như không phải là yếu tố quan trọng trong tỷ lệ tử vong. Tuy nhiên, phạm vi thể tích bị giới hạn [26], điều này cho thấy rằng một mức độ nhất định của bảo vệ phổi được sử dụng rất thường xuyên, nhưng ở rất ít bệnh nhân có thể tích khí lưu thông trên 10 hoặc thấp hơn 6 mL/kg. Không có sự khác biệt về tỷ lệ sống sót ở những bệnh nhân có thể tích khí lưu thông bằng hoặc lớn hơn giá trị trung bình là 7.1 mL/kg PBW [26]. Ngoài ra, việc sử dụng thể tích khí lưu thông thấp hơn ở những bệnh nhân mắc ARDS nặng có thể liên quan đến các tác động gây nhiễu tiềm ẩn, rất khó để phân tích hoàn toàn trong dữ liệu quan sát thuần túy [26]. Tuy nhiên, trong tất cả các phân tích, áp lực (áp lực cực đại, áp lực cao nguyên, áp lực đẩy và PEEP) mang trọng lượng lớn hơn so với thể tích khí lưu thông trong tiên lượng [26].
Áp lực Cao nguyên
R2.2.1 – Khi thể tích khí lưu thông được đặt ở mức khoảng 6 mL/kg PBW, áp lực cao nguyên phải được kiểm soát liên tục và không được vượt quá 30 cmH2O để giảm tỷ lệ tử vong.
GRADE 1 +, KHUYẾN NGHỊ MẠNH
R2.2.2 – Các chuyên gia khuyên rằng không nên tăng thể tích khí lưu thông khi áp lực cao nguyên dưới 30 cmH2O, trừ trường hợp tăng CO2 máu kéo dài, rõ rệt mặc dù đã giảm khoảng chết của dụng cụ và tăng tần số thở.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận:
Thể tích khí lưu thông, áp lực cao nguyên và áp lực đẩy có liên quan chặt chẽ với nhau [độ giãn nở tĩnh = thể tích khí lưu thông/(áp lực cao nguyên – tổng PEEP)] và tất cả đều tham gia vào VILI. Thông khí cơ học nên hạn chế VILI, do đó hạn chế tử vong. Ngay cả khi VILI ban đầu được quan sát thấy khi áp dụng áp lực cao nguyên cao với thể tích khí lưu thông cao [16], thì vẫn có ít tổn thương phổi so với cùng một áp lực cao nguyên khi thể tích khí lưu thông giảm do độ cứng của thành ngực [13], một tình huống gặp phải trong bệnh nhân béo phì bệnh lý.
Nghiên cứu LUNG SAFE báo cáo rằng áp lực cao nguyên không được theo dõi ở 60% bệnh nhân ARDS thở máy và tỷ lệ bệnh nhân không đáng kể, mặc dù được thở với thể tích khí lưu thông dưới 8 ml/kg PBW, có áp lực cao nguyên trên 30 cmH2O, đặc biệt là những người bệnh ARDS mức độ vừa đến nặng [2]. Một nghiên cứu phụ trợ của LUNG SAFE đã chỉ ra rằng áp lực cao nguyên, có thể được sửa đổi bởi bác sĩ hồi sức, có mối tương quan chặt chẽ và tích cực với tỷ lệ tử vong [26]. Áp lực cao nguyên là một yếu tố nguy cơ tử vong độc lập, vì nó phản ánh mức độ nghiêm trọng (liên quan đến độ giãn nở phổi kém) hoặc thở máy không đầy đủ [27].
Cách duy nhất để theo dõi áp lực cao nguyên thường xuyên là thông khí cho bệnh nhân có tạm dừng cuối thì hít vào, không nên quá dài, để tạo điều kiện cho tăng tần số thở, hoặc quá ngắn, để máy thở có thể đo được áp lực. Nên sử dụng tạm dừng 0,2-0.3 giây khi điều chỉnh máy thở.
Ở một bệnh nhân nhất định, áp lực cao nguyên là sự phản ánh không hoàn hảo của tình trạng quá căng phổi [28]. Điều này đặc biệt ở những bệnh nhân có độ giãn nở bất thường của thành ngực và ở một số bệnh nhân béo phì. Mối quan hệ giữa áp lực cao nguyên và tỷ lệ tử vong hoặc nguy cơ mắc barotrauma ít rõ ràng hơn ở những bệnh nhân này [29], điều này có thể cho thấy khả năng chịu áp lực cao nguyên cao hơn 30 cmH2O một chút, với điều kiện là thể tích khí lưu thông giảm để hạn chế VILI [13]. Trong mọi trường hợp, áp lực cao nguyên không còn liên quan đến chấn thương khi nó được giữ dưới 30 cmH2O.
Năm nghiên cứu ngẫu nhiên và có đối chứng đã so sánh một chiến lược về lượng khí lưu thông thấp và giới hạn áp lực cao nguyên với một chiến lược sử dụng thể tích khí lưu thông và áp lực cao nguyên cao hơn [17, 18, 20, 21, 30]. Sự giảm đáng kể tỷ lệ tử vong ở nhóm có thể tích và áp lực hạn chế chỉ được ghi nhận trong 2 nghiên cứu [20, 21] trong đó sự khác biệt về áp lực cao nguyên là đặc biệt lớn giữa 2 chiến lược được thử nghiệm. Khi 5 nghiên cứu này được gộp lại, có một mối quan hệ chặt chẽ giữa áp lực cao nguyên và tỷ lệ tử vong [31]. Trong một nghiên cứu gần đây ở 478 bệnh nhân, áp lực cao nguyên 29 cmH2O đã được xác định là ngưỡng bắt đầu tăng tỷ lệ tử vong của bệnh viện [32]. Ngay cả ở những bệnh nhân được thở máy với áp lực đẩy trên 19 cmH2O, nhưng áp lực cao nguyên dưới 30 cmH2O sẽ cho phép giảm đáng kể tỷ lệ tử vong, tác động lớn hơn áp lực đẩy dưới 19 cmH2O khi áp lực cao nguyên đã trên 30 cmH2O [32]. Những kết quả này đã được xác nhận trong cùng một nghiên cứu trong một đoàn hệ khác nhau gồm 300 bệnh nhân [32].
Áp lực đẩy
R2.3 – Dữ liệu khả dụng không cho phép khuyến nghị được thực hiện liên quan đến cài đặt máy thở chỉ dựa trên giới hạn áp lực đẩy. Giới hạn này có thể được dự tính như là một công cụ để hạn chế áp lực cao nguyên trong một số trường hợp đặc biệt.
KHÔNG KIẾN NGHỊ
Cơ sở lý luận:
Một nghiên cứu hồi cứu đã đánh giá lại ảnh hưởng của áp lực đẩy đến tiên lượng, bằng phương pháp phân tích thống kê phức tạp của chín nghiên cứu ngẫu nhiên có kiểm soát về chiến lược thông khí (so sánh các giá trị khác nhau của thể tích khí lưu thông và PEEP, trong ARDS) [33]. Các tác giả kết luận rằng áp lực đẩy là yếu tố dự báo tốt nhất về tỷ lệ tử vong trong các nghiên cứu này. Tuy nhiên, như chính các tác giả thừa nhận, đây là một nghiên cứu hồi cứu các nghiên cứu với mục đích chính là không kiểm tra mức độ sử dụng của áp lực đẩy. Kể từ đó, không có nghiên cứu ngẫu nhiên nào chứng thực giá trị của việc giới hạn áp lực đẩy. Ngược lại, kết quả của nghiên cứu quan sát LUNG SAFE [2, 26] cho thấy không có sự vượt trội rõ ràng về áp lực đẩy so với áp lực cao nguyên như là một yếu tố dự báo nguy cơ tử vong. Điều tương tự cũng đúng khi dữ liệu của hai nghiên cứu cho thấy khả năng sống sót được cải thiện trong ARDS (theo dùng thuốc chẹn thần kinh cơ và tư thế nằm sấp) được kết hợp [34]. Cần thận trọng về vai trò của áp lực đẩy, và các nghiên cứu khác thậm chí còn mang lại một số lo ngại về tính hợp lệ của khái niệm sinh lý học này. Không giống như áp lực cao nguyên, tương ứng với căng chướng phổi động và tĩnh, áp lực đẩy tương ứng với sự căng chướng phổi động. Một nghiên cứu ngẫu nhiên có kiểm soát về PEEP [35] (cho thấy rằng một PEEP cao hơn có liên quan đến tỷ lệ tử vong cao hơn) dường như đặt ra câu hỏi về giá trị tiên đoán của áp lực đẩy. Thật vậy, áp lực cao nguyên thấp hơn ở nhóm có tỷ lệ tử vong thấp hơn, trong khi áp lực đẩy thấp hơn ở nhóm có tỷ lệ tử vong cao hơn [35].
Phân tích một loạt các bệnh nhân ARDS thở máy có biểu hiện tâm phế cấp tính [36] cho thấy rằng khi áp lực cao nguyên được giữ ở mức đủ thấp (<27 cmH2O), áp lực đẩy được dự đoán gây ra tâm phế cấp và tử vong. Do đó, một nghiên cứu ngẫu nhiên được thiết kế để chứng minh giá trị tiên đoán của việc áp lực đẩy nên hạn chế để áp lực cao nguyên xuống dưới 30 cmH2O hoặc thậm chí 28 cmH2O trong hai nhóm. Ngoài ra, thể tích khí lưu thông phải được giới hạn ở mức 6 mL/kg, PEEP là cài đặt máy thở duy nhất có thể thay đổi. Do đó, điều này sẽ giúp so sánh hai mức PEEP trong quá trình thông khí với áp lực cao nguyên hạn chế. Đây chính xác là những gì nghiên cứu EXPRESS đã làm và kết quả của nó là âm tính [37].
Trong điều kiện thực tế, tốt nhất là trước tiên phải đo lường và hạn chế áp lực cao nguyên, một cách tiếp cận mà nghiên cứu LUNG SAFE [2] đã chỉ ra rõ ràng là không được sử dụng đầy đủ. Chỉ sau khi hạn chế đủ áp lực cao nguyên, chúng ta mới có thể dự tính hạn chế áp lực đẩy trong những trường hợp khi độ giãn nở phổi giảm nghiêm trọng bắt buộc sử dụng PEEP không đầy đủ để đảm bảo điều chỉnh oxygen hóa (ví dụ, trong trường hợp khi PEEP là 6-8 cmH2O và thể tích khí lưu thông 6 mL/kg sẽ tạo ra áp lực cao nguyên khoảng 30 cmH2O ở một bệnh nhân bị thiếu oxy máu kéo dài). Trong trường hợp này, có thể hữu ích để giảm áp lực đẩy bằng cách hạn chế thể tích khí lưu thông, đồng thời tăng PEEP, nếu thủ thuật này được dung nạp tốt về mặt huyết động.
Khu vực 3: Huy động phế nang
Áp lực dương cuối thì thở ra
R3.1.1 – PEEP là một thành phần thiết yếu trong việc quản lý ARDS và các chuyên gia khuyên bạn nên sử dụng giá trị trên 5 cmH2O ở tất cả các bệnh nhân biểu hiện ARDS.
Ý KIẾN CHUYÊN GIA
R3.1.2 – PEEP cao có lẽ nên được sử dụng ở những bệnh nhân mắc ARDS mức độ vừa hoặc nặng, nhưng không phải ở những bệnh nhân mắc ARDS mức độ nhẹ.
GRADE 2 +, KHUYẾN NGHỊ MẠNH
R3.1.3 – Các chuyên gia khuyên nên dự trữ PEEP cao cho những bệnh nhân cải thiện tình trạng oxygen hóa mà không làm giảm đáng kể tình trạng độ giãn nở hệ thống hô hấp hoặc tình trạng huyết động. Cài đặt PEEP nên được cá nhân hóa.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận:
PEEP là một phần không thể thiếu trong chiến lược thông khí bảo vệ. Tác động có lợi dự kiến của PEEP cao là tối ưu hóa việc huy động phế nang, một mặt, làm giảm shunt trong phổi, do đó cải thiện oxygen hóa động mạch, và mặt khác, làm giảm lượng mô phổi tiếp xúc với đóng mở phế nang, do đó giảm nguy cơ VILI [38, 39]. Ngược lại, các tác động xấu của PEEP cao là tăng thể tích phổi cuối thì hít vào, do đó làm tăng nguy cơ volutrauma [13], ảnh hưởng xấu lên huyết động liên quan đến giảm tiền tải và trên hết là tăng hậu tải thất phải [40, 41]. Khi PEEP tổng hằng định, tác động của PEEP nội sinh, trong ARDS, giống hệt với PEEP bên ngoài [42, 43].
Mức độ ảnh hưởng có lợi và có hại của PEEP cao thay đổi rất nhiều từ bệnh nhân này sang bệnh nhân khác và không thể dự đoán được từ dữ liệu lâm sàng đơn giản có sẵn ở đầu giường. Tuy nhiên, các nghiên cứu sử dụng CT scan ngực đã chỉ ra rằng, trung bình, lượng mô phổi có thể huy động được với PEEP cao sẽ lớn hơn khi tỷ lệ PaO2/FiO2 đo được với PEEP thấp (5 cmH2O) [44, 45].
Một phân tích post-hoc của 2 thử nghiệm ngẫu nhiên cho thấy, ở những bệnh nhân ngẫu nhiên dẫn đến tăng PEEP, tỷ lệ tử vong tại bệnh viện thấp hơn khi có tăng tỷ lệ PaO2/FiO2 sau khi tăng PEEP [46].
Về mặt cá nhân hóa, ảnh hưởng của PEEP cao về mặt huy động không thể được đánh giá từ những thay đổi trong độ giãn nở hệ hô hấp [45, 47]. Không có thông số cơ học về khí hoặc hô hấp dễ dàng có sẵn ở đầu giường cho phép định lượng nguy cơ volutrauma gây ra do sử dụng PEEP cao. Trung bình, các mức PEEP được sử dụng trong các thử nghiệm ngẫu nhiên so sánh giữa các loại PEEP “cao” và “vừa phải” lần lượt là 15,1 ± 3,6 cmH2O và 9,1 ± 2,7 cmH2O [24]. Do đó, 12 cmH2O có thể được xem xét – được coi là ngưỡng trên mà PEEP có thể đủ tiêu chuẩn cao.
Không có sự khác biệt đáng kể về tỷ lệ tử vong được tìm thấy trong 3 thử nghiệm ngẫu nhiên lớn so sánh tác động của PEEP “cao” và “trung bình” ở bệnh nhân ARDS được thở máy với thể tích khí lưu thông 6 ml/kg PBW [37, 48, 49]. Một phân tích tổng hợp dữ liệu cá nhân từ các bệnh nhân trong 3 thử nghiệm này cho thấy PEEP cao có liên quan đến việc giảm đáng kể 5% tỷ lệ tử vong ở bệnh viện ở những bệnh nhân mắc ARDS trung bình hoặc nặng (34,1% so với 39,1%, p < 0,05) , trong khi nó có liên quan đến tỷ lệ tử vong cao hơn (27,2% so với 19,4%, p = 0,05) ở những bệnh nhân mắc ARDS nhẹ [50].
Ở những bệnh nhân mắc ARDS vừa hoặc nặng, cài đặt PEEP cá nhân sử dụng áp lực xuyên phổi cuối thì thở ra không dẫn đến giảm tỷ lệ tử vong so với PEEP sử dụng thang PEEP/FiO2 [51].
Thông khí dao động tần số cao
R3.2. – Không nên sử dụng thông khí dao động tần số cao ở bệnh nhân ARDS.
GRADE 1 -, KHUYẾN NGHỊ MẠNH
Cơ sở lý luận:
Thông khí dao động tần số cao (HFOV) là một chế độ thông khí không thông thường, được đề xuất để cải thiện trao đổi khí trong khi bảo vệ chống lại VILI bằng cách sử dụng một thể tích khí lưu thông bên dưới hoặc bằng khoảng chết giải phẫu [52]. Dòng khí liên tục tạo ra áp lực căng đường thở liên tục (cPaw) để huy động nhu mô phổi, trong khi các dao động hình sin của màng ở tần số hô hấp cao (3-8 Hz) tạo ra thể tích khí lưu thông. Lưu lượng khí và bơm phồng của van bóng cho phép điều chỉnh cPaw, xác định oxygen hóa theo tỷ lệ. Thể tích khí lưu thông tăng theo biên độ của các chuyển động của màng và giảm khi tần số tăng, điều này giải thích tại sao việc loại bỏ CO2 tỷ lệ nghịch với tần số được sử dụng.
Nhiều nghiên cứu sinh lý đã cho rằng HFOV rất hữu ích trong việc quản lý ARDS. Nhờ các cơ chế trao đổi khác với trao đổi đơn giản bằng đối lưu [53], HFOV cho phép giảm thể tích khí lưu thông nhiều hơn và giảm biên độ của các biến động theo chu kỳ trong áp lực xuyên phổi, do đó cho phép sử dụng cPaw cao để tối ưu hóa việc huy động phổi. Bằng cách tăng tỷ lệ nhu mô thông khí, việc huy động gây ra trong HFOV có thể làm giảm “stress” và “strain” phổi, giảm lực cắt liên quan đến việc mở và đóng phế nang không ổn định và hạn chế VILI. Do đó, các đặc tính thông khí trong HFOV làm cho nó lý tưởng về mặt bảo vệ phổi [52, 54].
Một số nghiên cứu lâm sàng đã báo cáo rằng HFOV cải thiện oxygen hóa ở người lớn mắc ARDS và giảm oxy máu kháng trị trong thông khí thông thường [55-58]. Ba nghiên cứu ngẫu nhiên báo cáo xu hướng giảm tỷ lệ tử vong khi HFOV được sử dụng như một chế độ điều trị ban đầu ở 58, 148 và 125 bệnh nhân ARDS, tương ứng [59- 61]. Tuy nhiên, việc sử dụng thể tích khí lưu thông quá mức trong nhóm đối chứng sẽ hạn chế giá trị của các nghiên cứu này, điều này không cho phép khuyến nghị HFOV là chế độ thông khí chính cho ARDS.
Gần đây, 2 thử nghiệm ngẫu nhiên lớn không tìm thấy lợi ích của HFOV so với thở máy thông thường với thể tích khí lưu thông = 6 mL/kg, giới hạn áp lực cao nguyên và PEEP tùy theo mức độ nghiêm trọng ARDS [62, 63]. Trong nghiên cứu của OSCILLATE, một chiến lược huy động tích cực trong HFOV thậm chí còn được kết hợp với sự gia tăng đáng kể về tỷ lệ tử vong [62]. Có thể việc sử dụng cPaw cao gây ra tình trạng quá căng phổi mà không làm tăng thông khí trong phế nang bị xẹp hoặc ứ dịch, đặc biệt ở những bệnh nhân có tổn thương không đồng nhất và một tỷ lệ hạn chế nhu mô có thể huy động. Việc sử dụng áp lực cao cũng có thể gây ra sự gia tăng hậu tải thất phải, suy tâm thất phải [64] và mất ổn định huyết động đòi hỏi phải dùng thuốc vận mạch cao hơn [62]. Với chiến lược chuẩn độ cPaw dựa trên áp lực phế nang trung bình được sử dụng trước khi bắt đầu HFOV và đáp ứng về mặt oxygen hóa, Young et al. không tìm thấy sự khác biệt về tỷ lệ tử vong trong nghiên cứu OSCAR khi HFOV được so sánh với thở máy thông thường ở bệnh nhân ARDS [63]. Năm 2016, nghiên cứu LUNG SAFE tiết lộ rằng HFOV đã được sử dụng ở 1,2% bệnh nhân ARDS [2].
Một số phân tích tổng hợp có hệ thống của 5 nghiên cứu ngẫu nhiên đã đánh giá các điểm cuối thứ cấp, chẳng hạn như trao đổi khí và tỷ lệ mắc barotrauma [65-68]. Họ đã không cho thấy sự cải thiện đáng kể trong trao đổi khí hoặc giảm tỷ lệ barotrauma với HFOV. Một phân tích tổng hợp gần đây của dữ liệu cá nhân cho thấy HFOV có thể cải thiện tỷ lệ tử vong ở những bệnh nhân bị thiếu oxy nặng hơn [66].
Các phương thức lý tưởng cho chuẩn độ cPaw, tần số dao động và giám sát HFOV được xác định kém. Cụ thể, các nghiên cứu là cần thiết để xác định xem việc đánh giá áp lực xuyên phổi bằng cách đo áp lực thực quản có hữu ích trong việc điều chỉnh cPaw, cải thiện việc huy động phổi và tránh tình trạng quá căng phổi [69]. Trong khi chờ kết quả của một nghiên cứu đang tiến hành thử nghiệm giả thuyết này (Lâm sàng Trials.gov NCT02342756), HFOV nên được giới hạn trong các thử nghiệm lâm sàng ở những bệnh nhân mắc ARDS nặng trong đó thở máy thông thường đã thất bại, mặc dù đã áp dụng tư thế nằm sấp, và nên được thực hiện trong trung tâm có kinh nghiệm đáng kể về HFOV.
Huy động
R3.3 – Thủ thuật huy động có lẽ không nên được sử dụng thường xuyên ở bệnh nhân ARDS.
GRADE 2 -, KHUYẾN NGHỊ MẠNH
Cơ sở lý luận:
Trong trường hợp bị mất huy động rõ ràng (hút đàm qua nội khí quản, ngắt kết nối do tai nạn hoặc theo kế hoạch, đặt nội khí quản …), có thể sử dụng một thủ thuật huy động cẩn thận. Nếu giảm oxy máu là kháng trị (PaO2/FiO2 <100 mmHg) mặc dù tối ưu hóa trị liệu, một thủ thuật huy động có thể được dự kiến trong trường hợp không có chống chỉ định.
Không có thủ thuật huy động nào được ưa thích hơn cái khác. Quy trình được khuyến nghị nên kéo dài không quá 10-20 giây và áp lực đường thở không được vượt quá 30-40 cmH2O. Thủ thuật huy động nên được thực hiện cẩn thận và nên ngưng nếu an toàn về huyết động kém.
Bệnh nhân ARDS thường xuyên xuất hiện tình trạng xẹp phổi, làm giảm thể tích phổi thông khí, giảm oxy máu và làm tăng VILI [70]. Việc thực hiện thủ thuật huy động, bằng cách áp dụng áp lực đường thở cao thoáng qua, nhằm mở lại phổi bị xẹp để tăng số lượng các đơn vị phế nang tham gia trao đổi khí [71].
Một số thủ thuật khác nhau được sử dụng, chẳng hạn như áp dụng áp lực dương liên tục (30 -40 cmH2O) trong 30-40 giây, hoặc tăng PEEP dần dần và giữ áp lực đẩy hằng định hoặc tăng áp lực đẩy dần dần với PEEP hằng định [72, 74]. Các thủ thuật huy động cải thiện quá trình oxygen hóa và độ giãn nở động [75-77]. Bằng cách áp dụng áp lực trong phế nang cao, nó có thể gặp nguy cơ mắc barotrauma liên quan đến sự quá căng của phế nang. Bằng cách tăng áp lực trong lồng ngực, nó có thể làm giảm trở lại tĩnh mạch ngoại biên và tiền tải tâm thất phải, do đó gây ra sự mất ổn định huyết động (đặc biệt ở bệnh nhân giảm thể tích máu) [73].
Các thủ thuật huy động đã được đánh giá trong 8 nghiên cứu ngẫu nhiên có kiểm soát [21, 35, 49, 78-82] trong tổng số 2735 bệnh nhân từ năm 1998 đến 2018. Bản chất của các thủ thuật được sử dụng và áp lực đường thở mục tiêu trong quá trình thủ thuật khác nhau đáng kể học. Bốn trong số 8 nghiên cứu khuyến nghị áp dụng áp lực đường thở dương liên tục là 40 cmH2O trong 40 giây [21, 49, 80, 82]. Bảy trong số 8 nghiên cứu đã kết hợp thủ thuật huy động với việc áp dụng PEEP cao, với mục đích giữ cho phế nang được huy động mở [21, 35, 49, 78-81].
Trong 8 nghiên cứu, việc sử dụng các thủ thuật huy động không có liên quan đáng kể đến việc giảm tỷ lệ tử vong vào ngày 28 (RR = 0,89, 95% CI [0,89-1,07]). Trong nghiên cứu duy nhất không có sự đồng can thiệp, các thủ thuật huy động có liên quan đến giảm tỷ lệ tử vong (110 bệnh nhân, RR = 0,81, 95% CI [0,69-0,95]). Trong mỗi nghiên cứu trong 7 nghiên cứu (2625 bệnh nhân) có tỷ lệ PaO2/FiO2 ở ngày 1, cao hơn đáng kể ở những bệnh nhân được quản lý bằng cách sử dụng một thủ thuật huy động (trung bình của trung bình: 205,9 mmHg so với 158,3 mmHg) [21, 35, 49, 78-81]. Điều này cải thiện PaO2/FiO2 kéo dài đến ngày 77 (trung bình của trung bình: 231,2 mmHg so với 195,1 mmHg) trong cùng 7 nghiên cứu (2625 bệnh nhân) [21, 35, 49, 78-81]. Không có bằng chứng nào cho thấy việc thủ thuật huy động làm tăng nguy cơ mắc barotrauma (RR = 1,25, 95% CI [0,93-1,67]) trong 6 nghiên cứu [21, 35, 49, 78, 80, 81]. Ngược lại, tình trạng huyết động trở nên tồi tệ hơn đáng kể (RR = 1,22, 95% CI [1,04-1,45]) [35, 81].
Vẫn chưa có biện pháp huy động tối ưu đã được chứng minh, đáng chú ý là giảm thiểu nguy cơ huyết động và nguy cơ barotrauma, trong khi vẫn duy trì hiệu quả về mặt oxygen hóa phổi. Một nghiên cứu gần đây [80] mở ra một khả năng mới bằng cách điều chỉnh chỉ định huy động bằng các kết quả quét CT (lan tỏa hoặc khu trú) trong ARDS. Việc tìm kiếm một nhóm đối tượng tốt hơn trong số các bệnh nhân ARDS có thể cung cấp thông tin mới liên quan đến ảnh hưởng của thủ thuật huy động đến tỷ lệ tử vong.
Khu vực 4: Thông khí tự phát
Thuốc chẹn thần kinh cơ sớm và ngắn hạn
R4.1 – Thuốc chẹn thần kinh cơ có lẽ nên được xem xét ở những bệnh nhân ARDS có tỷ lệ PaO2/FiO2 <150 mmHg để giảm tỷ lệ tử vong. Thuốc chẹn thần kinh cơ nên được sử dụng bằng cách tiêm truyền liên tục sớm (trong vòng 48 giờ sau khi bắt đầu ARDS), không quá 48 giờ, với ít nhất là đánh giá hàng ngày.
GRADE 2 +, KHUYẾN NGHỊ MẠNH
Cơ sở lý luận:
Ba thử nghiệm ngẫu nhiên đã thử nghiệm tác dụng của việc bổ sung thuốc chẹn thần kinh cơ đối với an thần sâu ở giai đoạn ban đầu của ARDS [83-85]. Kết quả chính của chỉ một trong những thử nghiệm này là tỷ lệ tử vong [85]. Một thử nghiệm mở ngẫu nhiên (Đánh giá lại về phong tỏa thần kinh cơ sớm [ROSE]) về phương pháp hơi khác nhau hiện đang được phân tích [86]. Nghiên cứu ACURASYS [85] bao gồm 339 bệnh nhân bị ARDS với tiến triển dưới 48 giờ và với tỷ lệ PaO2/FiO2 <150 mmHg, PEEP ≥ 5 cmH2O và thể tích khí lưu thông từ 6-8 mL/kg PBW trong một nghiên cứu đa trung tâm mù đôi, giả dược. Bệnh nhân được đưa vào sau khi tối ưu hóa thở máy xâm lấn. Cisatracurium ambylate là chất ức chế thần kinh được sử dụng. Tỷ lệ tử vong trong 90 ngày không khác nhau giữa bệnh nhân được điều trị bằng cisatracurium và những người được điều trị bằng giả dược (tương ứng 31,6% so với 40,7%; p = 0,08). Tuy nhiên, tỷ lệ nguy hiểm cho tỷ lệ tử vong trong 90 ngày ở nhóm cisatracurium là 0,68 (95% CI 0,48 -0,98; p = 0,04), sau khi điều chỉnh tỷ lệ PaO2/FiO2, áp lực cao nguyên và điểm số APACHE II khi đưa vào [85]. Tỷ lệ sống sót được cải thiện ở những bệnh nhân có tỷ lệ PaO2/FiO2 <120 mmHg. Có nhiều ngày còn sống và ngày không thở máy vào ngày 90 trong nhóm cisatracurium (HR 1.41; p = 0.01), và không có sự khác biệt giữa các nhóm về tỷ lệ liệt cơ mắc phải trong ICU [85].
Oxygen hóa (PaO2/FiO2) tăng khi sử dụng các thuốc chẹn thần kinh cơ ở bệnh nhân ARDS [83, 84, 87, 88].
Trong một nghiên cứu hồi cứu, cisatracurium không vượt trội so với atracurium [89]. Ngược lại, thời gian thở máy và thời gian lưu lại ICU hơi ngắn nhưng ngắn hơn đáng kể ở những bệnh nhân mắc hoặc có nguy cơ mắc ARDS được điều trị bằng cisatracurium, so với những người được điều trị bằng vecuronium [90].
Độ sâu của chẹn thần kinh cơ cần thiết là không rõ. Nghiên cứu ACURASYS sử dụng cisatracurium liều cao (37 mg/giờ) [85].
Các thuốc chẹn thần kinh cơ có thể có tác dụng có lợi trong việc hạn chế các nỗ lực hô hấp và hiệu ứng Pendelluft, và trong việc tăng áp lực xuyên phổi qua đường hô hấp [88].
Thông khí tự phát sớm
R4.2.1 – Dữ liệu có sẵn không cho phép khuyến nghị liên quan đến chiến lược thông khí tự phát thường quy trong giai đoạn cấp tính của ARDS.
KHÔNG KHUYẾN NGHỊ
R4.2.2 – Sau giai đoạn cấp tính của ARDS, các chuyên gia đề xuất rằng thông khí với chế độ áp lực cho phép thông khí tự phát có thể được sử dụng khi đảm bảo rằng thể tích khí lưu thông được tạo ra gần 6 mL/kg PBW và không vượt quá 8 mL/kg PBW.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận:
Thuật ngữ thở tự nhiên dùng để chỉ hoạt động của các cơ hô hấp, chịu trách nhiệm thông khí tự phát (SV) ở bệnh nhân thở máy. Tầm quan trọng của SV phụ thuộc vào cường độ của những nỗ lực hít thở và vào trở kháng của hệ hô hấp [91]. Những nỗ lực hô hấp tự phát có mặt ở hầu hết các bệnh nhân thở máy, ngoại trừ những người được gọi là thở máy có kiểm soát bị liệt cơ và/hoặc an thần sâu. Thở tự nhiên có các trình tự rất khác nhau tùy thuộc vào chế độ thông khí được sử dụng [92]. Trong quá trình thông khí có kiểm soát được hỗ trợ (có thể được bảo đảm áp lực hoặc thể tích), các nỗ lực hô hấp có xu hướng tăng thông khí phút bằng cách kích hoạt máy thở (thông qua bộ kích hoạt hít vào). Trong bối cảnh này, thể tích khí lưu thông có thể làm tổn thương phổi (khái niệm về tổn thương phổi tự gây ra cho bệnh nhân) [93]. Sự tương tác có thể phức tạp hơn và chịu trách nhiệm cho sự không đồng bộ máy thở của bệnh nhân, trong một số trường hợp làm tăng thể tích khí lưu thông và có thể làm xấu đi tiên lượng [94, 95]. Sự không đồng bộ có thể được hạn chế bằng cách điều chỉnh các cài đặt máy thở hoặc bãi bỏ bằng cách sử dụng các biện pháp thuốc chẹn thần kinh cơ.
Với các chế độ thông khí kiểm soát áp lực cụ thể, không cung cấp khả năng đồng bộ hóa hít vào (không có kích hoạt như trong thông khí giải phóng áp lực đường thở hoặc APRV), các nỗ lực hô hấp tạo ra SV, được đặt chồng lên trên các chu kỳ thở máy [91]. Các nỗ lực hô hấp tự phát có tác dụng lành mạnh (cải thiện oxygen hóa, huy động phế nang, phòng ngừa các tổn thương cơ hoành do thông khí), cần được cân bằng với các tác động xấu (tăng áp lực xuyên phổi và thể tích khí lưu thông, tăng áp lực mạch máu trong mô kẽ phổi và nguy cơ phù nề mạch máu) [91]. Cân bằng nguy cơ lợi ích phụ thuộc vào mức độ nghiêm trọng của bệnh hô hấp và mức độ SV [91]. SV trên 30 hoặc 50% tổng thông khí phút có thể có hại. Nếu độ thông khí được xác định bởi cài đặt trên máy thở tăng và/hoặc nếu thuốc an thần quá sâu, SV có xu hướng giảm. Ngược lại, SV tăng nếu cài đặt trên máy thở không đủ và/hoặc nếu thuốc an thần không đủ hoặc trong trường hợp nhiễm toan chuyển hóa [92].
SV có thể được điều chỉnh bằng thuốc an thần và theo mức độ thông khí được cung cấp bởi máy thở.
Thông khí điều khiển áp lực không đồng bộ (như APRV) ủng hộ SV bằng cách hạn chế sự không đồng bộ được quan sát với thông khí hỗ trợ/kiểm soát áp lực hoặc thể tích. SV liên quan đến thông khí kiểm soát áp lực không đồng bộ (như APRV) có liên quan đến tăng nỗ lực hô hấp, có thể được phát hiện bằng các biến thiên của áp lực tắc đường thở.
Tác dụng có lợi của SV đối với oxygen hóa và cơ học hô hấp đã được chứng minh trên các mô hình động vật và được xác nhận bởi các nghiên cứu lâm sàng ở một số ít bệnh nhân. Một nghiên cứu ngẫu nhiên ở một trung tâm so sánh SV ở APRV so với thông khí kiểm soát áp lực (an thần và chẹn thần kinh cơ) ở 30 bệnh nhân được thở máy với đa chấn thương cho thấy tác dụng thuận lợi của SV đối với trao đổi khí, cơ học hô hấp và thời gian thông khí [96]. Chiến lược an thần, sự khác biệt lớn giữa các nhóm về phương thức thông khí và số lượng nhỏ bệnh nhân ngăn cản kết luận được đưa ra liên quan đến lợi ích của SV. Những trở ngại về phương pháp này được tìm thấy trong hầu hết các nghiên cứu đánh giá lợi ích của SV.
Trong một thử nghiệm ngẫu nhiên ở một trung tâm gần đây ở 138 bệnh nhân được thở máy trong ít nhất 48 giờ với tỷ lệ PaO2/FiO2 <250 mmHg, chiến lược thông khí bảo vệ (PBW 6 ml/kg, áp lực cao nguyên <30 cmH2O, PEEP được hướng dẫn bởi Bảng PEEP-FiO2 theo Giao thức ARDS-Net) được so sánh với APRV (khí lưu thông 6 ml/kg PBW, áp lực cao nguyên <30 cmH2O, PEEP 5 cmH2O) được thiết kế để khuyến khích SV [97]. Chiến lược an thần là phổ biến cho hai nhánh nghiên cứu. Số ngày không thông khí vào ngày 28 (điểm cuối chính) lớn hơn đáng kể ở nhánh APRV. Tương tự như vậy, các thông số độ giãn nở và oxygen hóa đã được cải thiện đáng kể trong APRV, trong khi có yêu cầu an thần ít hơn [97]. Thể tích khí lưu thông và áp lực đẩy tương đương nhau ở hai nhánh, trong khi PEEP và áp lực cao nguyên thấp hơn đáng kể trong APRV [97]. Những hạn chế chính của nghiên cứu này là nó là nghiên cứu một trung tâm duy nhất, có rất ít bệnh nhân và kinh nghiệm của các nhà trị liệu hô hấp đã điều chỉnh các thiết lập APRV, rất khó để làm chủ [97]. Tuy nhiên, nghiên cứu này cho thấy tính khả thi của một chiến lược được thiết kế để đạt được mức độ điều chỉnh của SV (khoảng 30% thông khí phút). Các biến chứng không thường xuyên hơn ở nhánh APRV, trong đó tỷ lệ tràn khí màng phổi thấp (4.2%) [97].
Một chế độ không đồng bộ (như APRV) đã được kết hợp (nghiên cứu sinh lý ngẫu nhiên chéo) với thông khí được kiểm soát áp lực hoàn toàn hoặc một phần [98]. Thể tích khí lưu thông và áp lực xuyên phổi thấp hơn đáng kể trong nhóm không đồng bộ, trong khi SV có liên quan đến nỗ lực hô hấp tăng, có thể được phát hiện bằng cách theo dõi áp lực tắc đường thở [98].
Một thử nghiệm đa trung tâm ngẫu nhiên, có kiểm soát đã kết hợp với tác động của thông khí khuyến khích một cách có hệ thống SV với thông khí kiểm soát/hỗ trợ, cho một chiến lược nhất định trong cài đặt thể tích khí lưu thông, áp lực hít vào, PEEP, an thần, cai PEEP và cai máy giúp thở. Thử nghiệm này (BiRDS) đã kết thúc sau khi thu nhận 700 bệnh nhân và kết quả đang chờ xử lý (www.clinicaltrials.gov/ NCT01862016). Nghiên cứu trước đây cho phép điều chỉnh mức độ an thần và thông khí để đạt được mục tiêu của SV.
Khu vực 5: Tư thế nằm sấp
R5.1 – Nên sử dụng tư thế nằm sấp ở bệnh nhân ARDS với tỷ lệ PaO2/FiO2 <150 mmHg để giảm tỷ lệ tử vong. Các phiên ít nhất 16 giờ liên tục nên được thực hiện.
GRADE 1 +, KHUYẾN NGHỊ MẠNH
Cơ sở lý luận:
Việc sử dụng tư thế nằm sấp ảnh hưởng (PP) trong ARDS đã được nghiên cứu trong 8 thử nghiệm ngẫu nhiên có đối chứng, 5 trong số đó là lớn [10, 45, 99-101] và 3 nhỏ hơn [102-104]. Phân tích tổng hợp gần đây nhất đã kết luận rằng không có sự khác biệt có ý nghĩa thống kê về tỷ lệ tử vong giữa nhóm PP và nhóm nằm ngửa [105]. Phân tích tổng hợp này bao gồm 3 phân tích độ nhạy về vai trò của thông khí bảo vệ, thời gian điều trị PP và mức độ nghiêm trọng của thiếu oxy máu tại thời điểm đưa vào. Khi giao thức thử nghiệm được cung cấp cho thông khí cơ học bảo vệ, đã giảm đáng kể tỷ lệ tử vong có lợi cho PP [105]. Việc giảm tỷ lệ tử vong này có ý nghĩa đối với PP kéo dài hơn 12 giờ, nhưng nó không dành cho các phiên PP ngắn hơn [105]. Việc giảm tỷ lệ tử vong có lợi cho PP rất có ý nghĩa đối với hầu hết bệnh nhân thiếu oxy bị ARDS trung bình đến nặng, nhưng không đáng kể đối với bệnh nhân ít thiếu oxy máu (ARDS nhẹ).
Nghiên cứu PROSEVA [10] được thực hiện ở 27 đơn vị chăm sóc đặc biệt cho thấy giảm đáng kể tỷ lệ tử vong ở bệnh nhân ARDS bao gồm sau thời gian ổn định 12 đến 24 giờ với tỷ lệ PaO2/FiO2 <150 mmHg liên quan đến PEEP ít nhất 5 cmH2O, FiO2 ít nhất 60% và thể tích khí lưu thông 6 ml/kg PBW. Điều này đã xác nhận một phân tích tổng hợp ưu tiên trên dữ liệu cá nhân [106]. Trong nhóm PP thử nghiệm PRO- SEVA, bệnh nhân có trung bình 4 phiên PP trong 17 giờ liên tục (giao thức lên kế hoạch các phiên ít nhất 16 giờ). PP được tiếp tục ngay cả khi không cải thiện oxygen hóa.
PP là không tốn kém và đơn giản để thực hiện. Tối ưu hóa sự an toàn của PP đòi hỏi mỗi bộ phận phải có quy trình bằng văn bản và đào tạo cụ thể các đội điều dưỡng.
Khu vực 6: Trao đổi khí ngoài cơ thể
Oxygen hóa qua màng ngoài cơ thể tĩnh mạch – tĩnh mạch
R6.1 Việc quản lý ARDS bao gồm PEEP cao, các thuốc chẹn thần kinh cơ và tư thế nằm sấp. Quyết định sử dụng ECMO cần được đánh giá sớm bằng cách liên hệ với một trung tâm chuyên gia.
GRADE 2 +, KHUYẾN NGHỊ MẠNH
Cơ sở lý luận:
Một số nghiên cứu đã đánh giá hiệu quả của ECMO trong ARDS. Thử nghiệm CESAR đa trung tâm [107] đã chọn ngẫu nhiên 180 bệnh nhân để chuyển đến trung tâm ECMO để xem xét cho ECMO hoặc hỗ trợ thở máy thông thường. Kết cục chính của tử vong và/hoặc tàn tật nặng sau 6 tháng ít gặp hơn ở nhóm ECMO, nhưng sự giải thích của nó bị giới hạn bởi một số lượng lớn bệnh nhân nhóm chứng không được thở máy bảo vệ và thực tế là 25% trong số các bệnh nhân được chọn ngẫu nhiên để chuyển và xem xét cho nhóm ECMO không thực sự nhận được ECMO [107].
Hai nghiên cứu kiểm soát trường hợp hồi cứu sử dụng kết hợp điểm số xu hướng [108, 109] cho thấy lợi ích của việc chuyển bệnh nhân mắc ARDS liên quan đến A (H1N1) trong đại dịch cúm năm 2009 đến trung tâm giới thiệu ECMO chuyên sâu.
Thử nghiệm ngẫu nhiên EOLIA [110] đã đánh giá hiệu quả của việc bắt đầu sớm ECMO tĩnh mạch trong ARDS nặng trong khi tránh các sai lệch về phương pháp của CESAR. Thử nghiệm đa trung tâm này bao gồm 249 bệnh nhân bị ARDS nặng khi thở máy dưới 7 ngày. Bệnh nhân được chọn ngẫu nhiên vào nhóm ECMO sớm đã được đặt ống thông tĩnh mạch – tĩnh mạch qua da ngay lập tức, trong khi bệnh nhân nhóm đối chứng được điều trị bằng thở máy giao thức. Khi đưa vào, tỷ lệ PaO2/FiO2 trung bình là 72, điểm SOFA là trên 10 và 75% bệnh nhân được dùng thuốc vận mạch [110]. Cần lưu ý rằng tất cả các bệnh nhân trong nhóm đối chứng đều nhận được các thuốc chẹn thần kinh cơ và 90% trong số họ có các phiên điều trị PP kéo dài. Tỷ lệ tử vong trong sáu mươi ngày trong nhóm ECMO thấp hơn 11% (35% so với 46%), mặc dù sự khác biệt không đạt được ý nghĩa thống kê (p = 0,09) [110]. Ngược lại, nguy cơ thất bại điều trị ở ngày 90 (tử vong ở nhóm ECMO, tử vong hoặc chéo đối với ECMO trong nhóm đối chứng) cao hơn đáng kể ở nhóm đối chứng [110]. Các biến chứng liên quan đến ECMO không thường xuyên và ít trường hợp đột quỵ được quan sát thấy trong nhóm ECMO. Cứu hộ ECMO đã được sử dụng ở 28% bệnh nhân đối chứng do thiếu oxy kháng trị [110]. Những bệnh nhân này bị bệnh nặng và tình trạng lâm sàng của họ xấu đi nhanh chóng trong vài giờ trước khi bắt đầu sử dụng ECMO. Tỷ lệ tử vong của họ là 57% và 6 ECMO tĩnh mạch – động mạch cần thiết trong khi tiến hành hồi sức tim phổi [110].
Mặc dù phân tích thường quy của nghiên cứu này là âm tính – theo nghĩa thống kê chặt chẽ (tỷ lệ tử vong trong 60 ngày, 35% so với 46%, p = 0,09), một phân tích post-hoc Bayes về EOLIA [111] với nhiều giả định khác nhau về niềm tin và hiểu biết về hiệu quả của ECMO trong ARDS đã cho thấy rằng xác suất sau giảm tử vong với ECMO như trong thử nghiệm EOLIA, là rất cao (từ 88 đến 99%). Hơn nữa, thử nghiệm EOLIA cho thấy ECMO an toàn khi được cung cấp tại các trung tâm chuyên gia có số lượng bệnh nhân lớn [110]. Nó cho phép ứng dụng thông khí bảo vệ cực kỳ trong đó áp lực và thể tích do máy thở được tạo ra giảm đáng kể, do đó bảo vệ phổi khỏi tổn thương phổi do thông khí hơn. Thử nghiệm EOLIA cũng đã chứng minh sự liên quan và hiệu quả của mạng lưới bệnh viện để truy xuất an toàn trên ECMO những bệnh nhân bị bệnh nặng nhất 24/7 với nhóm di động ECMO đến trung tâm giới thiệu ECMO [110].
Loại bỏ CO2 ngoài cơ thể lưu lượng thấp
R6.2 – Dữ liệu có sẵn không cho phép khuyến nghị được thực hiện liên quan đến việc sử dụng loại bỏ CO2 ngoài cơ thể lưu lượng thấp trong ARDS.
KHÔNG KHUYẾN NGHỊ
Cơ sở lý luận:
Loại bỏ CO2 ngoài cơ thể lưu lượng thấp hoặc tĩnh mạch (ECCO2R) cho phép cái gọi là chiến lược thông khí siêu bảo vệ (thể tích khí lưu thông < 6 mL/kg PBW và giảm áp lực và tần số hô hấp) trong ARDS, bằng cách kiểm soát tăng CO2 máu gây ra bởi sự giảm thông khí phút. Mười nghiên cứu đã thử nghiệm phương pháp này [112-121], nhưng mức độ chứng cứ tổng thể là rất thấp. Trong thử nghiệm ngẫu nhiên có kiểm soát gần đây bao gồm 79 bệnh nhân, số ngày không dùng máy thở ở ngày 60 không khác nhau giữa các nhóm đối chứng và ECCO2R, mặc dù phân tích post hoc cho thấy lợi ích của ECCO2R đối với bệnh nhân thiếu oxy nhất (PaO2/FiO2 <150 mmHg khi đưa vào) [113].
Các nghiên cứu quan sát cho thấy rằng tăng CO2 máu có tác dụng tiên lượng không thuận lợi trong ARDS; nó được kết hợp trong phân tích đa biến với rối loạn mạch máu phổi và chức năng tâm thất phải [36] và với tử vong [19]. ECCO2R có thể làm giảm PaCO2 ở bệnh nhân ARDS tăng CO2 máu nhận thông khí bảo vệ thông thường (thể tích khí lưu thông khoảng 6 mL/kg PBW) [112, 115, 116, 122-124] hoặc thông khí siêu bảo vệ [117, 120]. Tuy nhiên, tác dụng tích cực của việc kiểm soát chứng tăng CO2 máu đối với tỷ lệ mắc bệnh và tử vong vẫn chưa được chứng minh trong ARDS.
Tác dụng của ECCO2R đối với PaO2 ở bệnh nhân ARDS là không đáng kể, một số nghiên cứu báo cáo sự cải thiện [119-122] và nhiều nghiên cứu khác không có tác dụng đáng kể [112, 114, 115, 117, 118, 124, 125]. Bởi vì ECCO2R chỉ hỗ trợ cải thiện oxy máu cận biên, ECMO tĩnh mạch – tĩnh mạch là cần thiết ở những bệnh nhân thiếu oxy nhất. Cuối cùng, ECCO2R có liên quan đến một loạt các biến chứng (chảy máu, huyết khối và nhiễm trùng) cần được cân bằng với các lợi ích tiềm năng của nó [126].
Khu vực 7: Nitric oxide dạng hít
R7.1 – Các chuyên gia đề xuất rằng oxit nitric dạng hít có thể được sử dụng trong trường hợp ARDS bị thiếu oxy máu nặng mặc dù đã thực hiện chiến lược thông khí tiên tiến và tư thế nằm sấp, và trước khi dự tính sử dụng ECMO tĩnh mạch.
Ý KIẾN CHUYÊN GIA
Cơ sở lý luận:
Ban đầu được coi là một chất gây ô nhiễm, oxit nitric (NO) là một loại khí phổ biến, không mùi và không màu, có tính chất được chứng minh bởi Furchgott, Ignarro, Murad và Moncada với công việc này họ được trao giải thưởng Nobel [127]. Được sản xuất bởi các tế bào nội mô, NO gây ra sự giãn nở bằng cách tăng mức độ chu kỳ của GMP trong các tế bào cơ trơn. Tùy thuộc vào nồng độ của nó, NO, ngoài các đặc tính vận mạch của nó, tạo ra nhiều tác dụng chống viêm hoặc kích thích tiềm năng thú vị trong môi trường ARDS [128]. Đáng chú ý, nó làm giảm kích hoạt bạch cầu và phản ứng viêm, giảm kết tập tiểu cầu, có tác dụng giãn phế quản và tạo điều kiện cho việc sản xuất chất hoạt động bề mặt.
Khi hít vào, NO khuếch tán vào các khu vực thông khí nơi nó gây giãn mạch trước khi liên kết nhanh với hemoglobin bằng phản ứng với ion sắt và sắt (ferrous and ferric) của heme để tạo thành hemoglobin nitrosyl hóa [128]. Bằng cách phản ứng với oxyhemoglobin, dạng chiếm ưu thế trong phổi, NO tạo thành methemoglobin và nitrat và không dẫn đến giãn mạch toàn thân. Khoảng 70% NO hít (iNO) được loại bỏ dưới dạng nitrat trong nước tiểu [129]. iNO là thuốc giãn mạch máu phổi chọn lọc có khả năng cải thiện trao đổi khí bằng cách giảm shunt và kiểm soát tăng áp động mạch phổi và suy tâm thất phải, có tiên lượng không đáng kể trong ARDS [130, 131]. Ngoài ra, tác dụng của nó đối với tiểu cầu và bạch cầu có thể chứng minh giá trị điều trị trong ARDS.
Hít NO làm giãn các mạch phổi ở các khu vực được thông khí và cải thiện tỷ lệ thông khí- tưới máu bằng cách ưu tiên phân phối lại lưu lượng máu đến các khu vực này. Mười một thử nghiệm ngẫu nhiên báo cáo sự cải thiện tỷ lệ PaO2/FiO2 sau 24 giờ điều trị [132]. Tuy nhiên, sự cải thiện này là nhất thời và chỉ có một nghiên cứu dựa trên 4 thử nghiệm cho thấy sự cải thiện vẫn tồn tại sau 96 giờ điều trị [132]. Lưu ý rằng đáp ứng sẽ lớn hơn nếu có tăng áp động mạch phổi, nồng độ có khả năng cải thiện oxygen hóa thường dưới 5 phần triệu (ppm) [133], và nồng độ trên 10 ppm đôi khi có liên quan đến việc làm xấu đi tỷ lệ PaO2/FiO2, có thể là do sự khuếch tán NO vào các khu vực không được thông khí [134].
Cho đến nay, 8 nghiên cứu ngẫu nhiên trong tổng số 1025 người trưởng thành mắc ARDS, trong đó có ít nhất 10 nghiên cứu được điều trị bằng iNO, đã đánh giá tác động của điều trị này đến tỷ lệ tử vong [133, 135-140]. Không có nghiên cứu nào trong số này tìm thấy sự cải thiện đáng kể về khả năng sống sót sau 28 ngày hoặc dài hạn. Các phân tích của các nghiên cứu ngẫu nhiên có sẵn cho thấy iNO không thay đổi thời gian thở máy, thời gian chăm sóc đặc biệt hoặc khởi phát các biến chứng barotrauma. Được công bố từ năm 1997 đến 2004, hầu hết các nghiên cứu này đều có nguy cơ sai lệch tương đối khiêm tốn, nhưng chúng phải chịu một số vấn đề về phương pháp nhất định làm phức tạp việc giải thích. Hầu hết các nghiên cứu này thiếu sức mạnh và đánh giá đáp ứng của bệnh nhân dị hợp về mặt nguyên nhân của ARDS. Các phương thức quản trị (nồng độ, thời gian, cách đánh giá đáp ứng, cai NO) và kiểm tra không được xác định đầy đủ và thay đổi rất nhiều từ nghiên cứu này sang nghiên cứu khác. Ngoài ra, những nghiên cứu này đã được tiến hành trước khi khái quát hóa các cấu trúc thông khí bảo vệ cho ARDS. Trong nghiên cứu gần đây nhất, ở 385 bệnh nhân, thể tích khí lưu thông được sử dụng trong 2 nhóm là 10 mL/kg [139]. Độ giãn nở chiến lược thông khí bảo vệ không được báo cáo trong bất kỳ nghiên cứu nào và không có quy trình cai thông khí cơ học hoặc tối ưu hóa thuốc an thần trong các nghiên cứu này. Do đó, rất khó để đưa ra kết luận dứt khoát về bất kỳ lợi ích nào của iNO trong ARDS.
Với tỷ lệ lợi ích-nguy cơ khá thuận lợi, các tác động sinh lý của iNO đối với việc giảm shunt trong phổi và cải thiện trao đổi khí, hoạt động của tâm thất phải và lưu lượng tim có thể giúp sử dụng NO trong ARDS nghiêm trọng khi đã thực hiện nằm sấp và tối ưu hóa thở máy mà vẫn không điều chỉnh được thiếu oxy. Dữ liệu từ các nghiên cứu sinh lý và các thử nghiệm lâm sàng chính cho thấy iNO có hồ sơ an toàn tốt và các tác dụng phụ tiềm ẩn của nó, đáng chú ý là methemoglobinemia, ức chế kết tập tiểu cầu và giãn mạch toàn thân, không có ý nghĩa trên lâm sàng nếu quan sát thấy một vài biện pháp phòng ngừa [135, 141-143]. Với sự hiện diện của oxy, NO được chuyển thành nitrite (NO2) và sau đó là nitrat (NO3). Tuy nhiên, nếu hít phải FiO2 cao, NO cùng với các loại oxy phản ứng có thể tạo thành các phân tử có khả năng gây độc, đặc biệt là peroxynitrite (ONOO−) [141]. NO cũng có thể liên kết với các axit amin như tyrosine và thay đổi posttranslational trong protein, chẳng hạn như ni-tơ hóa, nitrosyl hóa và nitrat hóa. Hơn nữa, nguy cơ nhiễm độc thận đã được mô tả trong một thử nghiệm lâm sàng [136] và trong một phân tích tổng hợp gần đây [132]. Một tổng quan hệ thống các thử nghiệm cho thấy nguy cơ nhiễm độc thận dường như chỉ giới hạn ở những bệnh nhân ARDS tiếp xúc với nồng độ iNO cao trong thời gian dài [144].
Để hạn chế nguy cơ biến chứng với iNO, cách phù hợp là: (1) giảm thiểu phơi nhiễm bằng cách sử dụng các hệ thống quản lý cho phép hít vào đồng bộ với lưu lượng hít vào và theo dõi trước nồng độ NO và NOx, (2) sử dụng tối thiểu nồng độ hiệu quả để cải thiện tỷ lệ PaO2/FiO2 và không duy trì iNO ở bệnh nhân không đáp ứng, (3) đánh giá lại đáp ứng và liều lượng cần thiết hàng ngày. Trong những trường hợp sử dụng kéo dài, cũng cần theo dõi tình trạng nhiễm trùng huyết. Cuối cùng, việc cai iNO nên được tư từ để hạn chế nguy cơ tăng áp lực động mạch phổi đột ngột.





