Thuốc Giảm Đau: Tác dụng, Nguyên tắc sử dụng, Lưu ý tác dụng phụ

Đau là một cảm giác rất khó chịu, có tính chất cảm tính, đi kèm với đó là những tổn thương có thật hoặc tiềm tàng của các tổ chức, hoặc được mô tả là có những tổn thương trước đó. Có rất nhiều mức độ đau khác nhau như đau do bong gân, đau do gãy xương, đau do ung thư giai đoạn xâm lấn. Bên cạnh đó cũng có rất nhiều thuốc giảm đau mức độ khác nhau. Ví dụ: Dùng NSAIDs để điều trị các cơn đau nhẹ, dùng Opioid để kiểm soát cơn đau nặng. Bài viết dưới đây Heal Central xin chia sẻ tới các bạn đọc tổng quan về các thuốc giảm đau cùng với nguyên tắc sử dụng chúng trong thực hành lâm sàng.
Thuốc giảm đau là gì?
Thuốc giảm đau là các thuốc có tác dụng giảm cảm giác đau, theo các cơ chế tác dụng khác nhau.
Thuốc giảm đau có số lượng rất lớn và được sử dụng nhiều trên lâm sàng, trong đó quan trọng nhất và cũng là phổ biến nhất là 2 nhóm thuốc:
Paracetamol (Acetaminophen) và các thuốc chống viêm không steroid (NSAIDs): Các thuốc này chủ yếu dùng cho đau ngoại vi. Một số thuốc trong nhóm này có thể mua mà không cần đơn của bác sĩ (OTC). Ví dụ: Ibuprofen, Naproxen, Indomethacin, Aspirin, Diclofenac, Sulindac, Meloxicam, Piroxicam, Celecoxib.
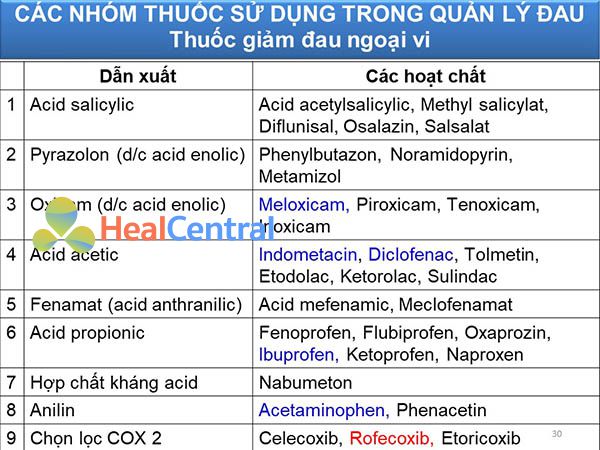
Các thuốc giảm đau opioid: Các thuốc nhóm này dùng chủ yếu cho đau nội tạng, các loại đau mà nhóm thuốc trên không đáp ứng được. Còn được gọi là thuốc giảm đau trung ương. Các thuốc nhóm này được Nhà nước quản lý rất chặt chẽ và không thể mua dễ dàng được. Ví dụ: Tramadol, Codeine, Morphine, Pethidine, Methadone, Fentanyl.
Tại sao thuốc giảm đau lại quan trọng?
Đau là một triệu chứng khó chịu. Nhiều người, đặc biệt là người già, trẻ em và một số đối tượng nhạy cảm khác, họ chịu đau kém hơn người trưởng thành khỏe mạnh. Hầu như không có ai thích cảm giác đau. Nếu quá đau đớn, bệnh nhân có thể bị sốc. Một số trường hợp bệnh lý thì lại làm cho bệnh nhân đau đớn liên tục (ví dụ như ung thư), làm giảm chất lượng cuộc sống. Vì vậy thuốc giảm đau thực sự rất quan trọng.
Vấn đề nổi cộm hiện nay là sự lạm dụng nhiều thuốc giảm đau trên lâm sàng, đến từ cả phía bác sĩ cũng như bệnh nhân. Đặc biệt các thuốc giảm đau ngoại vi bị lạm dụng rất nhiều, cùng với kháng sinh và các corticoid. Vì vậy chúng ta thực sự cần một cơ chế pháp lý tốt hơn để quản lý việc sử dụng các loại thuốc giảm đau này.
Các nhóm thuốc giảm đau trên lâm sàng
Paracetamol (Acetaminophen)
Paracetamol, hay còn gọi là Acetaminophen, là một thuốc giảm đau ngoại vi kinh điển và có vô số biệt dược chứa Paracetamol trên thị trường. Nó phổ biến đến nỗi không rõ biệt dược gốc của nó là thuốc nào. Các biệt dược có thể kể đến chứa Paracetamol trên thị trường Việt Nam bao gồm Panadol, Panadol cảm cúm, Tiffy, Efferalgan, Ultracet.
Paracetamol mặc dù là một thuốc giảm đau ngoại vi và cũng không có cấu trúc steroid, nhưng nó không được xếp vào nhóm các NSAIDs vì thuốc này không có tác dụng chống viêm, nó chỉ có tác dụng hạ sốt và giảm đau.
Paracetamol được chỉ định cho các trường hợp đau nhẹ đến trung bình: Đau răng, đau họng, đau cơ – xương – khớp, đau đầu, đau nửa đầu, đau bụng, sốt, cảm cúm, cảm lạnh. Paracetamol có thể phối hợp với nhiều dược chất khác như Dextromethorphan, Codeine, Loratadine, Ephedrine, Pseudoephedrine.
Paracetamol nhìn chung là một thuốc an toàn và lành tính, có thể sử dụng cho nhiều đối tượng, ít tác dụng phụ, không gây loét dạ dày như các thuốc NSAIDs, không ảnh hưởng đến chức năng thận, không ảnh hưởng đến khả năng kết tập tiểu cầu.
Quá liều Paracetamol có thể gây viêm gan tối cấp và suy gan, có thể dẫn đến tử vong. Đã có những trường hợp tự tử bằng Paracetamol. Giải độc đặc hiệu ngộ độc Paracetamol bằng N-acetylcystein, một loại thuốc long đờm. Thông thường liều dùng Paracetamol là 10-15 mg/kg cân nặng. Nếu làm tròn tính cho người trưởng thành thì là khoảng 500-1000 mg/lần, mỗi lần dùng cách nhau 4-6 giờ, tối đa 4000 mg/ngày. Tuy nhiên mức liều này cũng rất tương đối, có những trường hợp uống vượt quá mức liều tối đa nhiều lần mà không gặp phải vấn đề gì. Nguyên nhân được cho là do đáp ứng khác nhau giữa các cá thể.
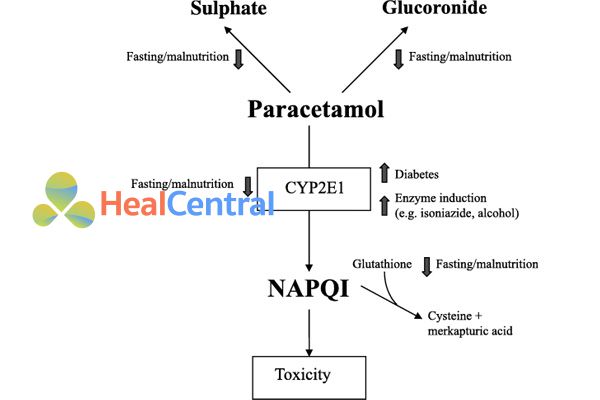
Bình thường ở gan, Paracetamol sẽ được chuyển hóa theo 2 con đường chính là liên hợp glucuronide và liên hợp sulfate làm mất hoạt tính của thuốc, ngoài ra sẽ có một phần nhỏ thuốc được chuyển hóa theo con đường CYP2E1 tạo ra NAPQI (N-acetyl-p-benzoquinone imine), đây là một chất độc với tế bào gan và nhanh chóng được bất hoạt bằng glutathione. Khi quá liều Paracetamol, lượng NAPQI tạo ra quá nhiều, nguồn glutathione nội sinh để bất hoạt NAPQI không đủ, dẫn đến lượng NAPQI tăng cao và gây hoại tử tế bào gan, gây ra viêm gan tối cấp và suy gan.
N-acetylcystein sẽ cung cấp nhóm –SH (thiol, sulfhydryl) tự do để làm nguyên liệu tổng hợp thêm glutathione, từ đó giúp giảm lượng NAPQI trong tế bào gan. Các phân tử N-acetylcystein cũng có thể trực tiếp làm bất hoạt tế bào gan nhờ nhóm –SH tự do này.
Thuốc chống viêm không steroid (NSAIDs)
Đây là một nhóm thuốc rộng lớn với vô số thuốc đã được tiếp thị trên thị trường, nhưng cũng đã có những thuốc phải rút khỏi thị trường. Các thuốc nhóm này đều tựu chung lại có 4 tác dụng như sau:
- Hạ sốt.
- Giảm đau.
- Chống viêm.
- Ức chế kết tập tiểu cầu.
Cơ chế tác dụng của nhóm các thuốc này liên quan đến sự ức chế một enzyme có tên là cyclooxygenase (COX), bao gồm 2 đồng phân là COX-1 và COX-2 (Paracetamol ức chế 2 enzyme này ở ngoại vi rất yếu nên không gây ra tác dụng chống viêm). COX-1 còn được gọi là COX sinh lý, đóng góp nhiều vai trò quan trọng trong sinh lý bình thường của cơ thể. COX-2 còn được gọi là COX bệnh lý, thường tìm thấy ở các ổ viêm (nó cũng chịu một trách nhiệm nhỏ trong các quá trình sinh lý bình thường). Các thuốc của chúng ta đều ức chế cả 2 enzyme này, điều quan trọng chỉ là chúng ức chế enzyme nào nhiều hơn.
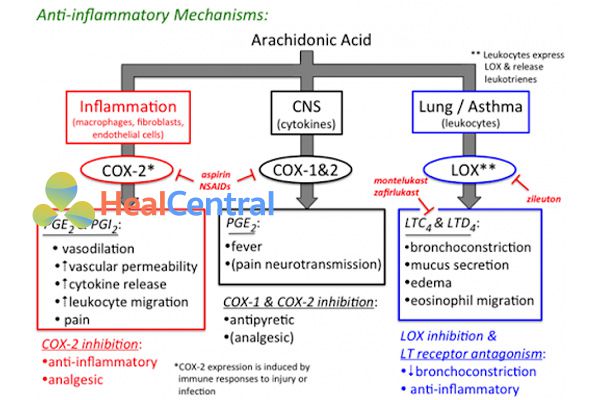
NSAIDs ức chế 2 enzyme là COX-1 và COX-2, từ đó làm giảm tổng hợp cả các prostaglandin sinh lý cũng như bệnh lý. Giảm tổng hợp prostaglandin bệnh lý làm giảm đáp ứng viêm, giảm đau do viêm.
Ta có thể phân chia NSAIDs ra làm 2 nhóm dựa trên mức độ ức chế chọn lọc COX:
- Ức chế COX không chọn lọc: Đa số các NSAIDs rơi vào nhóm này, ví dụ như Ibuprofen, Naproxen, Aspirin, Diclofenac…
- Ức chế chọn lọc COX-2: Celecoxib, Piroxicam và Meloxicam liều thấp (liều cao không còn ức chế ưu tiên COX-2 nữa).
Do các NSAIDs giảm chuyển acid arachidonic theo con đường COX nên nó được tăng cường đi vào theo con đường LOX (lipoxygenase), làm tăng tổng hợp leukotriene gây co thắt cơ trơn khí phế quản, có thể gây nên cơn hen giả. Do đó chống chỉ định sử dụng NSAIDs cho những bệnh nhân bị hen phế quản.
Các chỉ định của NSAIDs bao gồm các trường hợp đau từ nhẹ đến trung bình: Sốt, đau răng, đau cơ – xương – khớp, đau do chấn thương, đau bụng, đau đầu và đau nửa đầu, đau bụng kinh, sốt, cảm lạnh, cảm cúm.
Aspirin là một thuốc rất đặc biệt trong nhóm này, nó được sử dụng chủ yếu cho chỉ định dự phòng huyết khối động mạch nguyên phát hoặc thứ phát do có tác dụng chống kết tập tiểu cầu. Mặc dù các NSAIDs không chọn lọc COX khác cũng có tác dụng chống kết tập tiểu cầu, nhưng các tác dụng của các NSAIDs khác là do ức chế COX-1 có hồi phục, còn Aspirin thì ức chế COX-1 không hồi phục (do acetyl hóa enzyme), do đó nó mới được lựa chọn cho chỉ định này chứ không phải là các NSAIDs khác.
Các NSAIDs đều có tác dụng không mong muốn trên đường tiêu hóa rất nổi bật, đó là gây loét dạ dày – tá tràng. Cơ chế chính là do NSAIDs ức chế COX-1 ở dạ dày làm giảm tổng hợp prostaglandin sinh lý, làm giảm yếu tố bảo vệ dạ dày. Ngoài ra, cơ chế phụ là do các NSAIDs đều có bản chất là acid yếu, do đó khi uống gây kích ứng dạ dày. Các biện pháp khắc phục bao gồm: Dùng dạng giải phóng đặc biệt (viên bao tan trong ruột), dùng thêm các thuốc bảo vệ niêm mạc dạ dày (Misoprostol, Sucralfate) hoặc thuốc làm giảm yếu tố tấn công (thuốc kháng histamine H2 như Cimetidine, Ranitidine, Famotidine và Nizatidine; thuốc ức chế bơm proton như Omeprazole, Lansoprazole, Rabeprazole, Pantoprazole, Esomeprazole và Dexlansoprazole).
Thuốc ức chế COX-2 chọn lọc (Celecoxib) cho thấy tác dụng không mong muốn trên đường tiêu hóa giảm đi, nhưng tác dụng không mong muốn trên tim mạch lại tăng lên so với các thuốc ức chế COX không chọn lọc. Nguyên nhân là do bình thường sự ức chế COX-1 gây ức chế kết tập tiểu cầu (do ức chế thromboxan synthase tiểu cầu), còn ức chế COX-2 gây ức chế tổng hợp prostacyclin nội mạc mạch máu (hay prostaglandin I2, viết tắt PGI2), đây là yếu tố ức chế kết tập tiểu cầu. Do vậy khi ức chế cả 2 enzyme COX thì NSAIDs vẫn có tác dụng ức chế kết tập tiểu cầu, nhưng khi ức chế chọn lọc COX-2 thì thromboxan synthase không được ức chế đáng kể, trong khi PGI2 thì bị ức chế nhiều, do vậy Celecoxib làm tăng nguy cơ gây kết tập tiểu cầu, làm tăng nguy cơ các biến cố trên tim mạch.
Một tác dụng không mong muốn khác của các NSAIDs là trên thận. Các NSAIDs đều ức chế COX nên ức chế sự hình thành prostaglandin sinh lý ở tiểu động mạch đến, làm co tiểu động mạch đến, dẫn đến giảm mức lọc cầu thận và có thể gây suy thận.
NSAIDs cũng có thể liên quan đến một số tình trạng nghiêm trọng như hội chứng Stevens-Johnson, hội chứng Lyell, viêm da tróc vảy… nhưng tỷ lệ hiếm.
Thuốc giảm đau opioid
Các thuốc giảm đau nhóm này đều là các thuốc giảm đau trung ương, có tác dụng mạnh và giảm đau sâu trong nội tạng. Về cấu trúc, các thuốc đều có liên quan cấu trúc với Morphine, một loại thuốc giảm đau opioid nổi tiếng được chiết xuất từ nhựa cây thuốc phiện Papaver somniferum. Người ta có thể sử dụng trực tiếp Morphine làm thuốc giảm đau, hoặc dùng nó để bán tổng hợp ra Codeine là một thuốc giảm đau yếu hơn, đồng thời giảm ho, hoặc tổng hợp toàn phần các thuốc nhóm này dựa trên cấu trúc khung cơ bản tương tự Morphine, như Methadone, Pethidine, hay Fentanyl.
Từ “opioid” dùng để mô tả tất cả các thuốc có cơ chế tác dụng thông qua receptor opioid. Trong khi đó, từ “opiate” được sử dụng để mô tả các alkaloid có cấu trúc tự nhiên: Morphine, Codeine, Thebaine và Papaverine.
Trong phần này chúng ta sẽ nói trọng tâm chỉ về các thuốc opioid được sử dụng chủ yếu với tác dụng giảm đau mà không nói chi tiết đến các opioid đặc biệt khác (ví dụ như một số thuốc đối kháng receptor opioid như Naloxone hay Naltrexone).
Nhìn chung, các thuốc giảm đau opioid đều là thuốc chủ vận receptor opioid. Các receptor này trong cơ thể được biết đến nhiều nhất là 3 loại: µ, δ và κ. Trong đó receptor µ chịu trách nhiệm quan trọng nhất trong tác dụng giảm đau của các opioid. Nếu chia ra cụ thể hơn, chúng gồm các phân nhóm µ1 và µ2, δ1 và δ2, κ1, κ2 và κ3.
Bình thường trong cơ thể con người cũng tồn tại các peptide opioid nội sinh là endorphin, pentapeptide enkephalin và dynorphin. Các opioid nội sinh này cũng tác động thông qua các receptor opioid nhưng với các mức độ khác nhau. Nếu sắp xếp theo ái lực với các receptor opioid, ta có thể chia như sau: Ái lực trên receptor µ endorphin > enkephalin > dynorphin, δ thì enkephalin > endorphin và dynorphin và κ thì dynorphin >> endorphin và enkephalin. Các thuốc giảm đau trung ương opioid của chúng ta về thực chất cũng đem lại các tác dụng tương tự như các opioid nội sinh thông qua chủ vận thụ thể opioid.
Về cơ chế tác dụng, các thuốc chủ vận opioid này giúp giảm đau thông qua liên kết với thụ thể protein cặp đôi G đặc hiệu (GPCRs) nằm trong một số khu vực trên não và tủy sống, đóng vai trò truyền tín hiệu và điều hòa cảm giác đau. Một số tác dụng có thể là qua trung gian thụ thể opioid trên đầu dây thần kinh cảm giác ngoại biên.
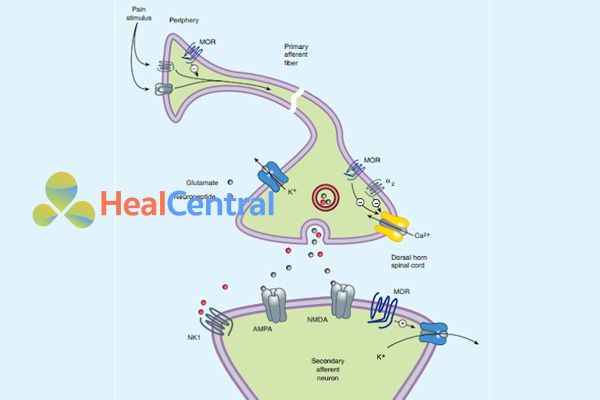
Kích thích đau ở ngoại vi có thể bị giảm (trong tình trạng viêm) bởi các opioid tác động lên thụ thể µ (MOR) do MOR làm giảm dẫn truyền tín hiệu đau, đồng thời kích thích MOR bằng opioid cũng ức chế kênh calci, làm ion calci không đi được vào trong tế bào và từ đó ức chế giải phóng các chất dẫn truyền thần kinh từ các bọc dự trữ. Các opioid cũng tác động lên MOR ở màng sau synap làm hoạt hóa kênh kali, kênh kali mở làm ion kali đi ra ngoài tế bào nhiều hơn (do bình thường nồng độ ion kali nội bào cao hơn ngoại bào), màng sau synap trở nên ưu phân cực và khó khử cực hơn. Sự hiệp đồng theo 3 cơ chế tác dụng này làm cho opioid trở thành thuốc giảm đau mạnh và chọn lọc nội tạng do cắt đứt dẫn truyền cảm giác đau.
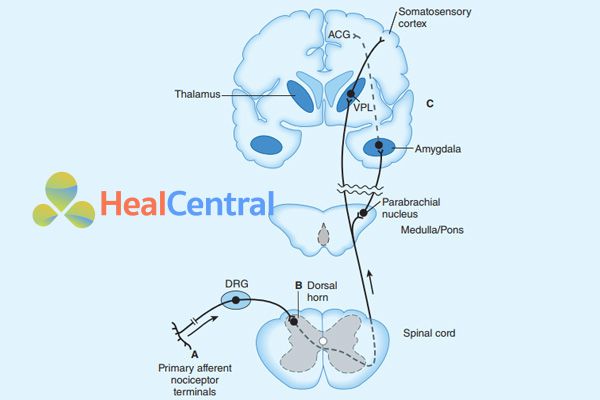
A: Tác dụng trực tiếp của opioid trên các mô ngoại vi bị viêm hoặc phá hủy (hình trên). B: Ức chế ở tủy sống (hình trên). C: Vị trí tác dụng ở hạch hạnh nhân.
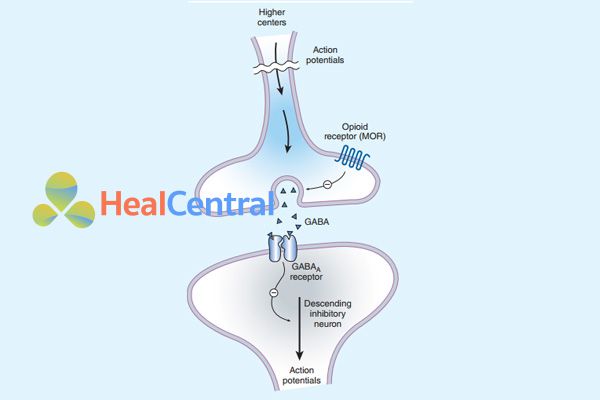
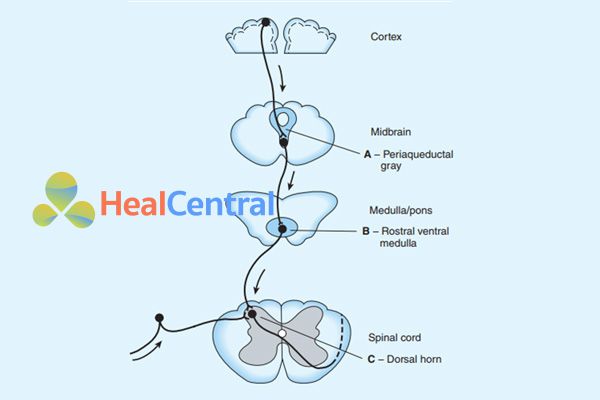
Về chỉ định giảm đau, các thuốc nhóm này được chỉ định cho các trường hợp đau từ trung bình đến nặng, đau kéo dài do phẫu thuật, ung thư (khối u chèn ép)… mà các thuốc như Paracetamol hoặc NSAIDs thường không đáp ứng.
Khi sử dụng lâu, các opioid đều dẫn đến hiện tượng dung nạp và lệ thuộc thuốc, thậm chí có thể gây lạm dụng và gây nghiện. Chính vì vậy đây là nhóm thuốc được Nhà nước quản lý rất gắt gao và không thể mua được dễ dàng.
Các opioid đều có nhiều tác dụng phụ, nhưng chúng đều có một tác dụng không mong muốn khá nguy hiểm, đó là ức chế trung tâm hô hấp ở hành não, đặc biệt là ở trẻ em. Các thuốc giảm đau opioid thông thường có thể không thường xuyên được sử dụng ở trẻ em, nhưng Codeine là một opioid có thể thường xuyên được chỉ định cho trẻ em hơn do nó có tác dụng giảm ho (cơ chế thông qua ức chế trung tâm ho ở hành não). Khi sử dụng đường uống, khoảng 10% Codeine được chuyển thành Morphine có hoạt tính giảm đau. Codeine bị chống chỉ định cho trẻ em dưới 12 tuổi.
Một số tác dụng không mong muốn khác ít nguy hiểm hơn như buồn nôn, nôn, táo bón. Đặc biệt táo bón là một tác dụng phụ rất đặc trưng và không dung nạp được, có nghĩa là táo bón không giảm đi theo thời gian sử dụng opioid.
Các nguyên tắc cơ bản sử dụng thuốc giảm đau.
Phân loại và đánh giá đau trên bệnh nhân
Đau là một cảm giác khó chịu và mang tính chất rất cảm tính, khó xác định cũng như đo lường, do vậy “đau là những gì bệnh nhân nói”.
Đau là triệu chứng, không phải là một bệnh. Có nhiều bệnh có thể dẫn đến cảm giác đau. Việc điều trị triệu chứng đau có cần thiết hay không còn phụ thuộc vào người bệnh. Có những trường hợp đau không cần thiết phải điều trị. Nhưng ở một số trường hợp khác, khi đau ảnh hưởng đến chất lượng cuộc sống của bệnh nhân, thì điều trị triệu chứng này lại thực sự cần thiết và đóng vai trò quan trọng.
Phân loại đau
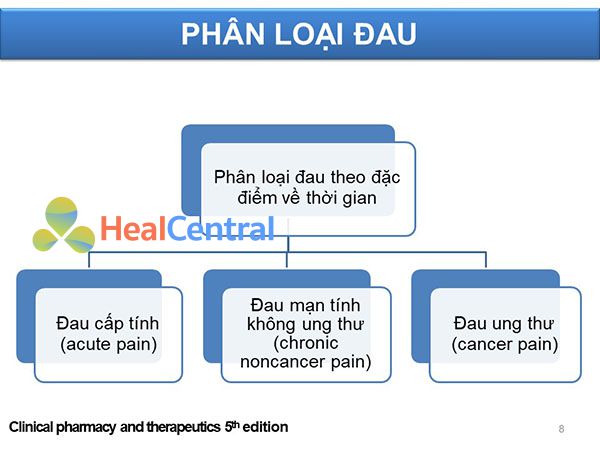
Chúng ta sẽ sử dụng hệ thống phân loại đau theo đặc điểm về thời gian, bao gồm:
– Đau cấp tính: Đau xảy ra một cách đột ngột, thường là đau cảm thụ và dễ xác định nguyên nhân như chấn thương, phẫu thuật, thủ thuật y khoa, sản khoa… Khi loại bỏ được nguyên nhân, đau thường hồi phục dần.
– Đau mạn tính: Đau xảy ra trong một thời gian dài, có thể có các cơn đau cấp tính xen kẽ hoặc không. Thường khó xác định căn nguyên của đau mạn tính, có thể liên quan đến các tình trạng mạn tính và bị ảnh hưởng bởi nhiều yếu tố. Đau mạn tính thường ảnh hưởng đến tâm lý nhiều, có thể gây mất ngủ, trầm cảm.
– Đau ung thư: Thực chất đây là một phân loại đặc biệt vì nó chiếm một vai trò quan trọng. Việc đảm bảo chất lượng cuộc sống cho bệnh nhân ung thư, đặc biệt là những bệnh nhân ung thư giai đoạn cuối, là cực kì quan trọng, vì khi này bệnh nhân không còn sống được lâu nữa. Đau ung thư bao gồm cả đau cấp tính và đau mạn tính. Đau ung thư có thể có nhiều nguyên nhân: Khối u chèn ép cơ quan, hóa trị, xạ trị, phẫu thuật hay thủ thuật sinh thiết… Đau ung thư lại được chia ra thành đau cấp tính (đột ngột) và đau mạn tính (còn gọi là đau nền).
Đánh giá đau
Để khai thác thông tin cho đánh giá đau, cần chú ý ưu tiên những mô tả của chính bệnh nhân, đánh giá thông qua hành vi (mức độ ảnh hưởng đến các hoạt động, chức năng) và đánh giá thông qua người khác nếu cần (đối với trẻ em, người người trí tuệ giảm sút…).
Cần đánh giá đau một cách toàn diện:
– Xác định nguyên nhân gây đau (nếu có thể).
– Các đặc điểm của đau:
- Trình tự thời gian xuất hiện cơn đau.
- Vị trí cơn đau.
- Đánh giá mức độ đau (thông qua công cụ đánh giá cụ thể).
- Tính chất cơn đau.
- Các yếu tố ảnh hưởng làm cơn đau giảm bớt hoặc nặng lên.
- Các triệu chứng khác đi kèm với cơn đau.
Tiền sử bệnh nhân: Các bệnh lý hoặc tình trạng mắc kèm, các thuốc đang dùng, tình trạng đau tương tự có xuất hiện trước đây hay không…
Một số xét nghiệm và các thông tin khác.
Về công cụ đánh giá đau, có 2 kiểu công cụ:
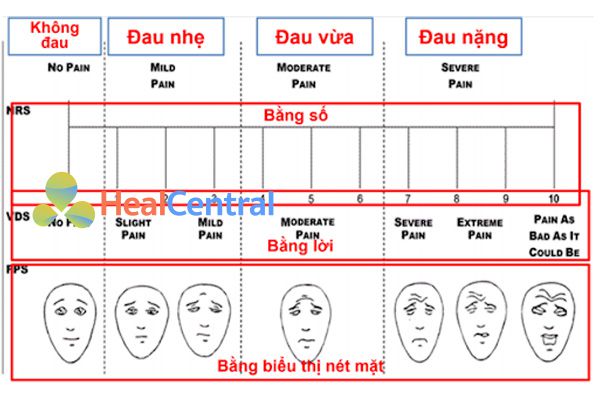
Công cụ đánh giá 1 khía cạnh: Các đại diện tiêu biểu là công cụ NRS (thang điểm đau dạng số), VAS (thang nhìn) và FPS (thang đánh giá đau bằng khuôn mặt). Mỗi loại thang đánh giá có ưu và nhược điểm riêng và cần được áp dụng cho phù hợp.
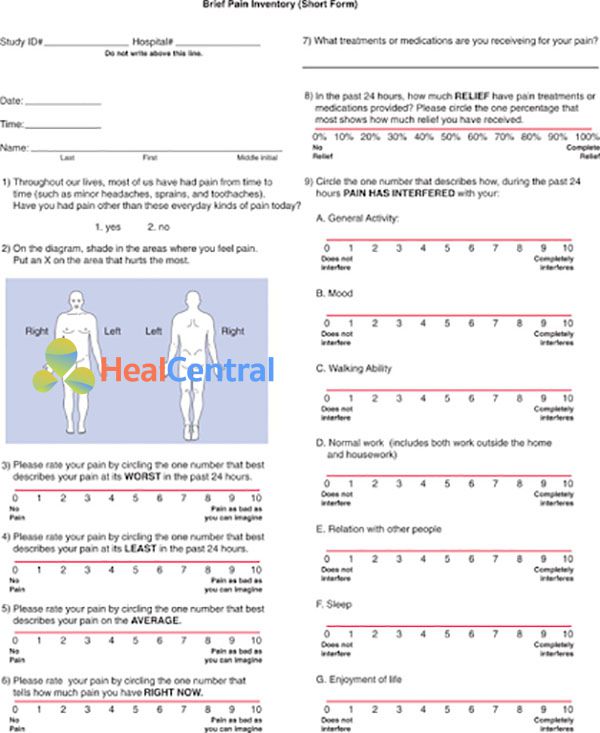
Công cụ đánh giá nhiều khía cạnh: Được ưu tiên sử dụng hơn công cụ đánh giá 1 khía cạnh. Các thang được khuyến cáo theo hướng dẫn của WHO năm 2018 trong quản lý đau ung thư bao gồm: Thang BPI (Brief Pain Inventory), thang CPOT (Critical Care Pain Observation Tool) dành cho bệnh nhân hồi sức tích cực, thang PAINAD (Pain Assessment in Advanced Dementia Scale) dành cho bệnh nhân suy giảm trí tuệ và thang IPOS (tích hợp trong thang đánh giá hiệu quả chăm sóc giảm nhẹ).
Nguyên tắc sử dụng thuốc giảm đau ngoại vi
Các thuốc giảm đau ngoại vi được tính đến ở đây bao gồm Paracetamol và các thuốc NSAIDs khác, tính cả đường toàn thân hoặc đường tại chỗ. Các thuốc hay được dùng là: Paracetamol, Aspirin, Etodolac, Diclofenac, Sulindac, Indomethacin, Ibuprofen, Naproxen, Meloxicam, Piroxicam, Celecoxib.
Sử dụng thuốc giảm đau ngoại vi có 4 nguyên tắc sau;
- NV1: Chọn thuốc phù hợp với người bệnh.
- NV2: Tôn trọng mức liều tối đa. Khi đã vượt quá liều tối đa, tác dụng giảm đau không tăng, nhưng tác dụng không mong muốn lại tăng.
- NV3: Phối hợp thuốc giảm đau theo nguyên tắc.
- NV4: Áp dụng các biện pháp không dùng thuốc hoặc dùng thuốc khác để giảm tác dụng không mong muốn.
Nguyên tắc sử dụng thuốc giảm đau trung ương
Thuốc giảm đau trung ương có thể được chia ra theo mức độ tác dụng là thuốc giảm đau trung ương mạnh và thuốc giảm đau trung ương yếu.
| Thuốc giảm đau trung ương | Độ mạnh |
| Morphine | 1 |
| Codeine | 0.1 |
| Tramadol | 0.2 |
| Pethidine | 0.1 |
| Hydromorphone | 7 |
| Methadone | 2-10 (liều lặp lại) |
| Fentanyl (hệ phân tán qua da) | 150 |
Bảng. Độ mạnh của một số opioid so với Morphine (quy ước độ mạnh = 1).
Lưu ý rằng bảng trên không quyết định được opioid nào là thuốc giảm đau trung ương mạnh hay yếu, vì nó còn phụ thuộc vào một yếu tố nữa, đó là liều tối đa mà bệnh nhân có thể dung nạp. Dù cho một thuốc có độ mạnh chỉ là yếu, nhưng lại có thể sử dụng liều cao để bù đắp thì nó vẫn có thể là thuốc giảm đau trung ương mạnh (ví dụ như Pethidine).
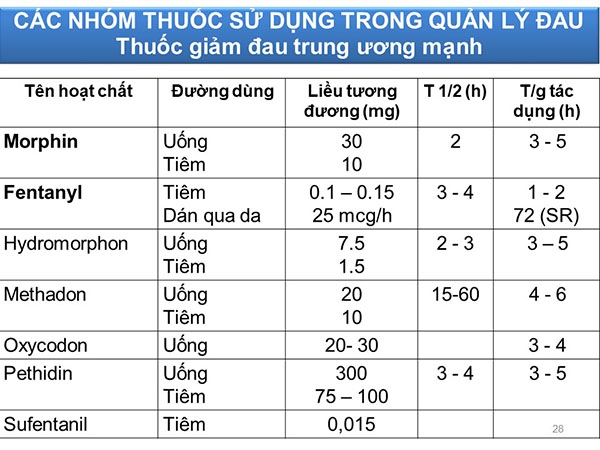
| Thuốc giảm đau trung ương | Đường dùng | Liều tương đương (mg) |
| Morphine | Uống
Tiêm |
30
10 |
| Codeine | Uống
Tiêm |
200
130 |
| Tramadol | Uống
Tiêm |
100
50 |
| Pethidine | Uống
Tiêm |
300
75-100 |
| Hydromorphone | Uống
Tiêm |
7.5
1.5 |
| Methadone | Uống
Tiêm |
20
10 |
| Fentanyl | Tiêm
Dán qua da |
0.1-0.15
25µg/h |
Bảng. Các thuốc giảm đau trung ương cùng với liều tương đương. Tất cả đều là thuốc giảm đau trung ương mạnh, trừ Codeine và Tramadol là thuốc giảm đau trung ương yếu.
Sử dụng thuốc giảm đau trung ương có 4 nguyên tắc sau:
- TW1: Chỉ sử dụng trong đau ở mức độ trung bình hoặc nặng mà thuốc giảm đau ngoại vi không đủ hiệu lực (áp dụng cho đau mạn tính).
- TW2: Phối hợp hoặc sử dụng đơn độc tùy mức độ đau.
- TW3: Với đau ung thư, cần dùng thuốc đều đặn để nồng độ thuốc ổn định trong máu.
- TW4: Áp dụng các biện pháp hỗ trợ và thuốc khác để giảm tác dụng không mong muốn.
Các thuốc hỗ trợ điều trị đau
Ngoài các thuốc giảm đau trung ương và ngoại vi thì các thuốc hỗ trợ điều trị đau dưới đây cũng được sử dụng.
Thuốc an thần (Diazepam, Clonazepam): Đau do co thắt cơ, đau thần kinh.
Thuốc giãn cơ (Dantrolene, Baclofen): Đau do co thắt cơ.
Thuốc chống động kinh (Carbamazepine, Gabapentin, Phenytoin, Pregabalin): Đau thần kinh, đau nửa đầu.
Glucocorticoid (Dexamethasone, Prednisolone): Đau do chèn ép thần kinh, phù nề, tăng áp lực nội sọ.
Một số nhóm thuốc khác chưa được đưa vào như thuốc chống trầm cảm 3 vòng, thuốc chống loạn nhịp.
Áp dụng một số nguyên tắc cơ bản sử dụng thuốc giảm đau cho đau cấp tính và đau do ung thư
Sử dụng thuốc giảm đau cho đau cấp tính
Mục tiêu điều trị:
- Điều trị sớm.
- Nếu kiểm soát đau không đầy đủ, kịp thời chỉnh lại phác đồ.
- Giảm đau ở mức độ chấp nhận được.
- Tạo điều kiện loại bỏ nguyên nhân gây đau, hỗ trợ bệnh nhân phục hồi.
Chiến lược điều trị:
- Điều trị kết hợp giữa các thuốc giảm đau có cơ chế tác dụng khác nhau, áp dụng thêm cả biện pháp không dùng thuốc.
- Dự phòng hợp lý trước các tình huống mà biết trước sẽ gây đau cho bệnh nhân như phẫu thuật, thủ thuật.
Nguyên tắc giảm đau:
4 nguyên tắc của thuốc giảm đau ngoại vi (NV1, NV2, NV3 và NV4) cộng với 2 nguyên tắc của thuốc giảm đau trung ương (TW2 và TW4).
Nguyên tắc lựa chọn thuốc
Cần tính đến các yếu tố sau:
- Phù hợp với mức độ đau, loại đau. Phân loại mức độ đau có thể xem các công cụ đo lường ở trên, nhưng nó cũng có thể được dự đoán đơn giản dựa vào tình trạng của bệnh nhân. Ví dụ: Các trường hợp trật khớp, bong gân là đau nhẹ, các trường hợp phẫu thuật nội soi, xâm lấn tối thiểu, gãy xương kín và không vỡ vụn là đau trung bình, các trường hợp như phẫu thuật lớn, gãy xương hở, thay khớp toàn bộ là đau nặng.
- Phù hợp với tình trạng của bệnh nhân: Tuổi, chức năng gan, thận, bệnh mắc kèm, thuốc dùng cùng…
- Phù hợp về dược lực và dược động học, tính sẵn có, tác dụng không mong muốn chấp nhận được, giá cả phù hợp với tình hình kinh tế bệnh nhân…
Thuốc giảm đau ngoại vi
- Ưu tiên cho các trường hợp đau nhẹ và trung bình.
- Các NSAIDs có tác dụng như nhau. Đa phần các bệnh nhân sẽ đáp ứng tốt với mọi NSAIDs. Nếu có trường hợp không đáp ứng với NSAIDs này thì thường có thể sẽ đáp ứng với NSAIDs khác.
- Chú ý tôn trọng mức liều tối đa cho phép. Khai thác cẩn thận tiền sử dùng thuốc giảm đau của bệnh nhân. Tránh trường hợp bệnh nhân mua thuốc nhiều nơi, dẫn đến quá liều.
Bảng. Liều giảm đau tối đa trong 1 lần và 1 ngày của các thuốc NSAIDs.
Thuốc giảm đau trung ương
- Ưu tiên cho các trường hợp đau trung bình và nặng.
- Nên ưu tiên opioid tác dụng ngắn, cho phép điều chỉnh liều dễ dàng và an toàn hơn.
- Thời gian dùng thuốc: 3-5 ngày với đau trung bình, 7 ngày với đau nặng.
- Không có liều trần như các NSAIDs.
Nguyên tắc phối hợp
Phối hợp các thuốc khác cơ chế tác dụng: Có thể phối hợp NSAIDs với Paracetamol hoặc phối hợp thuốc giảm đau trung ương với thuốc giảm đau ngoại vi.
Phối hợp dạng dùng: Tiêm, uống hoặc dùng tại chỗ.
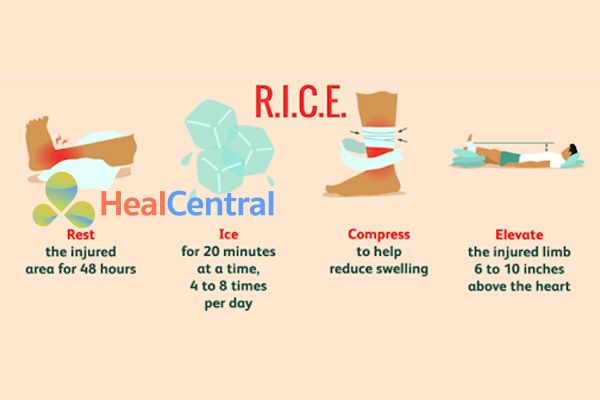
Phối hợp các biện pháp không dùng thuốc: Ví dụ như nguyên tắc RICE trong chấn thương.
- R: Rest. Thư giãn, nghỉ ngơi, để vùng chấn thương ổn định trong 48 giờ.
- I: Ice. Chườm đá 20 phút/lần, 4-8 lần/ngày. Chú ý không nên để đá tiếp xúc trực tiếp với vết thương mà nên bọc đã trong khăn.
- C: Compress. Băng ép lại bằng gạc để giảm sưng. Không băng quá chặt.
- E: Elevate. Để vị trí chấn thương cao hơn 6-10 inch so với tim. Điều này làm giảm lượng máu đến vết thương, giảm sưng và phù nề.
Giám sát tác dụng bất lợi của thuốc

Thuốc giảm đau ngoại vi:
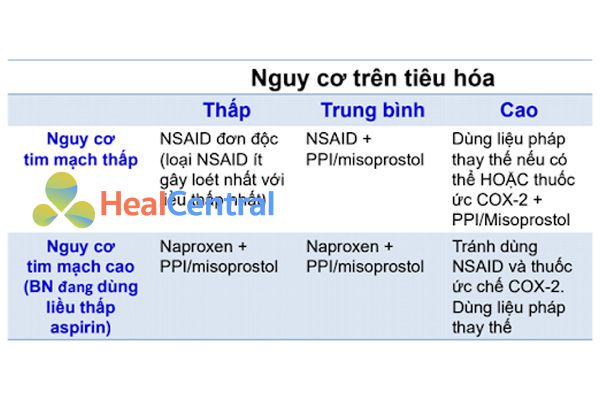
- Loét dạ dày – tá tràng do NSAIDs: Cả thuốc ức chế COX không chọn lọc và thuốc ức chế COX-2 chọn lọc đều có thể gây ra biến cố này, nhưng các thuốc ức chế COX không chọn lọc có tỷ suất cao hơn.
- Nguy cơ huyết khối tim mạch (trừ Aspirin và Naproxen): Cả thuốc ức chế COX không chọn lọc và thuốc ức chế COX-2 chọn lọc đều có thể gây ra biến cố này, nhưng các thuốc ức chế COX-2 chọn lọc có tỷ suất cao hơn. Hay xuất hiện hơn ở liều cao và dùng kéo dài.

Thuốc giảm đau trung ương:
Các tác dụng không mong muốn cần chú ý nhất khi sử dụng chúng trong đau cấp là buồn nôn, nôn và nguy cơ ức chế hô hấp.
- Buồn nôn, nôn là tác dụng không mong muốn phụ thuộc liều, khác nhau giữa các cá thể và gây khó khăn trong điều trị. Buồn nôn và nôn có thể được dung nạp khi dùng lâu dài (> 1 tuần). Cần cho bệnh nhân sử dụng cùng thuốc chống nôn (Metoclopramide, Haloperidol, Ondansetron…) nếu thấy bệnh nhân có nguy cơ nôn, đồng thời đảm bảo nhu động ruột ổn định. Thuốc chống nôn có thể chỉ cần dùng theo nhu cầu hoặc phải dùng đều đặn theo ngày tùy theo đánh giá của bác sĩ. Nếu sau 1 tuần vẫn còn các triệu chứng buồn nôn và nôn, nên xem xét nguyên nhân có thể gây nôn khác, thay đường dùng (uống à tiêm) hoặc thay opioid khác.
- Ức chế hô hấp cũng là tác dụng không mong muốn phụ thuộc liều và dung nạp nhanh. Là tác dụng gây nguy hiểm cho tính mạng, thường gặp khi quá liều. Thận trọng với các bệnh nhân có COPD (bệnh phổi tắc nghẽn mạn tính), hội chứng ngưng thở khi ngủ, hoặc dùng cùng với các thuốc an thần – gây ngủ khác. Hạn chế tác dụng không mong muốn này bằng cách tăng liều từ từ, chú ý nếu bệnh nhân có triệu chứng buồn ngủ (triệu chứng khởi đầu của ức chế hô hấp), và khi đã có hiện tượng ức chế hô hấp, cần cho bệnh nhân dùng ngay Naloxon cho đến khi các triệu chứng được cải thiện.
Chú ý: Codeine và Tramadol chống chỉ định cho trẻ < 12 tuổi và trẻ < 18 tuổi sau phẫu thuật cắt amidan và/hoặc V.A.
Sử dụng thuốc giảm đau cho đau do ung thư
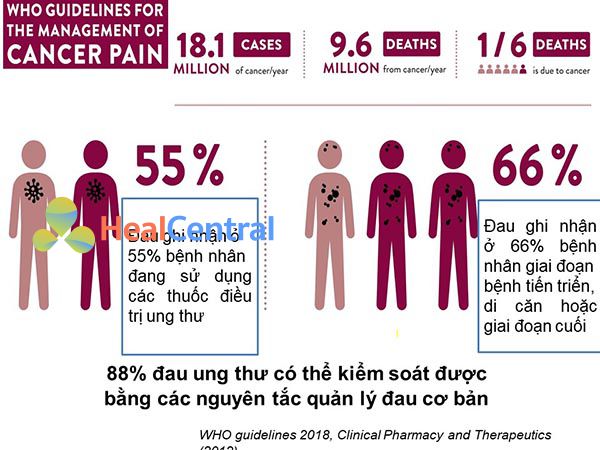
88% các trường hợp đau do ung thư hoàn toàn có thể kiểm soát được nhờ các nguyên tắc quản lý đau cơ bản.
Nguyên tắc chung tiếp cận quản lý đau do ung thư (WHO 2018)
- Giảm đau tối đa.
- Đảm bảo chất lượng cuộc sống bệnh nhân.
- Đánh giá toàn diện để định hướng điều trị.
- Đảm bảo an toàn (cho bệnh nhân, nhân viên y tế, người chăm sóc, cộng đồng và xã hội).
- Phối hợp điều trị bằng thuốc và các biện pháp hỗ trợ tâm lý.
- Tích hợp quản lý đau do ung thư vào chăm sóc ung thư toàn diện.
Chiến lược quản lý đau do ung thư:
- Đau cấp tính (đau đột ngột): Dùng thuốc liều cứu nguy khi cần thiết.
- Đau mạn tính (đau nền): Dùng thuốc đều đặn.
Nguyên tắc sử dụng thuốc giảm đau trong đau nền:
Cần áp dụng cả 4 nguyên tắc của thuốc giảm đau trung ương (TW1, TW2, TW3 và TW4) và 4 nguyên tắc của thuốc giảm đau ngoại vi (NV1, NV2, NV3 và NV4).
Lựa chọn và phối hợp thuốc giảm đau trong đau nền:
Chúng ta sử dụng bậc thang giảm đau 3 bước theo WHO 2018.
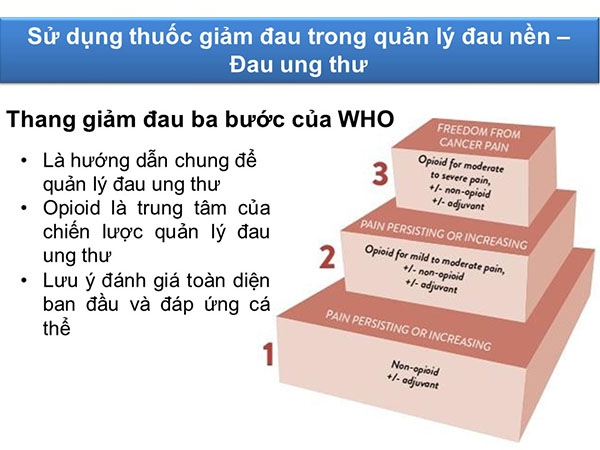
Bậc thang giảm đau này thường phải áp dụng đến cho các bệnh nhân ở giai đoạn cuối đời. Thuốc giảm đau trung ương opioid là trung tâm trong quản lý đau.
Lựa chọn thuốc phải căn cứ trên: Các đặc điểm của bệnh nhân (tuổi tác, tình trạng sức khỏe, các bệnh mắc kèm, các thuốc khác đang dùng…) và đặc điểm của thuốc (chỉ định, chống chỉ định, thận trọng và lưu ý…), cũng như tính sẵn có và chi phí điều trị.
Ưu tiên sử dụng thuốc giảm đau đường uống, cá thể hóa từng cá nhân cụ thể.
Cân nhắc phối hợp thuốc ở tất cả các bậc thang giảm đau của WHO.
Một số thuốc hỗ trợ đặc biệt:
- Ung thư đã di căn xương: Một số hormon, các chất tương tự hormon, bisphosphonate (Alendronate, Zoledronic acid…).
- Ung thư não, phổi: Glucocorticoid.
- Đau thần kinh: Một số thuốc chống động kinh (Carbamazepine, Gabapentin…), thuốc chống trầm cảm 3 vòng (Amitriptyline, Desipramine…). WHO không khuyến cáo sử dụng Ketamine.
Chú ý nguyên tắc về liều dùng với thuốc giảm đau ngoại vi (liều tối đa 1 lần và liều tối đa 24 giờ). Cần tôn trọng mức liều tối đa và tối ưu bậc thang điều trị cũng như nâng bậc khi cần thiết.
Với thuốc giảm đau trung ương, cần dùng thuốc đều đặn để có nồng độ ổn định trong máu.
Các thuốc giảm đau trung ương khác với thuốc giảm đau ngoại vi ở chỗ, chúng có hiện tượng dung nạp, tức là tác dụng giảm đau của thuốc giảm dần theo thời gian sử dụng. Trên lí thuyết thì các opioid không có liều trần để giảm đau.
Nguyên tắc quản lý các tác dụng không mong muốn của thuốc giảm đau
Thuốc giảm đau ngoại vi: Xem mục
Thuốc giảm đau trung ương: Các tác dụng không mong muốn nổi bật nhất của khi sử dụng các thuốc này trong kiểm soát đau nền ung thư và táo bón và vấn đề dung nạp thuộc, lệ thuộc và nghiện thuốc.
– Táo bón là tác dụng không mong muốn phụ thuộc liều và không dung nạp theo thời gian, xuất hiện ở 60-90% bệnh nhân dùng thuốc kéo dài. Táo bón làm ảnh hưởng đến chất lượng cuộc sống và khả năng làm việc của bệnh nhân, do đó đây là một vấn đề cần được giải quyết.
Nguy cơ táo bón tăng lên khi sử dụng opioid liều cao, ở những bệnh nhân già, lớn tuổi, ít vận động, ăn ít chất xơ, lười uống nước, có bệnh lý tiêu hóa, khối u tiêu hóa… Một số thuốc dùng cùng cũng có thể gây táo bón.
Khi táo bón, bệnh nhân cần ưu tiên sử dụng các biện pháp không dùng thuốc như ăn nhiều chất xơ, uống nhiều nước, chịu khó vận động… tuy vậy, phần lớn bệnh nhân cần dùng thuốc nhuận tràng. Chú ý cần đánh giá loại trừ các nguyên nhân khác có thể gây táo bón.
Các thuốc nhuận tràng thường sử dụng: Bisacodyl, Glycerin, Polyethylene glycol, Docusate natri, Lactulose, Sorbitol.
Nếu bệnh nhân không đáp ứng với thuốc nhuận tràng, cần hiệu chỉnh liều cũng như khoảng cách liều opioid phù hợp. Nếu táo bón nặng hơn, cân nhắc chuyển sang dùng Methadone hoặc Fentanyl dán qua da.
Hiện tượng dung nạp, phụ thuộc và nghiện có thể xảy ra khi dùng opioid dài ngày. Có 2 kiểu phụ thuộc opioid: Phụ thuộc về thể chất (dừng thuốc đột ngột có thể xuất hiện hội chứng cai, là hiện tượng thích nghi bình thường của hệ thần kinh) và phụ thuộc về tinh thần (nghiện). Một khi đã nghiện, bệnh nhân muốn sử dụng thuốc bằng mọi cách, bất chấp nguy hiểm cho bản thân hoặc cho những người xung quanh. Tuy nhiên, nghiện rất hiếm khi xảy ra khi sử dụng opioid với mục đích giảm đau.
Chú ý phân biệt “giả nghiện” với nghiện thực sự. Bệnh nhân giả nghiện có hành vi tìm kiếm thuốc do điều trị đau chưa đầy đủ và khi đã điều trị đầy đủ thì hành vi này thường mất đi.
Để hạn chế các vấn đề về dung nạp, phụ thuộc và nghiện do opioid, chúng ta cần:
- Tuân thủ tuyệt đối nguyên tắc TW1.
- Giảm sát bệnh nhân sát sao về số lượng thuốc, liều thuốc và mức độ đau.
- Đánh giá hành vi và thái độ bệnh nhân thường xuyên.
Nguyên tắc sử dụng thuốc giảm đau trong đau đột xuất
Với đau cấp tính (đau đột ngột) trong ung thư, WHO 2018 khuyến cáo dùng liều Morphine (dạng giải phóng ngay) cứu nguy (50-100% liều) mỗi 4 giờ.