Tác giả: Bác sĩ Đặng Thanh Tuấn
Tóm tắt
Bệnh nhân COPD và hen suyễn chiếm một tỷ lệ đáng kể thông khí cơ học trong ICU, và tỷ lệ tử vong với sự hỗ trợ thông khí có thể là đáng kể. Từ quan điểm sinh bệnh học, các bệnh lý này tăng sức đề kháng đường hô hấp, tăng căng chướng phổi, và khoảng chết phổi cao, dẫn đến tăng công thở. Nếu nhu cầu thông khí vượt quá cung lượng của các cơ hô hấp, suy hô hấp cấp tính sẽ xảy ra.
Mục tiêu chính của thông khí cơ học ở những bệnh nhân này là cải thiện trao đổi khí phổi và cho phép phần còn lại của các cơ hô hấp bị tổn hại phục hồi từ trạng thái mệt mỏi. Bằng chứng hiện tại hỗ trợ việc sử dụng thông khí áp lực dương không xâm lấn cho những bệnh nhân này (đặc biệt là ở COPD), nhưng thông khí xâm lấn cũng được yêu cầu thường xuyên ở những bệnh nhân có bệnh nặng hơn. Các bác sĩ phải thận trọng để tránh các biến chứng liên quan đến thông khí cơ học trong thời gian hỗ trợ thông khí. Một nguyên nhân chính gây ra bệnh suất và tử vong trong quá trình thông khí cơ học ở những bệnh nhân này là căng chướng phổi động (DH, dynamic pulmonary hyperinflation) với áp lực dương cuối kỳ thở ra nội tại (PEEP nội tại hoặc PEEP tự động). Mục đích của bài viết này là cung cấp một bản cập nhật ngắn gọn về các khía cạnh liên quan nhất để quản lý thông khí tối ưu ở những bệnh nhân này.
Mở đầu
Bệnh đường hô hấp tắc nghẽn mạn tính không chỉ bao gồm bệnh phổi tắc nghẽn mãn tính (COPD) và bệnh hen mãn tính mà còn cả các rối loạn như giãn phế quản, pneumoconiosis và bệnh phổi sau lao. COPD là một vấn đề sức khỏe và kinh tế lớn trong việc gia tăng tỷ lệ hiện nhiễm; trong năm 1990 nó là nguyên nhân gây tử vong phổ biến thứ sáu trên toàn thế giới, và đến năm 2020 bệnh này được dự đoán sẽ trở thành nguyên nhân phổ biến thứ ba gây tử vong. Tỷ lệ tử vong liên quan đến bệnh hen suyễn cũng rất đáng kể, với ước tính 1 – 8 ca tử vong trên 100.000 dân và năm. Việc phân loại đầy đủ hoặc sàng lọc để nhập viện vào đơn vị chăm sóc tích cực (ICU) là điều cần thiết trong số các bệnh nhân có nguy cơ.[1]
Mặc dù chỉ định chung cho hầu hết mọi bệnh trạng, bệnh nhân thuộc loại này không nên nhận hỗ trợ thông khí cơ học xâm lấn, vì tỷ lệ tử vong tăng đáng kể. Tuy nhiên, sự thất bại của thông khí cơ học không xâm lấn (hiệu quả trong ít nhất 75% các trường hợp, đặc biệt là COPD), hoặc theo chỉ định phẫu thuật, có thể dẫn đến kết cục gây tử vong. Sự không đồng nhất và sự hiện diện của các biến thể hỗn hợp là nguyên tắc của bệnh nhân thuộc loại này, với sự kết hợp thường xuyên các đặc điểm sinh lý bệnh hen (viêm cây khí phế quản và co thắt phế quản), khí thũng (mất độ giãn nở nhu mô) và viêm phế quản mãn tính (sự hiện diện của tăng bài tiết niêm mạc). Việc áp dụng các chiến lược chung cứng nhắc cho việc thông khí những bệnh nhân này có thể dẫn đến nguy hiểm trong cách tiếp cận quản lý. Hơn nữa, phải nhớ rằng bệnh nhân bị khí phế thũng và viêm phế quản mãn tính thường có các bệnh kèm theo nghiêm trọng thêm vào các yếu tố cần thiết khi lập kế hoạch điều trị – mục tiêu của chúng tôi là cải thiện trao đổi khí và đảm bảo phục hồi các cơ hô hấp. Ngoài hỗ trợ thông khí, nên bắt đầu điều trị nội khoa ngay lập tức (Bảng 1).
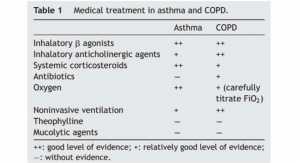
Oxy phải được dùng để điều chỉnh tình trạng thiếu oxy máu trong hen suyễn cấp tính, cũng như trong COPD – mặc dù trong trường hợp này, điều cần thiết là tránh sự gia tăng pCO2 và hậu quả của chứng gây nghiện (narcotic) do tăng CO2 máu; do đó chuẩn độ chính xác của FiO2 là cần thiết,[2] đảm bảo rằng SaO2 không vượt quá 90%. Nếu nhiễm toan hô hấp xấu đi xảy ra mặc dù thực hiện các biện pháp này, hỗ trợ thông khí sau đó được chỉ định rõ ràng.[3] Sau khi hỗ trợ như vậy đã được bắt đầu, một chẩn đoán phân biệt nên được thiết lập trong số các nguyên nhân có thể gây suy hô hấp (ví dụ, thuyên tắc mạch máu phổi, tràn khí màng phổi và tắc nghẽn đường hô hấp trên), với việc xác định yếu tố nguyên nhân gây nên hiện tượng này. Cần nhớ rằng suy tim (đặc biệt là suy tim phải) thường xuất hiện trong COPD mất bù.
Không có hệ thống nào được phát triển cho phép dự đoán tỷ lệ sống sót hoặc tỷ lệ thành công/thất bại trong cai máy thở của bệnh nhân đợt cấp COPD. Vì vậy, trừ khi bệnh nhân từ chối đặt nội khí quản bằng văn bản, hỗ trợ thông khí sẽ được cung cấp khi cần thiết. Ngừng hô hấp là sự kiện cuối của COPD và hen suyễn, và được báo trước bởi các dấu hiệu cảnh báo nhất định: thờ ơ, ngầy ngật, không nghe phế âm, nhịp tim chậm và hạ huyết áp. Tuy nhiên, rất khó để xác định mức độ nghiêm trọng của quá trình trước khi ngừng thở xảy ra; bệnh sử, thăm khám lâm sàng và đáp ứng ban đầu với điều trị vì thế có ích:
- Bệnh sử sẽ xác định tiên lượng trong đợt cấp COPD – xem xét cơ bản là tình trạng bệnh nền của bệnh nhân (được đánh giá bằng phép đo phế dung) và sự hiện diện của các bệnh đi kèm đáng kể. Trong bệnh hen suyễn, tiền sử thở máy là dấu hiệu của tiên lượng kém, giống như tình trạng ngày càng xấu đi mặc dù điều trị tối ưu bao gồm corticosteroid đường uống và thuốc chủ vận beta. Điều quan trọng là hen có thể biểu hiện dần dần, đáp ứng chậm và không đầy đủ với điều trị nội khoa, bài tiết và viêm đường thở quan trọng, hoặc theo cách đột ngột, với ưu thế co thắt phế quản và tiến triển theo hướng ngừng hô hấp trong vài phút hoặc vài giờ (trong trường hợp hiếm).[4]
- Các dấu hiệu lâm sàng trong COPD (ngủ gà, co rút khoảng liên sườn, thở nghịch chiều, vv) là nền tảng cho phân độ nặng bệnh nhân, và nhiễm toan đường hô hấp là yếu tố dự báo tốt nhất cho tình trạng kiệt sức của bệnh nhân. Xác định khí máu động mạch là rất cần thiết, cũng như so sánh với các mẫu trước đó. Các dấu hiệu lâm sàng của hen suyễn nặng là nhịp tim nhanh, nhịp thở nhanh, mạch nghịch, không có khả năng nói hết cụm từ trong một hơi thở duy nhất, và tốc độ lưu lượng thở ra tối đa (PEFR) < 50% giá trị bình thường về lý thuyết hoặc giá trị tốt nhất (< 200 l/phút nếu không biết). Dấu hiệu của các tình huống đe dọa tính mạng là không nghe phế âm, tím tái, lú lẫn hoặc hôn mê, nhịp tim chậm và hạ huyết áp, và PEFR không định lượng được. Phải nhớ rằng việc đo lường PEFR có thể nguy hiểm ở bệnh hen suyễn nặng và cơn đột ngột; mặc dù tình trạng co thắt phế quản trầm trọng hơn khi đo PEFR đã được mô tả, nó rất hữu ích cho việc đánh giá hiệu quả điều trị khi giai đoạn cấp tính đã qua.
- Đáp ứng ban đầu đối với điều trị ở bệnh nhân hen suyễn là một yếu tố tiên lượng quan trọng. Nếu bệnh nhân không cải thiện lâm sàng, sinh lý (khí máu) và máy móc (PEFR) trong vòng 1 – 2 giờ, cần phải xem xét hỗ trợ thông khí và cần đánh giá lại bệnh nhân (ban đầu mỗi giờ).[5] Trong COPD, ý nghĩa tiên lượng không giống như trong hen suyễn, vì đáp ứng với điều trị chậm hơn. Các khái niệm này được tóm tắt trong Bảng 2.
Cơ sở sinh lý
Bệnh nhân biểu hiện một loạt các yếu tố, như tăng sức đề kháng đường hô hấp (phù nề, tiết dịch, co thắt phế quản và xẹp), tăng căng chướng phổi (giảm độ giãn nở phổi và thành ngực), và khoảng chết sinh lý lớn – với hậu quả là gia tăng nỗ lực hô hấp. Nếu nhu cầu thông khí vượt quá khả năng của các cơ hô hấp, kết quả suy hô hấp cấp tính.[6] Mặc dù cơ học phổi tương tự nhau trong cả hai tình trạng, có một số khác biệt về mặt sinh lý cần được đề cập. Trong thực tế, COPD được đặc trưng bởi sự xẹp đường hô hấp lớn hơn, về cơ bản là phá hủy nhu mô phổi (đặc biệt là khí thũng), cũng như mất độ đàn hồi của phổi,[7] trong khi bệnh hen được đặc trưng bởi phì đại của thành ống dẫn khí thứ cấp sau tình trạng viêm, xẹp đường thở ít hơn mặc dù giảm đáng kể bán kính đường thở (tổn thương trung tâm ở hen so với tổn thương ngoại biên trong COPD), và sự tắc nghẽn có thể hồi phục – có thể tối thiểu hoặc kém nếu hen suyễn đã phát triển lâu.[8]
Tương tự như vậy, và đặc biệt là trong phổi bệnh nhân hen, sự phân bố không thống nhất của bệnh là một đặc điểm điển hình, cùng với sự biến đổi quan trọng trong sự phân bố tắc nghẽn phổi trong cùng một cá thể, những người có thể trải qua những thay đổi đáng kể trong vài phút. Cần tính đến yếu tố này khi lựa chọn chế độ thông khí (kiểm soát thể tích có lợi hơn kiểm soát áp suất, về cơ bản),[9] vì hậu quả của nó có thể là:
1) phân bố bất thường của tỷ lệ thông khí/tưới máu do sự tái phân phối tưới máu hướng tới các vùng thông khí thông thường;
2) tăng nguy cơ chấn thương khí áp (barotrauma); và
3) những trở ngại cho hồi lưu tĩnh mạch với sự thay đổi huyết động học, sốc và ngừng hô hấp tuần hoàn.[10]
Hơn nữa, giảm đường kính của thanh môn trong thời gian thở ra có thể được thêm vào tất cả các điều kiện này.[11] Ngược lại với bệnh nhân COPD, bệnh nhân hen phế quản thường biểu hiện áp lực đỉnh đường thở (Ppeak) cao (tràn khí màng phổi, tắc nghẽn đường thở do nút nhầy hoặc phù phổi cấp tính phải luôn luôn được nghi ngờ), và thường yêu cầu hỗ trợ thông khí lớn hơn để hiệu chỉnh hoặc cải thiện độ pH của chúng.
Giới hạn của lưu lượng khí (limitation of airflow) ảnh hưởng đến hiệu quả của cơ chế hô hấp theo các cách sau:
1) tăng sự thay đổi áp suất cần thiết để khắc phục sức cản đường thở cho một lưu lượng khí nhất định;
2) căng chướng phổi quá mức, phần nào phản ứng lại sự tăng sức đề kháng bằng cách mở rộng đường kính đường thở nhưng cũng làm giảm độ giãn nở của hệ thống;
3) quá trình căng chướng phổi quá mức (và phá hủy nhu mô phổi) làm tăng khoảng chết thông khí, và do đó, cũng tăng thể tích phút cần thiết để điều chỉnh thông khí phế nang;
4) PEEP tự động hoặc PEEP nội tại (iPEEP) gây ra nỗ lực hô hấp lớn hơn để kích hoạt hô hấp; và
5) khả năng cơ hô hấp đối phó với sự gia tăng nỗ lực hô hấp bị thay đổi (thay đổi hình dạng thành ngực – cơ hoành, thay đổi trao đổi chất do thiếu oxy – toan máu, suy mòn ở bệnh nhân COPD, vv).
Thông khí cơ học trong COPD và hen suyễn
Một khi các cơ hô hấp không thể đáp ứng nhu cầu thông khí, bệnh nhân dần dần trở nên cạn kiệt. Đây là điểm chỉ định hỗ trợ thông khí để phá vỡ vòng luẩn quẩn. Mục đích của thông khí cơ học là cho cơ hô hấp nghỉ ngơi cho đến khi bắt đầu điều trị đối phó với nguyên nhân của đợt cấp và phục hồi tắc nghẽn phế quản.
Trong đợt cấp COPD nặng với nhiễm toan hô hấp, thường được chấp nhận rằng hỗ trợ thông khí ban đầu phải được cung cấp trên cơ sở không xâm lấn, vì điều này đã được chứng minh là làm giảm tỷ lệ nội khí quản, thời gian nằm viện ICU và tử vong. Chỉ khi biện pháp này không thành công (với ngoại lệ, ví dụ, có chỉ định phẫu thuật) bệnh nhân được chỉ định đặt nội khí quản.[12] Kết luận dựa trên chưa đủ bằng chứng được rút ra trong trường hợp hen suyễn. Mặc dù không có các tiêu chí xác định rõ ràng để bắt đầu hỗ trợ COPD và hen suyễn, các chỉ định có thể bao gồm ít nhất hai trong số các điều kiện sau:
(1) Khó thở mức độ vừa phải – nặng, với việc sử dụng các cơ hô hấp phụ và thở bụng;
(2) nhiễm toan tăng CO2 máu (pH <7,35); và
(3) thở nhanh (> 25 lần/phút).
Các chế độ thông khí được sử dụng rộng rãi nhất là hỗ trợ áp lực với PEEP và chế độ BIPAP nếu tần số hô hấp không đầy đủ.[13-16]
Không có các tiêu chí được xác định rõ ràng về sự bắt đầu thông khí cơ học xâm lấn trong COPD và hen suyễn. Trong COPD, cách tiếp cận được áp dụng rộng rãi nhất là đặt nội khí quản cho bệnh nhân nếu thông khí cơ không xâm lấn thất bại sau 1 giờ (tình trạng lâm sàng và khí máu trở nên tồi tệ hơn). Trong bệnh hen suyễn, đặt nội khí quản không nên trì hoãn quá lâu (luôn dựa trên các tiêu chí lâm sàng, ví dụ: giảm ý thức và tần số hô hấp), vì mục tiêu chính của thông khí cơ học là duy trì oxy hóa và tránh ngừng hô hấp. Một khi quyết định đặt nội khí quản đã được thực hiện, kiểm soát toàn bộ việc ngừng hô hấp – tuần hoàn của bệnh nhân là mối quan tâm ưu tiên, và kỹ thuật đặt NKQ này phải được thực hiện bởi bác sĩ lâm sàng với kinh nghiệm nhiều nhất – sử dụng đường kính ống lớn nhất có thể để giảm kháng lực của ống và tối ưu hóa việc thải trừ các chất bài tiết.[17]
Các yếu tố liên quan đến tổn thương phổi do máy thở gây ra để được xem xét và tránh khi ban đầu cài đặt máy là volutrauma/barotrauma, atelectrauma và oxy liên quan đến độc tính điều trị (FiO2 > 0,5 – 0,6). Trong ý nghĩa này, điều quan trọng là nhấn mạnh khái niệm về giảm thông khí có kiểm soát như một chiến lược thông khí chung trong ứng dụng cho cả hai bệnh — hạn chế các mục tiêu để duy trì oxy và thể tích phút tối thiểu cần thiết để tránh nhiễm toan nặng. Để có hiệu quả này, cần phải đạt được sự an thần sâu, và (đặc biệt trong trường hợp hen suyễn) việc sử dụng thuốc giãn cơ bán hủy ngắn cần thiết thay cho nguy cơ bị bệnh cơ (myopathy) ở những bệnh nhân này (đặc biệt là khi dùng corticosteroid); quản lý liều bolus với theo dõi chặt chẽ hơn.[18]
Các thông số máy thở được lập trình ban đầu có thể rất giống nhau ở cả hai bệnh, và chúng ta phải chọn chế độ kiểm soát hoặc thụ động (không có sự nhất trí về chế độ thông khí cụ thể) – cố gắng kéo dài thời gian thở càng dài càng tốt, tần số hô hấp thấp (10 – 14 lần/phút) và tỷ lệ I:E thấp, để giảm thiểu iPEEP và bẫy khí. Chiến lược chung là kết hợp một thể tích phút tương đối thấp (<115 ml/kg) với lưu lượng hít vào cao (80 – 100 l/phút) để đảm bảo thời gian hít vào ngắn và do đó tỷ lệ I:E thấp.[19] Không có lợi ích nào được chứng minh khi thời gian thở ra dài hơn 4 giây.[20]
Thông khí phải đủ để duy trì pH > 7,15, với thể tích khí lưu thông thấp (5 – 8 ml/kg) để tránh áp suất bình nguyên cao > 30 cmH2O. Chỉ định dùng bicarbonate để giải quyết toan hô hấp là vấn đề, và nên được thận trọng – đặc biệt là nếu bệnh nhân bị bất ổn huyết động hoặc tăng áp lực nội sọ. Tham số hướng dẫn là pH, không phải là pCO2, tránh kiềm máu, đặc biệt là ở người bệnh mãn tính.[21]
Việc điều chỉnh kích hoạt là cần thiết cho cả hai bệnh, thường điều chỉnh −1 đến -2 cmH2O đối với trigger áp suất và 2 l/phút đối với trigger dòng. Quá trình kích hoạt quá nhạy cảm sẽ kích hoạt nhiều chu kỳ hơn mức cần thiết, làm tăng nhiễm kiềm hô hấp, trong khi quá kích hoạt ”cứng” sẽ làm tăng nỗ lực hô hấp. Những lợi ích của việc trigger dòng và áp suất là rõ ràng ở chế độ thông khí bắt buộc ngắt quãng (IMV), không phải là quyết định trong chế độ thông khí hỗ trợ áp suất (PSV), và không có sự khác biệt trong các chế độ thông khí còn lại.[22] Điều chỉnh nồng độ oxy không những liên quan đến độc tính của nồng độ cao nhưng cũng làm giảm mức độ ức chế trung tâm hô hấp trong trường hợp COPD. Trong trường hợp này, cần chuẩn độ FiO2 để đạt được SatO2 ≥ 88%.
Quá căng phổi động và Auto-PEEP
Quá căng phổi động xuất hiện khi thể tích phổi ở cuối thời gian thở ra lớn hơn dung tích cặn chức năng (FRC) do hậu quả của sự làm trống phổi không đầy đủ, khi bắt đầu hít vào trước khi hoàn thành thở ra trước đó.[23] Một vòng luẩn quẩn được tạo ra, và nếu không được giải quyết, bệnh nhân dần dần trở nên kiệt sức cho đến khi trụy tim mạch và suy hô hấp xảy ra theo cách tương tự như được tạo ra bởi tràn khí màng phổi. Các biện pháp duy nhất đã được hiển thị để dự đoán các biến chứng của quá căng phổi là xác định thể tích cuối thì hít vào (Vei, end-inspiratory volume) trên FRC, tính trên tổng thể tích khí thở ra ở bệnh nhân liệt cơ sau 60 giây ngưng thở.[24] Trong bối cảnh này, Vei > 20 ml/kg được coi là dự đoán các biến chứng như hạ huyết áp và chấn thương khí áp. Giả sử rằng độ giãn nở của hệ thống hô hấp vẫn không đổi, Vei có thể được tính từ công thức sau, mặc dù chưa được xác nhận:
Vei = (Vtial x Pplateau) / (Pplateau – iPEEP)
Bởi vì những hạn chế trong tính toán Vei trong thực hành lâm sàng, iPEEP và Pplateau được sử dụng tại chỗ, vì cả hai đều tăng trong các tình huống của căng chướng phổi động. Ppeak cũng tăng, nhưng thiếu giá trị lâm sàng, vì nó tăng với sự gia tăng sức đề kháng đường hô hấp và lưu lượng hít vào cao – nhưng mất đi khi đạt đến phế nang. iPEEP được định nghĩa là sự xuất hiện tự phát của áp lực dương vào cuối thời gian thở ra ở mức độ phế nang, do không đủ thời gian thở, và có thể xuất hiện có hoặc không có giới hạn lưu lượng khí. Nhóm “có giới hạn lưu lượng khí” sẽ bao gồm bệnh nhân hen suyễn/co thắt phế quản và COPD, trong khi nhóm không có sự gia tăng sức đề kháng đường hô hấp, là do rút ngắn thời gian thở ra do thở nhanh không cân xứng có thể tạo ra auto-PEEP (ví dụ, toan chuyển hóa với tăng thông khí, và kiềm hô hấp nguyên phát). Đây là áp suất phế nang trung bình thấp nhất đạt được trong chu kỳ hô hấp, và được đo tốt nhất trong thủ thuật tắc van thở ra ở cuối thì thở ra trên bệnh nhân thư giãn (không nhất thiết bị dùng thuốc giãn cơ).[25] Trong quá trình này không có dòng chảy trong đường hô hấp và cân bằng áp suất được tìm thấy trong hệ thống, với việc xác định áp suất phế nang cuối thì thở ra trung bình (Hình 1).
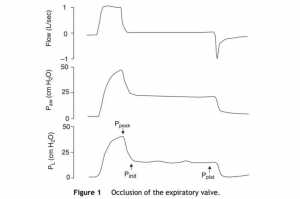
Sự hiện diện của PEEP tự động cũng có thể được phát hiện khi các nỗ lực hô hấp của bệnh nhân để kích hoạt là quá mức hoặc thậm chí không hiệu quả;[26] khi thở ra chủ động tiếp tục ở đầu thì hít vào tiếp theo; và, bằng cách sử dụng biểu đồ lưu lượng – thời gian, khi lưu lượng khí thở ra tiếp tục tồn tại ở cuối nguồn hít vào (Hình 2).[27] Nó cũng có thể được phát hiện bằng cách tăng mỗi bậc 3 cmH2O của PEEP ngoài, chỉ đến thời điểm mà ở đó áp suất cao nguyên và áp suất đỉnh cùng tăng, thì PEEP bên ngoài đã vượt quá PEEP tự động.[7]
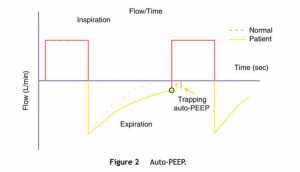
Việc tính toán iPEEP trong một bệnh nhân thở tự nhiên phức tạp hơn nhiều và khó áp dụng thực hành lâm sàng, do sự đóng góp thường xuyên của các cơ hô hấp khi thở ra chủ động. Thông qua việc xác định áp lực thực quản (Peso), điểm có áp lực âm trên đường cong Peso ngay trước khi khởi phát trigger mỗi thì hít vào. Nghi ngờ quá căng phổi khi hít vào bắt đầu trước khi lưu lượng thở ra trở về zero. Giá trị iPEEP được tính theo quy trình này thường thấp hơn giá trị xác nhận từ thở ra duy trì khi phát hiện giá trị iPEEP thấp nhất, nó mang lại giá trị trung bình.[28] Không có giá trị của iPEEP dự đoán chấn thương áp lực, mặc dù tăng liên tiếp của iPEEP phản ánh quá căng phổi. Có khuyến cáo để giảm thiểu nguy cơ bị chấn thương áp lực và chấn thương thể tích, Pplateau phải được giữ dưới 30 cmH2O.[15,16,29,30]
Việc áp dụng PEEP bên ngoài (ePEEP) nên được thực hiện bất cứ khi nào có iPEEP, với mục đích giảm các nỗ lực trigger. Nỗ lực vượt quá iPEEP là một trong những nguyên nhân chính gây suy hô hấp trong đợt cấp COPD, và hơn thế nữa là nguyên nhân chính gây thất bại trong cai máy thở của bệnh nhân tắc nghẽn luồng không khí. ePEEP có thể hữu ích để chống lại iPEEP. Tuy nhiên, ePEEP không nên được áp dụng cho bệnh nhân COPD trong khi ở chế độ thông khí có kiểm soát với mục đích tối đa hóa thở ra và ngăn ngừa quá căng phế nang khu vực – khi chế độ hỗ trợ được tiếp tục, cài đặt ePEEP làm giảm nỗ lực kích hoạt của bệnh nhân. ePEEP không nên được sử dụng trong bệnh hen suyễn nghiêm trọng.[31] Không dễ dàng để tính toán mức ePEEP đủ để được sử dụng. Theo nguyên tắc thác nước, bằng ePEEP với iPEEP sẽ ngụ ý giảm tối đa nỗ lực hô hấp mà không có nguy cơ quá căng phổi.[32]
1) có thể có tình huống đặc trưng bởi vừa có giới hạn lưu lượng khí và không có giới hạn lưu lượng khí
2) sự phân bố iPEEP trong COPD và hen suyễn thường không đồng nhất, và trong một số khu vực của phổi, iPEEP hiệu quả có thể thấp hơn iPEEP tĩnh được tính toán.
Hai khả năng này có thể dẫn đến sự gia tăng PEEP tổng nếu ePEEP = iPEEP, với hậu quả là chấn thương khí áp. Mặc dù thiếu bằng chứng khoa học đầy đủ, có một khuyến cáo rằng ePEEP phải khoảng 80% của iPEEP.
Nếu các điều ở trên vẫn là không đủ, vẫn còn một vấn đề khác: iPEEP thay đổi liên quan đến các thông số hô hấp (tần số hô hấp và thông khí), tư thế của bệnh nhân và những thay đổi về cơ học hô hấp liên quan đến quá trình bệnh và đáp ứng điều trị. Do đó, các giá trị của iPEEP được đo dưới sự thông khí có kiểm soát ở một bệnh nhân thư giãn có thể rất khác so với các thông số được tính toán theo thông khí tự phát — tình huống mà chúng tôi muốn áp dụng ePEEP. Trong thực hành lâm sàng rất hữu ích khi hỏi bệnh nhân về mức độ thoải mái và khó thở của họ trong khi chúng tôi tăng dần ePEEP, để bệnh nhân nhận thức được sự giảm bớt nỗ lực trigger do cân bằng ngược lại với iPEEP cho đến khi quá căng phế nang (khó thở sẽ tỷ lệ thuận với Vei, do đó bệnh nhân có thể nhận thấy sự gia tăng quá căng phổi). Do đó, ở bệnh nhân tắc nghẽn phế quản phải thở máy, chúng ta phải xác định auto-PEEP, áp dụng các mức ePEEP khác nhau (= iPEEP), và quan sát các thay đổi trong tổng PEEP.
Khái niệm tương tác tim phổi liên quan mật thiết đến tăng căng phổi quá mức, vì phổi, tim và tuần hoàn phổi nằm trong cùng một khoang (khoang ngực), với hậu quả thay đổi trong chức năng tim do các thay đổi trong áp lực khoang màng phổi.[33] Tăng căng phổi quá mức làm tăng áp lực dương trong lồng ngực, làm giảm hồi lưu tĩnh mạch và tiền tải của cả hai tâm thất, và làm tăng kháng lực mạch máu phổi và do đó tăng hậu tải thất phải. Hạ huyết áp là tác động phổ biến nhất của giảm tiền tải, và được thúc đẩy bởi giảm thể tích máu. Trong bối cảnh này, các tình huống phân ly điện cơ đã được mô tả [34]; do đó, nếu nghi ngờ tăng căng phổi quá mức ở bệnh nhân đang thở máy, thì nên ngắt kết nối với máy thở trong khoảng 20 – 30 giây. Do sự gia tăng hậu tải thất phải, căng phổi quá mức có thể dẫn đến suy thất phải cấp tính với sự giãn nở của tâm thất phải – gây ra sự dịch chuyển của vách liên thất và giảm thể tích tâm thất trái, do sự phụ thuộc lẫn nhau giữa hai tâm thất. Áp suất bên trong được truyền một phần đến tuần hoàn, và do đó ảnh hưởng đến các giá trị đo được của áp suất tĩnh mạch trung tâm và áp suất bờ mao mạch phổi – một thực tế phải được tính đến trong giám sát huyết động.
Cai máy thở
Cai máy thở từ thông khí cơ học là một trong những thách thức chính cho các BS hồi sức. Các nghiên cứu tiền cứu [35] đã cho thấy việc áp dụng các protocol để đẩy nhanh quá trình mà không làm tăng tỷ lệ thất bại. Việc sử dụng các tiêu chí lâm sàng trực quan đơn thuần là không đủ để đưa ra quyết định (độ nhạy 35%; độ đặc hiệu 79%).[36]
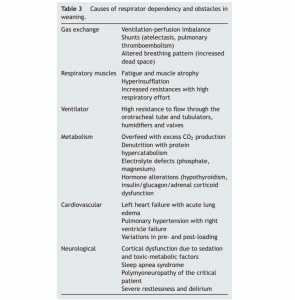
Thông khí cơ học có liên quan đến nhiều tác dụng phụ. Do đó, nên bắt đầu cai máy thở càng sớm càng tốt, đặc biệt là ở COPD. Để đánh giá thời điểm thích hợp để bắt đầu quy trình, cần xem xét cẩn thận các nguyên nhân có thể có của sự phụ thuộc vào máy thở và khó khăn trong cai máy thở (Bảng 3), cũng như các yếu tố cho phép chúng tôi dự đoán cai máy thở thành công (Bảng 4). Đặc biệt trong COPD và trong các tình huống khó khăn, việc sử dụng thông khí cơ học không xâm lấn được khuyến cáo sau khi rút ống, nhằm tránh sự cần thiết phải đặt nội khí quản lại.[37-39]
Nhiều hệ thống thông khí hỗ trợ mới mang lại lợi thế tiềm năng cho những bệnh nhân này trong giai đoạn chuyển tiếp, chẳng hạn như thông khí hỗ trợ theo tỷ lệ (PAV, proportional assisted ventilation) hoặc hỗ trợ thông khí điều chỉnh theo thần kinh gần đây (NAVA), có sẵn một số phương pháp cai máy thở thông khí. Mặc dù ưu thế của một tùy chọn cụ thể so với phương án khác chưa được chứng minh, nên thiết lập việc sử dụng protocol của phương thức được có sẳn [40]:
- Giảm dần sự hỗ trợ thông khí: FiO2, PEEP và mức PS có thể giảm dần, dựa trên kiểu thở, sự phù hợp của trao đổi khí, và sự ổn định huyết động và sự thoải mái của bệnh nhân. Cần nhớ rằng việc điều chỉnh mức PS theo tần số hô hấp là nguy hiểm, do nguy cơ hỗ trợ quá lớn những bệnh nhân này và do đó thúc đẩy sự đồng bộ của bệnh nhân – máy thở và các biến chứng của nó – như đã được chứng minh gần đây.[41] Điều thú vị là mức độ hỗ trợ càng lớn, tỷ lệ bệnh nhân thất bại với kích hoạt trigger càng cao – có thể là kết quả của việc tăng căng phổi quá mức, có thể giảm bằng cách áp dụng ePEEP, mặc dù có tranh cãi trong tài liệu liên quan đến.[42,43] Trong thực hành lâm sàng, những nỗ lực không hiệu quả để kích hoạt trigger sẽ không ngăn cản chúng ta tiếp tục quá trình cai máy thở, mặc dù phải thực hiện thử nghiệm bổ sung ePEEP và thậm chí có thể nói chuyện với bệnh nhân để thử và thiết lập PEEP lý tưởng, sử dụng các mức áp lực hỗ trợ khác nhau trong ngày.

- Nhiều thử nghiệm t hàng ngày: trong thử nghiệm t, bệnh nhân thở một cách tự nhiên, và tỷ lệ thành công là 70% đã được chứng minh sau 30 phút ngắt kết nối.[44] Không nên vượt quá 120 phút, để tránh mệt mỏi, vì ống nội khí quản làm tăng nỗ lực thở. Việc sử dụng áp lực hỗ trợ tối thiểu (ví dụ 5 mmHg) được khuyến cáo để tránh sức cản của ống, mặc dù kỹ thuật này chưa được đánh giá trong bất kỳ thử nghiệm lâm sàng nào cho đến nay.[45,46] Một cách khác là sử dụng máy thở mà không có áp lực hỗ trợ, nhưng vẫn giữ hệ thống báo động là cơ chế an toàn.
- SIMV (thông khí bắt buộc ngắt quãng đồng bộ): tần số hô hấp và thể tích khí lưu thông/áp lực hỗ trợ trong chế độ điều khiển và mức áp suất/kích hoạt hỗ trợ trong hơi thở tự phát được lập trình trong máy thở, với sự giảm dần mức trợ giúp. Phương pháp này đã tiết lộ hiệu quả thấp hơn trong các tài liệu gần đây và hiện không còn được khuyến cáo.[40]
Nếu quá trình cai máy không thành công, phải đánh giá lại các nguyên nhân có thể có ngay lập tức (Bảng 3), với việc áp dụng các biện pháp cụ thể [47], ngoại trừ bệnh nhân đang hồi phục do ảnh hưởng của thuốc an thần, thuốc giãn cơ, tràn khí màng phổi và xẹp phổi, sự thay đổi hô hấp hiếm khi được giải quyết trong một khoảng thời gian ngắn (ví dụ, vài giờ). Những bệnh nhân không vượt qua bài kiểm tra cai máy thở nên có thời gian nghỉ ngơi ở chế độ thông khí thoải mái trong ít nhất 24 h. Các chế độ kiểm soát thường được yêu cầu để thư giãn bệnh nhân, mặc dù nên được thực hiện với các chế độ hỗ trợ với mức độ áp lực hỗ trợ cao, bởi vì chúng cho phép đồng bộ hóa bệnh nhân – máy thở tốt hơn và ngăn ngừa teo cơ. Sau 24 h nghỉ ngơi, một giao thức cai máy mới nên được bắt đầu lại. Khi nó trở nên rõ ràng rằng bệnh nhân sẽ cần thông khí hỗ trợ lâu dài, cần phải xem xét kỹ lưỡng mở khí quản. Thời điểm mở khí quản sau khi thông khí cơ học kéo dài bao lâu vẫn chưa rõ.[48]





