Tác giả: Bác sĩ Nguyễn Phú Nguyên – Nguyễn Thế Bảo – Tăng Nguyễn Duy Đạt – Câu lạc bộ Nội khoa trường Đại học Y dược Cần Thơ.
Đặt vấn đề
Suy tim (heart failure) là một hội chứng lâm sàng phức tạp, thứ phát do những bất thường về cấu trúc và/hoặc chức năng tim (di truyền hay mắc phải) làm suy yếu khả năng đổ đầy hoặc bơm máu của thất, được nhận biết bởi bệnh cảnh đặc trưng về huyết động, với những đáp ứng của thận, thần kinh và thể dịch.
Theo Hiệp hội Tim mạch châu Âu (2016) định nghĩa: “Suy tim là một hội chứng lâm sàng đặc trưng bởi các triệu chứng điển hình (VD: khó thở, phù chân và mệt mỏi) mà có thể đi kèm với các dấu hiệu (VD: tĩnh mạch mạch cổ nổi, ran phổi và phù ngoại vi) gây ra bởi bất thường cấu trúc và/hoặc chức năng tim mạch, dẫn đến cung lượng tim giảm và/hoặc áp lực trong tim cao lúc nghỉ hoặc khi gắng sức/ tress”.
Hầu như tất cả các loại bệnh tim mạch đều dẫn đến tình trạng suy tim mạn, Trong thời đại có rất nhiều yếu tố nguy cơ tim mạch thì tỷ lệ mắc bệnh tim mạch ngày càng cao, số lượng người mắc bệnh tim mạch ngày càng nhiều và hậu quả là số người suy tim mạn ngày càng đông.
Về khía cạnh cá nhân , suy tim làm bệnh nhân rất khổ sở vì những triệu chứng mà nó đem lại và suy tim cũng rất nguy hiểm vì dự hậu tử vong cao. Về khía cạnh xã hội, suy tim làm giảm/mất sức lao động xã hội và làm tăng chi phí xã hội cho việc điều trị – nhất là trong các trường hợp suy tim nặng lên đòi hỏi phải nhập viện.

Hiện nay, dù đã có nhiều tiến bộ trong chẩn đoán và điều trị, nhưng suy tim vẫn tồn tại như một vấn đề khó giải quyết, được xã hội quan tâm.
Dịch tễ học suy tim
1. Tỷ lệ bệnh toàn bộ (Prevalence)
Nhiều công trình dịch tễ học đã được thực hiện và công bố nhưng trên thực tế khó so sánh các nghiên cứu với nhau, do có sự khác biệt về phương pháp nghiên cứu, đối tượng nghiên cứu và nhất là tiêu chuẩn dùng để chẩn đoán suy tim. Một số nghiên cứu tiêu biểu tại Mỹ:
- Theo Gibson (1963), tỷ lệ toàn bộ suy tim tại hai vùng ngoại ô Mỹ là 8,8‰ và 10,2‰. Tỷ lệ này tăng lên 64,9‰ và 67‰ cho lứa tuổi trên 65 cùng sống trong hai cộng đồng trên.
- Năm 1966, Garisson và cs nhận xét rằng, tỷ lệ bệnh toàn bộ ở Georgia là 17‰ và 35‰ tương ứng cho các nhóm tuổi 45 – 64 và 65 – 74. Tính chung cho độ tuổi từ 45 – 74 thì tỷ lệ này là 21‰.
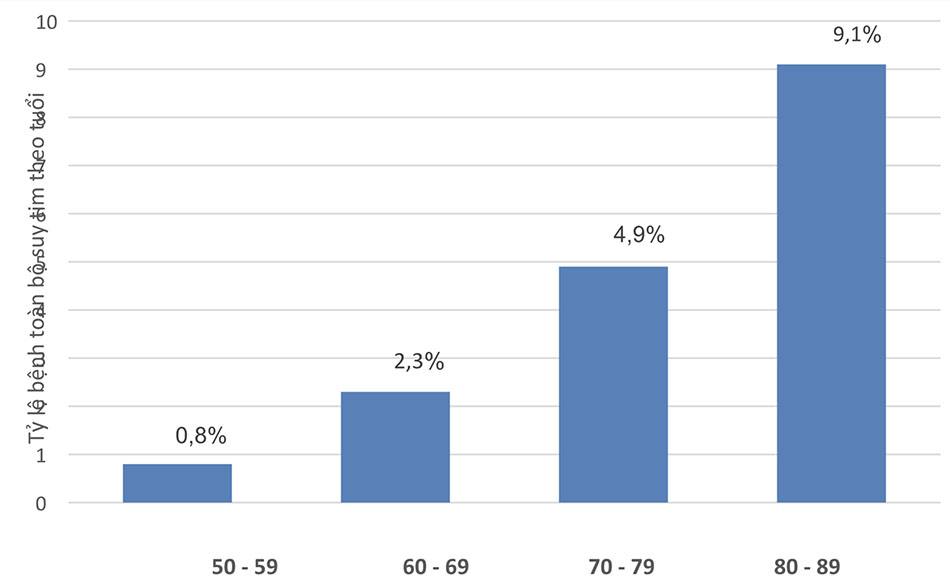
- Trong nghiên cứu Framingham (1971), tỷ lệ này là 3‰ cho độ tuổi dưới 63. Sau 34 năm theo dõi, nghiên cứu cho thấy tỷ lệ tăng theo tuổi, tỷ lệ hiện mắc suy tim là 8, 23, 49 và 91‰ tương ứng các nhóm tuổi 50 – 59, 60 – 69, 70 – 79 và trên 80.
- Theo nghiên cứu NHANES (National Health and Nutrition Examination Survey), tỷ lệ là 22,4% ở người trên 80 so với 13,3% năm 1994.
- Nghiên cứu Rotterdam (2007 – 2009), tỷ lệ suy tim ở nam cao hơn ở nữ và xu hướng tăng lên theo tuổi, tỷ lệ này là 0,9% ở nhóm tuổi 55 – 64 và 17,4% ở bệnh nhân trên 85 tuổi.
- Tiêu chuẩn dùng để chẩn đoán suy tim trong các nghiên cứu trên đều dựa vào lâm sàng, tiền sử bệnh (trừ nghiên cứu Framingham và NHANES có bổ sung X – quang).
| Bảng 2.1 Tỷ lệ bệnh toàn bộ suy tim tại Mỹ | |||
| Nghiên cứu | Năm xuất bản | Tỷ lệ bệnh toàn bộ | Tỷ lệ bệnh toàn bộ theo tuổi |
| Gibson | 1963 | 8,8 – 10,2‰ | 64,9 – 67‰ (>65t ) |
| Garisson | 1966 | 21‰ | 17‰ (45 – 64t) 35‰ (65 – 74t) |
| Framingham | 1971 | 3‰ | |
| NHANES | 2008 | 22,4% (>80t) | |
| Rotterdam | 2007 – 2009 | 0,9% (55 – 64t) 17,4% (> 85t) | |
Một số nghiên cứu tiêu biểu tại châu Âu:
- Nghiên cứu RCGP (Royal college of general practioners) năm 1955 tại xứ Wales, Anh quốc, cho thấy tỷ lệ bệnh toàn bộ suy tim là 3‰.
- Trong nghiên cứu Parameshwar (1992), thực hiện trên 30.204 người sống tại phía bắc Luân Đôn, tỷ lệ này là 3,9‰, nếu tính theo tuổi tỷ lệ này là 0,6‰ ở tuổi dưới 65 và 28‰ ở tuổi trên 65.
- Theo nghiên cứu Mair và cs ở Anh (1994), tỷ lệ bệnh toàn bộ là 15‰. Tỷ lệ này ở lứa tuổi trên 65 là 80‰.
- Theo Ericksson (1989), nghiên cứu dân số tại Thụy Điển, cho thấy tỷ lệ bệnh toàn bộ là 21‰, 43‰ và 130‰ tương ứng độ tuổi 50 – 54, 60, 67. Các nghiên cứu trên đều dựa vào lâm sàng để chẩn đoán suy tim.
- Nghiên cứu Landahl (1984), tỷ lệ suy tim ở độ tuồi 70 – 75 là 110 –170‰ ở nam và 80 – 100‰ ở nữ. Chẩn đoán suy tim dựa vào lâm sàng, tiền sử bệnh và X – quang lồng ngực.
- Theo Mair và cs nghiên cứu tại Đan Mạch, tỷ lệ này là 0,2‰ và 2,6‰ tương ứng nhóm tuổi 40 – 49 và trên 70 tuổi. Tiêu chuẩn chẩn đoán bổ sung thêm tiền căn điều trị suy tim.
- Tại Ý, theo Ambrosio, tỷ lệ này là 36, 111 và 141‰ tương ứng nhóm tuổi 65 – 69, 75 – 79 và trên 80 tuổi.
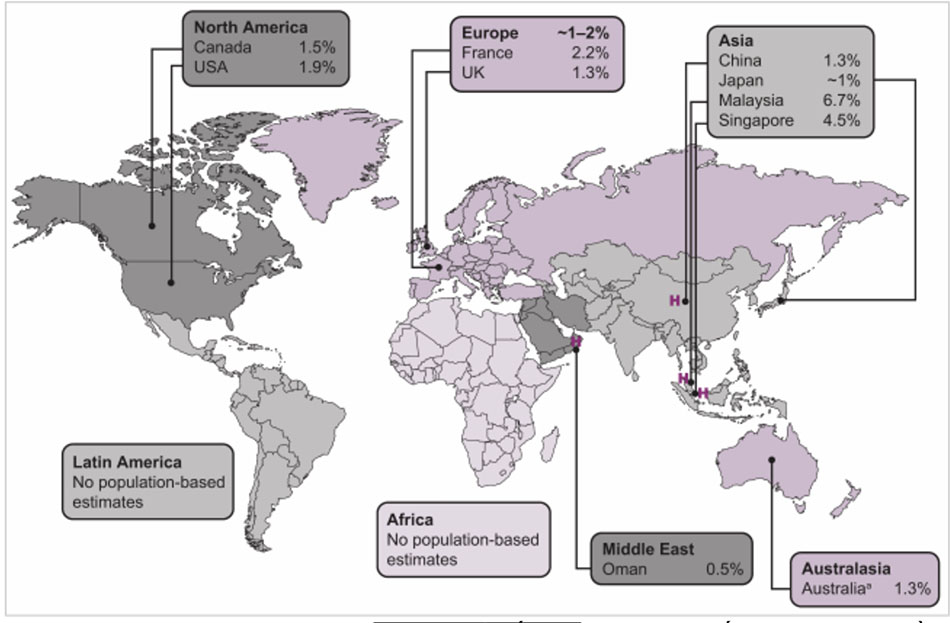
- Năm 2012, Hội tim mạch châu Âu, báo cáo tỷ lệ suy tim là 1 – 2% ở người trưởng thành ở các nước phát triển và trên 10% ở người trên 70 tuổi.
| Bảng 2.2 Tỷ lệ bệnh toàn bộ suy tim tại châu Âu | ||||
| Nghiên cứu | Nước | Năm | Tỷ lệ bệnh toàn bộ | Tỷ lệ bệnh toàn bộ theo tuổi |
| RCGP | Anh | 1958 | 3% | |
| Parameshwar | Anh | 1992 | 4% | 28‰ (>65t) |
| Mair | Anh | 1994 | 15% | 80‰ (>65t) |
| Ericksson | Thụy Điển | 1989 | 21‰ (50 – 54t)
43‰ (60t) 130‰ (67t) |
|
| Landahl | Thụy Điển | 1984 | 110 – 170‰ (nam)
80 – 110‰ (nữ) |
|
| Mair | Đan Mạch | 1994 | 0,2‰ (40 – 49t)
2,6‰ (>70t) |
|
| Ambrosio | Ý | 1994 | 36‰ (65 – 69t)
111‰ (75 – 79t) 114‰ (>80t) |
|
| ESC | Châu Âu | 2012 | 1 – 2% (người trưởng thành) | |
Ở các nước châu Á, một số báo cáo ghi nhận:
- Jakarta (Indonesia), tỷ lệ bệnh toàn bộ là 2,6 – 3,8‰. Bangkok (Thái Lan) , tỷ lệ này là 1,81‰. Tiêu chuẩn chẩn đoán suy tim dựa trên lâm sàng, qua nghiên cứu hồ sơ hoặc nghiên cứu về dân số.
2. Tỷ lệ bệnh mới phát hiện (Incidence)
Nghiên cứu Framingham thực hiện 1949, trên 5.209 người, tuổi 30 – 62 sau 34 năm theo dõi, công trình đã chứng minh tỷ lệ mắc mới cũng tăng theo tuổi, tỷ lệ này càng tăng gấp đôi cho mỗi 10 năm, ngoài ra nó còn thay đổi theo phái tính.
Kết quả cho thấy, ở nam, tỷ lệ này là 2, 5, 9, 17, 31‰ với nhóm tuổi 45 – 54, 55 – 64, 65 – 74, 75 – 84, 85 – 94. Ở nữ, tỷ lệ này là 1, 3, 6, 13 và 28‰, tương ứng cùng với các nhóm tuổi ở nam.
Theo Rodeheffer (1993), tỷ lệ mắc mới suy tim tại Mỹ là 1‰, tỷ lệ này là 16‰ cho lứa tuổi từ 65 – 67.
Theo Remes, tỷ lệ mắc mới suy tim trên 37.600 dân sống ở phía tây Phần Lan trong độ tuổi 45 – 74 là 4,1‰ ở nam và 3‰ ở nữ.
Trong nghiên cứu Ericksson, tỷ lệ này là 1,5; 4,3 và 10,2‰ tương ứng với các nhóm tuổi 50 – 54, 55 – 60 và 61 – 67.
| Bảng 2.3 Tỷ lệ mắc mới suy tim | ||||
| Nghiên cứu | Nước | Năm | Tỷ lệ bệnh mới phát hiện | Tỷ lệ bệnh mới phát hiện theo tuổi |
| Rodeheffer | Mỹ | 1993 | 1‰ | 16‰ (>65t) |
| Remes | Phần Lan | 1992 | 4‰ (nam)
3‰ (nữ) |
|
| Ericksson | Thụy Điển | 1989 | 1,5‰ (50 – 54t)
4,3‰ (55 – 60t) 10‰ (61 – 67t) |
|
Ở các nước châu Á, chưa ghi nhận số liệu. Trong một nghiên cứu về suy tim tại Malaysia, trong số các bệnh nhân nhập viện được chẩn đoán suy tim thì 30% là được chẩn đoán lần đầu.
3. Tiên lượng suy tim
Nghiên cứu Framingham (1948 – 1998) cho thấy tiên lượng suy tim không khả quan hơn tiên lượng bệnh ung thư.
Tỷ lệ sống 5 năm từ khi có chẩn đoán suy tim là 25% ở năm, 38% ở nữ, trong khi đó tỷ lệ này là 50% đối với bệnh ung thư.
Tỷ lệ này càng xấu khi suy tim càng nặng, tỷ lệ tử vong một năm là 60% cho bệnh nhân suy tim độ IV theo phân loại NYHA.
Nếu tính thời gian sống trung bình thì thời gian này là 1,66 năm ở nam và 3,17 năm ở nữ.
Theo ESC 2012, trước 1990, 60 – 70% tử vong trong 5 năm sau khi chẩn đoán và thường phải nhập viện nhiều lần.
Hiện nay, giảm 30 – 40% tỷ lệ nhập viện và giảm tỷ lệ tử vong sau 5 năm có ý nghĩa thống kê.
4. Ảnh hưởng của suy tim lên đời sống bệnh nhân
Theo hai công trình lớn tại Mỹ đã chứng minh bệnh suy tim làm giảm chất lượng sống nhiều hơn các bệnh mạn tính khác.
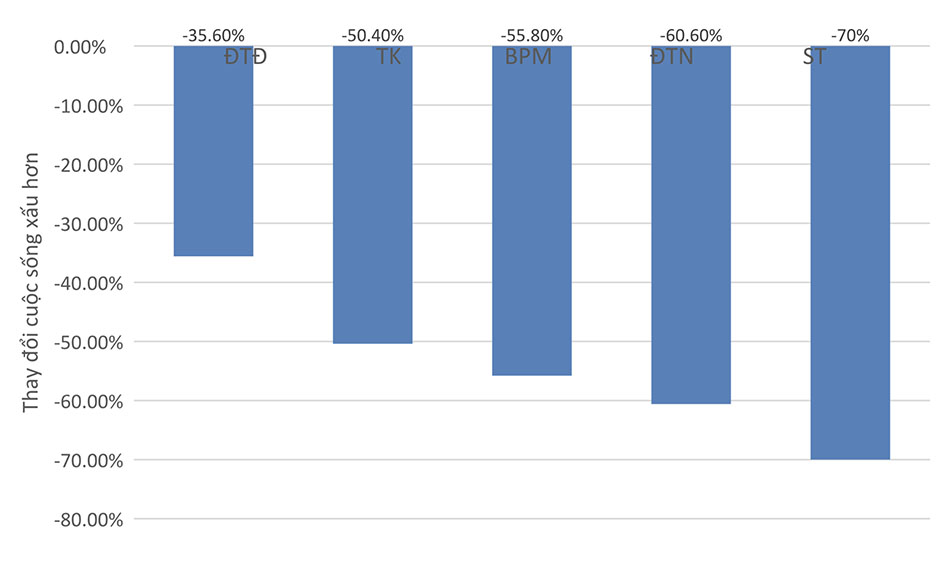
| Bảng 2.4 Các bệnh mạn tính và chất lượng cuộc sống | |
| Bệnh | Thay đổi chất lượng cuộc sống |
| Bệnh tiểu đường | -35,60% |
| Thấp khớp | -50,40% |
| Bệnh phổi mạn tính | -55,80% |
| Đau thắt ngực | -60,60% |
| Suy tim | -70,00% |
Bệnh nhân suy tim có nguy cơ nhồi máu cơ tim gấp 2,5 – 5 lần và nguy cơ đột quỵ cao hơn 4 lần so với người không suy tim.
Theo NHANES 2008: 57% bệnh nhân suy tim trên 60 tuổi không đi lại được, 11% không sinh hoạt hằng ngày được, 12% ảnh hưởng đến thị lực.
5. Suy tim và các chi phí xã hội
Chi phí xã hội dành cho vấn đề suy tim rất cao, chi phí này chiếm khoảng 1 – 2% ngân sách dành cho chương trình chăm sóc sức khỏe quốc gia ở các nước châu Âu.
2/3 chi phí tập trung tại bệnh viện, chi phí điều trị suy tim độ IV theo NYHA gấp 8 – 30 lần viện phí để điều trị suy tim độ II.
| Bảng 2.5 Chi phí y tế dành cho suy tim ở một số nước | |||
| Nước | Chi phí | % tổng chi phí y tế quốc gia | % chi phí tại bệnh viện |
| Mỹ (1989) | 9 tỷ USD | 1,5% | 71% |
| Anh (1990) | 360 triệu £ | 1,2% | 60% |
| Pháp (1990) | 11,4 tỷ FF | 1,9% | 64% |
| Bảng 2.6 So sánh các chi phí y tế tại Anh dành cho các loại bệnh | |
| Bệnh | Chi phí y tế/năm |
| Hen phế quản | 400 triệu £ |
| Đột quỵ | 334 triệu £ |
| Suy tim | 360 triệu £ |
Kết luận:
1. Tỷ lệ bệnh toàn bộ và tỷ lệ mới phát hiện suy tim đều tăng theo tuổi. Do tuổi thọ con người có xu hướng tăng dần, người ta dự đoán trong vài thập niên đến số người bị suy tim sẽ nhiều hơn.
2. Tiên lượng bệnh nhân suy tim có xu hướng tốt hơn, nhưng chưa đồng bộ.
3. Suy tim ảnh hưởng nặng nề lên sinh hoạt cá nhân lẫn gia đình nhiều hơn so với các bệnh mạn tính khác.
4. Chi phí xã hội dành cho suy tim khá cao, chiếm 1 – 2% tổng chi phí ngân sách quốc gia dành cho y tế.
Nguyên nhân suy tim
| Bảng 3.1 Bệnh học và các nguyên nhân suy tim theo ESC 2012 | |
| Phân suất tống máu giảm (<40%) | |
| Bệnh động mạch vành
Nhồi máu cơ tim. Thiếu máu cục bộ cơ tim. |
Bệnh cơ tim dãn nở không do thiếu máu cục bộ cơ tim.
Bệnh di truyền. Bệnh hệ thống. |
| Quá tải áp lực mạn tính
Bệnh van tim do hẹp. |
Tổn thương cơ tim do thuốc, độc chất
Rối loạn chuyển hóa. Do virus. |
| Quá tải thể tích mạn tính
Bệnh van tim do hở Shunt trong tim (trái – phải). Shunt ngoài tim. |
Bệnh Chagas
Nhịp chậm mạn tính Nhịp nhanh mạn tính |
| Phân suất tống máu bảo tồn (>40 – 50%) | |
| Bệnh cơ tim phì đại
Nguyên phát (bệnh cơ tim phì đại) Thứ phát (do tăng huyết áp). |
Bệnh cơ tim hạn chế
Bệnh hệ thống (amyloidosis, sarcoidosis) Bệnh ứ sắt. |
| Do tuổi | Do xơ hóa (Fibrosis).
Bệnh lý nội mạc cơ tim. |
| Bệnh tim – phổi | |
| Tâm phế.
Bệnh mạch máu phổi. |
|
| Tình trạng cung lượng tim cao | |
| Cường giáp.
Rối loạn dinh dưỡng (Beri Beri). |
Tăng lưu lượng máu quá mức.
Shunt động tĩnh mạch. Thiếu máu mạn. |
Yếu tố thúc đẩy suy tim
ESC 2016 đã đưa ra một danh sách các yếu tố thúc đẩy suy tim cấp hoặc làm nặng tình trạng suy tim trước đây của bệnh nhân. Xác định và điều chỉnh các yếu tố thúc đẩy là bắt buộc trong tiếp cận và xử trí bệnh nhân suy tim nhập viện.
| Bảng 3.2 các yếu tố thúc đẩy suy tim theo ESC 2016 |
| Hội chứng mạch vành cấp.
Rối loạn nhịp nhanh (VD: rung nhĩ, nhịp nhanh thất). Tăng huyết áp quá mức. Nhiễm trùng (VD: viêm phổi, viêm nội tâm mạc nhiễm trùng, nhiễm trùng huyết). Không tuân trị chế độ muối/dịch và thuốc đang dùng. Rối loạn nhịp chậm. Chất độc hại (rượu, chất kích thích, ma túy). Thuốc (VD: NSAIDs, corticoid, thuốc inotrop âm, hóa trị chất có độc cho tim). Đợt cấp của bệnh phổi tắc nghẽn mãn tính. Thuyên tắc phổi. Phẫu thuật và biến chứng quanh phẫu thuật. Tăng hoạt giao cảm, bệnh cơ tim liên quan đến stress. Rối loạn nội tiết/chuyển hóa (VD: rối loạn chức năng tuyến giáp, đái tháo đường, rối loạn chức năng thượng thận, mang thai và những bất thường chu sinh). Bệnh lý mạch máu não. Nguyên nhân cơ học cấp: hội chứng mạch vành cấp biến chứng vỡ tim (vỡ thành tự do, thông liên thất, hở van hai lá cấp tính), chấn thương ngực hoặc can thiệp tim mạch, viêm nội tâm mạc trên van tự nhiên hoặc van nhân tạo, bóc tách hoặc huyết khối động mạch chủ. |
Trên lâm sàng thường truy tìm để xác chẩn hoặc loại trừ nhanh các yếu tố thúc đẩy thường gặp thuộc về tim mạch, chúng ta cần nhớ thuật ngữ “CHAMP”: acute Coronary syndrom (hội chứng mạch vành cấp), Hypertension emergency (tăng huyết áp cấp cứu), Arrhythmia (rối loạn nhịp), acute Mechanical cause (nguyên nhân cơ học cấp), Pulmonary embolism (thuyên tắc phổi).

Ở Việt Nam, thường dùng thuật ngữ CHAMPID (bổ sung thêm hai yếu tố thúc đẩy bao gồm: I- Infection: Nhiễm trùng, D-Drug: Do dùng thuốc).
Một số phân loại suy tim
Theo vị trí:
Suy tim trái.
Suy tim phải.
Suy tim toàn bộ.
Theo cung lượng tim:
Suy tim cung lượng cao.
Suy tim cung lượng thấp.
Theo thời gian:
Suy tim mạn (chronic heart failure):
- Suy tim mạn ổn định (stable chronic heart failure).
- Suy tim mạn mất bù (decompensated chronic heart failure).
Suy tim cấp (acute heart failure).
| Bảng 3.3 Một số phân loại suy tim | |
| Theo vị trí | Suy tim trái |
| Suy tim phải | |
| Suy tim toàn bộ | |
| Theo cung lượng tim | Suy tim cung lượng cao |
| Suy tim cung lượng thấp | |
| Theo thời gian | Suy tim mạn:
|
| Suy tim cấp | |
Theo chức năng (phân suất tống máu – EF):
| Bảng 3.4 Phân loại suy tim theo chức năng theo AHA/ACC 2013 | ||
| Phân loại | EF | Mô tả |
| 1. Suy tim với EF giảm (HFrEF) | ≤40% | Còn gọi là suy tim tâm thu. Những nghiên cứu lâm sàng ngẫu nhiên chính thu nhận những bệnh nhân có EF giảm và chỉ có những bệnh nhân này những phương pháp điều trị có hiệu quả được chứng minh đến hôm nay. |
| 2. Suy tim với EF bảo tồn (HFpEF) | ≥ 50% | Còn gọi là suy tim tâm trương. Có vài tiêu chuẩn khác nhau được sử dụng để định nghĩa suy tim EF bảo tồn. Chẩn đoán suy tim tâm trương là một thử thách bởi vì phần lớn là chẩn đoán loại trừ những nguyên nhân không do tim khác gây triệu chứng giống suy tim. Đến nay, những phương pháp điều trị hiệu quả chưa được xác nhận. |
| a. EF bảo tồn, giới hạn | >40% đến <50% | Những bệnh nhân này rơi vào giới hạn, hoặc ở nhóm trung gian. Đặc điểm lâm sàng, điều trị và dự hậu tương tự như bệnh nhân suy tim EF bảo tồn. |
| b. EF bảo tồn, cải thiện | ≥40% | Người ta nhận thấy có một số ít bệnh nhân suy tim EF bảo tồn mà trước đó có EF giảm. Những bệnh nhân này có EF cải thiện hoặc hồi phục có thể có đặc điểm lâm sàng khác biệt với bệnh nhân suy tim EF bảo tồn hay EF giảm. Cần có thêm nhiều nghiên cứu hơn cho những bệnh nhân này. |
| Bảng 3.5 Phân loại suy tim theo chức năng theo ESC 2016 | |
| Phân loại | EF |
| 1. Suy tim với EF giảm hay suy tim tâm thu (HFrEF) | ≤40% |
| 2. Suy tim với EF bảo tồn hay suy tim tâm trương (HFpEF) | ≥50% |
| 3. Suy tim với EF khoảng giữa (HFmrEF) | >40% đến <50% |
Sinh lý bệnh
1. Các yếu tố ảnh hưởng đến cung lượng tim
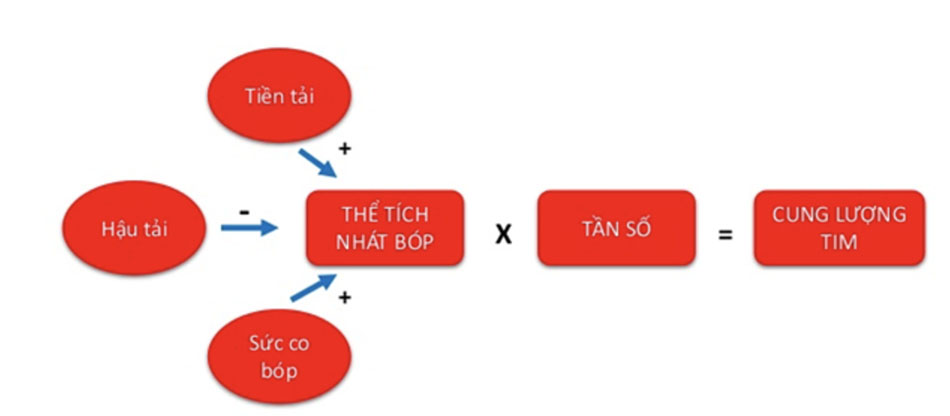
Sức co bóp nội tại của tim: Tự bản thân cơ tim có, không có mối tương quan với tiền tải, hậu tải.
Tiền tải: Sự chịu tải của tâm thất thời kỳ tâm trương, tương đồng với thể tích cuối tâm trương hay bằng với độ dài của sợi cơ tâm thất cuối tâm trương.
Hậu tải: Tất cả những gì tạo nên sức cản chống lại sự bơm máu ra của tâm thất. Cũng chính là sức căng thành tâm thất.
Tần số tim: Do tần số tim ảnh hưởng đến thời gian tâm trương (đổ đầy thất) nên ảnh hưởng đến thể tích mỗi nhát bóp (chịu ảnh hưởng bởi tiền tải) và lực co bóp cơ tim.
Cung lượng tim: CO = Thể tích nhát bóp mỗi phút x Tần số tim.
2. Một số khái niệm quan trọng
a. Định luật Laplace: Hậu tải thất trái = Stress thành tim = T = (P x r) /2t (với: T là sức căng thành, P là áp lực xuyên thành thất trái bằng P tâm thu TT – P áp lực khoang màng phổi ).
R: Bán kính lòng thất trái cuối tâm thu và t là bề dày thành thất trái).
Một ví dụ về tầm quan trọng của định luật Laplace: Bệnh nhân thứ nhất bị tăng huyết áp mạn có bán kính thất trái tâm thu (r) là 20mm, bề dày thành sau thất trái (t) là 10mm. Bệnh nhân thứ hai mắc bệnh cơ tim dãn có bán kính thất trái (r) là 30mm, bề dày thành sau thất trái (t) là 5mm. Giả sử áp lực khoang màng phổi bình thường như nhau bằng 0 và van động mạch chủ cả hai bệnh nhân bình thường. Nếu thầy thuốc vẫn duy trì một huyết áp tâm thu là 140mmHg cho cả hai bệnh nhân thì hậu tải của bệnh nhân thứ hai bằng ba lần hậu tải bệnh nhân thứ nhất.
Như vậy, trên lâm sàng thầy thuốc thường đồng nhất huyết áp và hậu tải mà quên mất những yếu tố cực kì quan trọng là kích thước buồng tim cũng như bề dày thành tim.
Ngoài ra, trong tự nhiên còn có một ví dụ thú vị về sức căng thành trong cấu tạo tim hình ống của hươu cao cổ.
b. Giãn năng: C = V/P là sự thay đổi thể tích khi áp lực thay đổi một đơn vị => với một thể tích cuối tâm trương nhất định (tiền tải) thì áp lực cuối tâm trương phụ thuộc vào giãn năng của thất. Khi giảm giãn năng làm cho áp lực cuối tâm trương tăng cao ở cùng một tiền tải => giảm đổ đầy thất (do cản trở tĩnh mạch trở về tim) tạo nên suy tim tâm trương (suy tim có phân suất tống máu bảo tồn).
3. Đáp ứng bù trừ của cơ thể và tim trong tình trạng suy tim
Suy tim bắt đầu sau một biến cố tim mạch, bất kể nguyên nhân gì thì hậu quả sau cùng đều làm giảm khả năng bơm của tim. Khi đó sẽ có nhiều cơ chế bù trừ được hoạt hóa nhằm giúp tim duy trì được chức năng co bóp bình thường, vì vậy bệnh nhân không có triệu chứng của suy tim (Suy tim còn bù). Tuy nhiên, theo thời gian các cơ chế này hoạt hóa quá mức -> tổn thương tâm thất nặng nề hơn, gây tái cấu trúc xấu hơn và bệnh nhân bắt đầu có triệu chứng (suy tim mất bù).
Tại tim:
- Tăng tần số tim: Thông qua phản xạ BainBridge nhờ các baroreceptor ở xoang động mạch cảnh và quai động mạch chủ (tần số tim sẽ tăng khi lượng máu về nhĩ tăng) là đáp ứng sớm nhất -> tăng cung lượng tim.
- Tuy nhiên, tăng tần số tim đồng nghĩa với gia tăng nhu cầu chuyển hóa và gây giảm tưới máu vành do rút ngắn thời gian tâm trương và có những nhát có bóp rỗng không hiệu quả (khi tăng quá 180 nhịp/phút gây giảm cung lượng tim).
- Cơ chế Frank – Starling: Khi suy tim tâm thu (EF giảm) với một đáp ứng khi tăng tiền tải, thể tích nhát bóp sẽ giảm (ở người bình thường thể tích nhát bóp tăng lên) -> ứ máu trong tâm thất thì tâm trương -> ở thì tiếp theo thể tích sẽ lớn hơn nên kích hoạt cơ chế Frank – starling giúp thể tích nhát bóp nhiều hơn nhằm duy trì cung lượng tim.
- Tuy nhiên, cơ chế bù trừ này có giới hạn, khi suy tim nặng có EF giảm nhiều, dù thể tích tâm trương có cao hơn, cung lượng tim không tăng thêm khi áp lực đổ đầy tiếp tục tăng -> ứ máu ngược dòng gây phù phổi.
- Giãn buồng tim: Giúp đáp ứng bù trừ với những nguyên nhân gây tăng tiền tải, thể tích cuối tâm trương của thất lớn -> các sợi cơ tim giãn -> tăng lực co bóp (theo định luật Frank – Starling) -> tăng cung lượng tim.
Tuy nhiên, khi thể tích tâm trương quá lớn tức chiều dài sợi cơ tim giãn tới một mức nào đó sẽ gây:
- Giảm lực co bóp cơ tim (theo định luật Frank – Starling).
- Tăng hậu tải và giảm tưới máu cơ tim (theo định luật Laplace) do tăng P, tăng r (có thể hiểu đơn giản khi tăng áp lực cuối tâm trương thất trái gây giảm tưới máu cơ tim do cơ tim được nuôi máu vào thì tâm trương và tăng áp lực cũng đè ép các mạch vành).
- – Nếu việc đáp ứng với tiền tải lâu ngày sẽ gây giãn buồng tim -> thành tim mỏng -> giảm khả năng co bóp (3).
Dày cơ tim: Giúp đáp ứng bù trừ với những nguyên nhân gây tăng hậu tải -> tăng đường kính các sợi sacrome -> tăng lực co bóp và giảm hậu tải (theo định luật Laplace) -> tăng cung lượng tim (đồng thời làm giảm nhu cầu tiêu thụ oxy cơ tim do tăng t).
Tuy nhiên, khi dày cơ tim cũng đồng nghĩa với việc buồng tim khó dãn -> giảm khả năng đổ đầy (4).
Ngoài tim
Thần kinh thể dịch:
- Hệ thần kinh giao cảm (đáp ứng khi huyết áp giảm): Giúp duy trì một huyết áp hệ thống đảm bảo tưới máu trong điều kiện cung lượng tim giảm, giúp tăng tần số, lực co bóp cơ tim, co tĩnh mạch giúp đẩy máu về tim tốt hơn (gia tăng tiền tải), hoạt hóa hệ thống renin – angiotensin – aldosterone (RAA) từ đó làm tăng cung lượng tim.
- Tuy nhiên, theo thời gian gây ra nhiều hậu quả thúc đẩy quá trình diễn tiến của suy tim: giảm đáp ứng với các thụ thể β ở cơ tim và cơ chế điều chỉnh lên của các protein G ức chế nên làm giảm độ nhạy của cơ tim với các catecholamin, tái cấu trúc cơ tim (phì đại, hoại tử, xơ hóa do chết tế bào theo chương trình). Đồng thời tăng sức cản ngoại vi (do làm co động mạch) làm tăng hậu tải -> giảm thể tích nhát bóp từ đó giảm cung lượng tim làm suy tim nặng hơn.
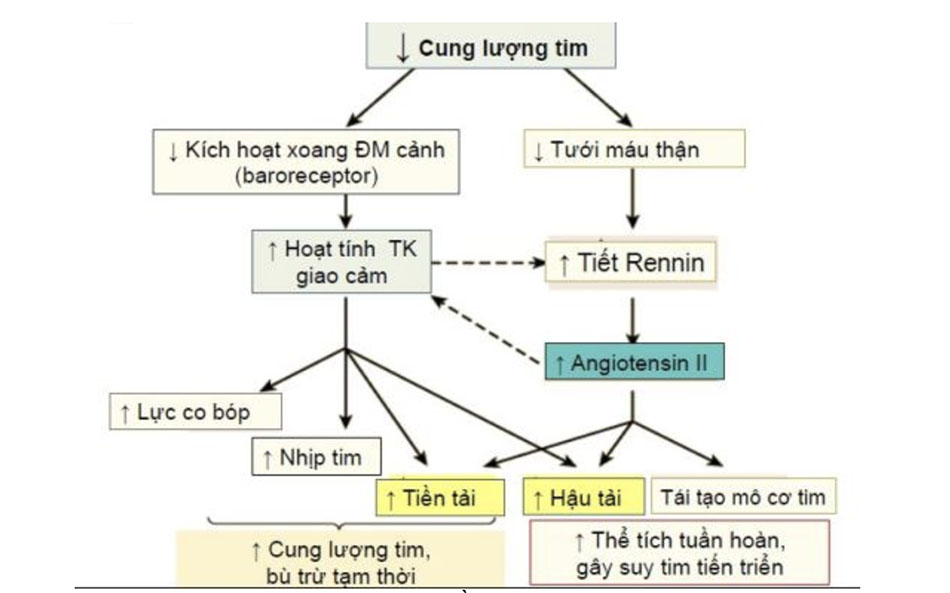
Hệ renin – angiotensin – aldosterone:
- Khi giảm cung lượng tim làm giảm tưới máu thận, ngoài ra còn do kích thích β 2 do hoạt hóa giao cảm -> Kích hoạt hệ RAA (cụ thể là các phức hợp cận cầu thận tiết ra renin giúp biến angiotensinogen -> angiotensin I và tại phổi angiotensin I sẽ được ACE chuyển đổi thành angiotensin II) -> chủ yếu giúp co mạch hệ thống và giữ muối nước (góp phần gia tăng tiền tải thông qua việc tăng sự chênh áp giữa mạch máu ngoại biên và nhĩ phải) làm tăng cung lượng tim (thông qua đáp ứng với tăng tiền tải theo định luật Frank – Starling) và đảm bảo huyết áp động mạch trung bình để tưới máu.
- Tuy nhiên, việc tăng nồng độ angiotensin II và aldosterone trong máu lâu dài sẽ dẫn đến những bất lợi: tăng tạo các cytokines, hoạt hóa đại thực bào và kích thích nguyên bào sợi -> xơ hóa và tái cấu trúc theo hướng bất lợi.
Peptid lợi niệu, vasopressin,…
- Bù trừ hệ thống: Tăng thể tích máu, tái phân bố dịch, tăng hồng cầu, tăng khả năng sử dụng oxy mô,…(Đây thực chất là những hệ quả do việc bù trừ tại tim và thần kinh thể dịch).
- Các cơ chế bù trừ trên cuối cùng vẫn sẽ dẫn đến hậu quả.
Giảm tưới máu: giảm cung lượng tim làm tái phân bố máu tưới các cơ quan, sẽ dồn máu từ ngoại biên về các cơ quan quý (tim, não) thông qua vai trò của hệ thần kinh giao cảm (cụ thể là catecholamin) và hệ RAA.
*Lưu ý: Hậu quả này không xảy ra ở suy tim cung lượng cao.
Tái định dạng (remodeling) và phì đại tâm thất theo hướng bất lợi làm suy tim ngày càng nặng hơn.
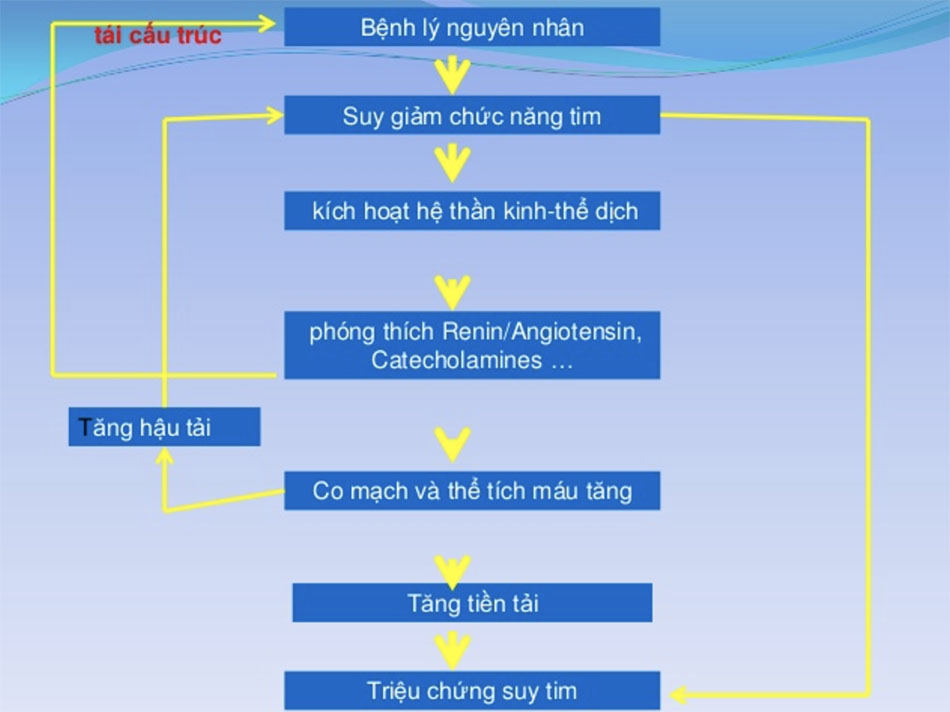
**Vì các hậu quả bất lợi việc hoạt hóa hệ thần kinh thể dịch lâu dài -> trên lâm sàng có nhiều loại thuốc được tạo ra nhằm cắt đứt các cơ chế bù trừ này.
Triệu chứng suy tim
Các triệu chứng trong suy tim thường không đặc hiệu cho suy tim, các triệu chứng có độ đặc hiệu cao cho suy tim thì có độ nhạy thấp và ngược lại. Các triệu chứng cơ năng và thực thể trong suy tim đôi khi rất khó chẩn đoán trong trường hợp bệnh nhân bị béo phì, lớn tuổi và bệnh phổi mạn.
1. Triệu chứng cơ năng
Mệt (Fatigue): do giảm cung lượng tim.
Khó thở khi gắng sức: do giảm cung lượng tim không đáp ứng được nhu cầu oxy cho cơ thể trong tình trạng cần lượng oxy nhiều hơn khi gắng sức. Suy tim càng nặng, khả năng gắng sức càng giảm.
Khó thở khi nằm (khó thở phải ngồi): do giảm khả năng co bóp của thất trái nên máu ứ ngược dòng về nhĩ trái -> ứ ngược về mạch máu phổi -> thoát dịch vào mô kẽ gây phù mô kẽ -> cản trở khả năng trao đổi khí. Đặc biệt tình trạng sung huyết phổi càng nặng thêm khi bệnh nhân nằm (khi nằm máu các tĩnh mạch ngoại biên về tim dễ dàng hơn do không chịu tác động của trọng lực). Khi tình trạng tăng áp phổi nặng nề, dịch từ mô kẽ sẽ thoát vào phế nang làm giảm dung tích sống và khả năng khuếch tán khí -> khó thở nặng hơn (cũng là cơ chế gây ran ẩm).
Khó thở kịch phát về đêm: cơ chế tương tự khó thở khi nằm, cộng thêm hoạt động ưu thế của thần kinh phó giao cảm về đêm làm giảm khả năng tống máu của tim -> sung huyết phổi nặng nề, hậu quả bệnh nhân đột ngột khó thở dữ dội, phải ngồi dậy để thở, nếu tình trạng ứ máu nặng làm tăng cao áp lực mạch máu phổi có thể gây vỡ -> máu tràn vào mô kẽ -> vào phế nang gây ho ra máu.
Phù: do tình trạng suy tim phải hoặc tăng áp phổi quá mức làm giảm khả năng tống máu của thất phải -> máu ứ ngược dòng về nhĩ phải -> ứ ngược về tĩnh mạch chủ trên (biểu hiện tĩnh mạch cổ nổi) và dưới (biểu hiện phù hai chi dưới, gan to). Khi làm nghiệm pháp ấn gan phồng cảnh làm máu từ tĩnh mạch chủ dưới đổ về nhĩ phải -> tăng áp lực nhĩ phải -> giảm lượng máu từ tĩnh mạch chủ trên đổ về -> tĩnh mạch cảnh trong nổi rõ ở tư thế Fowler.
Rối loạn bài tiết nước tiểu: tiểu đêm ở giai đoạn đầu của suy tim do đáp ứng bù trừ của hệ RAA làm tăng áp lực lọc và tăng tưới máu thận. Giai đoạn sau do cung lượng tim đã giảm đến mức không còn đáp ứng đủ máu để thận duy trì áp lực lọc bình thường làm giảm khả năng bài tiết nước tiểu.
Đánh trống ngực, hồi hộp, đau thắt ngực: Do đáp ứng bù trừ làm tăng nhịp tim và tăng sức co bóp khi cung lượng tim giảm. Đau thắt ngực là hậu quả của việc đáp ứng bù trừ như tăng tần số tim quá mức làm giảm thời gian tâm trương (thời gian tưới máu cơ tim), hoặc giãn buồng tim quá mức làm gia tăng áp lực cuối tâm trương (giảm tưới máu cơ tim + tăng hậu tải tức tăng nhu cầu oxy cơ tim).
| Bảng 5.1 Các phân tích gộp về độ nhạy, độ đặc hiệu, tỷ số tiên đoán dương, tỷ số tiên đoán âm của các triệu chứng cơ năng trong chẩn đoán suy tim | |||
| Mant (mọi đối tượng) | Madock (chăm sóc sức khỏe ban đầu) | Wang (khoa cấp cứu) | |
| Khó thở | 83
54 1,79 (1,3 – 2,47) 0,31 (0,12 – 0,79) |
1,15 (1,09 – 1,21)
0,50 (0,2 – 1,26) |
|
| Khó thở khi gắng sức | 84
34 1,3 (1,2 – 1,4) 0,48 (0,35 – 0,67) |
||
| Khó thở khi nằm | 44
89 3,91 (1,51 – 10,11) 0,63 ( 0,53 – 0,74) |
1,59 (0,89 – 3,58)
0,89 (0,77 – 1,04) |
50
77 2,2 (1,2 – 3,9) 0,65 (0,45 – 0,92) |
| Khó thở khi nằm ở bệnh nhân có tiền sử hen/COPD | 77
44 2,2 (1,2 – 3,9) 0,65 (0,45 – 0,92) |
||
| Khó thở kịch phát về đêm | 1,71 (1,12 – 2,23)
0,87 (0,75 – 0,99) |
41
84 2,6 (1,5 – 4,5) 0,7 ( 0,54 – 0,91) |
|
| Phù | 53
72 3,91 (1,51 – 10,11) 0,63 (0,53 – 0,74) |
51
76 2,1 (0,92 – 5,0) 0,64 ( 0,39 – 0,91) |
|
| Mệt | 1,03 (0,84 – 1,25)
0,98 (0,88 – 1,17) |
31
70 1,0 (0,74 – 1,4) 0,99 (0,85 – 1,1) |
|
| Mệt ở bệnh nhân có tiền sử hen/COPD | 74
34 1,1 (0,96 – 1,3) 0,79 (0,54 – 1,2) |
||
2. Triệu chứng thực thể
Da tái, tay chân lạnh: Do đáp ứng co mạch, do giảm cung lượng tim và giảm khả năng tống máu của tim đến những đầu chi xa ở cơ thể.
Ran phổi.
Tĩnh mạch cổ nổi, ấn gan phồng cảnh (+) ở tư thế Fowler.
Phù: trắng, mềm, ấn lõm, không đau, đối xứng hai bên, phù ít vào sáng sớm, nhiều về chiều, giảm khi kê cao chi. Ban đầu xuất hiện ở chi dưới, nếu tình trạng sung huyết ngày càng nặng có thể lan lên bụng, ngực và toàn thân, bao gồm các khoang ổ bụng và màng phổi gây tràn dịch màng bụng và màng phổi (thường gây tràn dịch màng phổi toàn bộ hoặc phải).
Mỏm tim lệch: xuống dưới ra ngoài (phì đại hoặc dãn thất trái), mỏm tim lệch chếch lên trên sang phải (phì đại hoặc dãn thất phải). Khám có thể thấy dấu Harzer (+).
Gan to ở giai đoạn đầu gọi là gan đàn xếp, giai đoạn sau ứ máu làm thiếu oxy kéo dài gây thoái hóa mỡ ở gan, tổ chức xơ phát triển gây xơ gan (xơ gan – tim).
| Bảng 5.2 Các phân tích gộp về độ nhạy, độ đặc hiệu, tỷ số tiên đoán dương, tỷ số tiên đoán âm của các triệu chứng thực thể trong chẩn đoán suy tim | |||
| Mant (mọi đối tượng) | Madock (chăm sóc sức khỏe ban đầu) | Wang (khoa cấp cứu) | |
| Tĩnh mạch cổ nổi | 52
70 1,73 (1,23 – 2,43) 0,68 (0,56 – 0,84) |
4,36 (2,66 – 7,44)
0,88 (0,83 – 0,91) |
39
92 5,1 (3,2 – 7,9) 0,66 (0,57 – 0,77) |
| Tĩnh mạch cổ nổi ở bệnh nhân có tiền sử hen/COPD | 41
90 4,3 (2,8 – 6,5) 0,65 (0,54 – 0,78) |
||
| Mỏm tim lệch | 15,96 (8,24 – 30,93)
0,58 (0,35 – 0,93) |
||
| Tiếng tim bất thường (T3 hoặc T4) | 11
99 12,1 (5,74 – 25,4) 0,9 (0,82 – 0,99) |
7,34 (1,56 – 32,37)
0,92 (0,77 – 0,96) |
13
99 11 (4,9 – 25) 0,88 (0,83 – 0,91) |
| Ran phổi | 51
81 2,64 (1,86 – 3,74) 0,61 (0,55 – 0,68) |
1,53 (1,17 – 1,19)
0,85 (0,64 – 0,94) |
60
78 2,8 (1,9 – 4,1) 0,51 (0,37 – 0,7) |
| Ran phổi ở bệnh nhân có tiền sử hen/COPD | 71
73 2,6 (2,1 – 3,3) 0,39 (0,28 – 0,55) |
||
| Gan to | 17
97 |
||
| Gan to ở bệnh nhân có tiền sử hen/COPD | 14
94 2,4 (1,2 – 4,1) 0,91 (0,84 – 1) |
||
Cận lâm sàng trong chẩn đoán suy tim
1. Tổng quan các cận lâm sàng trong chẩn đoán suy tim
| Bảng 6.1 Khuyến cáo về các xét nghiệm giúp chẩn đoán ở bệnh nhân nghi ngờ có suy tim (ESC 2012) | ||
| Khuyến cáo | Mức độ | Chứng cứ |
| Thực hiện cho tất cả bệnh nhân | ||
| Siêu âm tim (SAT) qua thành ngực nhằm đánh giá cấu trúc và chức năng tim, gồm chức năng tâm trương và đo phân suất tống máu thất trái giúp chẩn đoán suy tim, hỗ trợ và theo dõi điều trị, giúp đánh giá tiên lượng. | I | C |
| Điện tâm đồ 12 chuyển đạo nhằm xác định nhịp tim, tần số tim, hình dạng và thời gian của phức bộ QRS, các bất thường khác. Thông tin về điện tâm đồ cũng giúp cho việc điều trị và tiên lượng bệnh nhân. Một điện tâm đồ hoàn toàn bình thường không ủng hộ chẩn đoán suy tim tâm thu. | I | C |
Xét nghiệm sinh hóa máu (điện giải đồ, creatinin máu, độ lọc cầu thận ước đoán, men gan, bilirubin, ferritin, TIBC), chức năng tuyến giáp được khuyến cáo thực hiện nhằm:
|
I | C |
| Công thức máu toàn phần được khuyến cáo thực hiện nhằm: Xác định thiếu máu, là một nguyên nhân có thể gây triệu chứng cơ năng và thực thể giống suy tim và gây tình trạng suy tim nặng hơn. Giúp tiên lượng bệnh nhân. | I | C |
Đo nồng độ Natriuretic peptides (BNP, NT – proBNP, MR – proBNP) nhằm:
|
IIa | C |
| Chụp X – quang ngực thẳng nên được thực hiện nhằm chẩn đoán xác định hoặc loại trừ một số bệnh phổi như ung thư (không loại trừ được hen phế quản, COPD). X – quang ngực cũng giúp xác định tình trạng sung huyết phổi/phù phồi, một dấu hiệu giúp chẩn đoán ở bệnh nhân nghi ngờ suy tim trong bệnh cảnh khó thở cấp. | IIa | C |
| Thực hiện cho một số bệnh nhân chọn lọc | ||
| Cộng hưởng từ tim được khuyến cáo khi cần đánh cấu trúc và chức năng tim, đo phân suất tống máu thất trái, đặc điểm mô học tim. | I | C |
| Chụp mạch vành được chỉ định ở bệnh nhân suy tim có đau ngực, ở những người phù hợp với việc tái tưới máu mạch vành, để đánh giá giải phẫu học mạch vành. | I | C |
| Hình ảnh học đánh giá thiếu máu/sống còn cơ tim (siêu âm, cộng hưởng từ tim, SPECT hoặc PET) ở những bệnh nhân bị bệnh mạch vành, những người phù hợp với việc tái tưới máu mạch vành nhằm xác định khả năng phục hồi thiếu máu cục bộ cơ tim/sống còn cơ tim. | IIa | C |
| Chỉ định thông tim trái và phải ở những bệnh nhân chuẩn bị ghép tim, cấy thiết bị hỗ trợ chẩn đoán tuần hoàn cơ học nhằm đánh giá chức năng thất trái, phải và kháng lực động mạch phổi. | I | C |
Nghiệm pháp gắng sức nên được thực hiện:
|
IIa | C |
| Bảng 6.2 Khuyến cáo về các xét nghiệm giúp chẩn đoán ở bệnh nhân nghi ngờ có suy tim (ESC 2016) | ||
| SAT qua thành ngực được khuyến cáo cho việc đánh giá cấu trúc và chức năng cơ tim ở những bệnh nhân nghi ngờ suy tim để thiết lập chẩn đoán HFrEF, HFmrEF hoặc HFpEF. | I | C |
| SAT qua thành ngực được khuyến cáo để đánh giá EF để xác định bệnh nhân bị suy tim, những người HFrEF thích hợp cho điều trị bằng thuốc và thiết bị (ICD, CRT) dựa trên bằng chứng. | I | C |
| SAT qua thành ngực được khuyến cáo cho đánh giá các bệnh van, chức năng thất phải và áp lực động mạch phổi ở bệnh nhân đã được chẩn đoán HFrEF, HFmrEF hoặc HFpEF để xác định những người phù hợp cho sửa van. | I | C |
| SAT qua thành ngực được khuyến cáo cho việc đánh giá cấu trúc và chức năng cơ tim ở những người được tiếp xúc với điều trị mà khả năng có thể gây tổn hại cơ tim (ví dụ hóa trị). | I | C |
| Các kỹ thuật khác (bao gồm vận tốc Doppler mô tâm thu và các chỉ số biến dạng, VD: strain và strain rate), nên được xem xét trong siêu âm tim ở những người có nguy cơ phát triển suy tim để xác định rối loạn chức năng cơ tim ở giai đoạn tiền lâm sàng. | IIa | C |
| Cộng hưởng từ tim (MRI) được khuyến cáo cho việc đánh giá cấu trúc và chức năng cơ tim (bao gồm cả tim phải) ở những người có cửa sổ siêu âm hạn chế và những bệnh nhân bị bệnh tim bẩm sinh phức tạp (có tính đến những thận trọng/chống chỉ định cộng hưởng từ tim). | I | C |
| MRI tim với cản từ nên được xem xét ở những bệnh nhân có bệnh cơ tim dãn nhằm phân biệt giữa tổn thương cơ tim do thiếu máu cục bộ và không do thiếu máu cục bộ trong trường hợp dữ liệu hình ảnh khác và lâm sàng không rõ ràng (có tính đến những thận trọng/chống chỉ định cộng hưởng từ tim). | IIa | C |
| MRI tim được khuyến cáo xác định các đặc tính của mô cơ tim trong trường hợp nghi ngờ viêm cơ tim, amyloidosis, sarcoidosis, bệnh Chagas, bệnh Fabry bệnh cơ tim non – compaction và haemochromatosis (có tính đến những thận trọng/chống chỉ định đển cộng hưởng từ tim)…. | I | C |
| Hình ảnh gắng sức không xâm lấn (MRI tim, siêu âm tim gắng sức, SPECT, PET) có thể được xem xét để đánh giá thiếu máu cục bộ và khả năng sống còn cơ tim ở những bệnh nhân suy tim và bệnh mạch vành (xem xét tái thông mạch vành sau đó) trước khi quyết định tái thông mạch. | IIb | C |
| Chụp mạch vành xâm lấn được khuyến cáo ở những bệnh nhân suy tim và đau thắt ngực kháng với điều trị bằng thuốc hoặc loạn nhịp thất có triệu chứng hoặc ngừng tim được cứu sống (có dự kiến tái thông mạch máu vành) để thiết lập chẩn đoán bệnh tim thiếu máu cục bộ (BTTMCB) và độ nặng của nó. | I | C |
| Chụp mạch vành xâm lấn nên được xem xét ở những bệnh nhân suy tim và có xác suất trước test cho bệnh mạch vành là trung bình – cao và sự hiện diện của thiếu máu cục bộ trên các thử nghiệm lâm sàng không xâm lấn (có ý định tái thông mạch máu vành) để thiết lập chẩn đoán BTTMCB và độ nặng của nó. | IIa | C |
| CT tim có thể được xem xét ở những bệnh nhân suy tim và xác suất trước test của BTTMCB là thấp – trung bình hoặc ở những người có thử nghiệm lâm sàng không xâm lấn không rõ ràng nhằm để loại trừ hẹp động mạch vành. | IIb | C |
Tái đánh giá cấu trúc và chức năng cơ tim sử dụng hình ảnh không xâm lấn được khuyến cáo:
|
I | C |
2. Siêu âm tim qua thành ngực
a. Đánh giá chức năng tâm thu thất trái
Phân suất tống máu thất trái (PSTMTT) không phải là chỉ số đánh giá co bóp thất trái vì nó còn phụ thuộc vào thể tích, tiền tải, hậu tải, nhịp tim và chức năng van tim.
Trong suy tim với PSTMTT giảm thể tích nhát bóp vẫn còn duy trì, nhưng thể tích nhát bóp lại giảm ở bệnh nhân suy tim có PSTMTT bảo tồn và phì đại thất trái đồng tâm. PSTMTT có thể bảo tồn (và thể tích nhát bóp giảm) ở bệnh nhân hở van hai lá nặng. Vì vậy, phải phân tích PSTMTT kèm với bệnh cảnh lâm sàng.
b. Đánh giá chức năng tâm trương thất trái
Không có một thông số đo lường đơn độc nào có thể khẳng định chẩn đoán rối loạn chức năng tâm trương thất trái. Vì vậy, cần làm siêu âm kỹ càng kết hợp các dữ liệu từ siêu âm hai chiều và Doppler để chẩn đoán. Việc đánh giá bao gồm cả những bất thường về cấu trúc (phì đại thất trái, dãn nhĩ trái) và chức năng thất trái.
| Bảng 6.3 Những bất thường siêu âm thường gặp ở bệnh nhân suy tim | ||
| Thông số | Bất thường | Gợi ý lâm sàng |
| Các thông số liên quan đến chức năng tâm thu | ||
| Phân suất tống máu thất trái | Giảm (<50%) | Giảm co bóp toàn bộ thất trái |
| Phân suất co rút thất trái | Giảm (<25%) | Giảm co bóp thất trái |
| Rối loạn vận động vùng thất trái | Giảm động, vô động, loạn động | Nhồi máu cơ tim, thiếu máu cơ tim, bệnh cơ tim, viêm cơ tim |
| Kích thước thất trái cuối tâm trương | Tăng (đường kính >60 mm, >32 mm/m 2 , thể tích > 97 mL/m 2 ) | Khả năng suy tim quá tải thể tích |
| Kích thước thất trái cuối tâm thu | Tăng (đường kính >45 mm, >25 mm/m 2 , thể tích > 43 mL/m 2 ) | Khả năng suy tim quá tải thể tích |
| Khoảng thời gian vận tốc đường thoát thất trái | Giảm (< 15cm) | Thể tích nhát bóp thất trái giảm |
| Các thông số liên quan đến chức năng tâm trương thất trái | ||
| Các chỉ số rối loạn chức năng tâm trương thất trái | Bất thường hình dạng phổ van hai lá, vận tốc mô, tỷ lệ E/e | Mức độ rối loạn chức năng tâm trương thất trái và gợi ý áp lực đổ đầy. |
| Chỉ số thể tích nhĩ trái | Tăng (thể tích >34 mL/m 2 ) | Áp lực đổ đầy thất trái tăng (trước đây hoặc hiện tại). |
| Chỉ số khối thất trái | Tăng (>95 g/m 2 ở nữ và >115 g/m 2 ở nam) | Tăng huyết áp, hẹp van động mạch chủ, bệnh cơ tim phì đại |
| Các thông số liên quan đến chức năng van tim | ||
| Cấu trúc và chức năng van | Hẹp hoặc hở van (đặc biệt là hở van hai lá và hẹp van động mạch chủ) | Có thể là nguyên nhân hoặc hậu quả của suy tim (hở van hai lá thứ phát) Đánh giá độ nặng và ảnh hưởng lên huyết động. Xem xét phẫu thuật |
| Các thông số khác | ||
| Chức năng thất phải (e.g.TAPSE) | Giảm (TAPSE <16 mm) | Rối loạn chức năng tâm thu thất phải |
| Vận tốc đỉnh qua dòng hở van ba lá | Tăng (>3,4 m/s) | Áp lực tâm thu thất phải tăng |
| Áp lực tâm thu động mạch phổi | Tăng (>50 mmHg) | Khả năng tăng áp động mạch phổi |
| Tĩnh mạch chủ dưới | Dãn, không xẹp theo hô hấp | Rối loạn chức năng thất phải, tăng áp lực nhĩ phải, khả năng tăng áp động mạch phổi quá tải |
| Màng ngoài tim | Tràn dịch, tràn máu màng tim, vôi hóa màng tim | Đánh giá chèn ép tim, bệnh lý ác tính, bệnh hệ thống, viêm màng ngoài tim cấp và mạn, viêm màng ngoài tim co thắt |
3. Siêu âm tim qua thực quản
Chỉ định khi:
- Siêu âm âm tim thường qua thành ngực có chất lượng kém (bệnh nhân béo phì, bệnh phổi mạn tính, thở máy).
- Bệnh lý van tim phức tạp (bệnh van hai lá, van tim nhân tạo).
- Nghi ngờ viêm nội tâm mạc nhiễm trùng hoặc một số bệnh tim bẩm sinh.
- Xác địch huyết khối tiểu nhĩ do rung nhĩ.
| Bảng 6.5 Các thông số về rối loạn chức năng thâm trương thất trái | ||
| Thông số | Bất thường | Ý nghĩa lâm sàng |
| e’ | Giảm (< 8 cm/s vách, < 10 cm/s thành bên hoặc < 9 cm/s trung bình) | Chậm thư giãn thất trái |
| Tỷ lệ E/e^a | Cao (> 15) | Áp lực đổ đầy thất trái tăng |
| Thấp (< 8) | Áp lực đổ đầy thất trái bình thường | |
| Trung bình (8 – 15) | Chưa rõ ràng (cần đo đạt thêm các thống số khác) | |
| Tỷ lệ E/A^b | Hạn chế (> 2) | Áp lực đổ đầy thất trái tăng .
Quá tải thể tích. |
| Giảm thư giãn (< 1) | Chậm thư giãn thất trái.
Áp lực đổ đầy thất trái bình thường. |
|
| Bình thường (1 – 2) | Không thể kết luận (có thể giả bình thường). | |
| Dòng van hai lá trong nghiệm pháp Valsalva | Thay đổi từ kiểu ‘giả bình thường’ đến ‘giảm thư giãn’ (với giảm tỷ lệ E/A3 đến 0,5) | Áp lực đổ đầy thất trái tăng (bộc lộ bởi nghiệm pháp Valsalva) |
| Khoảng thời gian (A pulm – A mitral) | > 30 ms | Áp lực đổ đầy thất trái cao |
4. Natriuretic peptides (các peptide lợi niệu)
a. Cấu tạo
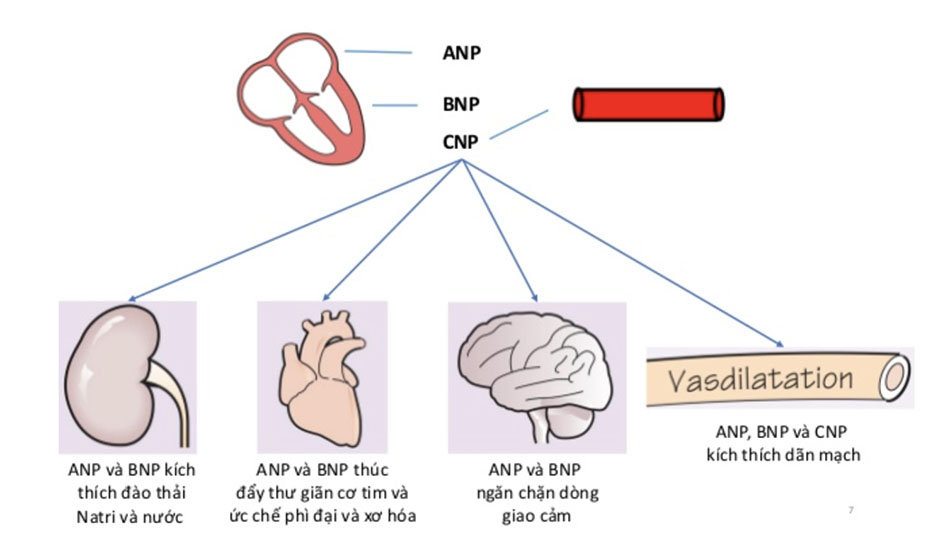
Ba peptid lợi niệu chủ yếu – peptide lợi niệu type A (ANP), peptid lợi niệu type B, peptid lợi niệu type C – đo ảnh hưởng của tình trạng quá tải thể tích hoặc hoạt tính giao cảm trên hệ tim mạch, ngoài ra còn có peptid lợi niệu type D (DNP), type V (VNP) và urodilatin ở thận.
Peptide natri lợi niệu tâm nhĩ (ANP – atrial natriuretic peptide) có 28 accid amin; Peptide natri lợi niệu não (BNP – Brain natriuretic peptide) có 32 acid amin; Peptide natri lợi niệu type C (CNP – C type natriuretic peptide) có 53 acid amin; và Peptide natri lợi niệu type D có 38 acid amin. Gen của ANP và BNP nằm trên cùng đoạn xa nhánh ngắn của nhiễm sắc thể số 1, gen của CNP nằm trên nhiễm sắc thể số 2; còn gen của DNP thì chưa giải mã được.
RNA thông tin dài 1kb giải mã tiền chất của ANP, sau khi được giải mã thì tiền chất của ANP có 126 acid amin. Sau đó, tiền chất ANP bị thủy phân mất đi đoạn 98 acid amin, còn lại 28 acid amin có gốc carboxyl trở thành ANP hoạt hóa. Nhiều tài liệu cho rằng proANP (tiền chất của ANP) có tính chất kích thích tố lợi niệu thải natri quan trọng hơn cả ANP. ANP hiện diện ở mô tâm thất bào thai và trẻ sơ sinh, trong tâm thất bị phì đại và ANP có ít ở mô tâm thất người trưởng thành. Tuy nhiên, tâm nhĩ người trưởng thành là nguồn dự trữ chính của ANP.
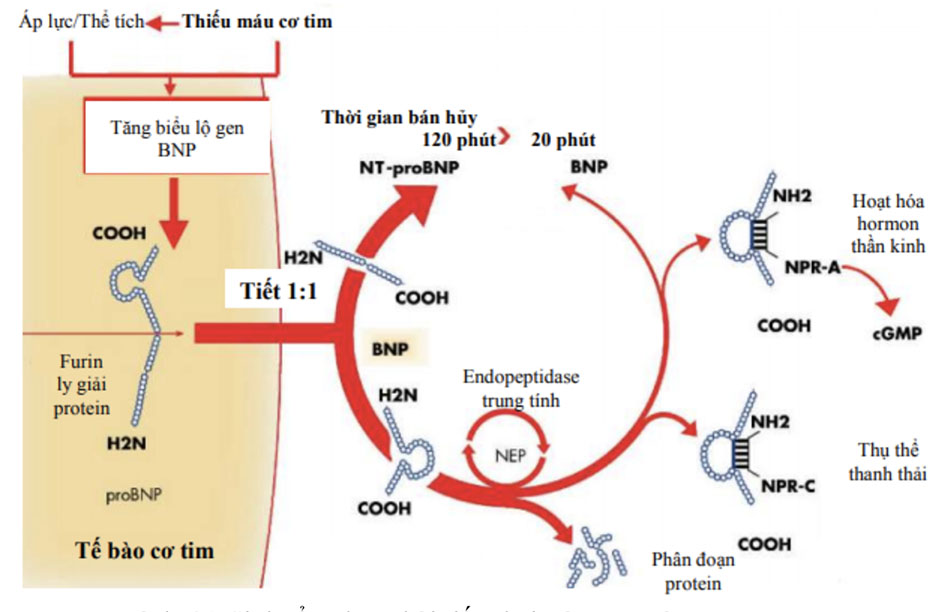
Gen biểu lộ BNP nằm trên nhiễm sắc thể số 1. Ở người khỏe mạnh gen này chủ yếu ở tâm nhĩ. Khi có tình trạng bệnh lý ảnh hưởng đến tâm thất như suy tim, gen biểu lộ BNP tại thất sẽ tăng cao. Sau khi giải mã gen BNP, sản phẩm đầu tiên là pre – proBNP1 – 134. Peptide này nhanh chóng tách bỏ 26 amino acid để tạo thành prohormon với 108 amino acid, proBNP1 – 108. Sau đó, proBNP1 – 108 được chia tách bởi các men thủy phân protein gồm furin và corin thành 2 phần: đoạn cuối 76 amino acid (NT – proBNP1 – 76) không hoạt tính sinh học và phân tử 32 amino acid (BNP1 – 32) có hoạt tính sinh học, đặc trưng bởi cấu trúc vòng 17 amino acid được liên kết bởi cầu nối disulfide cysteines.
Phân tử BNP1 – 32 được phân tách thành BNP3 – 32 bởi dipeptidyl peptidase IV hoặc BNP7 – 32 bởi peptidase meprin A. Các peptide này có ít hoạt tính sinh học. Sự khác biệt chính giữa NT – proBNP so với BNP là tính ổn định cao và không gắn kết với các thụ thể của phân tử NT – proBNP.
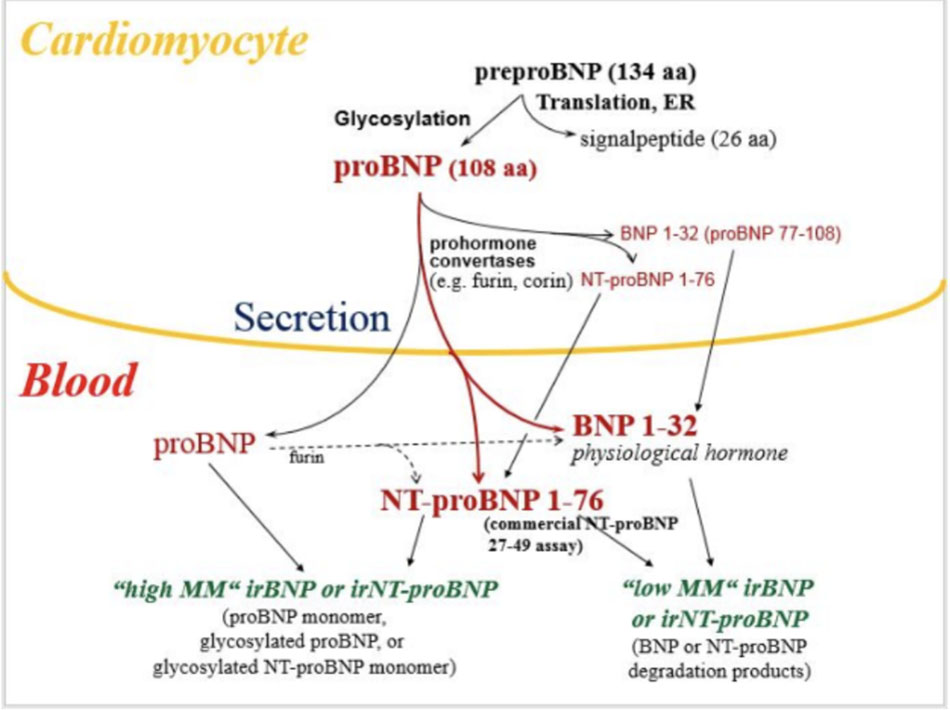
b. Sinh học
ANP được tổng hợp tại tâm nhĩ, tích trữ dưới dạng hạt và phóng thích vào tuần hoàn ngay cả khi chỉ có các kích thích nhẹ như tập thể dục. BNP tích trữ rất ít dưới dạng hạt, được tổng hợp và phóng thích từng đợt bởi tâm thất. Peptid bài niệu C được các tế bào nội mạc sản xuất và có thể có tác dụng bảo vệ trong tình huống tái cấu trúc sau nhồi máu cơ tim. Sau khi phóng thích vào tuần hoàn, ANP và BNP gắn kết các mô khác nhau gây dãn mạch, bài Natri niệu và lợi tiểu.
Quá tải thể tích hay áp lực thất trái làm tăng sức căng thành cơ tim, khởi động quá trình tổng hợp tiền chất peptid bài niệu type B (pre – proBNP). Pre – proBNP phân cắt thành proBNP và sau đó là BNP (dạng có hoạt tính), và dạng không có hoạt tính NT – proBNP. Các peptid bài niệu gắn vào các thụ thể chuyên biệt (NPRs) trên màng tế bào. NPR – A ưu tiên liên kết với ANP và BNP, NPR – B chủ yếu liên kết với CNP. Phức hợp peptid – thụ thể hoạt hóa men guanylyl cyclase, tạo ra các guanosin monophosphate (GMP) vòng. Tác dụng sinh học chính của BNP là thải natri niệu, lợi niệu, dãn mạch ngoại biên, ức chế hệ thống renin –angiotensin – aldosteron và thần kinh giao cảm. Ngoài ra, nồng độ BNP cũng còn ức chế sự co tế bào cơ thất, tiến trình tái dịnh dạng và viêm của tế bào cơ tim, cơ trơn. Phân tử BNP được thanh thải qua thận do gắn kết với thụ thể peptide thải natri niệu type C, cũng như bị phân cắt thành các phân đoạn protein thông qua hoạt động của men endopeptidase trung tính trong máu. Ngược lại, NT – proBNP không có cơ chế thanh thải chủ động mà nó được thải thụ động chính qua thận. Trước đây, các tác giả cho rằng NT – proBNP được thải duy nhất ở thận và phụ thuộc vào chức năng thận nhiều hơn BNP. Tuy nhiên, các nghiên cứu đã chứng minh rằng tỷ lệ bài tiết thận của BNP và NT – proBNP là như nhau và chỉ khoảng 15 – 20%.
| Bảng 6.4 Đặc điểm của BNP và NT – proBNP | ||
| BNP | NT – proBNP | |
| Acid amin | 32 | 76 |
| Trọng lượng phân tử (kdalton) | 3.5 | 8,5 |
| Thời gian bán hủy (phút) | 22 | 60-120 |
| Tính ổn định (giờ) | 6 | 72 |
Thanh thải:
|
Endopeptidase trung tính NRP – C |
Thận Thận |
| Tương quan với độ lọc cầu thận | Mạnh | |
| Tác dụng sinh học | Có | Không |
| Giới hạn lâm sàng | 0 – 5000 | 0 – 35000 |
Bệnh nhân suy tim có suy giảm hoạt tính BNP do thiếu hụt các dạng BNP hoạt tính cùng sự xuất hiện các phân tử đối kháng với hoạt tính BNP. Một số tác giả cho rằng đáp ứng bất thường với BNP của tế bào là một yếu tố gây trạng thái thiếu hụt tương đối BNP trong suy tim. Ngoài ra, sự tăng điều hòa của phosphodiesteases dẫn đến thanh thải nhanh chóng các tín hiệu dẫn truyền thứ phát (GMP vòng) mặc dù hoạt tính của các NPRs vẫn cao.
c. Ứng dụng trong chẩn đoán suy tim
Thường gia tăng khi có bệnh lý tim mạch hoặc có tăng áp lực trong buồng tim (ví dụ: rung nhĩ, thuyên tắc phổi, nguyên nhân ngoài tim như suy thận). Có nhiều nghiên cứu nhằm tìm ngưỡng trong loại trừ chẩn đoán suy tim của natriuretic peptides, chủ yếu là BNP và NT – proBNP. Ngưỡng chẩn đoán tùy thuộc vào triệu chứng cấp tính hay bệnh nhân có suy tim nặng hơn trên nền suy tim từ trước đó (suy tim cấp, nhập viện khoa cấp cứu) và bệnh nhân suy tim tiến triển từ từ (suy tim mạn, khám tại phòng khám).
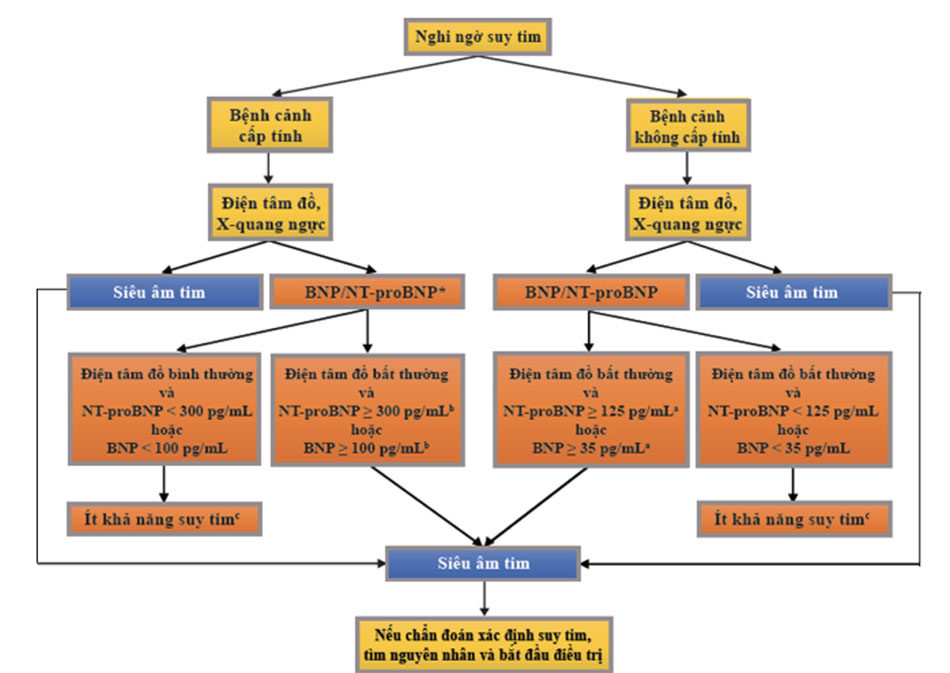
Trong bối cảnh không cấp, giới hạn trên bình thường của BNP là 35 pg/ml và của NT – proBNP là 125 pg/ml. Trong bối cảnh cấp tính, giới hạn bình thường có giá trị cao hơn nên được sử dụng của BNP là 100 pg/ml và của NT – proBNP là 300 pg/ml. Giá trị chẩn đoán loại trừ cao, nhưng giá trị chẩn đoán xác định thấp. Do đó, việc sử dụng các peptide được khuyến cáo để loại trừ suy tim, nhưng không phải để thiết lập chẩn đoán xác định.
| Bảng 6.4 Khuyến cáo sử dụng chất đánh dấu sinh học trong suy tim | |||
| Bệnh cảnh | Mức độ khuyến cáo | Mức độ chứng cứ | |
| Natriuretic peptides | |||
| Chẩn đoán hoặc loại trừ suy tim | Theo dõi, cấp cứu | I | A |
| Tiên lượng suy tim | Theo dõi, cấp cứu | I | A |
| Theo dõi điều trị trực tiếp | Theo dõi | IIa | B |
| Hướng dẫn điều trị suy tim mất bù cấp | Cấp cứu | IIb | C |
| Trong tổn thương cơ tim cấp | |||
| Phân tầng nguy cơ | Theo dõi, cấp cứu | I | A |
5. Điện tâm đồ (ECG)
Tìm nhồi máu cơ tim cấp hoặc cũ, thiếu máu cục bộ mới, túi phình thất trái với ST chênh lên ở hai đạo trình liên tiếp sau nhồi máu cơ tim hơn ba tháng, loạn nhịp chậm hoặc loạn nhịp nhanh đặc biệt với rung nhĩ đáp ứng thất nhanh, phì đại thất trái hoặc phải. Lớn nhĩ trái là dấu hiệu sớm của sự biến đổi độ chun dãn thất trái do phì đại thất trái và là biểu hiện thông thường của hở van hai lá và/hoặc hẹp van hai lá.
| Bảng 6.6 Các bất thường trên điện tâm đồ ở bệnh nhân suy tim | ||
| Bất thường | Nguyên nhân | Gợi ý lâm sàng |
| Nhịp nhanh xoang | Suy tim mất bù, thiếu máu, sốt, cường giáp | Đánh giá lâm sàng. Xét nghiệm chẩn đoán |
| Nhịp xoang chậm | Do thuốc chẹn beta, digoxin, verapamil, diltiazem, ivabradine.
Thuốc chống loạn nhịp Suy giáp. Hội chứng suy nút xoang. |
Xem lại thuốc điều trị. Xét nghiệm đánh giá |
| Nhịp nhanh nhĩ, rung nhĩ, cuồng nhĩ | Cường giáp, nhiễm trùng, bệnh van hai lá. Suy tim mất bù, nhồi máu cơ tim | Chậm dẫn truyền nhĩ thất, kháng đông, chuyển nhịp bằng thuốc, chuyển nhịp bằng sốc điện, cắt đốt điện sinh lý. |
| Nhịp nhanh thất | Thiếu máu cục bộ cơ tim, nhồi máu cơ tim, bệnh cơ tim, viêm cơ tim, hạ kali máu, hạ magne máu | Xét nghiệm đánh giá. Nghiệm pháp gắng sức, đánh giá tưới máu và/hoặc tính sống còn cơ tim, chụp mạch vành, thăm dò điện sinh lý tim, ICD |
| Nhồi máu cơ tim, thiếu máu cơ tim | Bệnh mạch vành | Siêu âm tim, đánh giá tưới máu và sống còn cơ tim, chụp mạch vành, tái tưới máu mạch vành |
| Sóng Q | Nhồi máu cơ im, block nhánh trái, bệnh cơ tim phì đại, kích thích sớm | Siêu âm tim, đánh giá tưới máu và sống còn cơ tim, chụp mạch vành |
| Phì đại thất trái | Tăng huyết áp, bệnh cơ tim phì đại, bệnh lý van động mạch chủ | Siêu âm tim, cộng hưởng từ tim |
| Block nhĩ thất | Nhồi máu cơ tim, ngộ độc digoxin, viêm cơ tim, bệnh u hạt, bệnh cơ tim di truyền (bệnh màng trong, bệnh do đột biến desmin), bệnh Lyme | Xem lại thuốc điều trị, bệnh hệ thống, tiền sử gia đình, xét nghiệm di truyền học, đặt máy tạo nhịp, ICD khi có chỉ định |
| Biện độ QRS thấp | Béo phì, khí phế thủng, tràn dịch màng tim, thoái hóa dạng bột | Siêu âm tim/cộng hưởng từ tim, XQ ngực, sinh thiết nội mạc cơ tim |
| QRS > 120ms hoặc hình ảnh block nhánh trái | Mất đồng bộ về điện học hoặc cơ học | Siêu âm tim, CRT – D, CRT – P |
6. X – quang ngực thẳng
Nhằm tìm các dấu hiệu sau như co thắt mạch máu thùy dưới và dãn mạch ở thùy trên. Dấu hiệu này gặp khi tăng áp lực tĩnh mạch phổi do suy thất trái, hẹp van hai lá, bệnh phổi tắc nghẽn mạn, phim X – quang chụp khi bệnh nhân nằm.
Phù phổi mô kẽ: đám mờ quanh rốn phổi, đường Kerley B hoặc A do vách liên thùy phù và dày lên. Đường Kerley B thường định vị ở ngoại vi vùng thùy dưới và là những đường ngang 1 – 3 cm và dày không quá 0,1 – 0,2 cm. Đường Kerley B thường xuất hiện thoáng qua khi áp lực tĩnh mạch phổi đạt khoảng 22 cmHg. Đường Kerley A ít gặp do mạch lympho dày lên và biểu hiện bằng những đường mỏng không nhánh, dài vài cm và kéo dài từ rốn đến phổi. Đường Kerley A và B xuất hiện thoáng qua nếu do suy thất trái và tồn tại lâu dài nếu kênh lympho bị tắc do khối u, nghẹt do bụi trong bệnh bụi phổi (pneumoconiosis), hoặc bị dày lên do viêm phế nang gây xơ hóa hoặc bệnh nhiễm sắt (hemochromatosis). Đường Kerley A và B cũng có thể do nhiễm siêu vi hoặc do nhạy cảm thuốc.
Phù phổi phế nang: hình cánh bướm, có thể một bên.
Tràn dịch màng phổi: mất góc sườn hoành, thường gặp bên phải hơn bên trái.
Dày rãnh liên thùy do ứ dịch, thấy rõ ở phim nghiêg.
Dãn động mạch phổi phải hoặc trái ở trung tâm. Bóng tim to. Bóng tim bình thường trong suy tim do:
- Nhồi máu cơ tim cấp ở bệnh nhân thiếu máu cục bộ cơ tim. Tĩm dãn có thể xảy ra không theo chiều ngang và bệnh nhân có nhồi máu cơ tim cũ một hoặc nhiều lần có biểu hiện suy tim nhưng bóng tim trên X – quang bình thường. Trường hợp này vùng giảm động hoặc loạn động có thể quan sát hoặc sờ thấy trên thành ngực và trên siêu âm tim.
- Hẹp van hai lá.
- Suy tim chủ yếu do rối loạn chức năng tâm trương.
Dấu hiệu giả suy tim trên X – quang cần loại trừ:
- Nhiễm trùng phổi, gồm tất cả nguyên nhân gây hội chứng nguy kịch hô hấp người lớn.
- Phù phổi dị ứng (heroin, nitrofurantoin).
- Viêm bạch huyết (lupusphagitis), ung thư di căn.
- Hội chứng ure huyết cao.
- Ứ đọng protein phế nang (alveolar proteniosis)…
7. Xét nghiệm thường quy
Xét nghiệm cơ bản ở bệnh nhân nghi suy tim gồm Hct để loại trừ thiếu máu là yếu tố thúc đẩy làm xấu thêm. Điện giải đồ để loại trừ hạ Natri máu. Hạ Natri máu có thể do thuốc lợi tiểu hoặc do ứ nhiều nước tự do. Hoạt hóa hệ RAA và arginine vasopressin góp phần hạ Natri máu do kích thích trung tâm khát và ảnh hưởng đến độ thanh thai giải nước tự do. Hạ Natri máu là yếu tố tiên lượng xấu, mặc dù có thể cải thiện nhờ thuốc ức chế men chuyển. Nồng độ Kali máu có thể giảm do lợi tiểu mất Kali hoặc nồng độ Kali máu có thể tăng do rối loạn chức năng thận bởi thuốc ức chế men chuyển làm xấu đi.
Đánh giá chức năng thận bằng creatinine huyết, rối loạn chức năng thận nhẹ có thể nặng thêm khi dùng ức chế men chuyển và sự tăng creatinine huyết đáng kể có thể hồi phục sau khi ngưng ức chế men chuyển hoặc tăng tưới máu thận do cung lượng tim được cải thiện.
Xét nghiệm chức năng gan bất thường khi bệnh nhân có áp lực thất phải tăng và sung huyết gan mãn. Men gan tăng, bilirubin tăng và TQ kéo dài thường gặp khi giảm chức năng tổng hợp của gan. SGOT, SGPT có thể tăng 5 đến 10 lần bình thường và sẽ trở lại bình thường sau điều trị hiệu quả. Tăng bilirubin máu nhẹ và phosphatase kiềm thường gặp. Một số hiếm trường hợp, có thể có xơ gan tim với giảm albumin huyết và TQ kéo dài. Cần theo dõi thận trọng chức năng gan và thận để chọn lựa thuốc điều trị suy tim sung huyết do có nhiều ảnh hưởng đến chức năng thận và gan.
8. Protein C reactive ( protein phản ứng C)
CRP được tổng hợp bởi tế bào gan chủ yếu do kích thích từ Interleukin 6. CRP tăng cao đáng kể trong thời gian ngắn sau sự khởi đầu của một quá trình viêm. Tuy nhiên, CRP không đặc hiệu và thường tăng trong các tình trạng nhiễm trùng, các bệnh viêm, hội chứng vành cấp, hút thuốc lá, ung thư tiến triển. CRP giảm phóng thích NO và tăng giải phóng endothelin – 1 và các phân tử bám dính nội mạc.
Tổn thương cơ tim dẫn đến tăng sản xuất các cytokine tiền viêm (tumor necrosis factor α, interleukin 6 và interleukin 18) dẫn đến suy chức năng cơ tim. Cung lượng tim giảm gây giảm tưới máu hệ cơ xương, kích hoạt bạch cầu đơn nhân để sản xuất các cytokine tiền viêm, tiếp tục làm suy yếu chức năng tim.
Tóm lại, CRP có lẽ là dấu hiệu viêm quan trọng nhất và được phân tích thường xuyên trong thực hành. Ích lợi của CRP đã được xác nhận trong việc dự đoán sự phát triển suy tim trong các quần thể có nguy cơ thấp và cao, cũng như giá trị tiên lượng ở bệnh nhân suy tim mạn tính. Trong thực hành, diễn giải nồng động CRP có phần bị cản trở bởi thực tế là nhiều ngưỡng chẩn đoán khác nhau đã được sử dụng trong nhiều nghiên cứu khác nhau, làm cho việc giải thích một tình huống tăng CRP cụ thể có thể bị khó khăn. Xác định các ứng dụng lâm sàng thực tế của hs CRP đòi hỏi phải tiếp tục với các nghiên cứu thống nhất sử dụng các xét nghiệm và ngưỡng chẩn đoán giống nhau.
9. Troponin
Hoại tử tế bào cơ tim xảy ra trong suy tim và có thể là sự phản ánh đoạn cuối con đường chung của tiến triển dai dẳng của suy tim. Mặc dù nồng độ troponin tim là dấu hiệu rất có giá trị xác nhận tổn thương tế bào cơ trong nhồi máu cơ tim, các sinh lý bệnh cơ bản gây tăng troponin trong suy tim có thể khác biệt với những cơ chế trong hội chứng vành cấp. Nhiều cơ chế, bao gồm viêm, xơ hóa mô kẽ, tăng sức căng thành, stress oxy hóa và hoạt hóa các neurohormonal, chịu trách nhiệm cho quá trình tái cấu trúc bất lợi đưa đến suy tim tiến triển. Troponin là một protein cấu trúc của tim tham gia vào phức hợp troponin – tropomyosin , với một số lượng nhỏ trong cytosol. Tăng nhẹ nồng độ troponin đã được ghi nhận trong một số bệnh tim mạch, bao gồm suy tim. Giả thuyết giải thích tại sao nồng độ troponin có thể tăng trong suy tim, ngay cả trong trường hợp không có thiếu máu cục bộ, bao gồm chấn thương cơ tim, mất toàn vẹn của màng tế bào, áp lực quá mức dẫn đến thiếu máu dưới nội mạc, apoptosis, hoặc phổi hợp các cơ chế.
Hai cơ chế chính làm tăng troponin tim là sự căng cơ tim và chết tế bào cơ tim:
- Sự căng cơ tim: sự quá tải thể tích và áp lực ở cả hai buồng thất dẫn đến tăng sức căng thành quá mức gọi là sự căng cơ tim, từ đó phá huỷ vi sợi cơ tim và tăng troponin tim. Ngoài ra, tăng troponin tim còn do sự tăng tiền tải, thiếu máu cơ tim.
- Chết tế bào cơ tim: các nhà nghiên cứu ghi nhận có sự liên kết giữa sức căng thành và chết chương trình của tế bào cơ tim. Sự mất cơ tim tiến triển đóng vai trò nổi bật trong sự thoái hoá cơ tim. Điều này giải thích tiên lượng xấu ở bệnh nhân suy tim tăng troponin. Ngoài ra các yếu tố góp phần làm chết tế bào cơ tim bao gồm: tăng kích hoạt hệ renin – angiostensin, kích thích giao cảm và hoạt hoá các chất trung gian gây viêm.
Kết luận:
- Các cận lâm sàng rất cần thiết trong việc góp phần chẩn đoán chính xác suy tim, không chỉ vậy mà còn hỗ trợ tìm nguyên nhân, điều trị và tiên lượng bệnh.
- Sự phát triển của nhiều chất chỉ điểm sinh học – đặc biệt là các peptide lợi niệu là chất chỉ điểm tiêu chuẩn đã tạo ra nhiều công cụ có giá trị để chẩn đoán và điều trị suy tim.
- Cần kết hợp các chất chỉ điểm sinh học và các xét nghiệm để đưa ra chẩn đoán, điều trị và tiên lượng thích hợp nhất.
Các tiêu chuẩn chẩn đoán suy tim
1. Tiêu chuẩn chẩn đoán suy tim theo Framingham
Để xác định chẩn đoán suy tim ít nhất có hai tiêu chuẩn chính hoặc một tiêu chuẩn chính và hai tiêu chuẩn phụ.
| Bảng 1.13 Tiêu chuẩn chẩn đoán suy tim theo Framingham | |
| Tiêu chuẩn chính | Tiêu chuẩn phụ |
| Cơn khó thở kịch phát về đêm hoặc khó thở phải ngồi.
Phồng tĩnh mạch cổ. Ran ở phổi. Tim to. Phù phổi cấp. Tiếng ngựa phi T3. Áp lực tĩnh mạch hệ thống tăng (> 16 cmH 2 O) Thời gian tuần hoàn > 25 giây. Phản hồi gan tĩnh mạch cổ dương tính. |
Phù cổ chân.
Ho về đêm. Khó thở khi gắng sức. Gan to. Tràn dịch màng phổi. Dung tích sống giảm 1/3 so với bình thường. Nhịp nhanh (≥ 120 lần/phút). |
| Tiêu chuẩn chính hoặc phụ: giảm cân ≥ 4,5 kg trong 5 ngày điều trị suy tim | |
Tiêu chuẩn của Framingham tương đối đơn giản và dễ sử dụng, không bao gồm siêu âm tim để đánh giá, độ nhạy rất cao nhưng độ đặc hiệu lại thấp, khả năng tiên đoán âm tốt. Điều này tương tự trong tiêu chuẩn Boston và Duke, khi đó cần có siêu âm để xác định chẩn đoán. Do vậy trên lâm sàng dùng tiêu chuẩn Framingham, Boston, Duke để sàng lọc ban đầu những bệnh nhân có khả năng suy tim thì có vẻ hợp lý hơn.
2. Tiêu chuẩn chẩn đoán suy tim theo Hiệp hội Tim mạch châu Âu (ESC)
a. ESC 2012
| Tiêu chuẩn | Chẩn đoán suy tim có phân suất tống máu giảm | Chẩn đoán suy tim có phân suất tống máu bảo tồn |
| 1 | Triệu chứng cơ năng điển hình của suy tim | Triệu chứng cơ năng điển hình của suy tim |
| 2 | Triệu chứng thực thể điển hình của suy tim | Triệu chứng thực thể điển hình của suy tim |
| 3 | Giảm phân suất tống máu thất trái | Phân suất tống máu thất trái bình thường hoặc giảm nhẹ, không dãn thất trái |
| 4 | Bệnh tim cấu trúc phù hợp (phì đại thất trái, dãn nhĩ trái) và/hoặc rồi loạn chức năng tâm trương. |
Tiêu chuẩn chẩn đoán suy tim theo ESC bắt buộc phải có bằng chứng về rối loạn chức năng thất trái tâm thu hoặc tâm trương, thường sử dụng là siêu âm tim. Bệnh nhân có triệu chứng suy tim thường vào viện vì hai bệnh cảnh chính là suy tim cấp vào khoa cấp cứu, và suy tim mạn tính tiến triển từ từ vào khám ngoại trú. ESC đã đưa ra lưu đồ chẩn đoán suy tim như sau và được ứng dụng rộng rãi trong thực hành lâm sàng:
b. ESC 2016
| Tiêu chuẩn | Suy tim EF giảm (HFrEF) | Suy tim EF khoảng giữa (HFmrEF) | Suy tim EF bảo tồn (HFpEF) |
| 1 | Triệu chứng ± dấu hiệu (dấu hiệu có thể không có trong giai đoạn sớm của suy tim hoặc ở những bệnh nhân đã điều trị lợi tiểu) | Triệu chứng ± dấu hiệu (dấu hiệu có thể không có trong giai đoạn sớm của suy tim hoặc ở những bệnh nhân đã điều trị lợi tiểu) | Triệu chứng ± dấu hiệu (dấu hiệu có thể không có trong giai đoạn sớm của suy tim hoặc ở những bệnh nhân đã điều trị lợi tiểu) |
| 2 | EF < 40% | EF 40-49% | EF ≥ 50% |
| 3 | 1. Peptide lợi niệu Na tăng (BNP > 35 pg/ml, NT – proBNP > 125 pg/ml).
2. Có ít nhất 1 trong các tiêu chuẩn thêm vào sau:
|
1. Peptide lợi niệu Na tăng (BNP > 35 pg/ml, NT – proBNP > 125 pg/ml).
2. Có ít nhất 1 trong các tiêu chuẩn thêm vào sau:
|
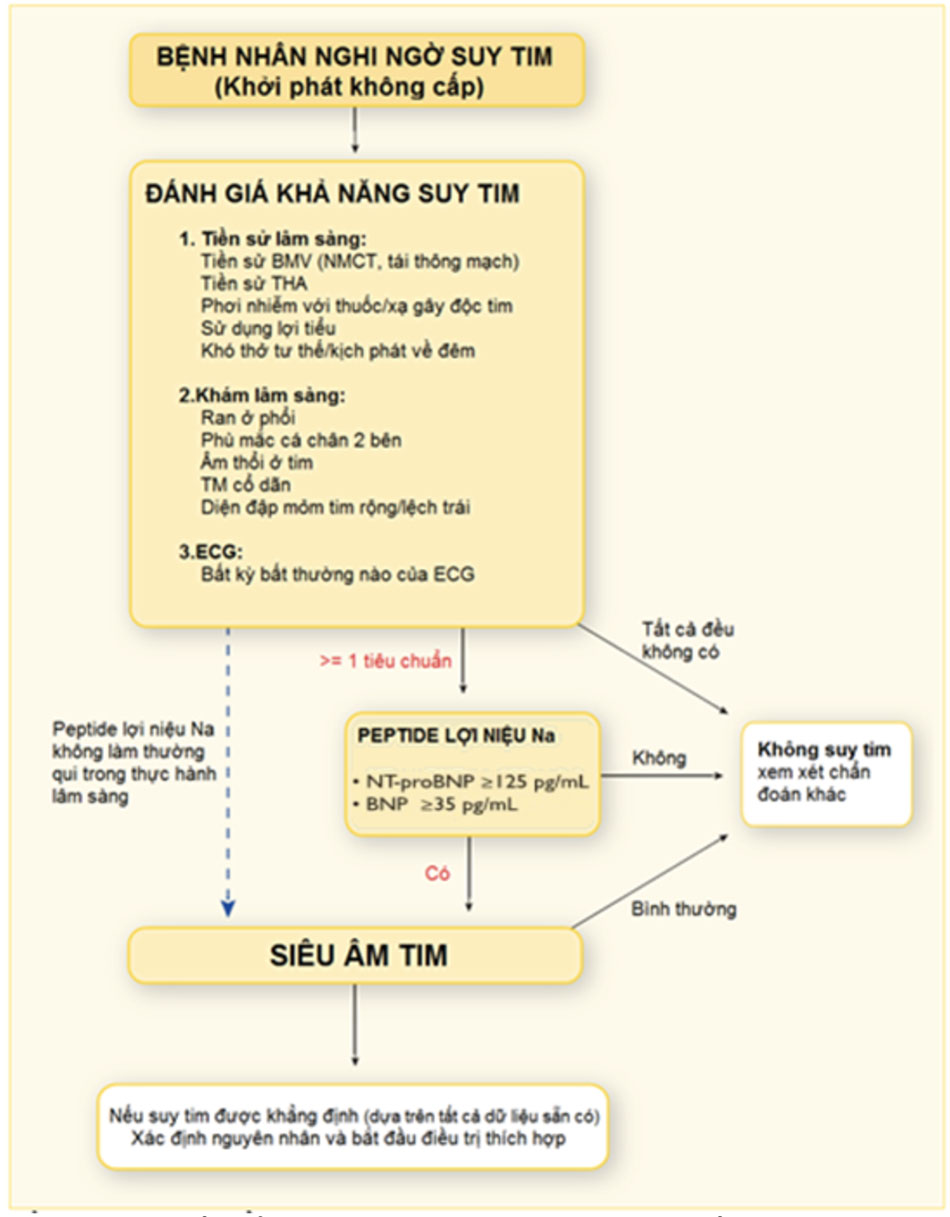
Khuyến cáo trên các tiêu chuẩn về chẩn đoán suy tim của ESC 2016 có vài điểm khác biệt so với khuyến cáo của ESC 2012: triệu chứng và dấu hiệu suy tim nay gộp lại thành một tiêu chuẩn (thay vì hai tiêu chuẩn như trước đây). Peptide lợi niệu Na là một tiêu chuẩn riêng và tiêu chuẩn thứ ba là có bất thường cấu trúc/chức năng thất trái (dày thất trái, lớn nhĩ trái, rối loạn chức năng tâm trương). EF sẽ giúp phân làm ba loại suy tim và khi bệnh nhân có EF < 40% cùng với triệu chứng và/hoặc dấu hiệu suy tim thì không cần các tiêu chuẩn khác.
Định nghĩa trên là đích đến cho câu trả lời có suy tim hay không, nhưng để có được những thành tố trong các tiêu chuẩn trên, cần có một qui trình để đi đến đích. Chúng ta cùng quan sát lưu đồ dưới đây bao gồm trình tự các bước cần thực hiện để khẳng định chẩn đoán:
Độ nặng của suy tim
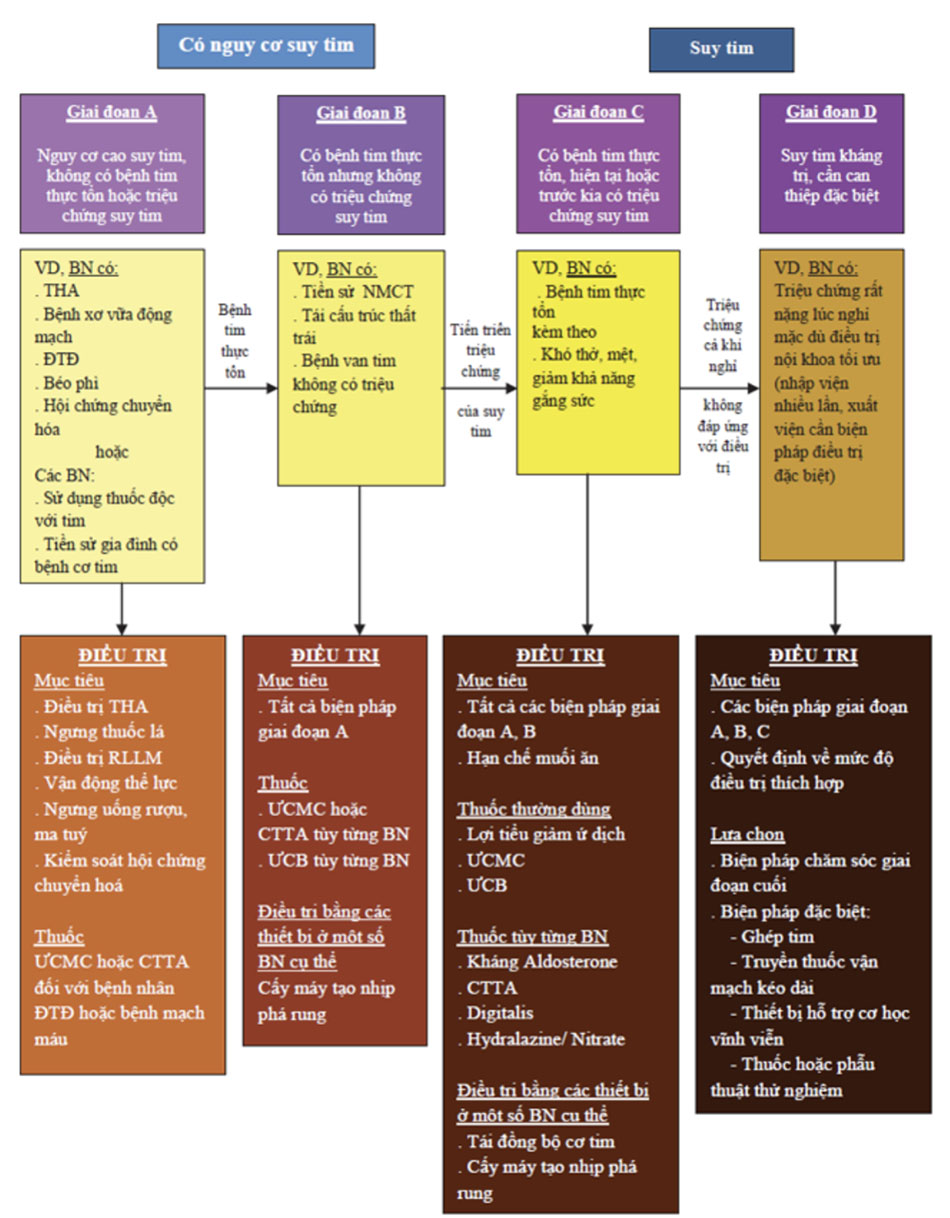
Việc phân độ suy tim đóng vai trò hết sức quan trọng trong việc điều trị và tiên lượng bệnh nhân suy tim. Đối với bệnh nhân suy tim mạn tính, thường sử dụng trên lâm sàng là phân độ chức năng tim trong suy tim theo NYHA và phân giai đoạn suy tim theo AHA/ACC. Sự so sánh giữa hai phân độ này được liệt kê trong bảng sau:
| Bảng 7.1 So sánh phân giai đoạn suy tim theo AHA/ACC và phân độ chức năng tim trong suy tim theo NYHA | |||
| Phân giai đoạn suy tim theo AHA/ACC | Phân độ chức năng tim trong suy tim theo NYHA | ||
| A | Nguy cơ cao suy tim, nhưng không có bệnh lý cấu trúc tim và không có triệu chứng cơ năng suy tim. | ||
| B | Có bệnh lý cấu trúc tim nhưng chưa có triệu chứng cơ năng của suy tim. | I | Không hạn chế hoạt động thể lực. Các hoạt động thông thường không gây mệt, khó thở hay hồi hộp. |
| C | Có bệnh lý cấu trúc tim, có triệu chứng cơ năng của suy tim trong hiện tại hoặc tiền sử, đáp ứng với điều trị nội khoa. | I | Không hạn chế hoạt động thể lực. Các hoạt động thông thường không gây mệt, khó thở hay hồi hộp. |
| II | Hạn chế nhẹ hoạt động thể lực. Thoải mái khi nghỉ ngơi, nhưng những hoạt động thông thường gây mệt, khó thở hay hồi hộp. | ||
| III | Hạn chế rõ hoạt động thể lực . Thoải mái khi nghỉ ngơi, nhưng hoạt động dưới mức thông thường gây mệt, khó thở hay hồi hộp. | ||
| IV | Không vận động thể lực nào mà không gây khó chịu. Triệu chứng cơ năng của suy tim xảy ra ngay khi nghỉ ngơi, chỉ một vận động thể lực, triệu chứng cơ năng gia tăng. | ||
| D | Suy tim kháng trị, đòi hỏi phải có các biện pháp điều trị đặc biệt. | IV | Không vận động thể lực nào mà không gây khó chịu. Triệu chứng cơ năng của suy tim xảy ra ngay khi nghỉ ngơi, chỉ một vận động thể lực, triệu chứng cơ năng gia tăng. |
Phân độ suy tim theo NYHA chú trọng đến khả năng gắng sức của bệnh nhân. Còn phân giai đoạn theo AHA/ACC chú trọng đến sự hình thành và tiến triển của suy tim.
Phân độ suy tim theo NYHA có ưu điểm đơn giản, dễ vận dụng, có thể áp dụng cho các bệnh tim khác nhau, có ích trong nhiều nghiên cứu về tỷ lệ bệnh suất mới mắc, tiên lượng, tử suất, diễn tiến, hậu quả của biện pháp điều trị. Tuy nhiên, nó vẫn có khuyết điểm như mô tả rối loạn chức năng mơ hồ, bỏ qua dấu hiệu thực thể và các thăm dò huyết động nên không đánh giá được những rối loạn không triệu chứng.
Ngoài ra, dựa dựa vào sự suy giảm nhận oxy tối đa khi gắng sức để sắp độ hoạt động, có ý nghĩa về mặt tiên lượng. Phương pháp này có ưu điểm là đo lường được sự trao đổi khí liên quan đến gắng sức, do đó cho một định lượng khách quan và tính lập lại tốt hơn (reproducible). Tuy nhiên, cách phân độ này lại khó vận dụng trên lâm sàng và ít phổ biến.
| Bảng 7.2 Phân độ chức năng tim trong suy tim sung huyết theo sự tiêu thụ Oxy tối đa (VO 2 max) | ||||
| Độ | Độ nặng | VO 2 max, mL/kg/phút | Ngưỡng yếm khí, mL/kg/phút | Chỉ số tim tối đa, L/phút/m 2 |
| A | Không đến nhẹ | >20 | > 14 | > 8 |
| B | Nhẹ đến trung bình | 16 – 20 | 11 – 14 | 6 – 8 |
| C | Trung bình đến nặng | 10 – 15 | 8 – 11 | 4 – 6 |
| D | Nặng | 6 – 9 | 5 – 8 | 2 – 4 |
| E | Rất nặng | < 6 | 3 – 4 | < 2 |
Điều trị suy tim
1. Tổng quan điều trị suy tim có EF giảm
a. Mục tiêu điều trị:
- Giảm triệu chứng cơ năng và thực thể, cải thiện chất lượng cuộc sống, tăng khả năng họat động.
- Giảm tỷ lệ nhập viện vì suy tim.
- Giảm tỷ lệ tử vong, kéo dài tuổi thọ.
b. Mục đích điều trị:
- Giải quyết nguyên nhân căn bản: tùy từng nguyên nhân mà có phương pháp điều trị nội khoa hay ngoại khoa thích hợp.
- Giải quyết yếu tố thúc đẩy: phát hiện, điều trị, phòng ngừa các yếu tố thúc đẩy. Điều trị các bệnh kết hợp.
Kiểm soát tình trạng suy tim ứ huyết
- Tăng sức co bóp cơ tim.
- Giảm công cơ tim.
- Kiểm soát ứ muối – nước
c.Biện pháp điều trị không dùng thuốc:
Điều chỉnh lối sống.
Cân bằng dịch:
- Hạn chế muối, < 2 – 3g/ngày, tùy từng trường hợp. Có thể thay Natri bằng Kali nhưng phảỉ cực kỳ cẩn thận theo dõi.
- Theo dõi cân nặng mỗi ngày để phát hiện sớm thừa dịch.
- Nước uống theo mức độ khát, < 1,5 – 2 lít/ngày. Hạn chế nước sao cho Natri máu > 130 mmol/l Vận động thể lực: tùy trường hợp cụ thể Những biện pháp khác: thở oxy, lọc máu, chủng ngừa, thở áp lực dương (bệnh nhân có cơn ngưng thở khi ngủ), theo dõi sát bệnh nhân ngoại trú.
d. Điều trị bằng thuốc cho bệnh nhân suy tim có EF giảm
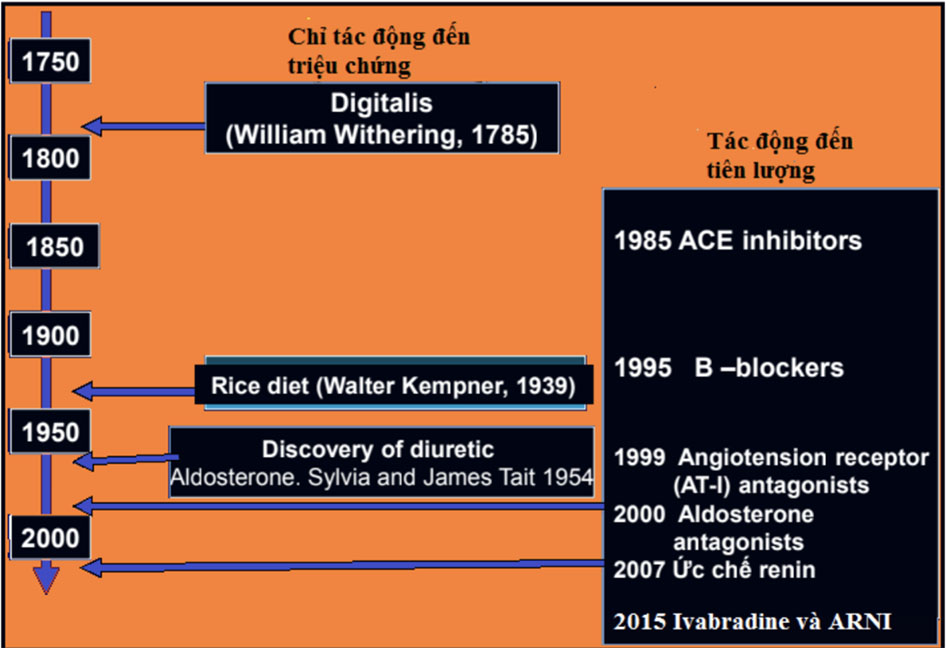
Điều trị suy tim mạn đã có lịch sử hơn 200 năm. Có thể liệt kê thứ tự các thuốc điều trị suy tim theo thời gian như sau:
- Năm 1785: William Withering dùng digoxin để điều trị suy tim.
- Năm 1939: Walter Kemper đề xuất chế độ ăn kiêng để điều trị suy tim.
- Năm 1954: Sylvia và James Tait phát hiện ra thuốc lợi tiểu.
- Năm 1985: dùng thuốc ức chế men chuyển angiotensin để điều trị suy tim.
- Đầu những năm 90, bắt đầu nghiên cứu dùng thuốc chẹn β trong điều trị suy tim và đến năm 1999 đã có đủ chứng cứ dùng thuốc chẹn β trong điều trị suy tim.
- Năm 1999: dùng thuốc chẹn thụ thể angiotensin trong điều trị suy tim.
- Năm 2000: xác nhận vai trò của thuốc đối kháng thụ thể mineralocorticoid trong điều trị suy tim.
- Năm 2007, nghiên cứu sử dụng thuốc ức chế renin trong điều trị suy tim.
- Năm 2015, ivabradine và ARNI được FDA Mỹ chấp nhận trong chỉ định điều trị suy tim với những lợi ích đã được chứng minh.
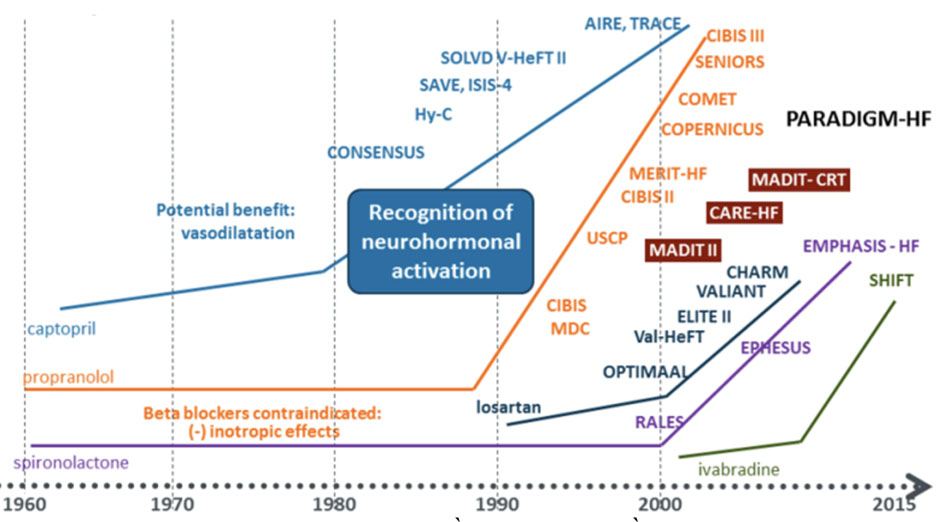
Có thể sắp xếp các loại thuốc điều trị suy tim theo hiệu quả như sau:
- Các thuốc có lợi ích, cải thiện được tỷ lệ tử vong:
-
- Chẹn thụ thể angiotensin và neprilysin.
- Ức chế men chuyển angiotensin/chẹn thụ thể angiotensin.
- Chẹn β.
- Đối kháng thụ thể mineralocorticoid.
- Chẹn kênh I f .
-
- Các thuốc cải thiện triệu chứng:
-
- Lợi tiểu.
- Digoxin liều thấp.
- Nitrates.
-
- Các thuốc có thể gây hại, cần cân nhắc dùng tùy từng trường hợp:
-
- Các thuốc tăng co bóp cơ tim, giống giao cảm.
- Thuốc chống loạn nhịp.
- Chẹn kênh calci.
- Digoxin liều cao.
-
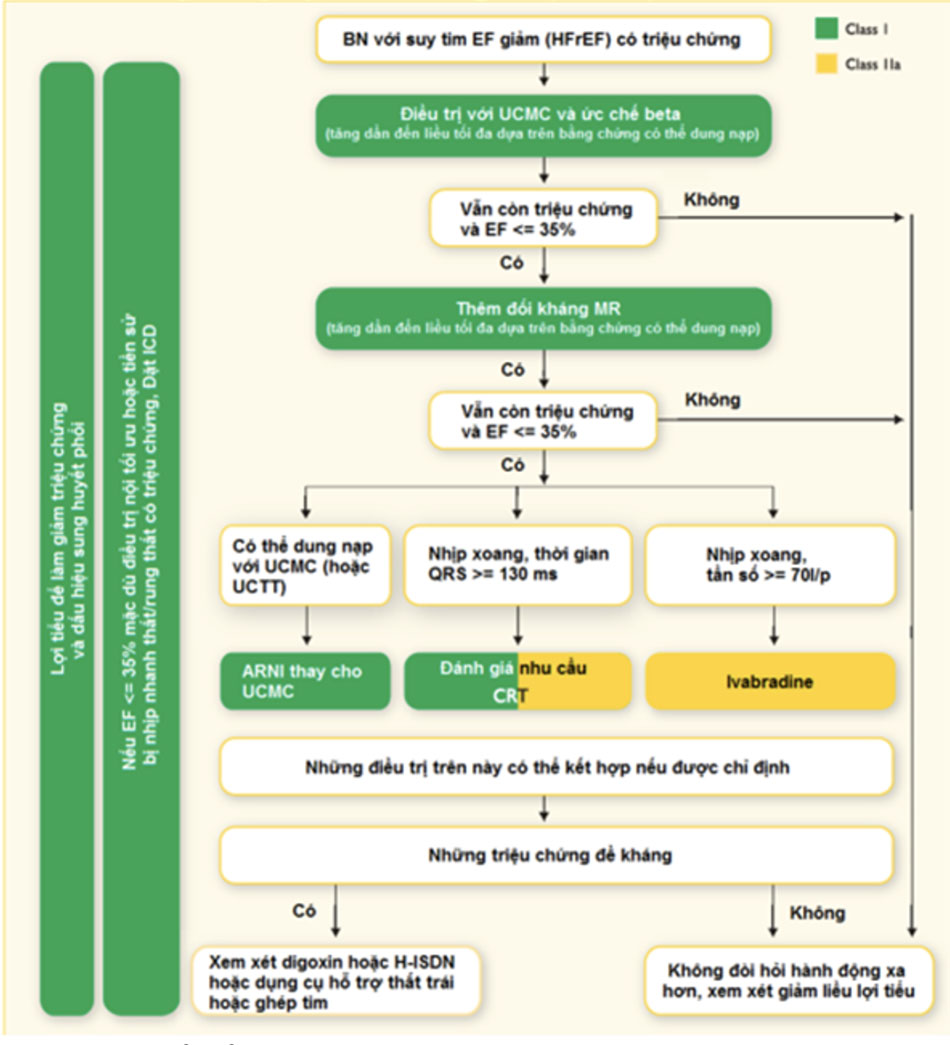
e. Hướng dẫn điêu trị suy tim theo các khuyến cáo ESC, AHA/ACC, VNHA
Tùy từng giai đoạn suy tim mà có chiến lược điều trị cụ thể.
Kết luận:
1. Điều chỉnh lối sống và dùng thuốc đều đặn với sự theo dõi sát là biện pháp hàng đầu trong điều trị suy tim.
2. Khi tình trạng suy tim nặng hơn sẽ cần đến các can thiệp đặc biệt.
3. Thầy thuốc phải áp dụng linh hoạt các khuyến cáo trên từng bệnh nhân có các vấn đề riêng, cụ thể.
2. Thuốc ức chế hệ hệ renin – angiotensin trong điều trị suy tim
a. Vài nét lịch sử của thuốc ức chế men chuyển angiotensin (ACEi) và chẹn thụ thể angiotensin (ARBs) trong điều trị suy tim
Lịch sử của các chất ACEi bắt đầu nǎm 1954, khi tầm quan trọng của enzym này được thừa nhận lần đầu.
Nǎm 1968, hợp chất đầu tiên có khả nǎng ức chế chuyển angiotensin I thành angiotensin II được tách chiết từ nọc rắn Bothrops jararaca chứa yếu tố tăng cường tác dụng bradykinin bằng cách ức chế kininase II.
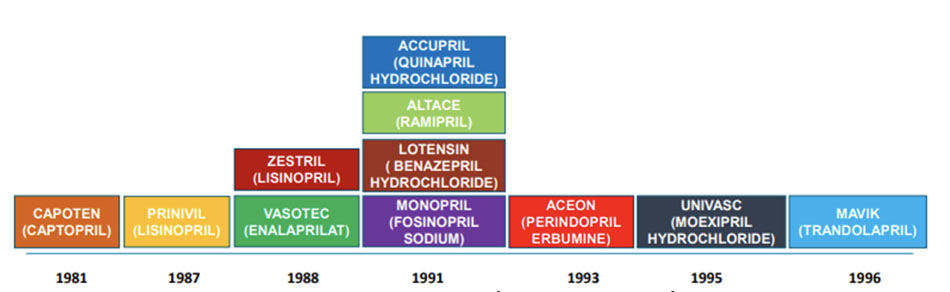
Năm 1977, chất ACEi đường uống đầu tiên được khám phá là captopril. Đến năm 1981, captopril trở thành chất ACEi đầu tiên được phép sử dụng trên lâm sàng.
Sau đó, lần lượt các chất ACEi tiếp theo ra đời và được FDA chấp nhận: lisinopril (1987, 1988); enalapril (1988); quinapril, ramipril, benazepril, fosinopril (1991), perindopril (1993), moexipril (1995), trandolapril (1996).
Nhiều công trình lớn đã chứng tỏ được lợi ích của thuốc ACEi trong điều trị suy tim:
- 1987: CONSENSUS (Cooperative North Scandinavian Enalapril Survival Study).
- 1991: V – HeFT II (Vasodilator – Heart Failure Trial II), SOLVD (The Studies of Left Ventricular Dysfunction).
- 1992: SAVE ( Survival And Ventricular Enlargement Trial).
- 1993: AIRE (Acute Infarction Ramipril Efficacy).
- 1994: ATLAS (Assessment of Treatment with Lisinopril and Survival).
- 1995: TRACE (Trandolapril Cardiac Evaluation).
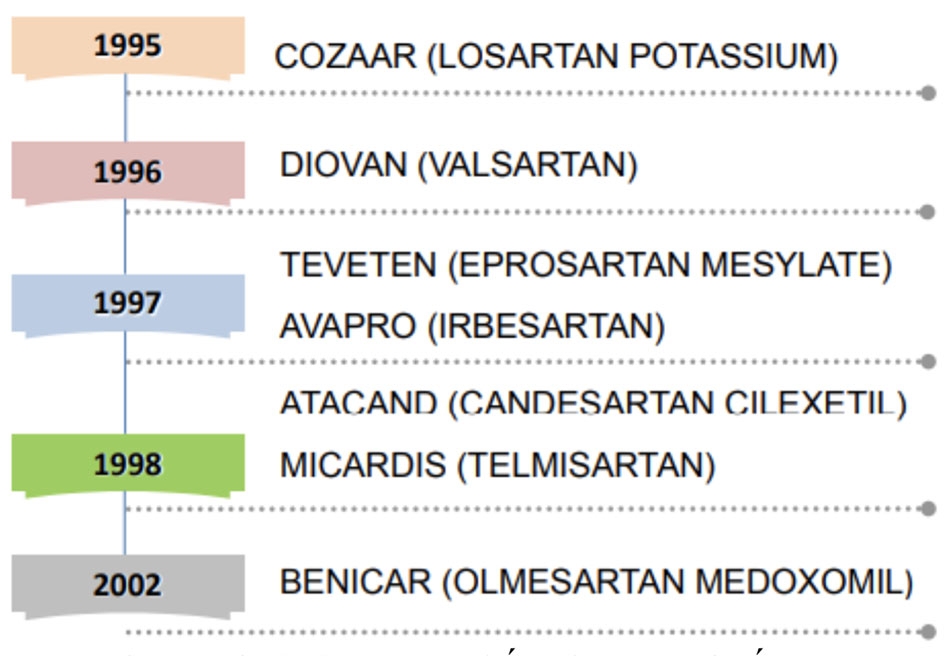
Thuốc ARBs ra đời muộn hơn rất nhiều so với thuốc ACEi, nhưng không vì vậy mà nó bị bỏ lại so với người anh em của minh. Từ thập niên 90, các chất đối kháng thụ thể type 1 của angiotensin II đã được sáng chế và thử nghiệm, lần lượt các thuốc ARBs được công nhận trên lâm sàng: lorsartan (1995), valsartan (1996), eprosartan và irbesartan (1996), candesartan và telmisartan (1997), olmesartan (2002).
Các công trình thử nghiệm cũng đã cho thấy lợi ích của thuốc ARB trong điều trị bệnh nhân suy tim:
- 1986: ELITE I (Evaluation of Losartan In The Elderly I).
- 1997: ELITE II.
- 2001: Val – HeFT (Valsartan in Heart Failure Trial).
- 2003: CHARM (Candesartan in Heart Failure: Assessment of reduction in Mortality and Morbidity) – Alternative, VALIANT (Valsarta in Acute Myocardial Infraction Trial).
Thập niên 80 – 90 đánh dấu sự ra đời của quan niệm mới về tiến trình suy tim, đó là sự gia tăng hoạt động của hệ thần kinh giao cảm và hệ thống renin – angiotensin: cơ chế thần kinh thể dịch. Những biện pháp làm giảm sự hoạt hóa thần kinh thể dịch sẽ kéo dài đời sống và đem lại hiệu quả lâu dài về mặt huyết động cho bệnh nhân suy tim. Như vậy, thuốc ức chế hệ renin – angiotensin đã trở thành “hòn đá tảng” trong việc điều trị bệnh nhân suy tim.
b. Tác động của hệ renin – angiotensin lên tiến trình suy tim và cơ chế tác động của thuốc ức chệ hệ renin – angiotensin
Như đã biết, hoạt hóa hệ RAA là một yếu tố quan trọng liên quan đến hoạt hóa hệ thống thần kinh kinh thể dịch – một trong những cơ chế bù trừ quan trọng trong cơ chế bệnh sinh của suy tim. Mặc dù, các cơ chế bù trừ của hoạt hóa hệ thần kinh thể dịch là có lợi trong giai đoạn đầu của suy tim, nhưng về lâu dài đã được chứng minh là có hại và làm tình trạng suy tim ngày càng trầm trọng. Cụ thể, dưới tác động của hệ RAA, sự tăng nồng angiotensin II và aldosterone trong máu lâu dài sẽ dẫn đến những bất lợi: tăng tạo các cytokines, hoạt hóa đại thực bào và kích thích nguyên bào sợi -> xơ hóa và tái định dạng theo hướng bất lợi.
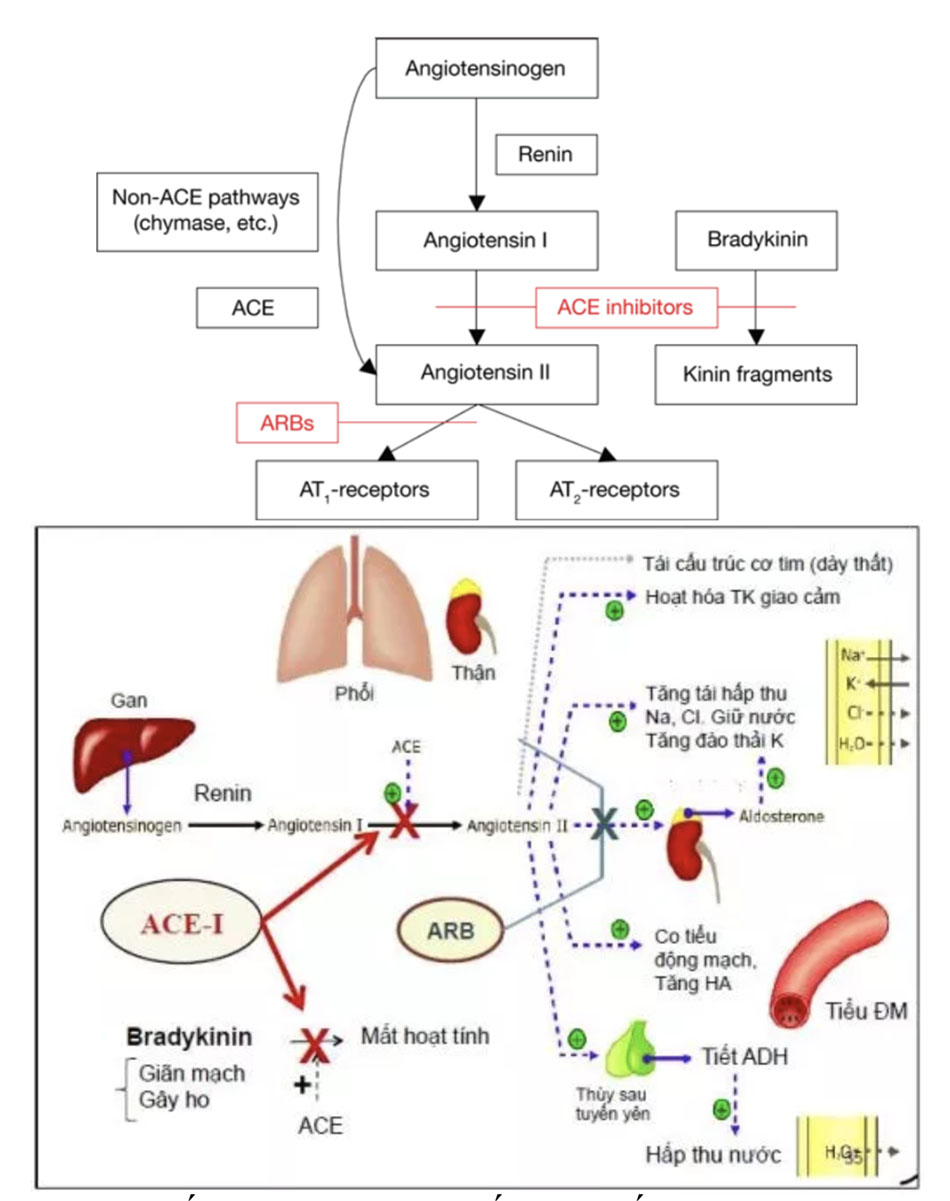
Theo quan điểm kinh điển, cơ chế tác dụng chính của thuốc ACEi trong điều trị suy tim là giảm tình trạng co mạch do angiotensin II. Ngoài ra, sự giảm angiotensin II cũng dẫn đến hạn chế phóng thích aldosterone từ tuyến thượng thận, từ đó làm giảm tình trạng giữ muối và nước. Tuy nhiên, hiệu quả của nhóm thuốc này không chỉ đơn giản là ảnh hưởng đến nồng độ angiotensin II trong máu. Bởi vì, kininase có cấu trúc tương tự như men chuyển, từ đó thuốc ACEi cũng cản trở quá trình thoái giáng của bradykinin – một hoạt chất gây phóng thích các chất dãn mạch có nguồn gốc nội mạc (NO, prostaglandin). Quan trọng hơn, thông qua việc ức chế hệ RAA tại mô mạch máu, thận và tim, thuốc ACEi chống lại các hiện tượng bất lợi như tái định dạng mạch máu và cơ tim, tình trạng viêm, tạo huyết khối, cũng như hạn chế tốc độ tiến triển bệnh lý thận. Tất cả tác dụng này giúp giải thích hiệu quả lâm sàng của thuốc ACEi trong điều trị suy tim.
Tuy nhiên, angiotensin II vẫn tồn tại kéo dài tại mô lẫn lưu hành trong máu mặc dù bệnh nhân đang sử dụng thuốc ACEi. Điều này được giải thích rằng angiotensin I có khả năng chuyển dạng thành angiotensin II không chỉ thông qua men chuyển, mà còn nhờ một số yếu tố khác như chymase tại cơ tim hay các cathepsin . Dựa trên cơ sở việc thuốc ACEI có khả năng để “lọt lưới” angiotensin II, nhóm thuốc ARBs đã được phát triển, đó là những thuốc gắn cạnh tranh trên thụ thể type 1 của angiotensin II – thụ thể chịu trách nhiệm cho hầu hết tác dụng bất lợi, và sau đó phân ly từ từ khỏi các thụ thể này, từ đó ngăn chặn tác dụng của angiotensin II trên thụ thể type 1. Các thuốc ARBs gắn với receptor AT 1 với ái lực và độ chọn lọc cao hơn 10.000 lần đối với receptor AT 2 . Mức độ ái lực của receptor AT 1 đối với ARBs là candesartan > irbesartan = eprosartan > telmisartan = valsartan = EXP 3174 (chất chuyển hóa có hoạt tính của losartan) > losartan.
Sự khác biệt rõ ràng giữa thuốc ARBs và ACEi là ARBs không làm tăng mức kinin. ACEi ức chế sự thoái giáng bradykinin hiệu quả hơn ức chế sự chuyển hóa tạo angiotensin II. Bradykinin giúp:
- Giãn mạch, cải thiện trương lực và cấu trúc mạch máu.
- Tăng khả năng ly giải huyết khối.
- Bảo vệ mạch máu chống lại sự kết tập tiểu cầu và bạch cầu được hoạt hóa.
- Chống lại phản ứng viêm và chết tế bào theo chương trình trong các bệnh lý mạch máu và thận.
Mặt khác, dù thuốc ARBs không có tác dụng ức chế sự thoái giáng bradykinin nhưng lại có sự tăng hoạt receptor AT 2, dẫn đến các kết cục có lợi tương tự:
- Giãn mạch, chống tái cấu trúc bất thường.
- Ổn định mảng xơ vữa, chống lại phản ứng viêm trong các bệnh lý mạch máu và thận.
- Điều hòa sự tăng sinh bất thường bằng chết tế bào theo chương trình.
c. Hiệu quả và các thử nghiệm lâm sàng của thuốc ức chế hệ renin – angiotensin trong điều trị suy tim
Tác dụng cải thiện huyết động trong suy tim được thể hiện qua việc cải thiện thể tích nhát bóp ở bệnh nhân suy chức năng tâm thu thất trái bằng cách dãn mạch giảm kháng lực đường thoát.
Các thuốc gây dãn tiểu động mạch ngoại vi làm đường cong biểu diễn chức năng tâm thu thất dịch chuyển lên trên và sang trái, cải thiện cung lượng tim trong khi không ảnh hưởng nhiều đến huyết áp. Những thuốc làm dãn tĩnh mạch gây tái phân bố máu từ trung tâm ra ngoại vi, từ đó giảm triệu chứng do tăng áp lực đổ đầy thất. Khác với hydralazine (chủ yếu dãn tiểu động mạch) và nitrates (dãn động mạch và tĩnh mạch), thuốc ACEi và ARBs là những thuốc dãn mạch có tác dụng trên cả tiểu động mạch, động mạch và tĩnh mạch.
Nhiều thử nghiệm lâm sàng tiền cứu có đối chứng giả dược đã chứng minh lợi ích của thuốc ACEi trong việc cải thiện khả năng gắng sức, cân bằng muối nước, triệu chứng lâm sàng, sự hoạt hóa thần kinh thể dịch, chất lượng cuộc sống và sống còn ở bệnh nhân suy tim mạn. Các kết quả tương đồng nhau trong những nghiên cứu đa trung tâm là cơ sở khoa học vững chắc cho vấn đề sử dụng thuốc ACEi trong điều trị suy tim. Một vài nghiên cứu tiêu biểu được điểm lại ngay sau đây.
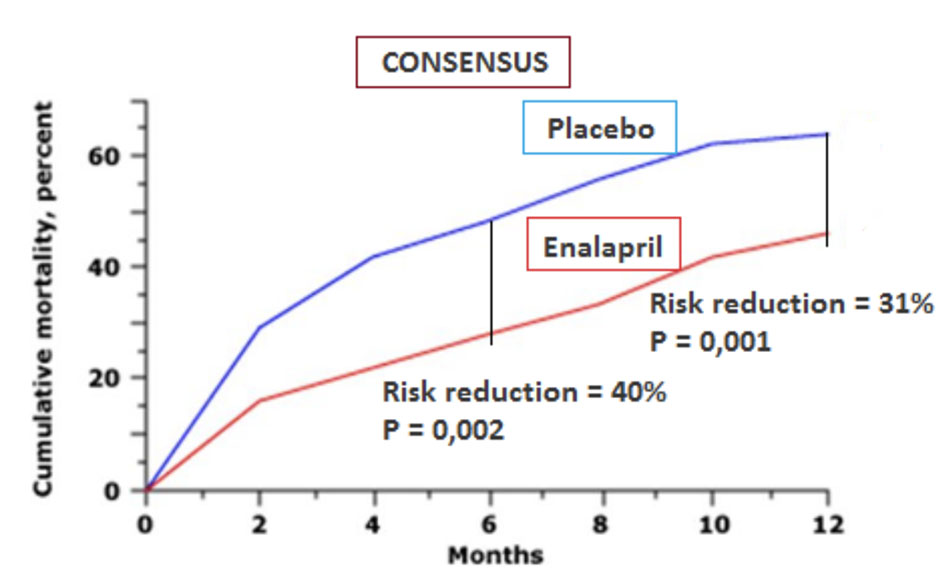
CONSENSUS: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm đối chứng giả dược trên 253 bệnh nhân suy tim, EF ≤ 40%, NYHA IV, trên nền điều trị cơ bản gồm digoxin, lợi tiểu, và các thuốc dãn mạch không phải ACEi. Sau 6 tháng, tỷ lệ tử vong do mọi nguyên nhân giảm hơn 40% trong nhóm enalapril so với nhóm placebo (26% so với 44%, p = 0,002). Sau 12 tháng, tỷ lệ tử vong giảm 31% (p = 0,001). Đến cuối nghiên cứu, tỷ lệ này là 27% (p = 0,003). Ngoài ra, nghiên cứu còn ghi nhận việc giảm kích thước tim và yêu cầu các loại thuốc khác.
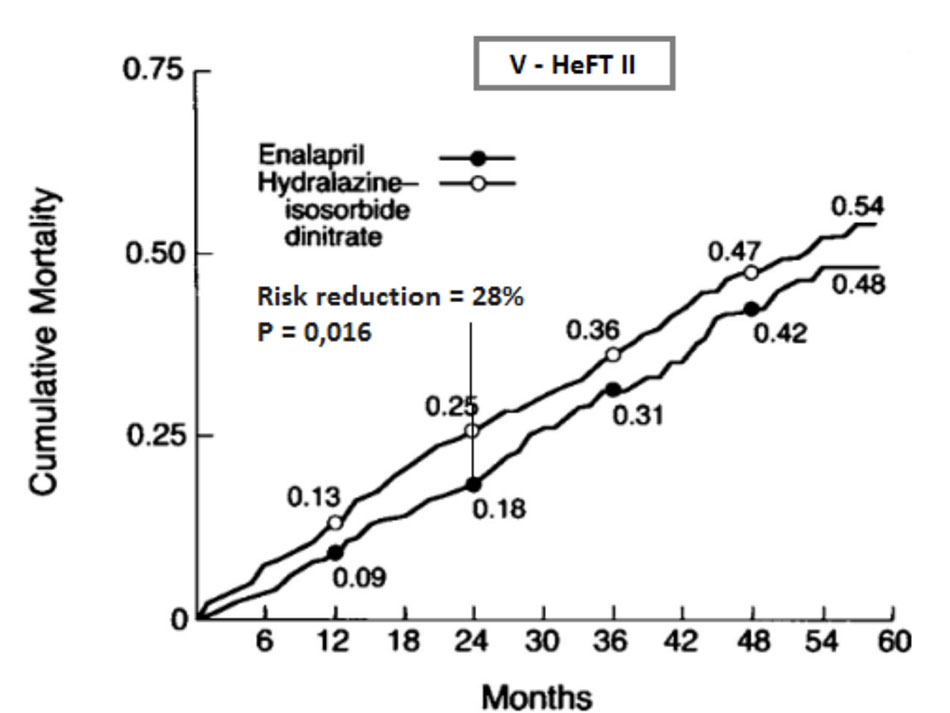
V – HeFT II: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng với hydralazine/ isosorbide dinitrate trên 804 bệnh nhân nam suy tim, NYHA II – III, trên nền điều trị cơ bản gồm digoxin và lợi tiểu. Sau hai năm, tỷ lệ tử vong thấp hơn đáng kể ở nhóm enalapril so với nhóm hydralazine/isosorbide dinitrate (18% so với 25%, p = 0,016), mức giảm tỷ lệ tử vong là 28%. Dù vậy, lợi ích này không đạt được ý nghĩa thống kê trong toàn bộ thời gian của theo dõi (p = 0,08). Giảm tỷ lệ tử vong với enalapril chủ yếu là do tỷ lệ tử vong đột ngột thấp hơn. Không có sự khác biệt đáng kể về tỷ lệ nhập viện giữa hai nhóm (18,9% so với 18,4%).
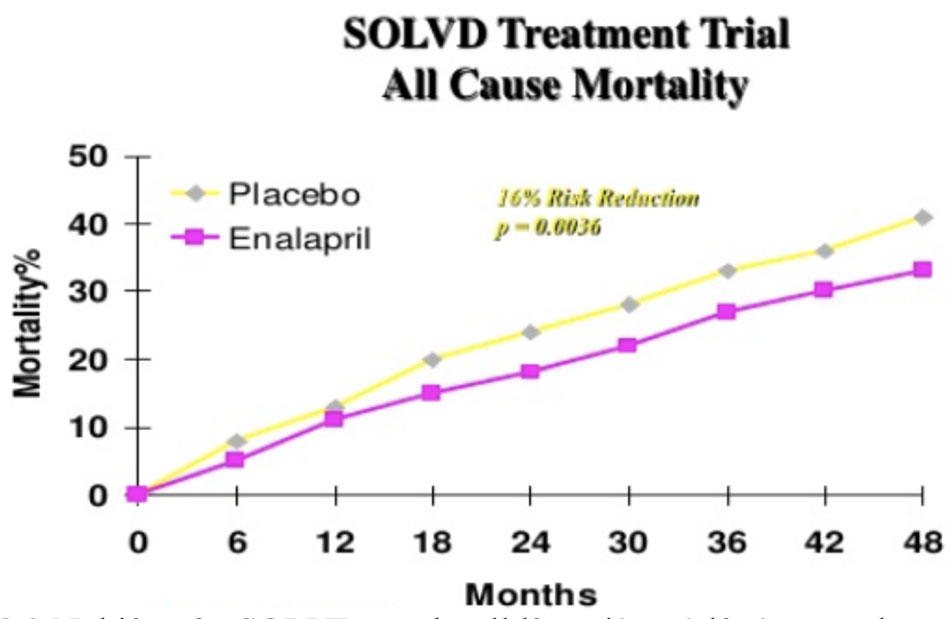
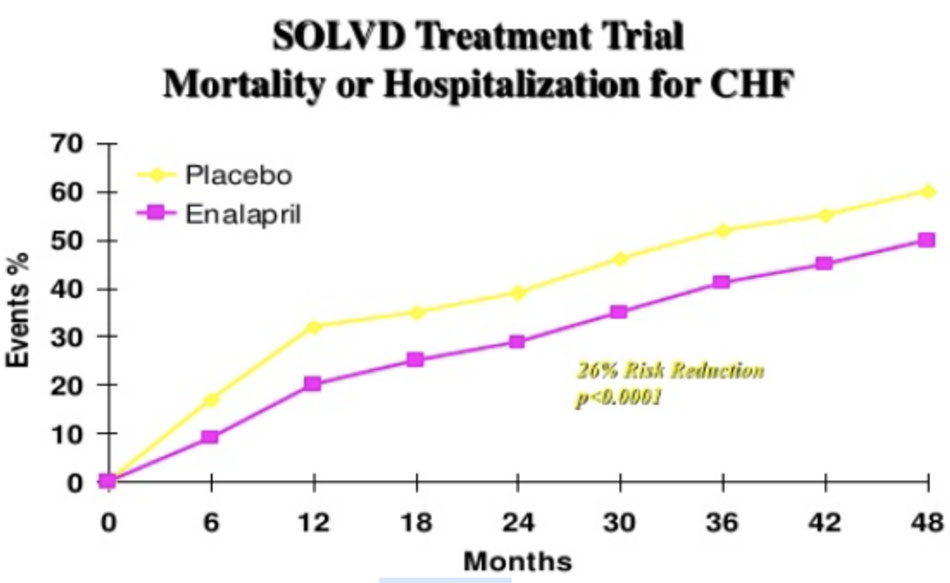
SOLVD: nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược trên 2569 bệnh nhân suy tim, NYHA II – III (90%), EF ≤ 35%, trên nền điều trị với digitalis, lợi tiểu và nitrate. Sau 4 năm theo dõi, nhóm enalapril có ít bệnh nhân tử vong hơn so với nhóm placebo (452 so với 510, p = 0,0036), mức giảm tỷ lệ tử vong do mọi nguyên nhân là 16%. Ngoài ra, tiêu chí gộp tử vong do mọi nguyên nhân/nhập viện vì suy tim cũng giảm 26% (p < 0,0001).
Nghiên cứu SAVE thực hiện trên bệnh nhân suy tim vừa, EF ≤ 40%, theo dõi 42 tháng. Nhóm có Captopril giảm được 20% tử vong và 36% diễn tiến bệnh đến nặng, so với nhóm placebo.
Nghiên cứu AIRE và nghiên cứu TRACE (EF ≤ 35%) đều cho kết quả giảm tương tự. Cải thiện tử vong lần lượt là 27% và 20% ở nhóm có ACEi.
Mặc dù các thử nghiệm lâm sàng đã chứng minh lợi ích của thuốc ACEi với liều cao trong điều trị suy tim, thực tế thì các thuốc này thường chỉ được dùng với liều thấp vì lo ngại về tác dụng phụ. Mối lo lắng này có lẽ phần nào được giải tỏa nhờ kết quả nghiên cứu ATLAS.
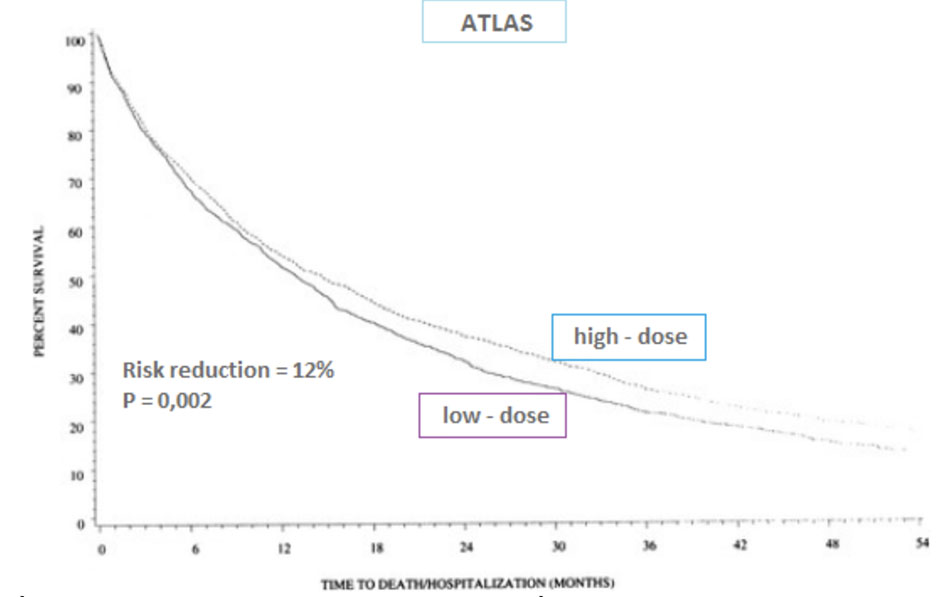
ATLAS: nghiên cứu ngẫu nhiên, mù đôi, so sánh giữa hai nhóm sử dụng lisinopril liều thấp (2,5 – 5mg/ngày) và liều cao (32,5 – 35mg/ngày) trên 3164 bệnh nhân suy tim, NYHA II – IV, EF ≤ 30% . Sau thời gian theo dõi trung bình 46 tháng, lisinopril liều cao vượt trội hơn trong hiệu quả giảm tiêu chí gộp là tử vong do mọi nguyên nhân/tỷ lệ nhập viện vì suy tim (p = 0,002), mức giảm tiêu chí gộp là 12%. Tuy nhiên, không có sự khác nhau giữa hai nhóm khi xét đơn lẻ từng tiêu chí. Mặc dù, chóng mặt và suy thận thường gặp hơn ở nhóm liều cao, tỷ lệ ngưng thuốc vì tác dụng phụ ở hai nhóm là tương tự nhau khoảng 18%.
Sự xuất hiện trên thị trường của các chất ARBs (như losartan, irbesartan, valsartan, candesartan, eprosartan và telmisartan) đã dẫn đến việc hoàn thành hai thử nghiệm lớn so sánh chất ACEi với losartan trong điều trị suy tim. Chất ACEi vẫn là thuốc đầu bảng điều trị suy tim; tuy nhiên, chất ARBs được coi là thuốc thay thế ở bệnh nhân bị ho do ACEi.
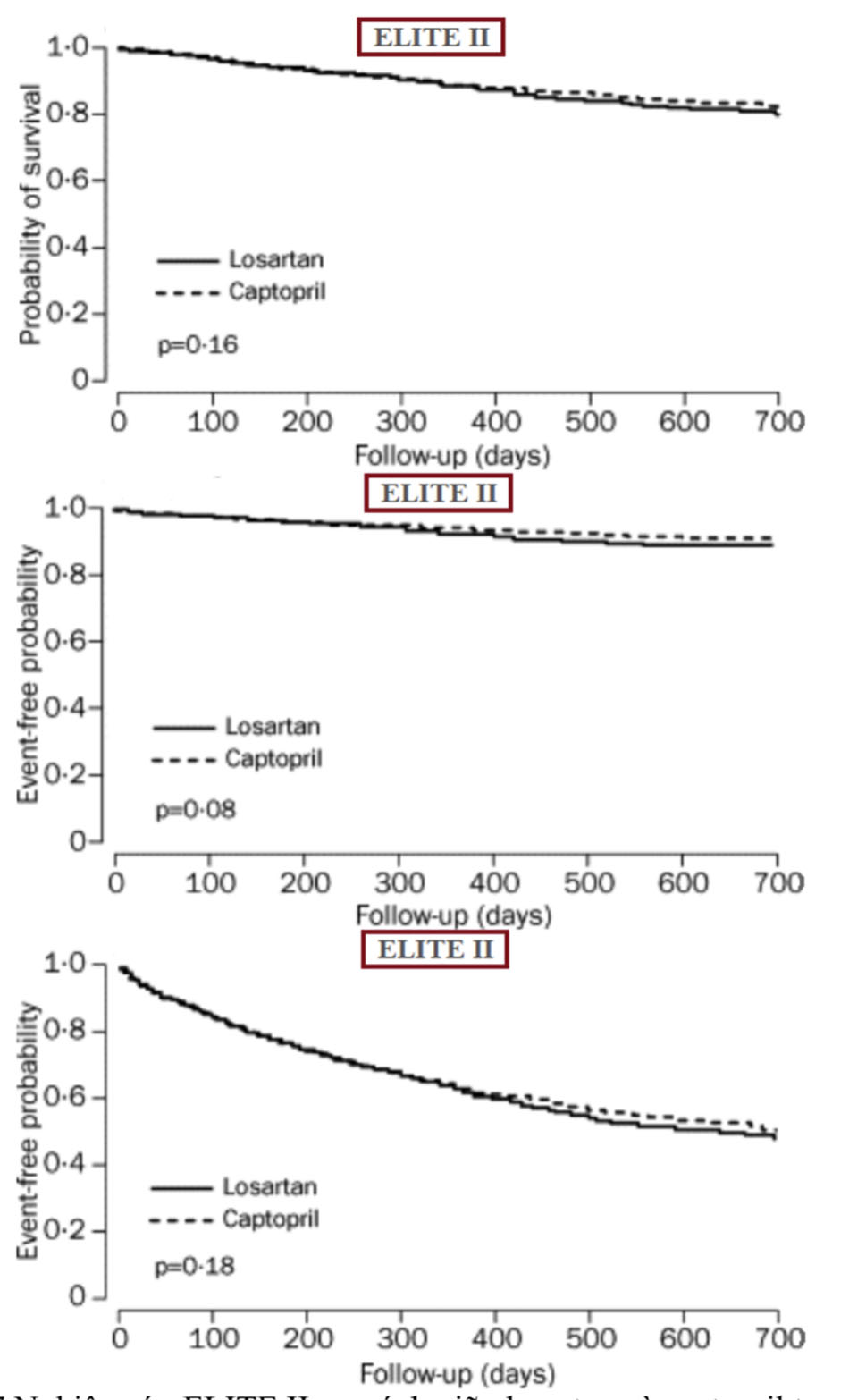
ELITE I: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng với captopril trên 722 bệnh nhân suy tim, tuổi ≥ 65, NYHA II – IV, EF ≤ 40%. Sau 48 tuần theo dõi, điều trị bằng losartan có tỷ lệ tử vong do mọi nguyên nhân thấp hơn so với captopril (4,8% so với 8,7%, p = 0,035), mức giảm tỷ lệ tử vong do mọi nguyên nhân là 46%. Đồng thời, ít bệnh nhân losartan ngừng điều trị vì những tác dụng bất lợi (12,2% so với 20,8%, p = 0,002). Không có bệnh nhân điều trị bằng losartan ngừng điều trị do ho so với 14 bệnh nhân trong nhóm captopril.
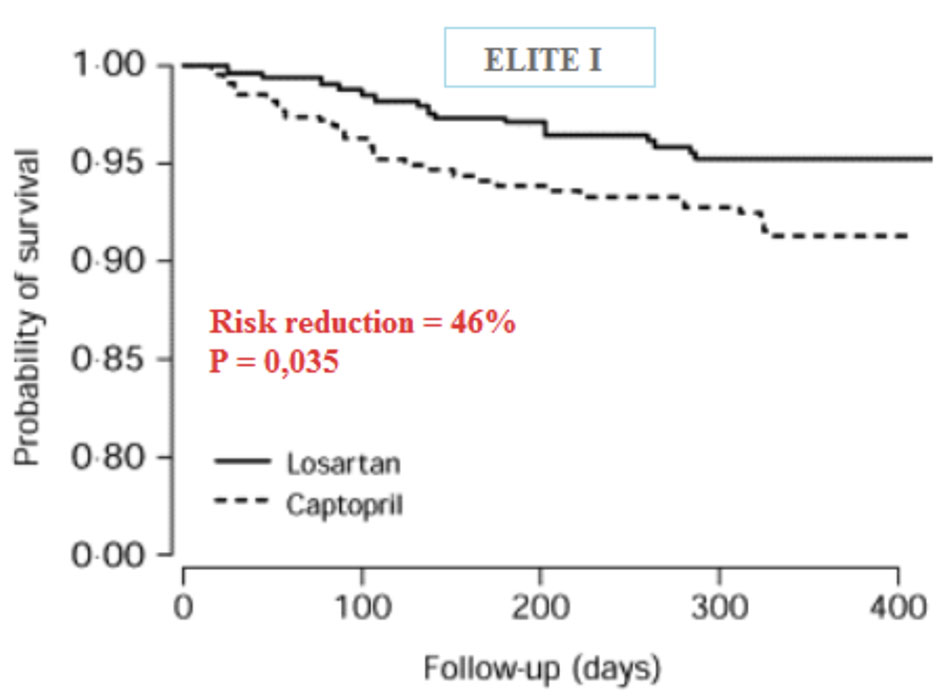
ELITE II: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng với captopril trên 3152 bệnh nhân suy tim, tuổi ≥ 60, NYHA II – IV, EF ≤ 40%. Nhóm captopril có tỷ lệ tử vong do mọi nguyên nhân thấp hơn 13% những không đạt ý nghĩa thống kê (p = 0,16). Về các tiêu chí phụ (đột tử do tim, tiêu chí gộp tử vong do mọi nguyên nhân/nhập viện vì suy tim) thì losartan có khuynh hướng tốt hơn captopril, những cũng không có ý nghĩa trên phương diện thống kê. Tuy nhiên, tỷ lệ ngưng thuốc vì tác dụng phụ của nhóm lorsatan thấp hơn (9,4% so với 14,5%, p < 0,001). Một số tác giả cho rằng lợi ích của losartan thấp hơn captopril có lẽ do không được dùng với liều tối ưu trong nghiên cứu.
Ở bệnh nhân suy tim không dung nạp thuốc ACEi, thuốc ARBs là lựa chọn thay thế với hiệu quả đã được chứng minh qua nghiên cứu CHARM – Alternative.
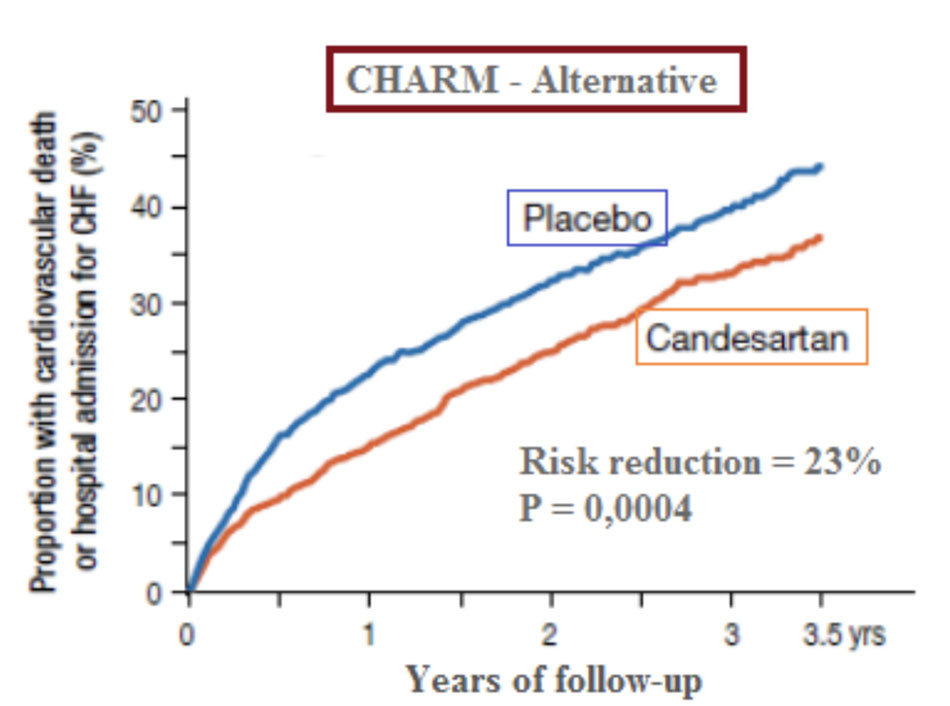
CHARM – Alternative: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng giả dược trên 2028 bệnh nhân suy tim, NYHA II – IV, EF ≤ 40%, không dung nạp với thuốc ACEi do ho (72%), tụt huyết áp (13%), hoặc suy thận (12%). Sau theo dõi trung bình 33,7 tháng, tiêu chí gộp tỷ lệ tử vong do tim mạch/nhập viện vì suy tim ở nhóm candesartan thấp hơn so với nhóm placebo (33% so với 40%, p = 0,0004), mức giảm tỷ lệ này là 23%. Riêng tiêu chí tử vong do mọi nguyên nhân, kết quả không có ý nghĩa về mặt thống kê (p = 0,072).
Như đã biết, việc phối hợp các thuốc trong điều trị các bệnh lý tim mạch là rất thường quy, suy tim cũng không phải là ngoại lệ. Vậy câu hỏi đặt ra là liệu có thể phối hợp hai nhóm thuốc ACEi và ARBs với nhau được không, khi cả hai trên cơ bản đều tác động lên một cơ chế trong tiến trình suy tim? Về lý thuyết, phối hợp hai nhóm thuốc này có thể đạt hiệu quả tốt hơn so với sử dụng đơn lẻ. Trên lâm sàng, một số thử nghiệm cũng đã được thực hiện để đánh giá sự phối hợp này. Tiêu biểu phải kể đến hai thử nghiệm Val – HeFT và CHARM – Added.
Val – HeFT: nghiên cứu ngẫu nhiên, mù đôi, nhóm song song, đối chứng giả dược trên 5010 bệnh nhân suy tim, NYHA II – IV, EF ≤ 40%, trên nền điều trị cơ bản gồm thuốc ACEi (93%) và chẹn β (36%). Nhóm dùng valsartan có tiêu chí gộp là tỷ lệ tử vong do mọi nguyên nhân/nhập viện vì suy tim thấp hơn so với nhóm placebo, mức giảm tỷ lệ này là 13,2% (p = 0,009). Trong đó, tỷ lệ nhập viện vì suy tim giảm 28% (p < 0,001), nhưng không ảnh hưởng đến tỷ lệ tử vong do mọi nguyên nhân.
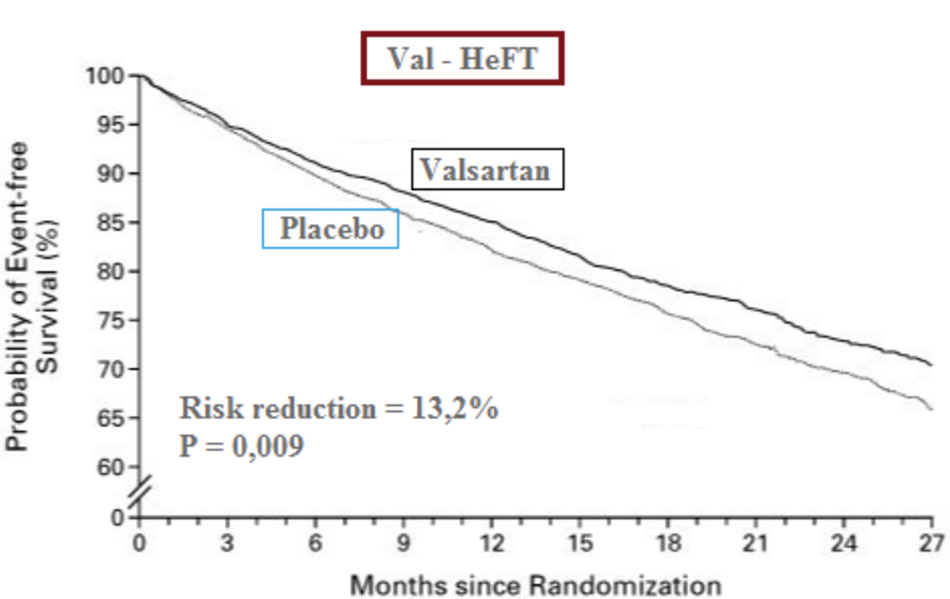
CHARM – Added: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng giả dược trên 2548 bệnh nhân suy tim, NYHA II – IV, EF ≤ 40%, dung nạp với thuốc ACEi. Trong thời gian theo dõi khoảng 41 tháng, tỷ lệ tử vong do tim mạch/nhập viện vì suy tim giảm 15% ở nhóm candesartan so với nhóm placebo (p = 0,011). Tuy nhiên, sự phối hợp trong nghiên cứu này ghi nhận có tăng nguy cơ suy thận và tăng kali máu.
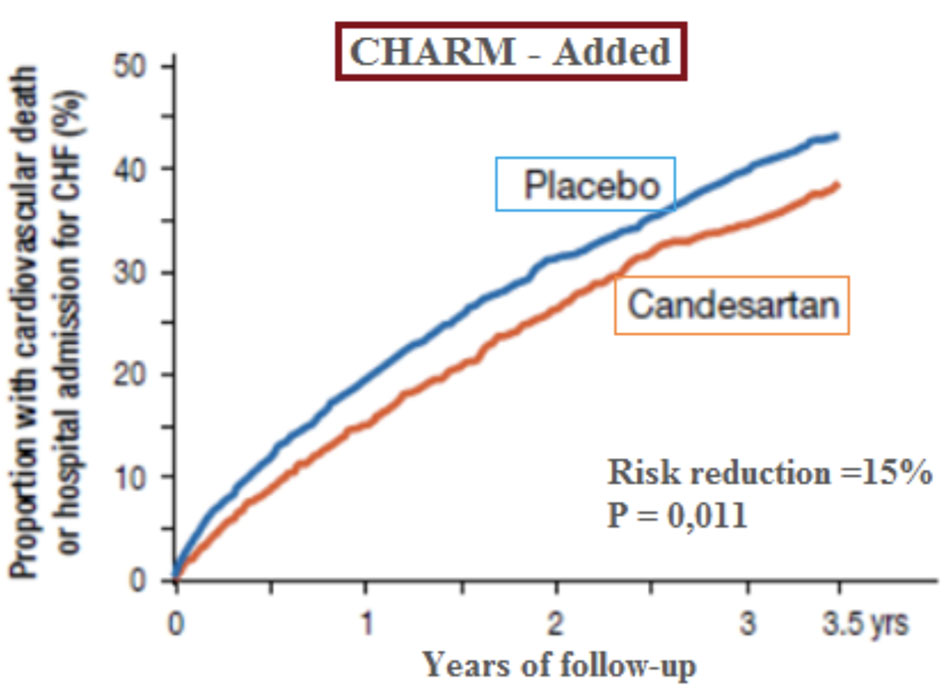
Ở chiều ngược lại, trong nghiên cứu VALIANT thì sự phối hợp này là không có hiệu quả.
VALIANT: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, thực hiện trên 14703 bệnh nhân nhồi máu cơ tim cấp trong vòng 10 ngày trở lại, có suy tim và/hoặc EF ≤ 40% sau đó. Theo dõi điều trị trung bình 24,7 tháng ghi nhận kết quả, tỷ lệ tử vong do mọi nguyên nhân đều giảm ở ba nhóm (19,9% với valsartan, 19,5% với captopril và 19,3% khi phối hợp cả hai), sự khác biệt giữa các nhóm không có ý nghĩa thống kê. Đồng thời, tiêu chí gộp là tử vong do tim mạch/tái nhồi máu/nhập viện vì suy tim cũng giảm (31,1% giống nhau ở hai nhóm valsartan và captopril, 31,9% khi phối hợp cả hai), sự khác biệt này cũng không có ý nghĩa thống kê. Tuy nhiên, khi kết hợp hai thuốc thì tác dụng phụ lại xảy ra nhiều hơn khi sử dụng một thuốc đơn thuần (29,4% với valsartan, 28,4% với captopril và 34,8% khi kết hợp cả hai), sự khác biệt này là có ý nghĩa trên phương diện thống kê (P < 0,05).
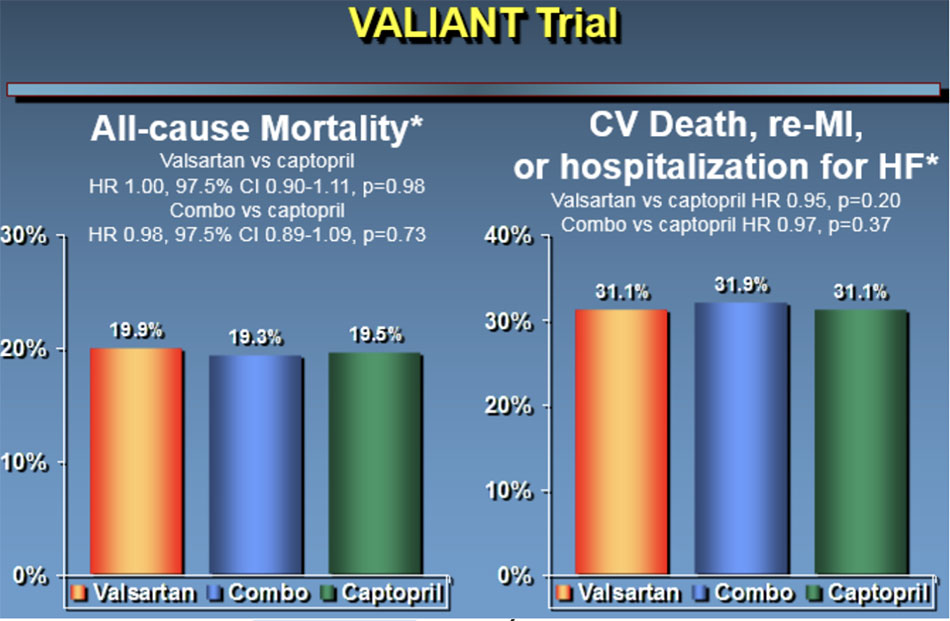
Như vậy, có sự đối lập giữa các nghiên cứu với nhau về lợi ích khi phối hợp hai nhóm thuốc ACEi và ARBs. Sự khác biệt về đặc điểm dân số nghiên cứu, nguy cơ tim mạch và chế độ điều trị giữa hai nhóm suy tim ổn định là nhồi máu cơ tim cấp có lẽ là lý do đưa đến những kết quả khác nhau. Tuy nhiên, các nghiên cứu đều có một điểm chung là sự phối hợp này sẽ làm tăng các tác dụng có hại, đặc biệt nguy hiểm trên bệnh nhân có bệnh đái tháo đường type 2, suy giảm chức năng thận, tăng kali máu… Bằng chứng quan trọng từ các thử nghiệm lâm sàng như ONTARGET, ALTITUDE, VA NEPHRON – D và từ các phân tích gộp của Makani (trên 68000 bệnh nhân) đã chỉ ra rằng phối hợp điều trị hai thuốc cùng tác động trên hệ renin – angiotensin liên quan tới tăng nguy cơ biến cố có hại bao gồm hạ huyết áp, tăng kali máu và suy thận so với điều trị một thuốc, đặc biệt là trên bệnh nhân đái tháo đường có biến chứng trên thận. Đây là vấn đề cần đặc biệt chú ý, vì bệnh nhân suy giảm chức năng thận đã có thể phần nào tiến triển biến cố tăng Kali máu.
Ngày 23/05/2014, Ủy ban các sản phẩm thuốc sử dụng cho người (CHMP) đã chấp thuận về chống chỉ định phối hợp này. Ngày 09/09/2014, Uỷ ban châu Âu (EC) đã ra quyết định cuối cùng về việc chống chỉ định phối hợp các thuốc cùng tác động trên hệ renin – angiotensin. Thuốc tác động lên hệ renin – angiotensin gồm ba nhóm thuốc chính: chẹn thụ thể angiotensin (ARBs), ức chế men chuyển angiotensin (ACEi) và ức chế trực tiếp renin như aliskiren. Mọi việc phối hợp thuốc từ hai nhóm bất kỳ trong ba nhóm thuốc nói trên không được khuyến cáo, đặc biệt không được kết hợp thuốc ARBs với thuốc ACEi trên bệnh nhân đái tháo đường có biến chứng trên thận. Khi thực sự cần thiết phải kê đơn đồng thời cả hai thuốc, cần phải thực hiện dưới sự giám sát của chuyên gia kết hợp với sự giám sát chặt chẽ chức năng thận, lượng dịch trong cơ thể và cân bằng điện giải. Khuyến cáo này cũng bao gồm cả việc kết hợp đã được cấp phép của thuốc candesartan hoặc valsartan với nhóm ACEi trên bệnh nhân suy tim. Việc kết hợp aliskiren với thuốc ACEi bị chống chỉ định tuyệt đối trên bệnh nhân bị suy giảm chức năng thận hoặc bị đái tháo đường.
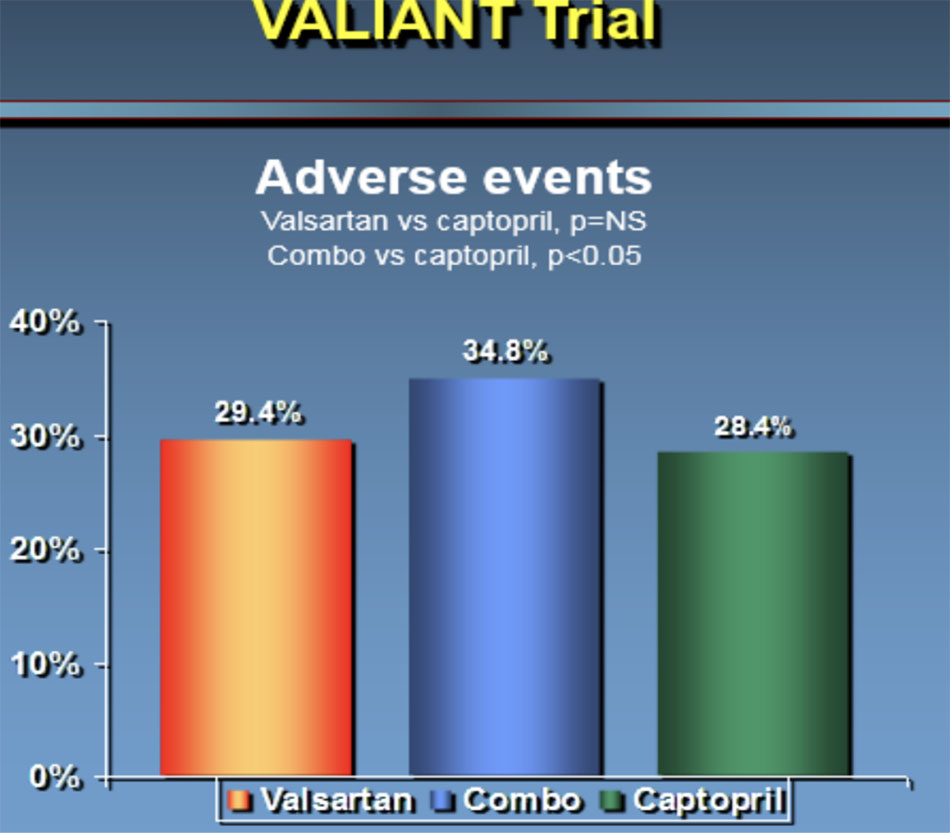
d. Sử dụng thuốc ức chệ hệ renin – angiotensin trong thực hành điều trị suy tim
Trong điều trị suy tim, thuốc ACEi là liệu pháp nền tảng, trong khi đó, thuốc ARBs là điều trị thay thế nếu bệnh nhân không dung nạp được với ACEi, thường là do ho khan kéo dài. Không khuyến cáo sử dụng đồng thời ACEi và ARBs, nhiều trường hợp là chống chỉ định kết hợp, chỉ bổ sung ARBs cho bệnh nhân khi vẫn còn triệu chứng dù đang dùng ACEi và chẹn β, mà không dung nạp được thuốc kháng aldosterone.
Sử dụng ACEi/ARBs là bắt buộc đối với bệnh nhân suy tim từ giai đoạn B và xem xét ở giai đoạn A, trừ khi có chống chỉ định:
- Hẹp động mạch thận hai bên hoặc một bên đối với bệnh nhân chỉ có một thận.
- Bệnh cơ tim phì đại và bệnh cơ tim hạn chế, viêm màng ngoài tim co thắt.
- Bệnh nhân suy thận, độ lọc cầu thận < 25 ml/phút, Kali máu > 5,5 mmol/l.
- Bệnh nhân thiếu máu nặng -> chống chỉ định với các thuốc giãn mạch.
- Giảm bạch cầu trung tính nặng đã có sẵn vì ảnh hưởng của ACEi trên bạch cầu.
- Mang thai và cho con bú bởi vì ACEi/ARBs gây ra thương tích và tử vong ở thai nhi.
- Bệnh rối loạn chuyển hóa Porphyria.
- Bệnh thận liên quan đến miễn dịch hoặc khi dùng tác nhân ảnh hưởng đến hệ thống miễn dịch.
Kiểm tra chức năng thận và điện giải. Bắt đầu với liều thấp, gấp đôi liều ≥ 2 tuần khi điều trị ngoại trú, có thể tăng liều nhanh hơn khi điều trị nội trú (nếu bệnh nhân dung nạp được) và ở những bệnh nhân có điều kiện theo dõi sát để đạt đến liều đích trong các thử nghiệm lâm sàng hoặc liều cao nhất bệnh nhân có thể dung nạp được. Kiểm tra lại sinh hóa máu (BUN, creatinin, Kali) 1 – 2 tuần sau khởi trị và 1 – 2 tuần sau khi có điều chỉnh liều sau cùng rồi mỗi 4 tháng sau đó.
Một khi đã đạt liều cao nhất có thể dung nạp, chúng ta cần duy trì lâu dài. Nếu bệnh nhân không thể dung nạp ACEi/ARBs liều cao, vẫn tiếp tục dùng liều thấp hoặc vừa, trong khi bắt đầu sử dụng chẹn β. Nghiên cứu ATLAS và HEAAL đã ghi nhận thuốc ACEi/ARBs liều thấp cũng cải thiện triệu chứng và tử vong ở bệnh nhân suy tim. Tuy nhiên, có nhiều trường hợp buộc phải ngưng sử dụng ACEi/ARBs do bất ổn về huyết động và chức năng thận, và đây là một dấu hiệu cảnh báo tiên lượng xấu.
Một vấn đề vẫn chưa có câu trả lời thống nhất là liệu lợi ích của ức chế men chuyển là đặc tính chung của cả nhóm nhất là liệu lợi ích của ACEi là đặc tính chung của cả nhóm hay chuyên biệt theo từng loại thuốc. Captopril, enalapril, lisinopril hiện tại được chỉ định trong điều trị suy tim có triệu chứng. Captopril, ramipril và trandolapril có chỉ định dùng cho bệnh nhân sau nhồi máu cơ tim. Enalapril là thuốc ACEi duy nhất có chỉ định dùng để phòng ngừa suy tim ở bệnh nhân không triệu chứng. Mặc dù không đủ dữ kiện để khẳng định lợi ích trong nghiên cứu lâm sàng có thể áp dụng cho cả nhóm, các phân tích tổng hợp ghi nhận rằng tác dụng cải thiện sống còn của những thuốc ACEi khác nhau là tương tự nhau, với hiệu quả thống nhất ở nhiều đối tượng bệnh nhân khác nhau. Mặt khác, chỉ có vài thuốc ARBs được chấp thuận trong điều trị suy tim: losartan, valsartan và candesartan.
| Bảng 8.1 Liều lương các thuốc ức chế hệ renin – angiotensin trong điều trị suy tim theo ESC 2016 | ||
| Liều khởi đầu (mg/ngày) | Liều mục tiêu (mg/ngày) | |
| ACEi | ||
| Captopril (a) | 6,25 x 3 | 50 x 3 |
| Enalapril | 2,5 x 2 | 20 x 2 |
| Lisinopril (b) | 2,5 – 5 | 20 – 35 |
| Ramipril | 2,5 | 10 |
| Trandolapril (a) | 0,5 | 4 |
| ARBs | ||
| Candesartan | 4 – 8 | 32 |
| Losartan (b,c) | 50 | 150 |
| Valsartan | 40 x 2 | 160 x 2 |
(a) : Ức chế men chuyển với liều mục tiêu trong thử nghiệm lâm sàng sau nhồi máu cơ tim. (b): Những thuốc này khi dùng liều cao hơn được chứng minh giảm tử vong và bệnh tật so với liều thấp, nhưng không có thử nghiệm lâm sàng ngẫu nhiên có kiểm chứng với placebo và liều tối ưu không biết chắc chắn. (c): Điều trị này không chứng minh giảm tử vong tim mạch hay tử vong do mọi nguyên nhân ở bệnh nhân suy tim hoặc sau nhồi máu cơ tim.
Quan điểm cho rằng tác dụng phụ dễ xảy ra hơn khi dùng ACEi liều cao hoặc cho bệnh nhân lớn tuổi là rất phổ biến. Tuy nhiên, kinh nghiệm từ các nghiên cứu CONSENSUS và SOLVD cho thấy tỷ lệ tác dụng phụ của ACEi là thấp và chấp nhận được so với lợi ích cải thiện sống còn. Ngoài ra, nghiên cứu ATLAS chứng tỏ sử dụng ACEi liều cao không làm tăng nguy cơ ngưng thuốc do tác dụng phụ. Việc nhân diện các yếu tố thúc đẩy và áp dụng những biện pháp cẩn trọng sẽ giúp ích trong vấn đề phòng tránh và xử trí các tác dụng phụ của ACEi.
Một số tác dụng phụ thường gặp khi sử dụng ACEi/ARBs: tụt huyết áp (tác dụng phụ quan trọng nhất xảy ra lúc mới sử dụng thuốc), suy chức năng thận, tăng Kali máu, protein niệu, phù mạch, ho khan (tác dụng phụ thường gặp nhất chiếm 5 – 20%), ngứa, phát ban, rối loạn vị giác. Tùy tửng trường hợp sẽ có hướng dẫn xử trí cụ thể:
- Tụt huyết áp:
-
- Nếu không có triệu chứng, thường không đòi hỏi thay đổi bất kỳ chế độ điều trị nào.
- Nếu bệnh nhân có triệu chứng xây xẩm hoặc choáng váng thường cũng sẽ cải thiện theo thời gian, cần xem xét giảm liều hoặc ngưng các thuốc nitrate, ức chế Ca và các thuốc dãn mạch khác nếu được.
- Nếu bệnh nhân không có triệu chứng và dấu hiệu của sung huyết phổi, cần xem xét giảm liều lợi tiểu.
-
- Chức năng thận diễn tiến xấu và tăng Kali máu: tăng BUN, creatinin và kali máu là tác dụng bản chất của thuốc ACEi/ARBs.
-
- Nếu tăng nhẹ không triệu chứng (creatinin tăng ≤ 50% giá trị nền trước đó, kali ≤ 5.5 mmol/l) là chấp nhận được.
- Nếu tăng vượt quá mức giới hạn này cần xem xét ngưng những thuốc đi kèm gây độc thận (VD như NSAID..) và gây tăng Kali máu (VD như lợi tiểu giữ Kali..) và giảm liều thuốc lợi tiểu nếu không có dấu hiệu sung huyết.
- Nếu creatinin và kali tăng dai dẳng mặc dù đã điều chỉnh các thuốc đi kèm cần giảm nửa liều ACEi/ARBs và kiểm tra lại sinh hóa máu 1 – 2 tuần sau, nếu vẫn đáp ứng không thích hợp cần hội chẩn chuyên khoa thận.
- Nếu Kali > 5.5 mmol/l hoặc creatinin tăng > 100% giá trị trước đó hoặc > 3.5 mg/dl (eGFR < 20ml/p/1.73m2 da), ACEi/ARBs nên ngưng và hội chẩn chuyên khoa thận, sinh hóa máu cần theo dõi thường xuyên và nghiêm ngặt hơn cho đến khi kali và reatinin máu về bình ổn.
-
- Phù mạch: là một biến chứng hiếm gặp nhưng có thể nguy hiểm đến tính mạng, có thể xảy ra sau vài tuần đến vài tháng sử dụng ACEi/ARBs, cơ chế tích tụ liên quan đến sự tích tụ bradykinin hoặc sản phẩm chuyển hóa của nó. Cần phải ngưng sử dụng ACEi/ARBs ngay lập tức.
- Ho: cần phải loại trừ những tình trạng diễn tiến xấu trước khi nghĩ ho do ACEi. Ho do ACEi không phải luôn luôn cần ngưng điều trị trừ khi triệu chứng ho quá khó chịu (chỉ ngưng khi ngủ) và phải có bằng chứng ho do ACEi (ho cải thiện sau khi ngưng ACEi và tái phát sau khi cho lại ACEi) trong trường hợp này, ARBs được khuyến cáo thay thế.
Kết luận:
1. ACEi/ARBs đã được chứng minh đem lại lợi ích sống còn cho bệnh nhân suy tim trên phương diện cả lý thuyết lẫn lâm sàng.
2. ACEi là thuốc nền tảng trong điều trị suy tim, là thuốc phải nghĩ đến đầu tiên khi kê toa cho bệnh nhân suy tim có EF giảm, trừ khi có chống chỉ định. ARBs là lựa chọn thay thế khi bệnh nhân không dung nạp hay ho không kiểm soát khi dùng ACEi.
3. Các thuốc ACEi khác nhau nhìn chung có tác dụng cải thiện sống còn tương đương nhau, có nhiều lựa chọn ACEi cho bệnh nhân. ARBs hạn chế hơn với ba thuốc khuyến cáo dùng cho bệnh nhân suy tim.
4. Theo dõi chặt chẽ bệnh nhân khi điều trị bằng thuốc ACEi/ARBs, cố gắng duy trì đến liều đích để đạt hiệu quả tối ưu. Luôn nhớ rằng có ACEi/ARBs là tốt hơn không có ACEi/ARBs.
3. Thuốc chẹn β (Beta blockers) trong điều trị suy tim
a. Vài nét lịch sử của thuốc chẹn β trong điều trị suy tim
Năm 1962, Sir James Black – nhà dược lý học người Anh đã phát triển thành công thuốc chẹn β đầu tiên, đó là propranolol.
Năm 1973, một bệnh nhân nữ 59 tuổi bị bệnh cơ tim dãn nở bị phù phổi cấp và nhịp tim nhanh được điều trị với practolol tiêm tĩnh mạch. Sau đó, bệnh nhân được uống alprenolol, rồi metoprolol. Ở tuổi 82, tình trạng bệnh nhân vẫn ổn định với metoprolol, digitalis, enalapril và lợi tiệu.
Năm 1975, Waggstein công bố 7 trường hợp điều trị suy tim với practolol đem lại những cải thiện về mặt huyết động.
Năm 1984, Cohn và cộng sự chứng minh tỷ lệ tử vong do suy tim gia tăng có liên quan đến nồng độ catecholamine trong máu.
Năm 1989, Bristow công bố nhiều kết quả nghiên cứu khoa học cơ bản cho thấy tình trạng hoạt hóa quá mức của hệ thần kinh giao cảm, sự giảm điều hòa các thụ thể β tại cơ tim bị suy.
Sau đó là nhiều công trình lớn chứng tỏ được lợi ích của thuốc chẹn β trong điều trị suy tim:
- 1993: MDC (Metoprolol in Dilated Cardiomyopathy).
- 1994: CIBIS (Cardiac Insufficiency Bisoprolol study ).
- 1996: U.S CARVEDILOL.
- 1997: CIBIS II, MOCHA (Multicenter Oral Carvedilol Heart Failure Assessment), PRECISE (Prospective Randomized Evalution of Carvedilol on Symtoms and Exersice), ANZ – TRIAL.
Các nghiên cứu về chẹn β trong suy tim là có thể coi là những “mẫu mực” của y học thực chứng đầu những năm 2000.
Như vậy, trong hai mươi lăm năm, từ 1973 đến 1997, quan điểm dùng thuốc chẹn β để điều trị suy tim đã thay đổi từ không thể chấp nhận được đến đáng tin cậy. Theo dòng thời gian, nhóm thuốc này cùng với ức chế men chuyển, trở thành một trong những thuốc bắt buộc trong điều trị suy tim với chức năng thất trái giảm.
b. Tác động của hệ thần kinh giao cảm lên tiến trình suy tim và cơ chế tác động của thuốc chẹn β
Thực tế, có mối liên hệ giữa hệ thần kinh giao cảm và hệ RAA lên tiến trình suy tim. Nghiên cứu SOLVD cho thấy có sự gia tăng nồng độ norepinephrin (NE), renin, arginin vasopressin, atrial natriuretic peptid khi tim bị suy và sự gia tăng này có ý nghĩa tiên lượng xấu. Như vậy, hoạt động của hệ thần kinh giao cảm được phản ánh qua nồng độ NE trong máu. Mức độ gia tăng NE tỷ lệ với mức độ rối loạn chức năng thất trái. Nghiên cứu V – HeFT cho thấy NE và renin là hai yếu tố có mối liên quan độc lập đến tỷ lệ tử vong.
Ngoài ra, nghiên cứu SOLVD còn chỉ ra sự tăng hoạt tính giao cảm xảy ra trước khi có suy tim lâm sàng. Như vậy, sự tăng hoạt động thần kinh giao cảm không phải đơn giản là hậu quả của suy tim và hoạt động này gây nên nhiều tác động xấu như gây độc trực tiếp trên cơ tim, gây loạn nhịp, giảm lưu lượng máu mạch vành, giảm thải Natri ở thận và thiếu oxy mô do hiện tượng co mạch. Những tác động đó cuối cùng dẫn đến tái định dạng thất và giảm chức năng co bóp, suy tim tiến triển ngày càng xấu.
Một trong hai khâu quan trọng trong tiến trình suy tim là sự tăng hoạt tính hệ RAA đã được giải quyết với nhóm thuốc ức chế hệ renin – angiotensin. Tuy nhiên, hoạt động của hệ thần kinh giao cảm vẫn chưa bị khống chế và sự ra đời của thuốc chẹn β đã giúp các nhà tim mạch học giải quyết một bài toán khó.
Cơ chế chính của thuốc chẹn β là đối kháng tranh chấp đặc hiệu với tác dụng β giao cảm của catecholamine thông qua các thụ thể β nhằm mục tiêu: bảo vệ cơ tim, ổn định nhịp tim, tái lập các phản xạ sinh lý, giảm tần số tim; từ đó làm chậm tiến triển hoặc thoái lui quá trình tái định dạng thất.
c. Hiệu quả và các thử nghiệm lâm sàng của thuốc chẹn β trong điều trị suy tim
Nhiều thử nghiệm lâm sàng đã được tiến hành từ năm 1975. Ban đầu chỉ là những công trình nhỏ và không ngẫu nhiên, tiếp theo sau là những công trình lớn, ngẫu nhiên, có so sánh với placebo được tiến hành. Phần lớn, nhưng không phải tất cả các nghiên cứu cho thấy có cải thiện về triệu chứng và giảm phân độ suy tim theo NYHA khi điều trị dài hạn với thuốc chẹn β. Những nghiên cứu không thấy có cải thiện phần lớn là những nghiên cứu ngắn hạn và số lượng bệnh nhân ít.
| Bảng 8.2 Kết quả một số nghiên cứu về chẹn β trên bệnh nhân suy tim | |||||
| Tác giả | Thuốc | Số bệnh nhân | EF | ETT | Triệu chứng |
| MDC (1993) | Metoprolol | 383 | +6% | +/- | + |
| Olsen (1995) | Carvedilol | 60 | +10% | + | |
| Bristow (1994) | Bucindolol | 139 | +4,6% | – | +/- |
| CIBIS (1994) | Bisoprolol | 641 | + | ||
| ANZ (1995) | Carvedilol | 415 | +5,1% | +/- | |
| PRECISE (1996) | Carvedilol | 276 | +5% | +/- | +/- |
| MOCHA (1996) | Carvedilol | 345 | +6% | +/- | +/- |
Trên bệnh nhân suy tim, sử dụng lâu dài thuốc chẹn β cho thấy có cải thiện về huyết động học: tăng stroke work index, tăng EF, giảm áp lực mao mạch phổi bít. Tuy nhiên, cardiac index thường không thay đổi do nhịp tim chậm. Còn mặt cải thiện về thiện về thời gian gắng sức thì những công trình cho thấy nhiều kết quả khác nhau.
Sự dụng thuốc chẹn β lâu dài cũng làm giảm số lần cần nhập viện vì nguyên nhân tim mạch, vì suy tim cũng như nhập viện do mọi nguyên nhân. Thuốc cũng làm giảm thời gian nằm viện.
| Bảng 8.3 Sử dụng chẹn β làm giảm tỷ lệ tái nhập viện ở bệnh nhân suy tim | |||
| Thử nghiệm | n | Nhập viện | p |
| MDC (1993) | 383 | 26% Metoprolol 44% Placebo | 0,04 |
| CIBIS (1994) | 641 | 19% Bisoprolol 28% Placebo |
0,01 |
| ANZ (1997) | 1094 | 14,1% Carvedilol 19,6% Placebo |
|
| CIBIS II | 2647 | Mọi nguyên nhân:
33,6% Bisoprolol Suy tim: 11,9% Bisoprolol |
0,002 0,00005 |
Những nghiên cứu trước đây cũng không cho kết luận rõ ràng về việc dùng thuốc chẹn β có làm giảm tỷ lệ tử vong hay không. Tuy nhiên, những nghiên cứu gần đây đã cho kết quả thuyết phục, đặc biệt là hai công trình CIBIS II và MERIT – HF.
CIBIS II (Cardiac Insufficiency Bisoprolol study II): nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược trên 2647 bệnh nhân suy tim, EF ≤ 35%, NYHA III – IV. Tỷ lệ tử vong ở nhóm bisoprolol thấp hơn so với nhóm dùng placebo (11,8% so với 17,3%, p < 0,0001), tử vong do mọi nguyên nhân giảm 34%.
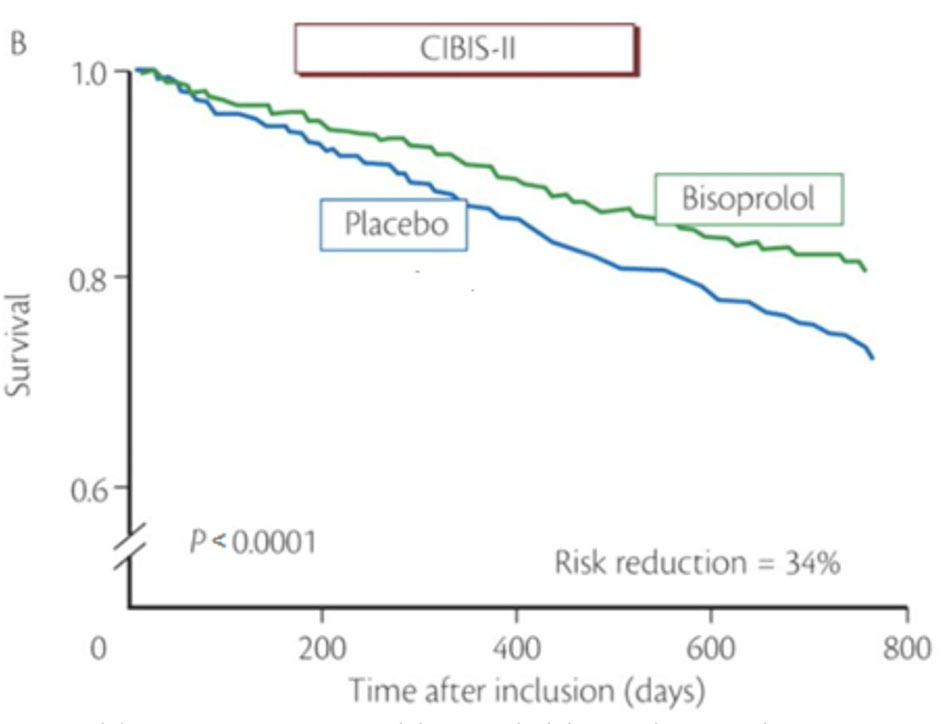
MERIT – HF (Metoprolol CR/XL Randomized Intervention Trial in Heart Failure): nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược trên 3991 bệnh nhân suy tim, EF ≤ 40%, NYHA II – IV. Tỷ lệ tử vong ở nhóm metoprolol CR/XL thấp hơn so với nhóm dùng placebo (7,2 so với 11%, p = 0,0062), tử vong do mọi nguyên nhân giảm 34%.
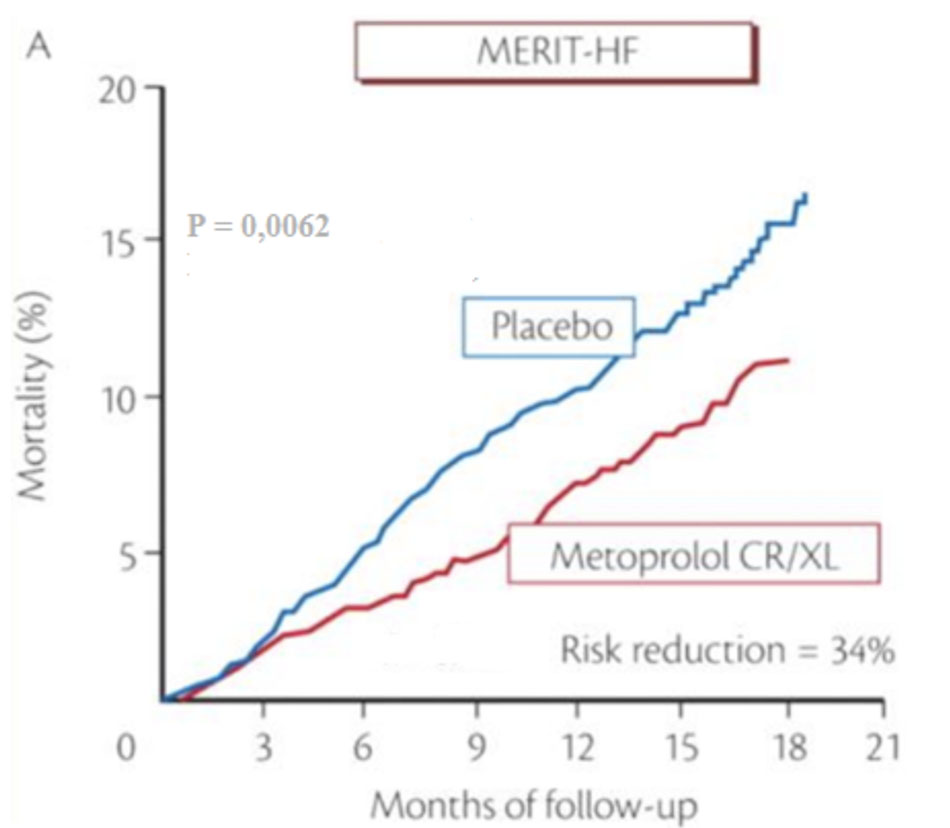
Trong một phân tích gộp (meta – analysis) từ 22 công trình thử nghiệm ngẫu nhiên, có so sánh với placebo về hiệu quả của chẹn β trên 10135 bệnh nhân suy tim cho thấy:
- Tỷ lệ tử vong giảm 35%.
- Tỷ lệ nhập viện giảm 36%.
Ngoài ra, một phân tích gộp khác từ 23 công trình thử nghiệm ngẫu nhiên, có so sánh với placebo về hiệu quả của chẹn β trên 19209 bệnh nhân suy tim (EF 17 – 36%) cho kết quả có ý nghĩa thống kê:
- Mức giảm tần số tim liên quan có ý nghĩa thống kê với tỷ lệ sống còn ở bệnh nhân suy tim được điều trị bằng thuốc chẹn β.
- Tần số tim giảm 5 nhịp/phút thì nguy cơ tử vong giảm 18%.
- Tần số tim lúc nghỉ khuyến cáo cho bệnh nhân suy tim là 70 chu kỳ/phút.
Tiếp sau đó là các công trình lớn nghiên cứu về thuốc chẹn β thế hệ thứ ba cũng đã cho những kết quả khả quan, tập trung nhiều vào carvedilol – một thuốc chẹn β không chọn lọc, đặc biệt được khẳng định qua công trình quan trọng COPERNICUS.
COPERNICUS (Effect of Carvedilol on Survival in Severe Chronic Heart Failure): nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đối chứng giả dược trên 2289 bệnh nhân suy tim, EF ≤ 25%, NYHA III – IV. Tỷ lệ tử vong ở nhóm carvedilol thấp hơn so với nhóm dùng placebo (11% so với 17%, p = 0,00013), tử vong do mọi nguyên nhân giảm 35%.
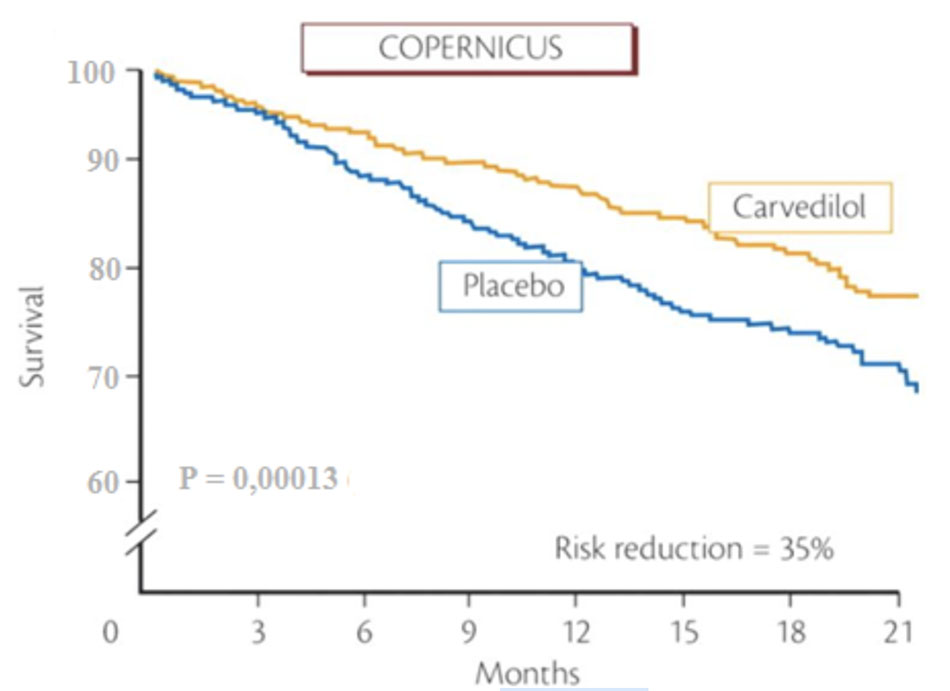
Trong thập niên gần đây, một thuốc chẹn β thế hệ thứ ba khác cũng đã được chứng minh là có tác dụng tốt trên bệnh nhân suy tim, đó là nebivolol. Nebivolol là một thuốc chẹn β có tính chọn lọc cao trên tim và gây dãn mạch ngoại biên qua trung gian NO.
SENIORS (Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors With Heart Failure): nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược trên 2128 bệnh nhân suy tim, tuổi ≥ 70 có tiền sử suy tim, hoặc EF ≤ 35%. Tiêu chí gộp chính là tử vong do mọi nguyên nhân và nhập viện do nguyên nhân tim mạch ở nhóm nebivolol thấp hơn so với placebo (31,1% so với 35,3%, p = 0,039), tiêu chí gộp chính giảm 14% . Ngoài ra, nebivolol cũng giúp tăng EF và giảm kích thước tim.
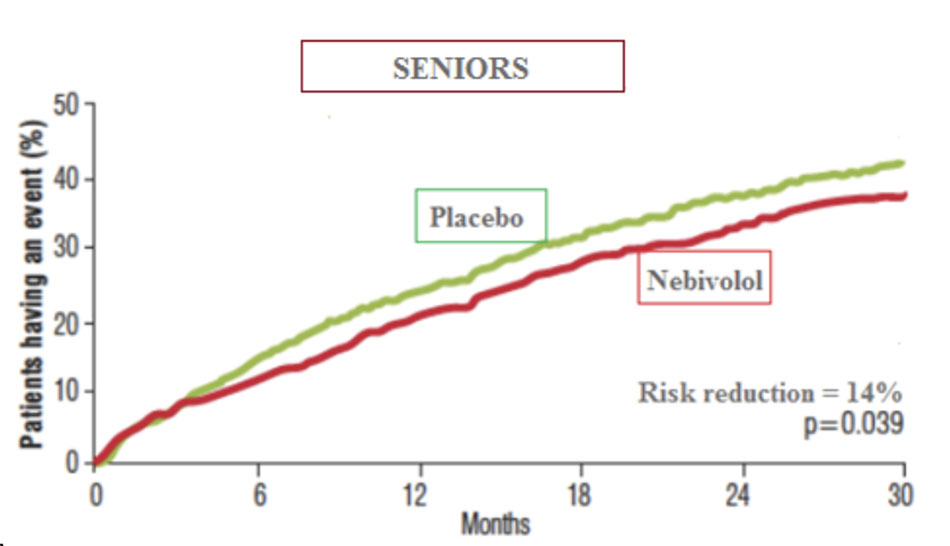
d. Thực hành lâm sàng thuốc chẹn β trong điều trị suy tim
Chúng ta sử dụng một trong bốn thuốc chẹn β đã được chứng minh là giảm tỷ lệ tử vong cũng như tiêu chí gộp tử vong/nhập viện (đó là metoprolol succinate, bisoprolol, carvedilol và nebivolol). Tại Hoa Kỳ, hiện chỉ có metoprolol succinate và carvedilol được công nhận, còn tại châu Âu thêm một thuốc được chấp nhận là bisoprolol. Việc điều trị lâu dài với chẹn β giúp làm giảm triệu chứng suy tim, cải thiện tình trạng lâm sàng của bệnh nhân và tăng cảm giác khỏe khoắn.
Chúng ta cho chẹn β ở mọi bệnh nhân suy tim có EF giảm khi tình trạng ổn định, trừ khi có chống chỉ định hay không dung nạp. Các thuốc chẹn β nên cho càng sớm càng tốt; ở các bệnh nhân ít triệu chứng hay đã thuyên giảm hay không cải thiện triệu chứng sau khi dùng thuốc, vẫn nên tiếp tục kê toa chẹn β do hiệu quả làm giảm nguy cơ tử vong và cải thiện tiến triển bệnh:
- Không sử dụng chẹn β trên những bệnh nhân suy tim nặng, mất bù, đang cần dùng thuốc bằng đường tĩnh mạch. Nghiên cứu COPERNICUS cho thấy có thể dùng carvedilol trên bệnh nhân suy tim nặng NYHA IV.
- Tôn trọng các chống chỉ định của thuốc: block nhĩ thất cao độ, nhịp chậm, suy nút xoang, hen phế quản, đợt cấp các bệnh phổi…
- Thêm thuốc chẹn β vào điều trị suy tim kinh điển: lợi tiểu + ức chế men chuyển +/- digitalis.
- Triệu chứng lâm sàng có thể chỉ cải thiện sau 2 – 3 tháng dùng thuốc.
Khởi đầu bằng liều rất thấp, tăng liều gấp đôi dần mỗi 2 – 4 tuần khi bệnh nhân dung nạp được thuốc ở liều thấp. Ta cần theo dõi chặt chẽ sinh hiệu và triệu chứng khi tăng liều. Các thầy thuốc nên cố gắng đạt được liều đích ngay cả khi triệu chứng không cải thiện, việc điều trị lâu dài nên duy trì để làm giảm các biến cố tim mạch. Không nên ngưng các thuốc chẹn β đột ngột vì có thể làm bệnh xấu đi.
| Bảng 8.4 Liều chẹn β theo khuyến cáo ESC 2016 | ||
| Chẹn β | Liều đầu (mg/ngày) | Liều đích (mg/ngày) |
| Metoprolol succinate (CR/XL) | 12,5 – 25 | 200 |
| Bisoprolol | 1,25 | 10 |
| Carvedilol | 3,125 x 2 | 25 x 2 (d) |
| Nebivolol (c) | 1,25 | 10 |
(c): Điều trị này không chứng minh giảm tử vong tim mạch hay tử vong do mọi nguyên nhân ở bệnh nhân suy tim hoặc sau nhồi máu cơ tim. (d): Có thể dùng liều tối đa 50mg hai lần mỗi ngày cho bệnh nhân nặng hơn 85kg.
Khi khởi đầu thuốc chẹn β, ta có thể gặp bốn loại tác dụng bất lợi sau: ứ dịch kèm suy tim nặng hơn, mệt mỏi, nhịp tim chậm và tụt huyết áp.
Tùy từng trường hợp sẽ có hướng dẫn xử trí cụ thể. Triệu chứng/dấu hiệu suy tim xấu đi (tăng khó thở, mệt mỏi, phù, tăng cân):
- Nếu sung huyết, tăng liều thuốc lợi tiểu hoặc giảm nửa liều ức chế β.
- Nếu mệt hoặc nhịp tim chậm đáng kể, giảm nửa liều ức chế β, đánh giá lại bệnh nhân trong 1 – 2 tuần sau, nếu không được cải thiện tìm tư vấn chuyên môn.
- Nếu tình trạng nặng hơn, ngừng điều trị ức chế β.
Nhịp chậm:
- Nếu < 50 chu kỳ/phút và triệu chứng suy tim nặng, cần giảm nửa liều ức chế β, hoặc nếu triệu chứng nặng hơn, xem xét ngừng ức chế β.
- Cần xem xét nhu cầu các thuốc làm chậm nhịp tim khác (VD: digoxin, amiodarone, diltiazem, hoặc verapamil). – Đo ECG để loại trừ block tim.
Huyết áp thấp:
- Nếu không có triệu chứng, thường không đòi hỏi bất kỳ sự thay đổi nào trong điều trị.
- Nếu có triệu chứng: trường hợp nhẹ (chóng mặt, choáng váng nhẹ, hoặc lẫn lộn và huyết áp thấp, xem xét lại nhu cầu nitrat, ức chế Ca, và các thuốc dãn mạch khác) giảm/dừng các thuốc này nếu được. Nếu không có dấu hiệu hoặc triệu chứng của sung huyết, xem xét việc giảm liều thuốc lợi tiểu.
Nguyên tắc chung:
- Trước khi điều trị, đánh giá kỹ lượng bệnh nhân là điều tối cần thiết.
- Sau khi bắt đầu điều trị, theo dõi cẩn thận bệnh nhân là điều bắt buộc.
Kết luận:
1. Chẹn β đã được chứng minh đem lại lợi ích sống còn cho bệnh nhân suy tim trên phương diện cả lý thuyết lẫn lâm sàng.
2. Bên cạnh các thuốc điều trị suy tim kinh điển, chẹn β cũng nên được cho ở mọi bệnh nhân suy tim có EF giảm khi tình trạng ổn định, trừ khi có chống chỉ định hay không dung nạp thuốc.
3. Hiện nay, chỉ có bốn thuốc chẹn β được công nhận trong điều trị suy tim tại Việt Nam: metoprolol succinate, bisoprolol, carvedilol và nebivolol.
4. Theo dõi chặt chẽ bệnh nhân khi điều trị bằng thuốc chẹn β, cố gắng duy trì đến liều đích để đạt hiệu quả tối ưu. Luôn nhớ rằng có chẹn β là tốt hơn không có chẹn β.
4. Thuốc đối kháng thụ thể mineralocorticoid và vai trò trong điều trị suy tim
a. Vài nét lịch sử của thuốc đối kháng thụ thể mineralocorticoid (MRAs) trong điều trị suy tim
Trong thập niên 50 của thế kỷ trước, sự hiểu biết ngày càng rõ về vai trò của việc phong bế tác dụng aldosterone – một hormon giữ muối và nước, trong cân bằng nội môi và kiểm soát huyết áp đã mở ra một cuộc tìm kiếm các hợp chất mới. Một loạt các hợp chất steroide đã được nghiên cứu, phát triển nhưng đáng tiếc kết quả lại không cho các tín hiệu khả quan.
Đến năm 1957, một chất ức chế tác dụng của aldosterone đã được nghiên cứu thành công, đó chính là spironolactone – một chất lợi tiểu đối kháng thụ thể mineralocorticoid.
Trong nghiên cứu này, lợi ích chủ yếu mà spinorolactone mang lại là bảo vệ bệnh nhân khỏi tình trạng hạ Kali máu liên quan hydrochlorothiazide.
Trong những năm 60 của thế kỷ XX, quan niệm về mô hình sinh bệnh học của suy tim là các rối loạn về huyết động học liên quan đến ứ đọng tuần hoàn và giảm cung lượng tim. Điều đó đưa đến việc các lợi tiểu là lựa chọn điều trị chính ở bệnh nhân suy tim bên cạnh các digitalis.
Cuối thập niên 80 – đầu thập niên 90, sự ra đời của quan niệm thần kinh thể dịch trong tiến trình suy tim đã đưa đến việc spironolactone không còn được ưa chuộng trong điều trị. Cuối thập niên 90, các công trình nghiên cứu lại diễn ra cho thấy nếu sử dụng spinorolactone ở liều thấp thích hợp sẽ làm chậm tiến triển suy tim và cải thiện tỷ lệ tử vong. Thuốc MRAs đã lấy lại chỗ đứng trong điều trị suy tim.
Đến năm 1984, chất ức chế tác dụng của aldosterone thứ hai được nghiên cứu thành công, đó chính là eplerenone – một dẫn xuất của spironolactone nhưng có tính chọn lọc cao hơn giúp ngăn ngừa một số tác dụng phụ. Tuy nhiên, mãi đến năm 2004, nó mới được FDA Mỹ chấp thuận.
Các thử nghiệm lâm sàng đã chứng minh được vai trò của thuốc MRAs trong điều trị suy tim:
- 1999: RALES (Randomized Aldactone Evaluation Study).
- 2003: EPHESUS (Eplerenone Post – AMI Heart Failure Efficacy and Survival Study).
- 2011: EMPHASIS – HF (Eplerenone in Mild Patients Hospitalization and Survival Study in Heart Failure).
b. Cơ chế tác động của thuốc đối kháng thụ thể mineralocorticoid
Như ta đã biết, aldosterone là một yếu tố tham gia vào cơ chế bù trừ trong suy tim thông qua hệ renin – angiotensin. Nhưng cũng như đã đề cập ở các phần trên, dưới tác dụng lâu dài của aldosterone lại đem đến những bất lợi cho tim. Vì vậy, hạn chế tác dụng của aldosterone là một điều cần thiết trong điều trị suy tim tiến triển. Trên cơ bản, việc sử dụng các thuốc ACEi/ARBs cũng gián tiếp ức chế sản sinh aldosterone từ đó hạn chế tác dụng của nó. Tuy nhiên, nên nhớ rằng sự điều hòa sản xuất aldosterone không đơn thuần là do hệ renin – angiotensin kiểm soát. Aldosterone được sản xuất từ các tế bào zona glomerulosa ở vỏ thượng thận, thông qua các con đường truyền tín hiệu phức tạp từ các hệ thống điều hòa chính gồm: nồng độ Kali huyết thanh, hệ renin – angiotensin và hormone tuyến thượng thận. Điều đó cho thấy thuốc MRAs vẫn cần thiết cho bệnh nhân suy tim.
Spironolactone và eplerenone ngăn chặn tác dụng của aldosterone bằng cách đối kháng cạnh tranh trên các thụ thể mineralocorticoid tại ống lượn xa và ống góp từ đó làm bất hoạt các kênh Na + , K + và bơm Na + – K + dẫn đến việc không tái hấp thu Natri và bài tiết Kali. Trong đó, tác dụng ngăn tái hấp thu Natri là có lợi vì hạn chế sự ứ đọng tuần hoàn, nhưng trái lại tăng Kali máu là một bất lợi cần xem xét kỹ cho bệnh nhân.
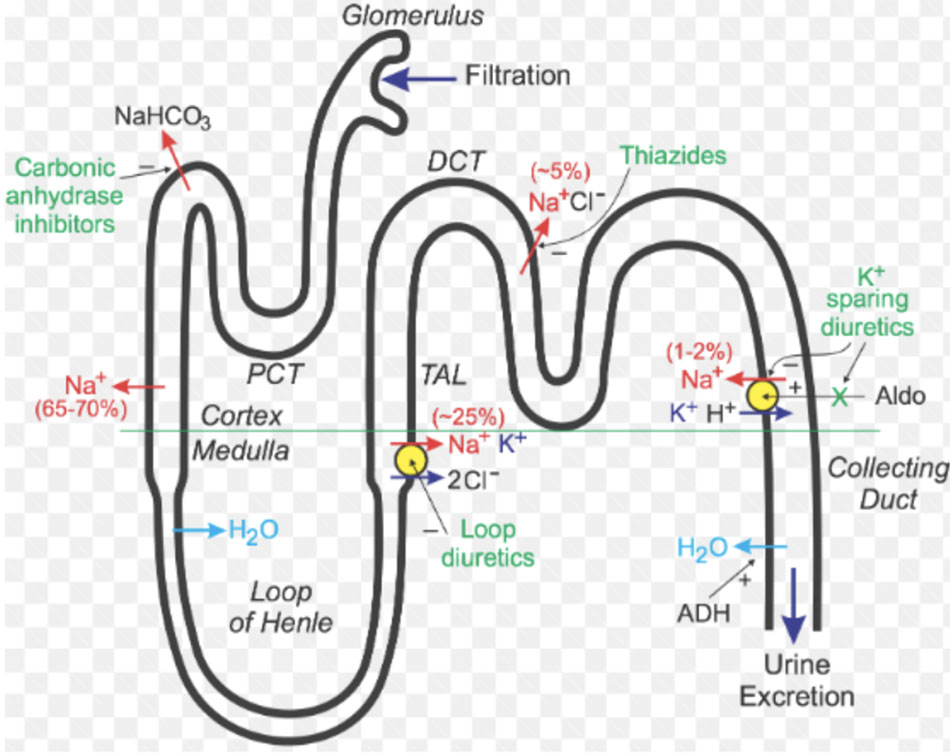
c. Hiệu quả và các thử nghiệm lâm sàng của thuốc đối kháng thụ thể mineralocorticoid trong điều trị suy tim
Nghiên cứu RALES là thử nghiệm lâm sàng quan trọng đầu tiên cho thấy lợi ích sống còn với thuốc MRAs: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đa quốc gia, đối chứng giả dược trên 1663 bệnh nhân suy tim, NYHA III – IV, EF ≤ 35%, trên nền điều trị ACEi + lợi tiểu quai +/- digoxin. Sau 24 tháng theo dõi, tỷ lệ tử vong do mọi nguyên nhân ở nhóm spironolactone thấp hơn nhóm placebo (34,6% soi với 45,9%, p < 0,001), mức giảm tỷ lệ này là 30%. Đồng thời, giảm nguy cơ tử vong do nguyên nhân tim mạch 31% (p < 0,001), nhập viện do suy tim 35% (p < 0,001) và cải thiện có ý nghĩa phân độ NYHA (p < 0,001).
| Bảng 8.5 Nghiên cứu RALES, so sánh hiệu quả giữa spironolactone và placebo trên bệnh nhân suy tim | ||||
| Spironolactone(%) | Placebo (%) | Risk reduction (%) | P | |
| All – cause mortality | 34,6 | 45,9 | 30 | < 0,001 |
| CV death | 27,5 | 37,3 | 31 | < 0,001 |
| Hospitalization for HF | – | – | 35 | < 0,001 |
| Gynecomastia | 9,1 | 1,3 | – | < 0,001 |
| Breast pain | 2 | 0,1 | – | 0,006 |
Hai công trình lớn là EPHESUS và EMPHASIS – HF đã chỉ ra những lợi ích rõ ràng của eplerenone trong điều trị suy tim.
EPHESUS: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, nhóm song song, đối chứng giả dược trên 6632 bệnh nhân sau nhồi máu cơ tim có biến chứng rối loạn chức năng thất trái và suy tim hay đái tháo đường, NYHA II – IV, EF ≤ 40%. Sau thời gian theo dõi trung bình 16 tháng, nhóm eplerenone giảm tỷ lệ tử vong do mọi nguyên nhân 15% (p = 0,008), giảm tỷ lệ tử vong do nguyên nhân tim mạch 17% (p = 0,005) và giảm tiêu chí gộp tử vong do nguyên nhân tim mạch/nhập viện vì suy tim 13% (p = 0,002) so với nhóm placebo.
EMPHASIS – HF: nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược trên 2737 bệnh nhân suy tim, NYHA II, EF ≤ 30% hoặc EF 30 – 35% có QRS > 130s. Sau theo dõi trung bình 21 tháng, giảm tiêu chí gộp tử vong tử vong do nguyên nhân tim mạch/nhập viện vì suy tim ở nhóm eplerenone so với nhóm placebo (18,3% so với 25,9%, p < 0,0001), mức giảm tỷ lệ này là 37%. Đồng thời, giảm tỷ lệ tử vong do mọi nguyên nhân khoảng 24% (p = 0,008) và tử vong do nguyên nhân tim mạch 24% (p = 0,01), giảm tỷ lệ nhập viện suy tim 42% (p < 0,001).
| Bảng 8.6 Tóm tắt kết quả từ hai nghiên cứu EPHESUS và EMPHASIS – HF, lợi ích của eplerenone trong điều trị suy tim | ||||
| EPHESUS | ||||
| Eplerenone (%) | Placebo (%) | Risk reduction (%) | P | |
| All – cause mortality | – | – | 15 | 0,008 |
| CV death | – | – | 17 | < 0,001 |
| CV death or Hospitalization for HF | – | – | 13 | 0,002 |
| EMPHASIS – HF | ||||
| Eplerenone (%) | Placebo (%) | Risk reduction (%) | P | |
| All – cause mortality | 12,5 | 15,5 | 24 | 0,008 |
| CV death | – | – | 24 | 0,01 |
| Hospitalization for HF | – | – | 42 | < 0,001 |
| CV death or Hospitalization for HF | 18,3 | 25,9 | 37 | < 0,001 |
d. Ứng dụng thuốc đối kháng thụ thể mineralorcorticoid trong điều trị suy tim
Thuốc MRAs được khuyến cáo điều trị cho bệnh nhân suy tim có EF giảm từ giải đoạn C trở đi hay dự phòng đột tử ở bệnh nhân suy tim sau nhồi máu cơ tim.
Ngoài tác dụng, của một lợi tiểu giúp làm giảm các triệu chứng suy tim, thuốc MRAs còn có khả năng ngăn chặn sự phì đại, xơ hóa cơ tim và cải thiện độ đàn hồi mạch máu từ đó tránh tái định dạng cơ tim và mạch máu. Với các lợi ích đã được chứng minh, thuốc MRAs nên được dùng trên các bệnh nhân suy tim đang điều trị nền với thuốc ACEi + chẹn β nhưng vẫn còn triệu chứng và EF giảm. Cùng với thuốc ACEi/ARBs và chẹn β thì thuốc MRAs đã tạo thành bộ ba cải thiện sống còn ở bệnh nhân suy tim. Sử dụng thuốc MRAs một cách thích hợp và thận trọng sẽ góp phần ngăn cản sự tiến triển, cải thiện sống còn và chất lượng cuộc sống ở bệnh nhân suy tim:
- Không nên sử dụng khi độ thanh thải creatinine < 30 ml/phút hoặc Kali máu > 5 mmol/l.
- Nên khởi đầu bằng liều thấp 12,5 mg spironolactone hoặc 25 mg eplerenone.
- Xem xét điều chỉnh liều lên sau 4 – 8 tuần. Kiểm tra sinh hóa máu tại thời điểm 1 và 4 tuần sau khi khởi trị/tăng liều và tại thời điểm 8 – 12 tuần; 6, 9, 12 tháng; và mỗi 4 tháng sau đó.
- Nguy cơ tăng Kali máu nếu dùng chung với liều cao ACEi/ARBs. Nên sử dụng ở liều thấp ở một trong hai nhóm.
- Phải tránh dùng chung với kháng viêm không steroid và chất ức chế cyclo oxygenase – 2 (COX – 2 inhibitors).
- Phải ngưng cho thêm Kali hoặc giảm liều nếu bệnh nhân đang bổ sung Kali.
| Bảng 8.7 Liều khuyến cáo thuốc MRAs theo ESC 2016 | ||
| Spironolactone | 25 | 50 |
| Eplerenone | 25 | 50 |
| Bảng 8.8 Liều khuyến cáo thuốc MRAs theo VNHA 2017 | ||||
| Eplerenone | Spironolactone | |||
| eGFR (ml/ph/1,73 m2) | ≥ 50 | 30 đến 49 | ≥ 50 | 30 đến 49 |
| Liều khởi đầu (chỉ khi K + máu ≤ 5 mEq/L) | 25 mg ngày 1 lần | 25 mg/lần, cách ngày |
12.5 đến 25 mg ngày 1 lần | 12.5 mg/lần mỗi ngày hoặc cách ngày |
| Liều duy trì (sau 4 tuần với K + máu ≤ 5 mEq/L) * | 50 mg ngày 1 lần | 25 mg ngày 1 lần | 25 mg 1 hoặc 2 lần/ngày | 12.5 đến 25 mg ngày 1 lần |
(*) sau liều khởi đầu, K + máu tăng ≤ 6.0 mEq/L hoặc chức năng thận xấu hơn, ngưng thuốc cho đến khi K + < 5.0 mEq/L. Cân nhắc sử dụng lại giảm liều sau khi hết tăng K + máu/hồi phục chức năng thận ít nhất được 72 giờ.
Khi sử dụng thuốc MRAs, bệnh nhân dễ gặp hai tác dụng không mong muốn là tăng Kali máu và nữ hóa tuyến vú ở nam. Hướng xử trí cụ thể sẽ được hướng dẫn dưới đây. Chức năng thận xấu đi/tăng Kali máu:
- Nếu Kali > 5,5 mmol/L hoặc creatinin > 221 mmol/L (2,5 mg/dL)/eGFR < 30 mL/phút/1,73 m2, giảm nửa liều và theo dõi sinh hóa máu chặt chẽ.
- Nếu Kali > 6,0 mmol/L hoặc creatinine > 310 mmol (3,5 mg/dL) eGFR < 20 mL/phút/1,73 m2, dừng ngay MRA. Tăng kali máu (> 6,0 mmol/L) không thường gặp trong thử nghiệm RALES và EMPHASIS – HF nhưng nó phổ biến hơn trong thực hành lâm sàng.
- Ngược lại, Kali ở mức bình thường – cao thường được mong muốn ở những bệnh nhân suy tim, đặc biệt đang dùng digoxin. – Điều quan trọng là tránh các thuốc tăng Kali khác (ví dụ như amiloride và triamterene) và các thuốc độc thận (ví dụ NSAID).
Nữ hóa tuyến vú: bệnh nhân nam được điều trị bằng spironolactone có thể phát triển sự khó chịu ở vú hoặc nữ hóa tuyến vú, trong trường hợp này các khuyến cáo đề nghị chuyển sang eplerenone.
Kết luận:
- MRAs đã được chứng minh đem lại lợi ích sống còn cho bệnh nhân suy tim trên phương diện cả lý thuyết lẫn lâm sàng.
- MRAs là thuốc được khuyến cáo sử dụng điều trị chỉ sau ACEi và chẹn β.
- Cả hai thuốc MRAs được chấp thuận có hiệu quả tương đương nhau, nên việc dùng thuốc là tùy thầy thuốc và bệnh nhân.
- Khởi đầu điều trị với liều thấp nhất, tăng liều nếu dung nạp tốt, điện giải/chức năng thận ổn định. Theo dõi chặt chẽ bệnh nhân khi điều trị bằng thuốc MRAs, nhất là khi có tình trạng tăng Kali máu.
5. Vai trò của tần số tim và hiệu quả của ivabradine trong điều trị suy tim
a. Vai trò của tần số tim trong dự hậu bệnh nhân suy tim
Các nhà khoa học đã chứng minh được rằng tần số tim có liên quan đến dự hậu tử vong của bệnh lý tim mạch. Các nghiên cứu về mặt dịch tễ học, về sinh lý bệnh học và đặc biệt là về lâm sàng đều có kết quả tương đồng là khi giảm tần số tim thì dự hậu tử vong của các bệnh lý tim mạch được cải thiện.
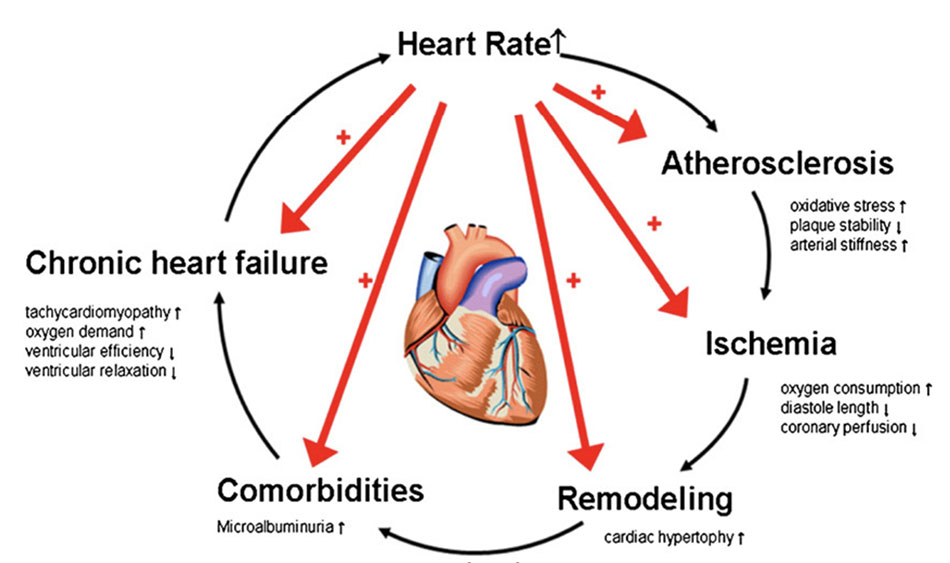
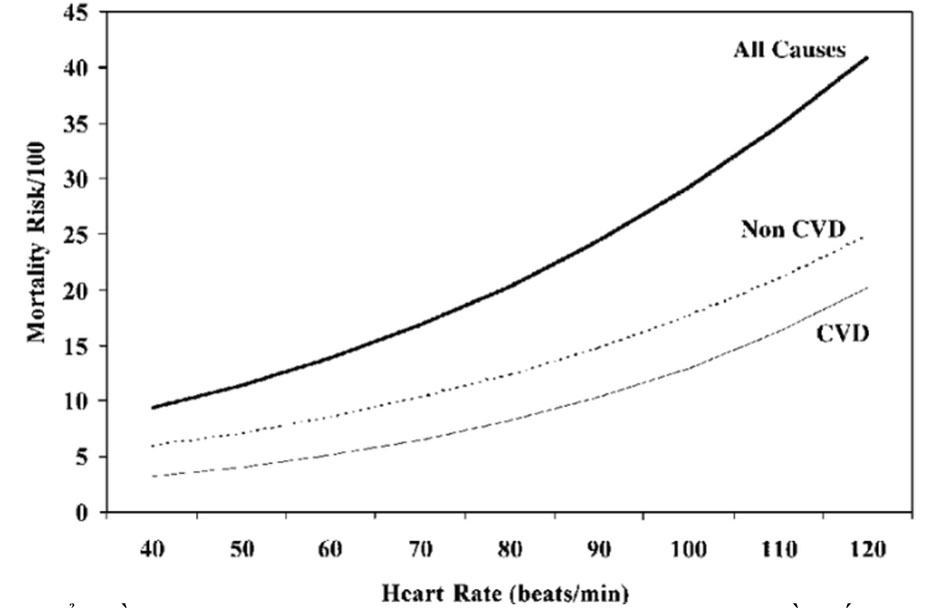
Ở đối tượng bệnh nhân suy tim, tần số tim cũng quyết định đến tiên lượng bệnh. Cho dù bệnh nhân có được dùng chẹn β hay không thì nhóm có tần số tim cao vẫn có tỷ lệ tử vong cao hơn một cách có ý nghĩa thống kê.
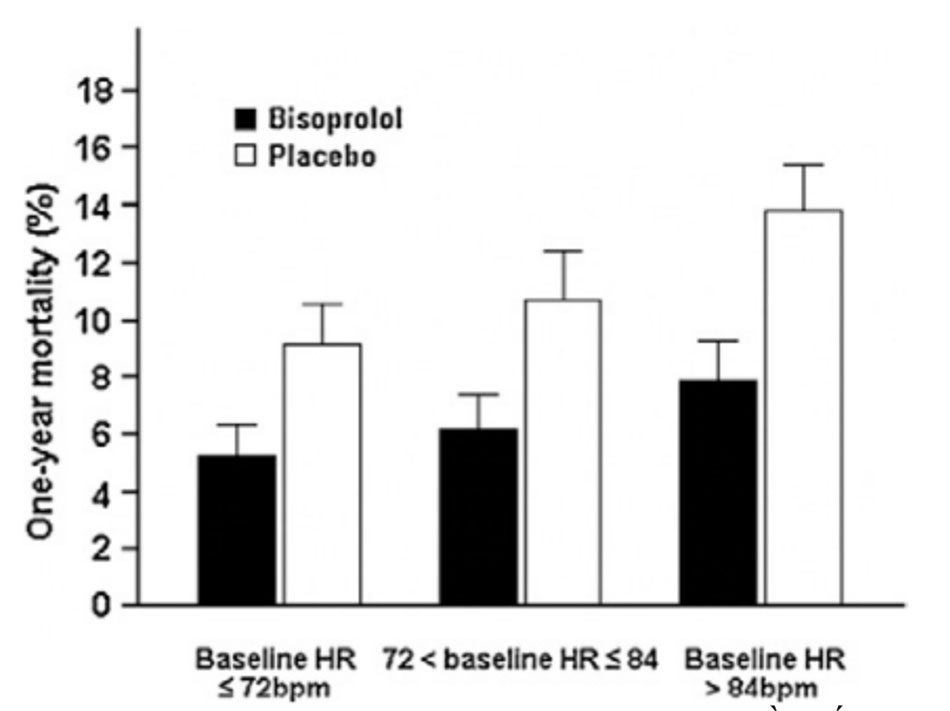
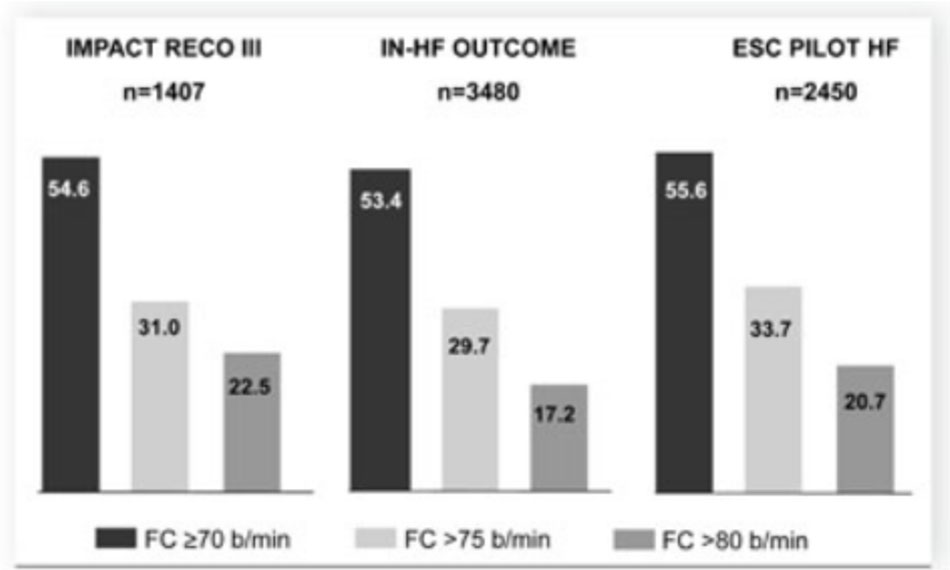
Như vậy, chúng ta thấy rằng tần số tim rất quan trọng đối với dự hậu của bệnh nhân có bệnh tim mạch nói chung và suy tim nói riêng. Chúng ta đã có đủ những nghiên cứu chỉ ra dù là người có bệnh tim mạch hay không có bệnh tim mạch thì thì tần số tim càng cao sẽ có tiên lượng không tốt bằng người có tần số tim thấp hơn.
Dựa trên những cơ sở và chứng cứ đó, một loại thuốc mới đã được nghiên cứu và những kết quả đưa ra là rất tích cực. Các bác sĩ tim mạch giờ đây đã có thêm một loại thuốc mới để giúp bệnh nhân cải thiện sự sống còn của minh cũng như cải thiện chất lượng cuộc sống. Đó chính là ivabradine.
b. Tìm hiểu về ivabradine và vai trò của thuốc nay trong các khuyến cáo hiện nay
Năm 1979, Di Francesco đã phát hiện ra kênh I f từ những nghiên cứu trên động vật. Đầu những năm 1990, ivabradine (S16257) được phát triển.
20/11/2014, MDA chấp nhận sử dụng Procoralan (ivabradine) trong điều trị đau thắt ngực và suy tim.
15/4/2015, FDA chấp nhận sử dụng ivabradine trong điều trị suy tim.
Hoạt của của kênh I f ảnh hưởng đến bốn pha của điện thế động nút xoang. Cơ chế tác động chính của ivabradine là ức chế chọn lọc kênh I f ở nút xoang từ đó làm giảm tốc độ khử cực chậm ở pha 4 của điện thế động nút xoang -> làm chậm nhịp xoang.
Qua các nghiên cứu của tác giả Colin, Simon, và Mulder rút ra được rằng ivabradine chỉ làm giảm tần số tim mà không ảnh hưởng đến các tính chất khác của tim. Lợi ích mà ivabradine mang lại là:
- Giảm nhu cầu tiêu thụ oxy cơ tim.
- Cải thiện được tưới máu mạch vành.
- Duy trì được khả năng co bóp cơ tim.
- Bảo vệ cho vùng cơ tim bị thiếu máu.
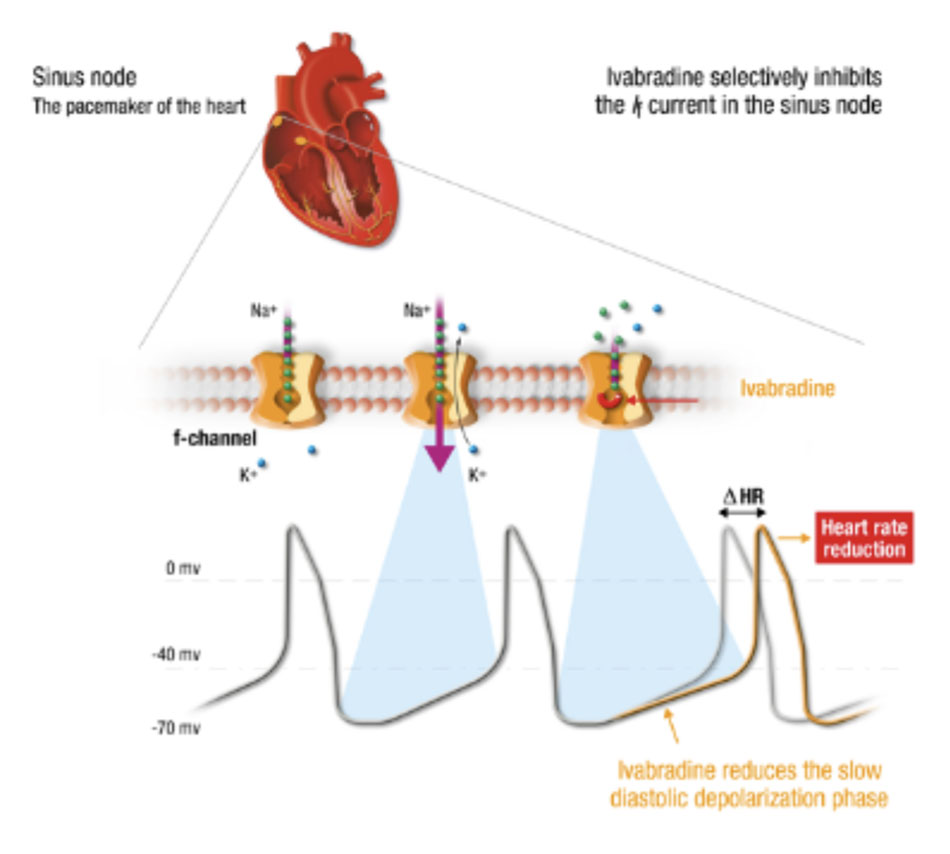
Nghiên cứu chính chứng minh tác dụng có lợi của ivabradine trong điều trị suy tim là SHIfT. Lúc bấy giờ, đây là nghiên cứu lâm sàng về suy tim lớn nhất được thực hiện được thực hiện ở 677 trung tâm trên 37 quốc gia.
SHIfT(Systolic Heart Failure treatment with the I f inhibitor ivabradine Trial): nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đa quốc gia, đối chứng giả dược trên 6505 bệnh nhân suy tim, NYHA II – IV, EF ≤ 35%, tần số tim ≥ 70 lần/phút, nhịp xoang. Sau thời gian theo dõi trung bình 22,9 tháng cho kết quả nhóm ivabradine làm giảm tỷ lệ tử vong do nguyên nhân tim mạch/nhập viên do suy tim nặng lên so với nhóm ivabradine (14,5% so với 17,7%, p < 0,0001), mức giảm tỷ lệ này là 18%. Đồng thời, ivabradine còn làm giảm nguy cơ nhập viện vì suy tim nặng lên 26% (p < 0,0001). Tuy nhiên, nếu chỉ tính riêng tiêu chí là tử vong do nguyên nhân tim mạch hay tử vong do mọi nguyên nhân thì ivabradine có làm giảm những không có ý nghĩa thống kê. Phân tích dưới nhóm cho thấy rằng kết quả của nghiên cứu cũng hằng định với giới tính, độ tuổi, nguyên nhân gây suy tim, mức độ suy tim ban đầu, bệnh nhân có đái tháo đường hoặc có dùng thuốc chẹn β trước nghiên cứu hay không.
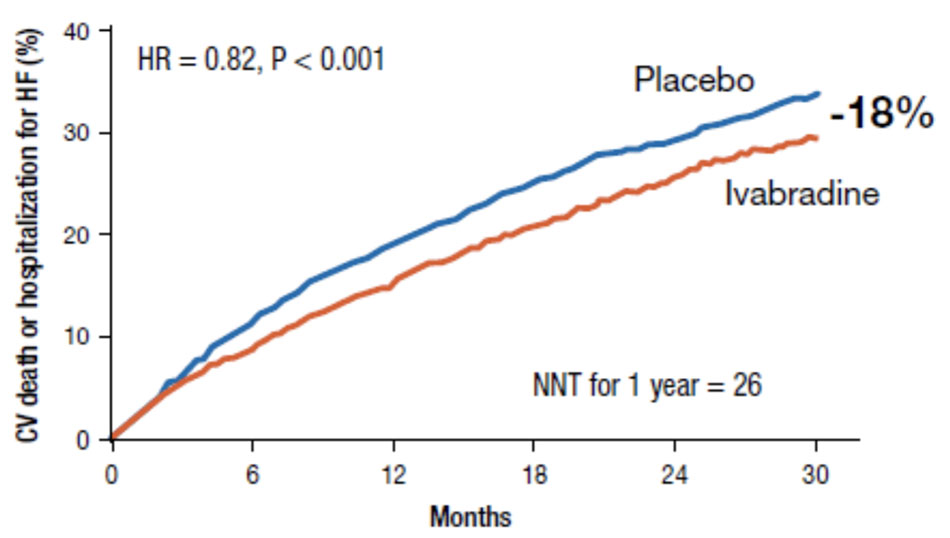
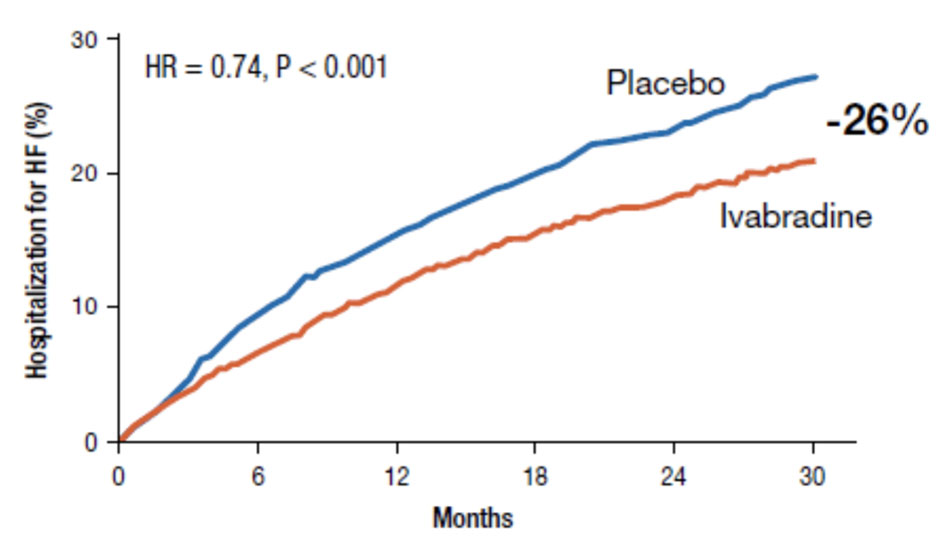
Qua các nghiên cứu dưới nhóm chỉ ra rằng với tác dụng làm giảm tần số tim, ivabradine góp phần cải thiện tình trạng tái cấu trúc cơ tim, cải thiện được các thông số của tim như chỉ số thể tích cuối tâm trương thất trái và phân suất tống máu thất trái từ đó cải thiện tiên lượng sống và chất lượng cuộc sống của bệnh nhân suy tim.
Dựa vào bảng câu hỏi đánh giá chất lượng cuộc sống “Kansas City Car – diomyopathy Questionaire” (KCCQ), sau thời gian theo dõi trung bình 24,5 tháng, kết quả thu được là:
- Bệnh nhân suy tim mạn biểu hiện triệu chứng có chất lượng cuộc sống thấp liên quan đến dự hậu xấu của bệnh.
- Tần số tim lúc nghỉ cao liên quan đến chất lượng cuộc sống thấp.
- Giảm tần số tim bằng ivabradine làm tăng chất lượng cuộc sống.
- Mức độ giảm tần số tim bằng ivabradine liên quan trực tiếp đến mức độ cải thiện chất lượng cuộc sống.
Nghiên cứu SHIfT – echo đưa ra bằng chứng về tác dụng cải thiện chức năng tim của ivabradine: nghiên cứu ngẫu nhiên, mù đôi, đa trung tâm, đa quốc gia, đối chứng giả dược trên 611 bệnh nhân suy tim mạn. Sau 8 tháng điều trị thu được kết quả: tần số tim của nhóm ivabradine giảm nhiều hơn so với nhóm placebo. Đồng thời, thay đổi thể tích cuối tâm thu (LVESVI) và tâm trương (LVEDVI) theo chiều hướng tốt, tăng phân suất tống máu thất trái có ý nghĩa về mặt thống kê.
| Bảng 8.9 Nghiên cứu SHIfT – echo, ivabradine giúp cải thiện chức năng tim | |||
| Hiệu quả điều trị | Ivabradine | Placebo | P |
| Thay đổi tần số tim lúc nghỉ sau 8 tháng (lần/phút) | -14,7 | -5,8 | < 0,001 |
| Thay đổi LVESVI sau 8 tháng (ml/m 2 ) | -7,0 | -0,9 | < 0,001 |
| Thay đổi LVEDVI sau 8 tháng (ml/m 2 ) | -7,9 | -1,8 | 0,002 |
| Thay đổi phân suất tống máu sau 8 tháng (%) | +2,4 | -0,1 | 0,0003 |
Dù mới chỉ có một nghiên cứu lớn, chuẩn về thuốc ivabradine trong điều trị suy tim mạn, nhưng có thể nói rằng đây là thuốc duy nhất được nghiên cứu đầy đủ các khía cạnh về mục tiêu điều trị suy tim mạn so vơi các thuốc đã được dùng trước đây. Theo khuyến cáo của ESC 2016: “Ivabradine được khuyên dùng để giảm nguy cơ nhập viện vì suy tim và chết do nguyên nhân tim mạch ở bệnh nhân có triệu chứng có EF ≤ 35%, có nhịp xoang và tần số ≥ 70/phút dù đã được điều trị bằng thuốc chẹn β với liều dựa trên chứng cứ (hoặc liều tối đa dung nạp được), thuốc ACEi (hoặc ARBs) và thuốc MRAs. Ivabradine được khuyên dùng để giảm nguy cơ nhập viện vì suy tim và chết do nguyên nhân tim mạch ở bệnh nhân có triệu chứng có EF ≤ 35%, có nhịp xoang và tần số ≥ 70/phút không dung nạp hoặc có chống chỉ định với thuốc chẹn β. Bệnh nhân này phải được điều trị bằng thuốc ACEi (hoặc ARBs) và thuốc MRAs.”
Ivabradine khi được sử dụng trên lâm sàng bắt đầu với liều thấp (5 mg x 2 lần/ngày), những bệnh nhân ≥ 75 tuổi, khởi trị liều thấp hơn là 2,5 mg x 2 lần/ngày. Liều hàng ngày có thể tăng lên đến liều đích 7,5 mg x 2 lần/ngày. Giảm liều có thể đến 2,5 mg x 2 lần/ngày hay dừng lại tùy thuộc vào nhịp tim lúc nghỉ của bệnh nhân. Tăng gấp đôi liều không ít hơn khoảng thời gian 2 tuần (tốc độ chậm hơn có thể cần thiết trong một số bệnh nhân). Mục tiêu là đạt liều đích, hoặc liều tối đa có thể dung nạp được dựa trên nhịp tim nghỉ của bệnh nhân. Nếu nhịp tim khi nghỉ là giữa 50 và 60 lần/phút, liều hiện tại nên được duy trì.Theo dõi nhịp tim, huyết áp, và tình trạng lâm sàng.
| Bảng 8.10 Liều khuyến cáo Ivabradine theo ESC 2016 | |
| Liều khởi đầu (mg/ngày) | Liều mục tiêu (mg/ngày) |
| 5 x 2 | 7,5 x 2 |
Khi sử dụng ivabradine, có thể gặp một số vấn đề sau: Nhịp tim khi nghỉ dai dẳng < 50 lần/phút hoặc nếu các triệu chứng nhịp chậm xảy ra:
- Giảm hoặc ngừng điều trị.
- Xem lại nhu cầu cho thuốc giảm tần số tim khác hoặc thuốc tác động vào quá trình chuyển hóa ivabradine tại gan.
- Đo lại ECG để loại trừ các rối loạn nhịp khác ngoài nhịp chậm xoang.
- Tầm soát nguyên nhân thứ phát của rối loạn nhịp chậm (VD: rối loạn chức năng tuyến giáp).
- Nếu bệnh nhân phát triển rung nhĩ dai dẳng/liên tục trong thời gian điều trị với ivabradine, thuốc nên được dừng lại.
Những hiện tượng về thị giác thường thoáng qua và biến mất trong vài tháng đầu điều trị ivbradine và không đi kèm với những rối loạn chức năng võng mạc nghiêm trọng.
Tuy nhiên nếu điều này gây khó chịu cho bệnh nhân xem xét ngừng ivabradine. Trong trường hợp không dung nạp lactose hoặc galactose (thành phần có trong viên thuốc ivabradine), nếu có triệu chứng có thể cần phải dừng thuốc.
Kết luận:
1. Giảm tần số tim có ý nghĩa là một mục tiêu trong điều trị suy tim mạn, đặc biệt với EF giảm.
2. Ivabradine là thuốc chẹn kênh I f đầu tiên được sử dụng trên lâm sàng có tác dụng làm giảm tần số tim.
3. Lợi ích ivabradine mang lại là giúp cải thiện chức năng tim, cải thiện chất lượng cuộc sống và giảm nguy cơ tử vong.
4. Kết hợp sớm ivabradine với chẹn β có tác động hiệp đồng đã được chứng minh.
6. Thuốc ức chế neprilysin kết hợp chẹn thụ thể angiotensin – bước đột phá trong điều trị suy tim.
Dù đã có những tiến bộ trong chẩn đoán và điều trị suy tim nhưng tỷ lệ tử vong vẫn còn cao, có nhiều nguyên nhân để lý giải cho điều đó. Một trong những nguyên nhân là các thuốc điều trị suy tim hiện nay vẫn chưa là tối ưu. Việc tìm hiểu bệnh học suy tim vẫn còn đang phát triển, hiện đang nghiên cứu tới mức phân tử, đồng nghĩa việc điều trị sẽ còn nhiều đột phá hơn nữa. Nhưng hãy trở lại với mô hình hiện tại, liệu có thuốc nào mang lại lợi ích tốt hơn tất thảy những thuốc mà ta đang dùng. Xin thưa câu trả lời đó là angiotensin receptor – neprilysin inhibitor (ARNI).
Cuối năm 2014, Nghiên cứu PARADIGM – HF, được công bố trên tạp chí New England Journal of Medicine, cho thấy ARNI có hiệu quả làm giảm tỷ lệ tử vong và tỷ lệ nhập viện do suy tim vượt trội so với enalapril (trong bối cảnh các ACEi vẫn được xem là tiêu chuẩn trong điều trị suy tim).
Năm 2015, ARNI được FDA chấp thuận trong điều trị suy tim. Năm 2016, ARNI có mặt trong các khuyến cáo điều trị suy tim của ACC/AHA/HFSA và ESC.
Đúng như cái tên của nó, LCZ696 – hợp chất ARNI đầu tiên, thực sự là một sự kết hợp hoàn hảo của một thuốc chẹn thụ thể angiotensin mà ta đã biết valsartan với một hoạt chất mới ức chế men neprlysin có tên sacubitril. Tác dụng của các peptide lợi niệu như đã biết là đối ngược lại với sự hoạt hóa hệ thần kinh giao cảm và hệ renin – angiotensin – aldosterone, ngăn cản sự tiến triển bất lợi trong tiến trình suy tim. Như vậy, sự kết hợp này bản chất là một sự tăng cường về tính lợi và một sự kiềm chế về tính hại trong tiến trình suy tim.
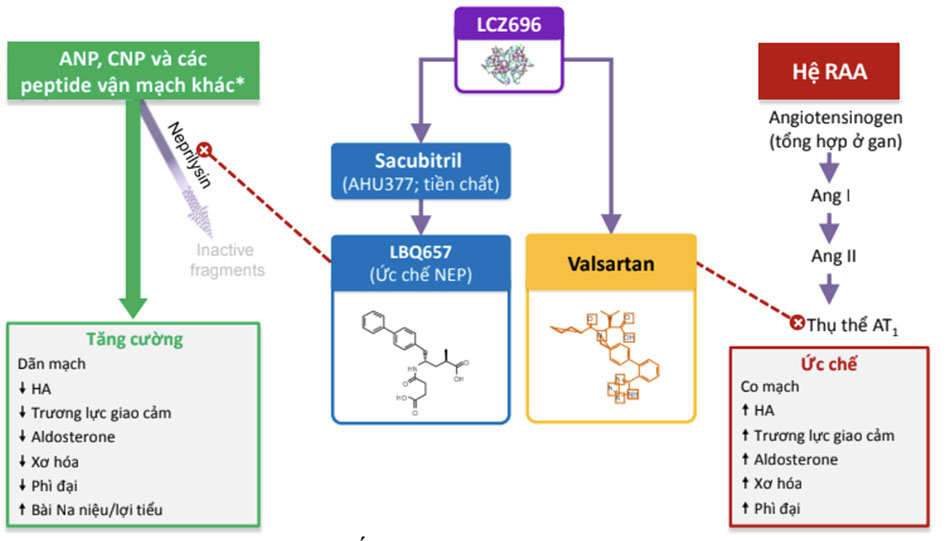
Trên phương diện lâm sàng, nghiên cứu PARADIGM – HF (Angiotensin –Neprilysin Inhibition versus Enalapril in Heart Failure) đã chứng tỏ được những hiệu quả vượt trội của LCZ696 so với enalapril.
PARADIGM – HF: nghiên cứu ngẫu nhiên, mù đơn, mù đôi, đa trung tâm, có đối chứng trên 8442 bệnh nhân suy tim, NYHA II – IV, EF ≤ 40%. Sau thời gian theo dõi trung bình 27 tháng, kết quả cho thấy so với enalapril, LCZ696 giảm 20% nguy cơ chết do nguyên nhân tim mạch (13,3% so với 16,5%, p = 0,00008), giảm 21% nhập viện vì suy tim (12,8% so với 15,6%, p = 0,00008) và giảm 16% (17% so với 19,8%, p = 0,0009) tử vong do mọi nguyên nhân. LCZ696 nói chung dung nạp tốt, ngoại trừ tỷ lệ hạ huyết áp có triệu chứng cao hơn, mặc dù không tăng tỷ lệ ngừng điều trị do hạ huyết áp. Không có sự khác biệt về tỷ lệ phù mạch.
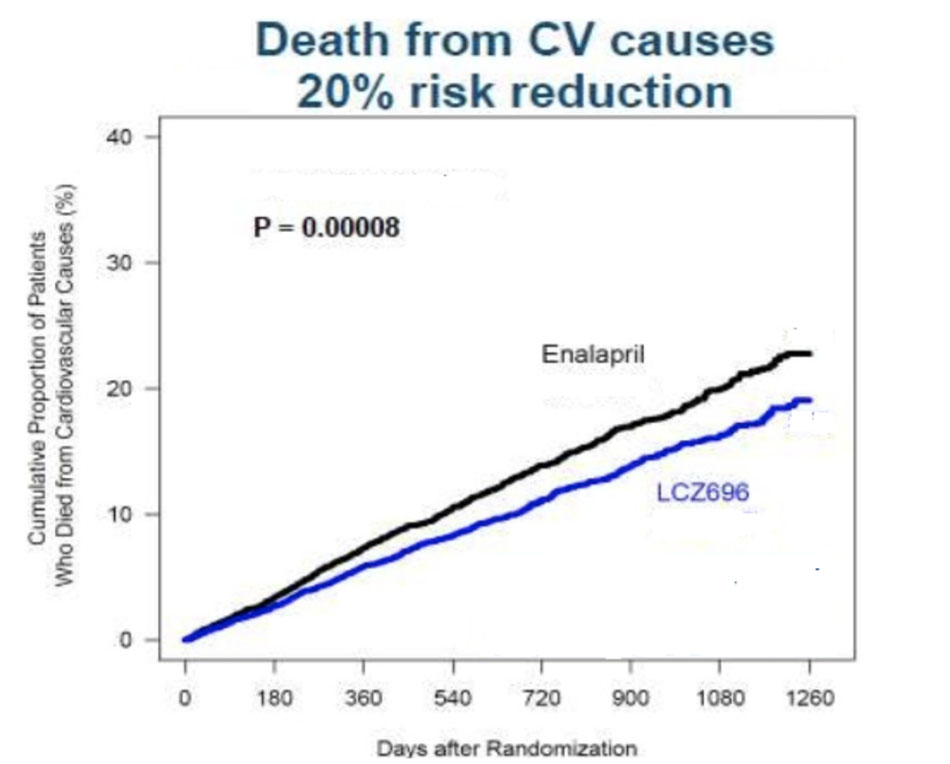
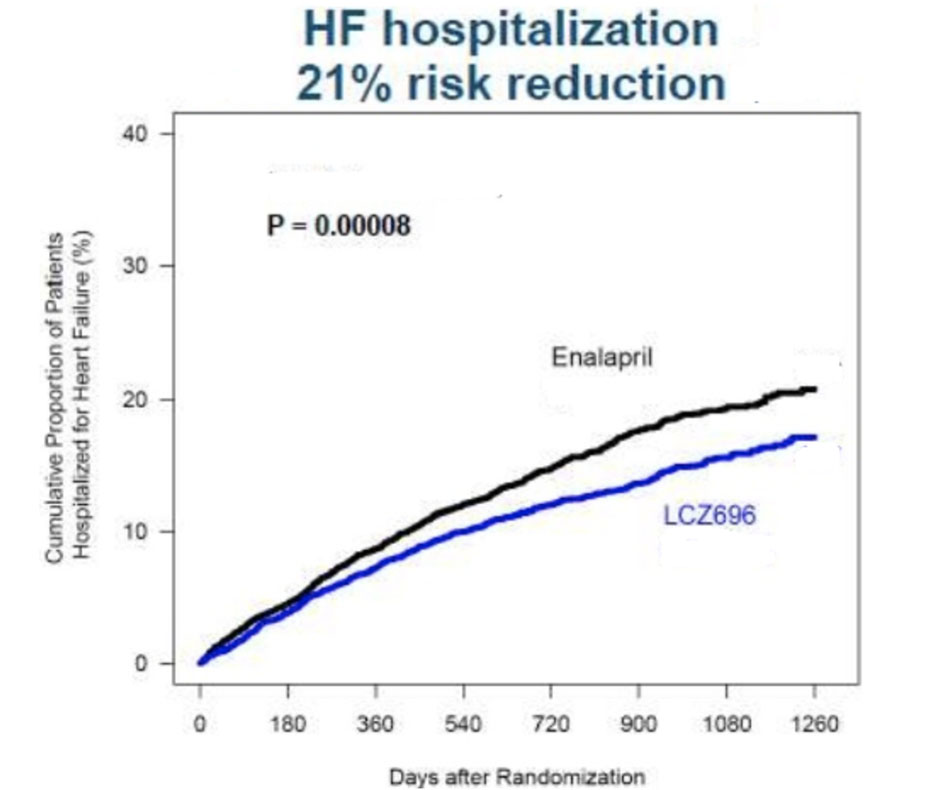
Ngoài ra, còn nhiều tiêu chí khác cho kết quả vượt trội của LCZ696 so với enalapril. Điều đó lý giải tại sao, LCZ696 đã chóng được FDA thông qua, và trong các khuyến cáo điều trị cũng đã nhanh chóng cập nhật và ghi rõ:
- Sacubitrl/valsartan được khuyến cáo thay thế cho thuốc ACEi nhằm giảm hơn nữa nguy cơ nhập viện vì suy tim và chết ở những bệnh nhân suy tim tâm thu theo dõi ngoại trú vẫn còn triệu chứng dù đã được điều trị tối ưu bằng một thuốc ACEi, một thuốc chẹn β và một thuốc MRAs (theo ESC 2016).
- Ở bệnh suy tim tâm thu mạn có triệu chứng (NYHA II hoặc III) dung nạp được thuốc ACEi/ARBs, việc thay thế bằng sacubitril/valsartan được khuyến cáo nhằm giảm hơn nữa tử vong – bệnh tật. Sacubitril/valsartan không được dùng chung với thuốc ACEi hoặc trong vòng 36 giờ sau liều cuối của một thuốc ACEi (theo ACC/AHA/HFSA).
Khi sử dụng sacubitril/valsartan điều trị bệnh nhân suy tim trên lâm sàng cần phải nằm rõ những điều sau đây:
- LCZ696 được FDA phê chuẩn ở 3 dạng liều: 24/26 mg, 49/51 mg và 97/103 mg tương ứng với sacubitril/valsartan (tên biệt dược là Ernesto).
- Sacubitril/valsartan không được dùng chung hoặc trong vòng 36 giờ sau liều cuối cùng của một ACEi. Không dùng sacubitril/valsartan ở bệnh nhân có tiền sử bị phù mạch.
- Liều khởi đầu khuyến cáo của sacubitril/valsartan là 49/51 mg x 2 lần/ngày. Ở những bệnh nhân trước đó chưa dùng hoặc dùng liều thấp của ACEi/ARBs, nên khởi đầu ở liều 24/26 mg x 2 lần/ngày. Tăng gấp đôi liều sau mỗi 2 – 4 tuần đến liều đích 97/103 mg x 2 lần/ngày theo khả năng dung nạp thuốc của người bệnh.
- Bệnh nhân suy thận nặng (eGFR < 30) hoặc suy gan trung bình (phân loại Child – Pugh B), liều khởi đầu là 24/26 mg.
- Nguy cơ hạ huyết áp, suy giảm chức năng thận, tăng kali máu và phù mạch là các lo ngại chính liên quan đến việc điều trị với sacubitril/valsartan.
- Tính an toàn khi sử dụng kéo dài sacubitril/valsartan còn cần thêm nhiều thời gian và nghiên cứu để xác nhận. ESC có đề cập đến khả năng ức chế neprilysin sẽ làm tăng lắng đọng các peptide β – amyloid ở não, có liên quan đến bệnh sinh của Alzheimer.
| Bảng 8.11 Liều khuyến cáo sacubitril/valsartan theo ESC 2016 | |
| Liều khởi đầu (mg/ngày) | Liều mục tiêu (mg/ngày) |
| 49/51 x 2 | 97/103 x 2 |
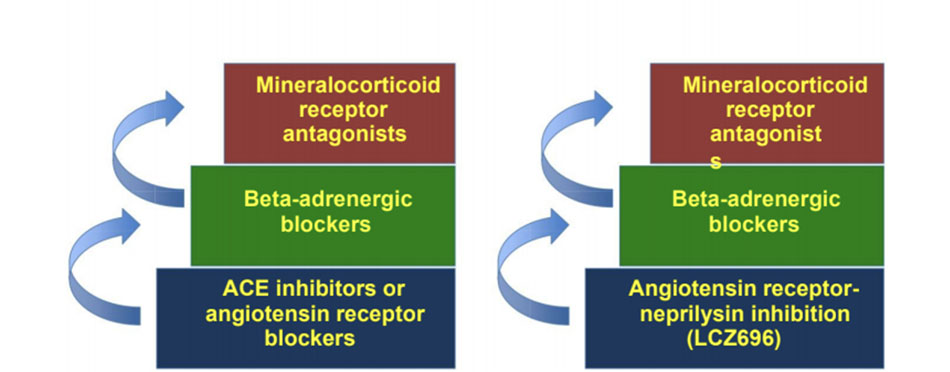
Kết luận:
1. ARNI đánh dấu một bước phát triển mới trong điều trị suy tim, là thuốc có khả năng cải thiện sống còn tốt nhất cho bệnh nhân suy tim.
2. Hiện ACEi và chẹn β vẫn là lựa chọn đầu tay trong điều trị suy tim có EF giảm, nhưng trong tương lại ARNI có thể thay thế vị trí đó như là một liệu pháp điều trị tối ưu hơn.
TÀI LIỆU THAM KHẢO
1. Đặng Vạn Phước, Châu Ngọc Hoa, Trương Quang Bình (2014). Suy tim trong thực hành lâm sàng.
2. Nguyễn Quang Tuấn (2015). Chẩn đoán và điều trị suy tim.
3. Lê Minh Khôi (2015). Sinh lý tim mạch ứng dụng trong lâm sàng.
4. Trương Quang Bình, Đặng Vạn Phước. Sinh lý bệnh của suy tim. Suy tim trong thực hành lâm sàng. Chủ biên Đặng Vạn Phước. Xuất bản lần thứ nhất. Nhà xuất bản Đại học quốc gia Thành phố Hồ Chí Minh. 2001: 15 – 32.
5. Lê Hoài Nam, Châu Ngọc Hoa. Suy tim. Bệnh học nội khoa. Chủ biên Châu Ngọc Hoa. Xuất bản lần thứ hai. Nhà xuất bản Y học. 2012: 107 – 122.
6. Tạp chí tim mạch học Việt Nam các kỳ 77, 78 ,79, 80, 81, 82, 83, 84.
7. Kanel. WB Epidemiology of heart failure scientific princeples and clinical practice, 1997: 279 – 287.
8. Sutton et al Epidemiology of heart failure in Europe. Heart failure scientific princeples and clinical practice, 1997: 289 – 293.
9. Heidenriech PA Forecasting the future of cardiovascular disease in the Unites States: a policy statement from the AHA Circulation. 2011; 123 (8): 933 – 44.
10. ACCF/AHA Guideline for the management of heart failure. Circulation 2013; 128; 1810 – 1852.
11. ESC Guidelines for diagnosis and treatment of acute and chronic heart failure 2012. Eu – ropean Heart Journal (2012) 33, 1787 – 1847. doi:10.1093/eurheartj/ehs104.
12. Yancy CW, Jessup M, Bozkurt B, et al. 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2013;62(16):e147 – e239.
13. The CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure. Results of the Cooperative North Scandinavian Survial Study (CONSENSUS). N Engl J Med 1987; 316:1429.
14. The SOLVD Investigation. Effects of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N Engl J Med 1992;327:685.
15. The Cardiac Bisoprolol Study II (CIBIS II): a randomized trial. Lancet, 1999, 353, 9146: 9 – 13.
16. MERIT – HF: Lancet 1999, 353, 6169: 2001 – 07.
17. Packer M, Bristow MR, Cohn JN, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure: U.S.Carvedilol Heart Failure Study Group. N Engl J Med. 1996; 334: 1349 0 55.





