Các điểm cần nhớ
1. Thể tích tống máu của một nhát bóp tạo ra áp lực đẩy máu vào trong lòng mạch từ đó hình thành nên huyết tâm thu, trong khi đó, kháng trở mạch ngoại biên cũng hình thành nên một mức áp lực khác – huyết áp tâm trương – do tạo ra một lực chống lại (elestance) thể tích nhát bóp trong thì tâm thu trước đó, gây ra dòng chảy trong các tiểu động mạch trong suốt thì tâm trương.
2. Hoạt động của bộ đôi “thất – mạch” sản sinh ra một bệnh cảnh lâm sàng có thể phân biệt hai trạng thái rối loạn huyết động trên bệnh nhân hồi sức:
- Bệnh nhân hạ huyết áp nhưng tim trạng thái tăng động (hypotension-hyperdynamic) – đó là những bệnh nhân choáng nhưng có sự gia tăng thể tích nhát bóp và cung lượng tim với lâm sàng mạch nẩy mạnh rõ dưới tay, huyết áp tâm trương thấp, giãn cách huyết áp dãn rộng, chi ấm (do kháng trở mạch ngoại biên thấp, cung lượng tim tăng nhưng lại tụt huyết áp hoặc shock nhiễm trùng).
- Bệnh nhân có tình trạng tụt huyết áp và giảm động tuần hoàn (hypotension-hypodynamic) – mạch nhẹ lăn tăn dưới tay, đôi khi khó bắt, huyết áp tâm trương cao, hiệu số huyết áp kẹp, chi lạnh ẩm, những dấu hiệu cho thấy thể tích nhát bóp và cung lượng tim thấp với sự gia tăng kháng trở mạch ngoại biên, như shock tim hay shock giảm thể tích.
3. Chức năng bơm của thất trái được diễn tả bằng mối liên quan với áp suất thất trái cuối thì tâm trương (LVEDP) mà nó được ước lượng bằng áp lực động mạch phổi bít (Ppw) và thể tích nhát bóp (SV); suy chức năng thất trái sẽ được biểu hiện với tăng Ppw và giảm SV có thể do suy chức năng tâm thu hay tâm trương hoặc cả hai.
4. Suy chức năng tâm thu, hay giảm sức co bóp, nghĩa là tăng thể tích cuối thì tâm thu lớn hơn trong khi chỉ tạo ra một áp lực xấp xỉ mức huyết áp trung bình; nguyên nhân thường gặp gây ra một suy chức năng tâm thu cấp ở bệnh nhân nằm hồi sức là thiếu máu cục bộ cơ tim, giảm oxi mô, toan máu, nhiễm trùng huyết, sử dụng các thuốc có hoạt tính inotrope âm gần đây (ức chế canxi, ức chế β..), hay đợt cấp trên nền mãn của bệnh lý cơ tim trước đó.
5. Suy chức năng tâm trương bao hàm một trạng thái giảm thể tích cuối thì tâm trương nhưng áp lực động mạch phổi bít lại gia tăng bởi vì tim không thể đổ đầy bình thường; nguyên nhân thường gặp của suy chức năng tâm trương trên bệnh nhân hồi sức bao gồm chèn ép tim cấp hay viêm co thắt màng tim, thông khí áp lực dương với PEEP không thích hợp, và những nguyên nhân khác gây gia tăng áp lực màng phổi như tràn khí màng phổi có áp lực, tràn dịch màng phổi lượng lớn, hội chứng tăng áp lực ổ bụng, tương tác 2 thất trong hội chứng suy thất phải cấp, các trường hợp gây “ cứng” thất trái như bệnh cơ tim phì đại.
6. Sự khác biệt sớm giữa suy chức năng tâm thu và tâm trương trên bệnh nhân hồi sức được phân biệt chủ yếu dựa vào hình ảnh động học trên siêu âm tim; điều đó tránh những biện pháp điều trị không thích hợp và không hiệu quả những nguyên nhân gây suy thất trái.
7. Hồi lưu tĩnh mạch trở về nhĩ được kiểm soát bởi một số đặc tính cơ học của hệ thống mạch (thể tích máu không lưu thông – unstress volume, sức chứa mạch máu, thể tích mạch máu); các yếu tố này kết hợp với nhau tạo ra một giá trị gọi là áp lực trung bình hệ thống (Pms); nó hình thành nên “lực đẩy” kiểm soát hồi lưu tĩnh mạch về nhĩ phải dựa trên mức kháng trở của dòng hồi lưu.
8. Với một mức Pms, hồi lưu tĩnh mạch gia tăng khi áp lực nhĩ phải giảm trong mức xác định của đường con hồi lưu tĩnh mạch, trong khi thể tích nhát bóp và cung lượng tim tăng khi áp lực nhĩ phải và tiền tải tăng được thể hiện trên đường cong chức năng tim (đường cong Frank-Starling; khi đó, tương tác với đường cong hồi lưu tĩnh mạch tại một giá trị xác định của áp lực nhĩ phải – thì thể tích hồi lưu tĩnh mạch = cung lượng tim).
9. Khi cung lượng tim không đầy đủ, truyền dịch, các đáp ứng của các áp cảm thụ quan (baroreceptor) hay các hóa cảm thụ quan (chemoreceptor) gây gia tăng Pms từ đó tăng hồi lưu tĩnh mạch và áp lực nhĩ phải; hiệu ứng này có thể có được một hiệu quả tương tự với các thuốc gây co tĩnh mạch như norepinephrine hay phenylephrine; hoặc thay vào đó; thuốc gây tăng hồi lưu tĩnh mạch như các thuốc có hoạt tính inotrope dương (dobutamine), giảm hậu tải thất trái (sodium nitroprusside, fenoldopam), nó sẽ giảm áp lực nhĩ phải do gia tăng cung lượng tim.
10. Trong shock giảm thể tích, máu và hồi sức dịch là thiết yếu, trong khi các thuốc gây co tiểu động mạch như norepinephrine có thể được sử dụng thoáng qua để cung cấp một mức huyết áp cao để tưới máu cho các cơ quan quí trong thời gian hồi sức, ở bệnh nhân shock nhiễm khuẩn, hồi sức dịch cần do tác động của hiện tượng dãn mạch, giảm Pms từ các hoát chất trung gian và nitric oxide được phóng thích từ quá trình viêm cấp, các inotrope như dobutamine sẽ được dùng để điều trị tình trạng ức chế cơ tim do viêm, thuốc co động mạch như norepinephrine cần để duy trì huyết áp mặc dù có tình trạng tăng cung lượng tim do giảm kháng trở mạch ngoại biên quá mức.
11. Trong shock tim, giảm tiền tải (morphine, nitroglycerine, furosemide) được cho là hiệu quả do gây giãn tĩnh mạch và giảm Pms, nhưng hồi lưu tĩnh mạch có thể gia tăng do cải thiện chức năng tim sẽ gây giảm áp lực nhĩ phải; các thuốc dãn động mạch sẽ gây tăng cung lượng tim từ những thất trái có tổn thương vì thể có thể gây tăng huyết áp mặc dù có tình trạng suy giảm co bóp, sẽ không gây tăng tiêu thụ oxi cơ tim một khi nhịp tim không tăng lên.
12. Kiểm soát đường thở sớm và thông khí áp lực dương liên tục sẽ giảm nhu cầu tiêu thụ oxi và ngăn ngừa toan hô hấp nhưng có thể gây giảm hồi lưu tĩnh mạch gây tụt huyết áp ở bệnh nhân có giảm thể tích tuần hoàn bởi sự gia tăng áp lực màng phổi và áp lực nhĩ phải; trong shock tim, thông khí áp lực dương và PEEP thích hợp có ít hiệu quả lên hồi lưu tĩnh mạch nhưng làm tăng cung lượng do giảm được hậu tải cho tim.
13. Phù phổi do tim và phù phổi do tăng tính thấm được làm giảm nhẹ bằng cách giảm Ppw, và cung lượng tim cũng như mức phân phối oxi cho mô phải được duy trì ở mức Ppw thích hợp với các thuốc giãn mạch và truyền máu; độ bão hòa oxi động mạch có thể được cải thiện bằng PEEP thích hợp mà không gây giảm cung lượng tim.
Suy chức năng thất trên bệnh nhân hồi sức
Bộ đôi “Thất – Mạch”
Hình 2 cho ta thấy hai sự kiện điển hình trong hai pha của một chu chuyển hoạt động thất: hoạt động co bóp tống máu (thì tâm thu) và hoạt động thư giãn làm đầy thất (thì tâm trương). Trong thì tâm trương, thất trái được làm đầy thông qua việc mở hoàn toàn van 2 lá nhận máu từ tâm nhĩ trái trong khi đó van động mạch chủ đóng. Sau kích thích điện và co bóp của thất trái trong thì tâm thu, một thể tích nhát bóp được tống vào đoạn gần của động mạch chủ. Bởi vì lượng máu tống ra nhiều hơn lượng máu còn trong đoạn xa ống động mạch và các tiểu động mạch, thành động mạch được căng phồng, do đó, một áp lực (P) tăng lên với một thể tích tăng lên, một đại lượng nghịch đảo với sức chứa của thành động mạch gọi là compliance mạch máu (C = ΔV/ΔP).
Khi thể tích thất giảm, thì khả năng hình thành một áp suất của thất cũng sẽ giảm, do bởi hoạt động của các sợi actin và các sợi myosin bắt chéo nó phụ thuộc vào chiều dài dãn ra của tế bào cơ tim, cho đến khi áp suất tâm thu giảm xuống thấp hơn huyết áp động mạch thì nó mới kết thúc. Sau đó van động mạch chủ đóng lại, điều đó biểu hiện bằng một dấu khấc trên sóng biểu diễn áp lực động mạch (hình 3). Khi thất thư giãn, van 2 lá mở ra, và thất được làm đầy theo đường biểu diễn V-P; đường biểu diễn mối liên quan giữa thể tích – áp lực bên trong thất trái tại thì tâm trương; sự làm đầy tâm trương còn được làm đầy bởi sự co bóp của nhĩ và bởi lực hút của thất sau thì tống máu trước đó. Trong suốt thì tâm trương, phần của thể tích nhát bóp được dữ trữ trong giường động mạch tiếp tục chảy đi với một mức kháng trở nào đó của mạch ngoại biên, có xu hướng giảm dần áp lực động mạch cho đến kỳ co bóp kế tiếp.
Bộ đôi “ thất – mạch” hoạt động như một bộ lọc thủy tĩnh để chuyển những nhát bóp ngắt quản của thể tích nhát bóp thành những dòng liên tục, tạo ra cung lượng tim. Điều đó còn làm giảm công hoạt động của tim bằng cách cho phép chuyển tiếp năng lượng của thất đến dòng máu được dữ trữ trong trong các ống tiểu động mạch và sự hồi lưu máu trong khi thất trái được thư giãn trong thì tâm trương. Kháng trở mạch hệ thống là sản phẩm tích phân của trở kháng mạch máu ngoại biên, và khi kết hợp với cung lượng tim sẽ tạo thành huyết áp (BP = Q x SVR) phân phối dòng máu đến các cơ quan theo nhu cầu chuyển hóa. Ví dụ, trong trường hợp shock tim hay shock giảm thể tích, các phản xạ giao cảm gây ra co thắt mạch máu, đặc biệt là các mạch tạng, ruột, thận, và giường mao mạch ở da, để bảo toàn dòng máu đến các cơ quan sống quí giá như tim, não bằng cách duy trì huyết áp động mạch chủ bình thường, hơn nữa, trong lúc sốt cao hay khó thở nhanh, các mạch máu cơ hô hấp sẽ chuyển qua chuyển hóa yếm khí cùng với các mô khác đang thiếu oxi để duy trì dòng O2 đủ cho cơ quan sinh tồn.
Đánh giá lâm sàng hệ tim mạch trên bệnh nhân với các vấn đề hồi sức là phải nhắm đến việc giải thích các trị số huyết áp tâm trương, áp lực mạch ( PP- pulse pressure), và các chỉ số của kháng trở lực ngọai biên như màu sắc da, mức đổ đầy nhanh chậm của giường mao mạch móng ngón tay và chỉ số nhiệt độ. Ví dụ, bệnh nhân có biểu hiện choáng với nhịp tim là 110l/phút, huyết áp 100/40 mmHg, chi ấm, phục hồi móng nhanh cho thấy bệnh nhân có tình trạng giảm kháng trở lực ngoại biên và tăng cung lượng tim (Hình 3). Do hiệu số huyết áp rộng (60mmHg) cho thấy thể tích nhát bóp lớn, khi nhân với nhịp tim sẽ gây tăng cung lượng tim, trị số huyết áp tâm trương thấp cho thấy sức cản ngoại biên thấp. Ngược lại, bệnh nhân tụt huyết áp cũng với nhịp tim như và huyết áp trung bình nhưng huyết áp là 80/65 mmHg, chi lạnh với phục hồi màu da chậm cho thấy bệnh nhân có cung lượng tim thấp, huyết áp tâm trương bảo tồn cho thấy có sự co mạch để bảo toàn sức cản ngoại biên. Giống như bên trái của hình 3, nếu như bệnh nhân có CVP cao nghi ngờ shock tim trong khi CVP thấp nghĩ do giảm thể tích tuần hoàn. Dĩ nhiên, mối quan hệ giữa hiệu số huyết áp và thể tích nhát bóp không thể định lượng được, bởi vì thật khó ước lượng một thứ khó xác định – sức chứa của mạch. Tuy nhiên, trên bệnh nhân hồi sức, những người mà sức chứa của mạch máu ít thay đổi trong lúc can thiệp cấp tính, việc thay đổi hiệu số huyết áp (PP) là chỉ số thay đổi sớm nhất của thể tích nhát bóp. Mối tương quan SV và PP là bằng chứng cho phương pháp đánh giá khả năng của huyết áp trong đáp ứng truyền dịch ở bệnh nhân thở máy. Như được diễn giải bên dưới, sự gia tăng áp lực trong lồng ngực trong suốt trong lúc thông khí áp lực dương ở bệnh nhân có giảm thể tích tuần hoàn có thể gây giảm hồi lưu tĩnh mạch về tim từ tuần hoàn ngoại biên. Điều đó gây giảm thể tích nhát bóp và có thể quan sát được hiện tượng thu hẹp lại khoảng cách huyết áp PP trên sóng động mạch.
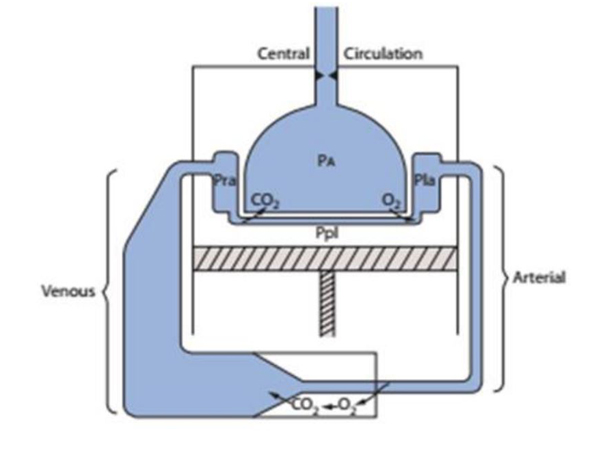
Hình 1. Giản đồ cho thấy tuần hoàn trước đó là bên nhĩ trái (Pla, áp lực nhĩ trái) trong một hệ thống động mạch có áp lực cao (thể tích thấp, compliance thấp, trở kháng cao) đến mô ngoại biên (nơi oxi rời khỏi mạch máu để sinh năng lượng và CO2) và trở về hệ thống tĩnh mạch có áp lực thấp (thể tích cao, compliance cao, nhưng trở kháng thấp), mà cuối cùng là nhĩ phải (Pra, áp lực nhĩ phải ). Dòng máu gần như tưới hoàn toàn phổi trước khi về nhĩ trái; mạch máu phổi áp sát các phế nang (Pa, áp suất trong phế nang) thúc đẩy trao đổi khí. Các mạch máu trung tâm này được bao bọc trong khoang ngực,và sàng là cơ hoành (hoạt động của nó được xem như là một cái piston). Giữa thành ngực và nhu mô phổi là một khoang ảo kín (Ppl, áp suất trong khoang màng phổi). Trong đó, Ppl có áp lực tương đương các áp lực bên ngoài các mạch máu và tim, trong khi đó áp lực Pa xem như là áp lực bên ngoài mạch máu phế nang. Việc sắp xếp giải phẫu là cơ chế nền tảng cho tương tác cơ học giữa hô hấp và tuần hoàn trên bệnh nhân hồi sức.
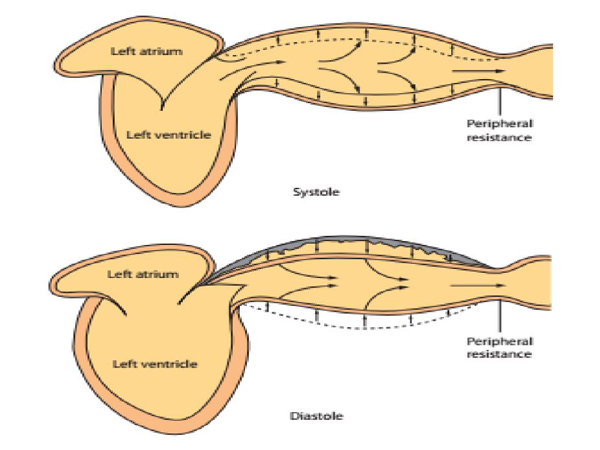
Hình 2. Trong suốt thì tâm thu, thể tích nhát bóp được tống ra tạo một dòng chảy hướng đến các mao mạch, nhưng hầu hết SV được dữ trữ trong các động mạch. Trong suốt thì tâm trương, sức elastic (xem như là độ đàn hồi mạch máu, nó có xu hướng chống lại sự dãn nở thành mạch gây ra do thể tích tích nhát bóp được tống ra) của thành mạch máu duy trì dòng máu mao mạch trong suốt thời kỳ trung gian giữa hai chu chuyển tim. Theo đó, khoảng cách huyết áp tương quan với thể tích nhát bóp, và huyết áp tâm trương gia tăng với sức kháng trở ngoại biên, nhịp tim, và sức chứa của mạch máu.
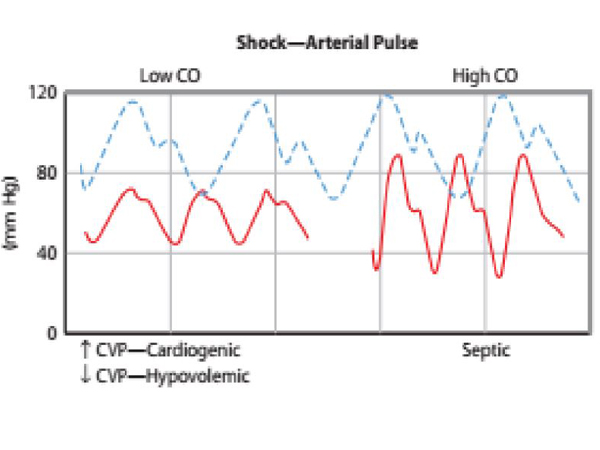
Hình 3. Giản đồ miêu tả sóng động mạch bình thường (các sóng dạng chấm); bên trái là sóng liên tục của tình trạng cung lượng tim thấp và bên phải là tình trạng có cung lượng tim cao là chìa khóa phân biệt với tình trạng bình thường.
Đường cong Starling của tim
Hình 4 thể hiện mối quan hệ Starling của tim. Trên trục hoành thể hiện áp lực của áp suất trong nhĩ trái – Pla, xấp xỉ với áp lực đổ đầy thất trái cuối thì tâm trương – LVEDP. Trục tung biểu diễn SV ( ml); đó là thể tích được tống ra sau mỗi nhịp tim được đo lường như là đại lượng thể hiện thể tích ra của thất. Một đại lượng đo lường khác bằng cách nhân SV với sự gia tăng áp lực để được SV đó trong thì tâm thu (SV × [BP − Pla]). Khi áp suất đổ đầy của tim gia tăng, thì thể tích tống máu và công làm việc của tim gia tăng theo một đường cong tuyến tính; ở mức áp lực đổ đầy cao hơn, có mức gia tăng SV thấp hơn tính trên 1 đơn vị tăng áp lực Pla. Trên đường biểu diễn Starling tronh hình 4A, với mức Pla bình thường (10mmHg ) có thể tích nhát bóp bình thường (75 ml) với cung lượng tim là 6 lít/p khi nhịp tim là 80l/p. Khi tình trạnh giảm thể tích làm giảm Pla còn 5mmHg, SV giảm còn 40ml, do đó giảm cung lượng tim, và khi đổ dịch gây gia tăng Pla lên 20mmHg, thì SV tăng lên 100ml và tăng cung lượng tim trên mức bình thường. Mối liên quan này là kiến thức cơ bản để hiểu chức năng thất của bệnh nhân hồi sức. Một chuyển dịch đường cong Starling lên trên hay về trái cho thấy sự gia tăng chức năng thất. Ngược lại, đường cong chuyển dịch xuống hay về phía phải với giảm SV trên 1 đơn vị đổ đầy thất cho thấy sự suy giảm chức năng thất. Trên đường cong biểu diễn dạng chấm, thể tích nhát bóp thấp tại điểm A với áp suất nhĩ trái 10mmHg có thể do giảm sức co bóp, hoặc gia tăng thứ phát của hậu tải như tăng huyết áp tạo ra một thể tích nhát bóp nhỏ tại điểm A, hoặc do thất trở nên cứng nên chỉ có thể làm đầy thất với áp lực nhĩ trái là 10mmHg từ đó tạo ra một SV như tại điểm A. Những thay đổi cơ chế khác nhau để giải thích cùng một thông tin cho thấy sự giới hạn khi phân tích huyết động trên đường cong Starling, do vậy cần nhiều công cụ hơn để giải thích chức năng thất trái.
Chức năng thất trái được biểu diễn bằng mối liên hệ Starling dựa trên cơ chế khả năng thư giãn (tâm trương) hay co bóp (tâm thu) thể hiện qua mối liên quan thể tích – áp lực của thất. Trong phần này sẽ nhìn lại các yếu tố ảnh hưởng lên chức năng tâm thu và tâm trương ở người khỏe mạnh và bệnh nhân hồi sức và những liên quan này sẽ tương quan ra sao trên đường cong Starling của tim. Trong hình 4B, áp lực thất trái cuối thì tâm trương – LVEDP và cuối thì tâm thu – LVESP được biểu diễn ngược với thể tích đáp ứng- LVEDV và LVESV. Đường cong liên tục biểu diễn thể tích – áp lực được đánh dấu tại vị trí (điểm xanh) LVEDP 10mmHg thì LVEDV bình thường là 120 ml. Khi thất co bóp, áp suất gia tăng trong giai đoạn đồng thể tích cho đến khi áp lực vượt qua áp lực trong động mạch chủ làm mở van động mạch chủ, và máu sẽ được tống đi cho đến khi van động mạch chủ đóng và LVSEV (thể tích thất trái cuối thì tâm thu ) còn 45 ml. Như vậy thể tích nhát bóp là 75 ml ( LVEDV – LVESV ), được biểu diễn trên đường cong Starling trong hình 4A. Khi tình trạng giảm thể tích tuần hoàn gây giảm LVEDV, LVEDP và SV sẽ giảm trên đường cong Starling ở trên; nếu thể tích dịch gia tăng thì LVEDV trở về vị trí 2, SV và LVEDP gia tăng trên đường cong Starling.
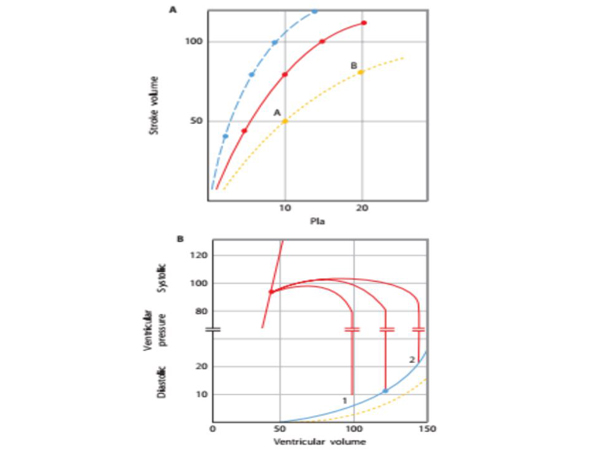
Hình 4. A. Đường cong Starling. Thể tích nhát bóp (SV, đơn vị ml; trục tung) được biểu diễn ngược lại với áp lực của nhĩ trái (Pla, đơn vị mmHg; trục hoành). Đường liên tục chính giữa thể hiện đường cong Starling của một thất bình thường so sánh đường cong bên dưới của một thất suy chức năng(đường AB dạng chấm vàng) và đường cong bên trên cho một thất được nở rộng chức năng (đường gạch nối xanh); tất cả ba đường trên có thể có chức năng tâm thu giống nhau nếu mối liên hệ thể tích – áp lực tâm trương hay hậu tải khác nhau. B. Tương quan thể tích thất trái (ml; trục hoành) với áp lực (mm Hg; trục tung) ; đoạn bị ngắt nhắm đến sự thể hiện mối liên quan thể tích – áp lực của thất trái trong thì tâm thu và tâm trương. Phần trên đã có thảo luận vê 3 đường biểu diễn khác nhau từ một đường cong tâm trương. Đường thể tích – áp lực tâm trương ngắt khúc thể hiện một buồng thất có compliance bình thường như là thất phải, nơi mà áp lực tâm trương ít thay đổi với mỗi thể tích.
Các áp suất trong tim như áp suất nhĩ trái được đo lường với phương diện áp suất khí quyển không thể hiện được áp suất xuyên thành, hay mức đổ đầy, các áp suất trong buồng tim được tính toán bằng áp suất khí quyển trong khi áp suất bên ngoài tim không phải là áp suất khí quyển. Áp suất chung quanh tim hầu hết tương đương với áp lực màng phổi, mà nó xu hướng âm khi thở tự nhiên ( -3 đến -10mmHg) và có thể trở nên rất âm trong trường hợp tắc nghẽn đường thở hay rất dương khi thông khí áp lực dương và PEEP. Để thuận tiện, các phần đề cập phía sau, các áp lực trong mạch máu là các áp lực xuyên thành, đổ đầy, và bất kỳ nguyên nhân nào gây thay đổi áp suất màng phổi và màng tim phải được chú ý!
Đường cong V-P và những rối loạn đổ đầy thất (Bảng 1)
Hình 4B Thể hiện LVEDV (thể tích thất trái cuối thì tâm trương) đối ngược với diễn tiến LVEDP (áp lực thất trái cuối thì tâm trương). Khi thể tích thất gia tăng từ mức zero, áp lực xuyên thành thất sẽ không bao giờ tăng vượt mức zero cho đến khi thể tích khoảng 50ml (thể tích đó người ta gọi là unstressed volume). Sau đó LVEDP gia tăng tuyến tính với mức gia tăng thể tích thất (khi đó thể tích đang tồn tại trong thất lúc này được gọi là stressed volume), ban đầu thì một thay đổi lớn thể tích sinh ra một thay đổi nhỏ áp lực trong buồng thất nhưng sau đó một thay đổi nhỏ thể tích thì lại sinh ra một thay đổi lớn áp lực. Nếu như màng ngoài tim bị cắt bỏ, thì đặc tính biến thiên V-P sẽ tuyến tính hơn, đó là một thay đổi lớn LVEDP thì cần một LVEDV cao hơn. Do đó màng ngoài tim hoạt động như một cái màng với dạng cho tồn tại một thể tích unstressed dữ trữ bao xung quanh tim, nhưng với LVEDV lớn hơn thì màng ngoài tim sẽ trở nên rất “cứng”. Ở mức thể tích tim cao hơn, thì hầu hết các áp suất xuyên thành cơ tim cũng là các áp suất xuyên thành màng ngoài tim với các đặc tính của đường cong V-P. Trong tình trạng tràn dịch màng tim thì thể tích unstressed của màng tim giảm đi do lượng dịch tràn. Khi thể tích dịch tràn đủ lớn, giảm thể tích cuối tâm trương liên quan đến áp lực cuối tâm trương.
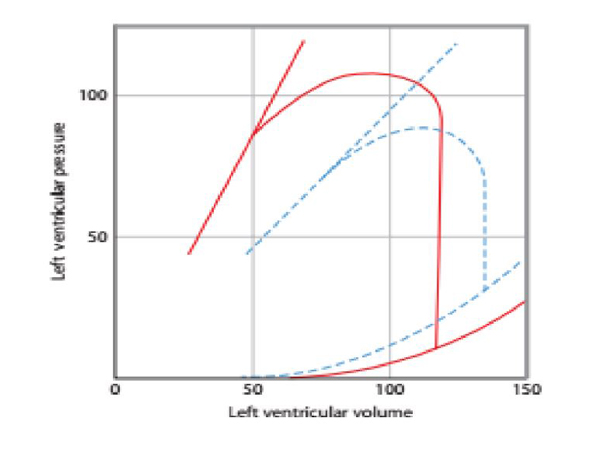
Hình 5. Giản đồ miêu tả mối liên quan thể tích áp lực LVEDV và LVEDP cũng như LVESP (áp suất thất trái cuối tâm thu) và LVESV (thể tích thất trái cuối tâm thu) trước (đường liên tục) và sau (đường ngắt quản) nhồi máu cơ tim cấp. Cơ tim bị nhồi máu gây giảm co bóp cơ tim nên sẽ gia tăng thể tích cuối thì tâm thu mặc dù áp suất hậu tải đã giảm đi; theo đó, LVEDV tăng cao do kết hợp với lượng hồi lưu tĩnh mạch đổ về, trong khi đó LVEDP lại gia tăng do thất trở nên cứng bởi cơ tim bị tổn thương mất hay giảm khả năng thư giãn. Dựa vào đó, suy chức năng thất trái được đặc trưng bởi giảm cung lượng tim và thể tích nhát bóp mặc dù gia tăng LVEDP, vì thế, điều trị mục tiêu làm giảm tiền tải, tăng sức co bóp, và giảm hậu tải.
Trở lại, áp suất màng ngoài tim gây giảm hồi lưu tĩnh mạch bởi gây tăng áp lực nhĩ phải, do đó tạo ra một thể tích cuối tâm trương và cung lượng tim thấp bất thường. Tràn khí màng phổi có áp lực, tràn dịch màng phổi lượng nhiều, sử dụng PEEP cao không thích hợp, hay hội chứng tăng áp lực ổ bụng có thể gia tăng áp lực bên ngoài tim (Ppl, mà lâm sàng là áp lực màng phổi hay áp lực thực quản ) sẽ gây giảm LVEDV cũng như SV mặc dù LVEDP tăng cao ( bảng -1).
| Bảng -1. Các nguyên nhân thường gặp gây suy chức năng tâm trương ở bệnh nhân hồi sức. |
Các lực đè ép bên ngoài:
Cơ tim trở nên cứng:
Sự tương tác 2 thất và đẩy lệch vách liên thất sang bên trái:
Các bất thường bên trong tim:
Các bất thường nhịp tim và van tim gây cản trở đổ đầy:
|
Phì đại thất trái hay những bệnh thâm nhiễm cơ tim (amyloidosis) đôi khi làm cứng sự thư giãn của thất mà khi đó cần một áp lực đổ đầy cao hơn để duy trì một SV đủ, và thời gian đổ đầy không đủ hoặc sự đồng bộ nhĩ thất kém sẽ gây suy giảm khả năng đổ đầy thất. Một sự chuyển dịch vách liên thất từ phải sang trái kết quả của sự tương tác hai thất cũng có thể làm cản trở đổ đầy tâm trương. Có lẽ, sự căng phồng của thất phải gây vách liên thất bung từ phải sang trái, do đó gây giảm thể tích unstressed và compliance của thất trái. Sự tương tác hai thất như trên cũng có thể ít tác động nếu như màng ngoài tim bị cắt bỏ, bởi vì do sự giới hạn của màng tim nên thành tự do của thất trái bị hạn chế di động, làm cho thất trái dễ bị tổn thương chức năng khi vách liên thất di lệch sang trái. Dựa theo đó, các bệnh lý gây cho thất phải bị bất thường đổ đầy (như thuyên tắc phổi cấp hay suy hô hấp cấp trên nền mảng do các bệnh phổi tắc nghẽn hay bệnh phổi hạn chế) làm cản trở cho khả năng làm trống thất phải, từ đó buộc nó phải làm việc với một thể tích cuối thì tâm trương cao hơn. Sau đó áp suất đổ đầy thất trái sẽ cao hơn mong đợi so với thể tích đổ đầy cuối thì tâm trương. Điều đó cũng cung cấp một cách giải thích tại sao PEEP thường liên quan tới một áp suất đổ đầy cao hơn để duy trì SV bình thường thậm chí ngay khi LVEDP được điều chỉnh về áp lực đổ đầy thật sự bằng cách trừ đi áp lực tăng thêm của áp suất màng phổi khi PEEP được cài đặt.
Thiếu máu cục bộ cơ tim cấp cũng gây lệch đường V-P lên trên và sang trái (hình 5). Có thể hình dung là, cơ tim bị tổn thương hay bị thiếu máu cục bộ làm thay đổi khả năng đàn hồi (elastance) hay khả năng thư giãn của thất trong thì tâm trương, một quá trình mà cần năng lượng ATP. Do đó, một áp lực đổ đầy thất cao hơn phải có với mỗi thể tích. Điều này giải thích ở bệnh nhân nhồi máu cơ tim hay thiếu máu cục bộ cơ tim thường cần một áp lực đổ đầy cuối thì tâm trương là 30mmHg để duy trì cung lượng tim bình thường trong khi người khỏe mạnh bình thường chỉ cần một LVEDP < 10 mmHg.
Đường cong V-P cuối thì tâm thu và sức co bóp
Đường cong V-P tâm trương bình thường được trình bày bởi đường liên tục ở góc dưới bên phải của hình 5. Chúng ta hãy xem xét hiệu ứng thất co bóp trong suốt kỳ tâm thu không tống ra bất kỳ máu nào, hay khi van động mạch chủ không thể mở. Một áp lực rất lớn được sinh ra trong thời kỳ co đồng thể tích này từ LVEDV trước đó, nhưng khi LVEDV giảm, áp suất hình thành được hình thành trong kỳ co đồng thể tích này ít đi – là một kết quả tạo thành từ sức mạnh từ chiều dài của sợi cơ tim. Đó là, sợi cơ càng ít căng thì áp suất sinh ra càng ít, một kết quả có được phụ thuộc từ chiều dài bắt cầu của các sợi actin-myosin.
Dĩ nhiên, van động mạch chủ mở trong giai đoạn sớm của thì tâm thu khi áp suất trong thất trái sinh ra trong co đồng thể tích vượt áp lực tâm trương trong quai động mạch chủ, thể tích thất trái giảm và SV được tống ra (xem hình 5). Quá trình có bóp rút ngắn thất chống lại hậu tải của van động mạch chủ cho đến khi thất đạt được một thể tích cuối thì tâm thu mà tại thời điểm đó, với thể tích đó, áp lực sinh ra trong buồng thất trái bắt đầu tương đương áp lực hậu tải, van động mạch chủ đóng, thời kỳ tống máu kết thúc. Nếu áp lực hậu tải giảm, thất trái sẽ tống ra nhiều hơn và thể tích cuối tâm thu sẽ thấp hơn, do đó SV sẽ tăng.
Các thuốc tăng sức co bóp (như: epinephrien, calcium, dobutamine, và dopamine) sẽ chuyển đường cong V-P cuối thì tâm trương lên trên và lệch trái; sau đó thất có thể co rút để tạo một thể tích cuối thì tâm thu nhỏ hơn cho mỗi mức hậu tải, vì thế gia tăng SV. Ngược lại, các thuốc có hoạt tính inotrope âm tính như metoprolol, thiếu máu cục bộ cơ tim, giảm oxi mô, toan máu sẽ đẩy đường V-P cuối tâm thu xuống dưới và lệch phải, như trong đường biểu diễn ngắt quảng V-P trong hình -5. Sau đó, thể tích cuối thì tâm thu gia tăng cho mỗi áp lực hậu tải, kết quả là SV giảm.
Tiếp cận tình trạng suy chức năng thất cấp tính
Các nội dung trên cung cấp những kiến thức cơ bản để hiểu sinh bệnh học và cách điều trị một suy chức năng thất ở bệnh nhân nhồi máu cơ tim cấp. Hình – 5 miêu tả liên quan V-P tâm thu và tâm trương bình thường và chỉ ra sự tống máu bình thường ( đường liên tục ). Từ LVEDV là 120ml và một LVEDP là 10mmHg, thất trái co bóp đồng thể tích cho đến van động mạch chủ mở ở mức 80mmHg. Máu sau đó được tống ra và huyết áp tâm thu tăng đến 110mmHg và giảm về mức LVESP 90mmHg và LVESV 50ml, khi đó van động mạch chủ sẽ đóng lạ hình thành một dấu khấc trên đường sóng động mạch. Theo đó, SV là 70 ml ở mức áp lực nhĩ trái Pla 10mmHg và cung lượng tim là 5,6L/phút khi nhịp tim là 80 lần/phút.
Nhồi máu cơ tim cấp sẽ đẩy đường V-P cuối kỳ tâm thu đủ để gây tăng thể tích cuối thì tâm thu 90ml tại mức LVESP là 75mmHg (đường chấm). Cũng tại thời điểm đó, thể tích cuối tâm trương được gia tăng lên 130ml do tích tụ cùng với hồi lưu tĩnh mạch, và áp suất cuối thì tâm trương gia tăng nhiều hơn mong đợi (LVEDP = 30mmHg) thể hiện đường V-P cuối thì tâm trương chuyển lên trên và sang trái (đường dạng chấm). Do đó, SV còn 40 ml và cung lượng tim còn 4,4 l/phút mặc dù phản xạ nhịp nhanh xuất hiện (110l/p) ở mức gia tăng áp lực đổ đầy, và huyết áp tâm thu giảm còn 90/70 mmHg dù có tăng kháng trở mạch ngoại biên.
Điều trị kinh điển bao gồm giảm tiền tải, các thuốc inotrope, và giảm hậu tải, bên cạnh tái lập và duy trì dòng chảy của mạch vành. Các can thiệp như là morphine, furosemide, và các nitrates giảm hồi lưu tĩnh mạch bằng cách giãn các tĩnh mạch để gia tăng các thể tích unstress và giảm áp lực trung bình hệ thống. Các hành động này đến lượt giảm LVEDV và LVEDP. Việc giảm thể tích cuối thì tâm trương tương xứng với sự thay đổi độ dốc của đường V-P sao cho giảm có ý nghĩa nhất LVEDP nhưng không giảm thể tích cuối thì tâm trương và SV, hoặc nhỏ không đáng kể. Hơn nữa, tác động xấu của việc giảm SV được bù trừ lại sự gia tăng sức co bóp và giảm hậu tải khi lực căng thành được giảm đi bởi giảm LVEDV và LVEDP. Việc giảm hậu tải và giảm tiêu thu O2 cơ tim cải thiện chức năng bơm thể hiện đường V-P lên trên và lệch trái, nghĩa là LVESV giảm và SV gia tăng. Ngoài ra, giảm áp lực cuối thì tâm trương giảm biến chứng phù phổi cấp. Các thuốc có hoạt tính inotrope dương như dopamine và dobutamine tác động trực tiếp lên cơ tim giảm thể tích cuối thì tâm thu và tăng SV. Dopamine còn gây co tĩnh mạch từ đó tăng Pms và hồi lưu tĩnh mạch, do đó, tăng SV thường liên quan tới gia tăng LVEDV, trong khi đó dobutamine có xu hướng tăng SV nhưng gây giảm LVEDV. Các thuốc gây giảm hậu tải như nitroprusside gây giãn các động mạch ngoại biên từ đó giảm áp suất cuối tâm thu và hậu tải; từ đó gây giảm thể tích cuối tâm thu và tăng SV. Nitroprusside và các thuốc dãn mạch khác còn giảm áp suất cuối thì tâm trương không thay đổi thể tích cuối thì tâm trương; hiệu quả này xuất hiện để cải thiện chức năng thất được nhìn thấy trên đường cong Starling, như đã nói ở trên. Việc giảm LVEDP sẽ làm giảm phù phổi và có thể giảm nhu cầu tiêu thụ oxi cơ tim bằng cách giảm áp lực xuyên thành. Để nâng cao hiệu quả từ việc giảm áp suất xuyên thành này, thì mối liên hệ V-P cuối thì tâm trương phải chuyển trái bởi tăng sức co bóp. Ở một vài bệnh nhân shock tim, điều trị thuốc giãn mạch là nhằm cải thiện SV và cung lượng tim mà không gây giảm thậm chí còn cải thiện được huyết áp, điều đó cho thấy là dãn động mạch thể tích cuối thì tâm thu khi sức co bóp được cải thiện.
Thông khí không xâm lấn 2 áp lực BiPAP (hay thông khí áp lực dương liên tục, CPAP) sẽ làm giảm cả tiền tải và hậu tải, bên cạnh hiệu quả cải thiện sự trao đổi khí và công thở. Cung lượng tim không giảm ngay khi áp lực xuyên thành giảm cho thấy nó cải thiện được chức năng bơm.
Một số bệnh lý khác đồng thời trên bệnh nhân hồi sức gây suy chức năng thất có đặc tính giảm SV với tăng áp lực nhĩ trái (xem bảng 1). Giảm oxi máu hay toan máu gây đè sụp đường V-P cuối thì tâm thu và gia tăng độ cứng của thất, như đường cong dạng chấm trên hình 5. Tăng huyết áp động mạch cấp gây tăng hậu tải vì thế SV giảm và tăng thể tích cuối tâm thu như trong đường biểu diễn V-P cuối thì tâm thu trên hình 5. Sau đó LVEDV tăng cùng với sự tích tụ của hồi lưu tĩnh mạch đổ về, vì thế LVEDP gia tăng, thường là nhiều hơn mong đợi do thất “cứng” trước đó do phì đại thất trái đáp ứng với tình trạng tăng huyết áp kéo dài. Theo đó, phù phổi là biến chứng thường xuyên, và nó đáp ứng với dãn mạch khi huyết áp tâm thu hạ xuống. Ở một vài hay tất cả các bệnh lý khác, suy chức năng tâm trương sẽ có những điều trị đặc biệt.
Khi bệnh nhân bị suy tim cấp hay suy cấp trên nền suy tim sung huyết mất bù, giảm LVEDP và LVEDV, duy trì sức co bóp thất trái, gia tăng thời gian tâm trương thích hợp, giảm tối thiểu thiếu máu cục bộ cơ tim là cần thiết. Các biện pháp đó còn điều trị cho tình trạng giảm tưới máu liên quan đến suy chức năng tâm trương. Suy chức năng van giống như suy chức năng tâm thu và tâm trương như gia tăng LVEDV và SV lại suy giảm. Với tình trạng trào ngược van động mạch chủ, sau khi một nhát tống máu rất mạnh mẽ, máu trong động mạch chủ một phần chảy ngược xuống thất trong thì tâm trương làm cho LVEDP gia tăng và huyết áp tâm trương giảm dưới mức 40 mmHg. Một LVEDV lớn sau đó tống đi một SV lớn làm cho huyết áp tâm thu gia tăng đến 120 mmHg, gây một giãn cách huyết áp 80mmHg, nhưng trào ngược động mạch chủ làm giảm SV hiệu quả và cung lượng tim thật sự thấp. Cũng nhận xét trường hợp chức năng van 2 lá bị trào ngược. Trong suốt thì tâm thu, một phân suất lớn máu bị trào ngược lên nhĩ trái, gây giảm SV và cung lượng tim nhưng gây tăng LVEDV và LVEDP khi nhĩ trái làm đầy thất trong thì tâm trương. Trong những tình huống này PP và huyết áp tâm thu sẽ giảm. Ở cả hai trường hợp, hoạt động thất giống như đường dạng chấm trong hình 5 và để cải hiện hoạt động cơ học thất về gần giống như đường liên tục nên sử dụng các thuốc dãn động mạch gây giảm kháng trở lực ngoại biên cho phép dòng máu chảy về ngoại biên hơn là bị trào ngược.
Kiểm soát cung lượng tim bởi hệ thống mạch máu
Tim hoạt động như một cái bơm để tạo một dòng chảy liên tục trong hệ tuần hoàn. Bởi vì cung lượng tim được tạo ra bởi SV và nhịp tim, do đó có một nhận định sai lầm rằng cung lượng tim được kiểm soát bởi tim. Sự thật là hồi lưu tĩnh mạch về thất phải được kiểm soát bởi hệ thống mạch máu, bên cạnh đó, tim nên được hiểu một cách chính xác là nó chỉ là một cái bơm cơ học có hoạt động tâm thu và tâm trương; các hoạt động này nó được xác định như thế nào phụ thuộc vào sự cung cấp của thể tích hồi lưu tĩnh mạch. Do đó, trong phần này sẽ nhìn lại cơ chế đặc trưng của hệ thống mạch máu như là một kiến thức nền tảng cho sự hiểu biết về sự kiểm soát cung lượng tim trên bệnh nhân và bệnh nhân hồi sức.
Sẽ sử dụng các khái niệm về các thành phần kiểm soát hồi lưu tĩnh mạch – VR: áp lực trung bình hệ thống – Pms; áp suất nhĩ phải – Pra; kháng trở hồi lưu – RVR theo quan điểm kinh điển của Guyton. Nội dung của mô hình đề cập đến kháng trở (R) và sức chứa (C) của hệ thống mạch và sự phân phối các thể tích máu làm sao kiểm soát VR, đặc biệt thông qua các áp cảm thụ quan (baroreceptors). Mô hình này còn cung cấp một giản đồ kết hợp các giá trị đơn lẻ Pra và VR với nhau trong mối tác động qua lại giữa chức năng tim và đường biểu diễn hồi lưu tĩnh mạch ở người bình thường và bệnh nhân hồi sức.
Áp lực trung bình hệ thống
Khi tim ngừng đập (giả thuyết), có một áp suất tương đương nhau tồn tại trong toàn hệ thống, và nó có một giá trị mới khoảng 10-15 mmHg, gọi đó là áp lực trung bình hệ thống – Pms. Áp lực này thấp hơn rất nhiều so với áp lực động mạch trung bình nhưng nó gần hơn với áp lực nhĩ phải. Khi dòng máu ngưng lại do tim ngưng co bóp, máu vẫn được dẫn từ nơi có áp lực cao nhưng có dung tích chứa thấp ở động mạch về phía có áp lực thấp nhưng dung tích chứa cao là tĩnh mạch, cung cấp cho sự dịch chuyển thể tích này là một áp lực đẩy.
Lúc tim đập lại, thất trái bơm máu từ tuần hoàn trung tâm vào tuần hoàn hệ thống, do đó gia tăng áp lực ở đây. Tại thời điểm đó, tim phải bơm máu lên phổi, làm cho áp lực nhĩ phải giảm, do dưới tác động của Pms, máu từ các hồ chứa tĩnh mạch ngoại biên sẽ đổ về nhĩ phải. Do đó, áp suất tại vị trí tĩnh mạch giảm thấp thoáng qua so với Pms, trong khi đó áp suất trong động mạch tăng cao hơn Pms với sự thành công của nhát bóp của tim. Quá trình này tiếp tục cho đến khi một trạng thái ổn định đạt được, khi đó áp suất động mạch đủ lớn để đẩy toàn bộ SV của mỗi nhịp tim chảy trong một hệ thống động mạch có kháng trở cao về các hồ chứa của tĩnh mạch. Pms không thay đổi giữa hai trạng thái không có dòng máu và trạng thái ổn định khi có dòng máu từ hoạt động tim bởi vì thể tích mạch và compliance mạch máu không thay đổi. Pms chính là áp lực đẩy VR về nhĩ phải khi tuần hoàn được khôi phục lại. Nó có thể được gia tăng để cải thiện hồi lưu tĩnh mạch khi gia tăng thể tích mạch hay bởi giảm thể tích unstress và compliance mạch máu. Hai cơ chế sau tác động thông qua các thụ thể của baroreceptor đáp ứng với tình trạng tụt huyết áp bằng cách gia tăng trương lực tĩnh mạch và thường xuất hiện chung với nhau. Thể tích unstress có thể giảm bằng cách nâng cao chân bệnh nhân nằm ngữa, chuyển các thể tích unstress ở hai chi dưới thành các thể tích stress thông qua cơ chế tăng VR và Pms. Khi chức năng tim được cải thiện bởi các thuốc tăng co bóp – inotrope dương hay giảm hậu tải, máu được chuyển từ tuần hoàn trung tâm thành các thể tích stress tại tuần hoàn ngoại biên do, đó gia tăng Pms và VR, hơn nữa, việc cải thiện chức năng bơm của thất sẽ làm giảm Pra từ đó làm tăng VR hơn nữa.
Hồi lưu tĩnh mạch và đường biểu diễn chức năng tim
Trước khi tim bắt đầu hoạt động như nói ở trên, Pra tương đương với áp suất trong toàn bộ hệ thống, Pms. Với mỗi nhịp tim hoàn chỉnh, Pra sẽ giảm thấp hơn Pms và VR tăng. Một biểu diễn điển hình được mô tả trong hình 6; khi áp lực nhĩ phải giảm từ 12 mmHg xuống còn 0 mmHg (như trên đường biểu diễn liên tục), thì hồi lưu tĩnh mạch gia tăng với một áp lực đẩy (Pms – Pra). Liên quan giữa VR và áp lực đẩy (Pms – Pra) là kháng trở hồi lưu (RVR = Δ[Pms − Pra]/ΔVR). Khi Pra rơi dưới mức 0 mmHg, thì VR không thể gia tăng được nữa do dòng máu bị giới hạn bởi các áp lực bên trong thành ngực. Điều đó xuất hiện khi áp suất này đè xẹp tĩnh mạch lớn. Hơn nữa việc giảm Pra và CVP liên quan đến việc đè ép mạch máu tiến triển hơn là một gia tăng VR.
Với một thể tích stress và một mức compliance mạch máu nào đó, Pms được duy trì và RVR tương đối hằng định. Trong trường hợp không tăng áp phổi hay suy thất phải, chức năng thất trái được xác định bởi Pra, và do đó, là do VR về tim phải. Tương quan với đường cong chức năng tim được trình bày trong hình 6. Trong đó cung lượng tim được biểu diễn bằng đường cong chức năng tim, với trục hoành là áp lực nhĩ phải, trục tung là cung lượng tim. Tim có thể tống ra một SV và cung lượng tim lớn hơn khi áp lực cuối tâm trương lớn hơn bởi vì thất càng căng cuối kỳ tâm thu thì tống ra một SV nhiều hơn so với thất ít căng dãn hơn dù kết quả có cùng một thể tích cuối kỳ tâm thu. Theo đó, khi Pra giảm, cung lượng tim cũng giảm trên đường cong chức năng tim. Tuy nhiên, VR sẽ tăng khi Pra giảm cho đến khi VR tương đương cung lượng tim tại một giá trị của Pra, tại điểm A giao nhau giữa VR và đường cong chức năng tim thể hiện cung lượng tim trên hình 6.
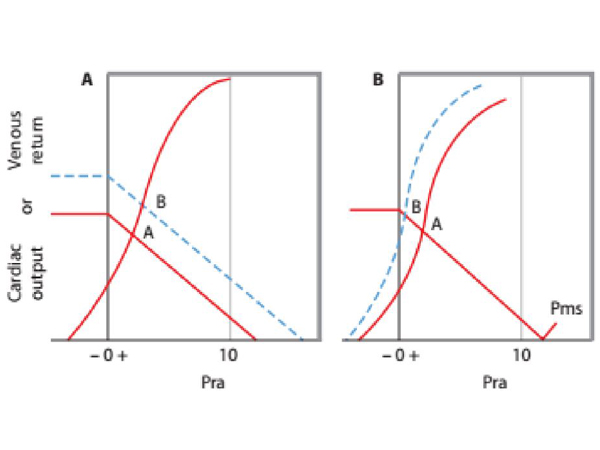
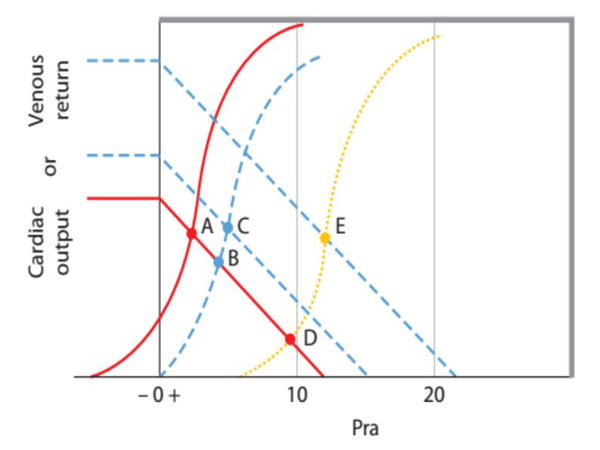
Hình 6. Kiểm soát cung lượng tim bởi hệ thống mạch. Hồi lưu tĩnh mạch hay cung lượng tim được biểu diễn trục tung và áp lực nhĩ phải – Pra là trên trục hoành. Đường thẳng liên tục là đường VR cho thấy VR tăng khi Pra giảm dưới mức Pra tương đương với áp lực trung bình hệ thống (Pms, nơi mà VR= 0), vì thế một đại lượng nghịch đảo của diễn tiến đường cong này là kháng trở của hồi lưu tĩnh mạch (RVR) [(Pms – Pra)/VR]. Đường cong liên tục đậm liên tục là đường biểu diễn chức năng tim, cung lượng tim tăng khi Pra tăng bởi vì thể tích cuối tâm trương tăng. Trong hình A, có sự giao nhau giữa hồi lưu tĩnh mạch và cung lượng tim tại điểm A và B tại một giá trị Pra. Khi cung lượng tim không đủ, VR có thể gia tăng bằng cách gia tăng Pms mà không thay đổi kháng trở hồi lưu, trên đường ngắt quảng VR trong hình B bên trái cho thấy đường cong chức năng tim không thay đổi tại mức cung lượng tim và Pra cao hơn. Trong hình bên phải, VR được gia tăng từ điểm A lên điểm B bằng cách gia tăng chức năng tim (như chúng ta thấy đường ngắt quảng của chức năng tim giao với đường VR tại điểm B). Theo đó, các thuốc có hoạt tính inotrope dương để gia tăng sức co bóp (dobutamine) có thể gia tăng VR bằng cách giảm Pra, nhưng sự gia tăng VR sẽ bị giới hạn bởi sự đè áp các tĩnh mạch lớn trong khoang ngực do các áp lực bên ngoài mạch máu tác động khi Pra thấp hơn 0; khi chức năng tim được cải thiện nó sẽ đẩy thể tích máu trung tâm ra ngoại biên, từ đó làm xu hướng tăng Pms và thúc đẩy gia tăng hồi lưu tĩnh mạch. Thông thường thì các inotrope khác (dopamine hay epinephrien) cũng tăng Pms và VR bởi co tĩnh mạch.
Khi cung lượng tim không đủ, VR có thể tăng lên theo một vài cách. Một trạng thái ổn định hơn để tăng VR bằng cách tăng Pms mà không thay đổi kháng trở hồi lưu, thể hiện ở đường ngắt quảng VR trong hình 6 bên trái. Một hồi lưu tĩnh mạch mới này tương tác với cung lượng tương tự như trên và chúng giao nhau tại điểm B. Đó là biện pháp gia tăng VR cũng làm tăng Pra. Do độ dốc của đường cong chức năng tim bình thường, một gia tăng VR lớn chỉ gây ra bởi một sự gia tăng Pra nhỏ. Ngoài ra, VR cũng được tăng lên bởi sự cải thiện chức năng tim như tăng sức co bóp hay giảm mức hậu tải của tim. Điều này được thể hiện bởi sự dịch chuyển đường cong chức năng tim hướng lên trên trong hình 6 bên phải. Sự gia tăng VR theo cơ chế này liên quan đến mức Pra giảm đi. Hơn nữa, trên tim bình thường, chỉ có một thay đổi nhẹ VR là có thể, chứ việc giảm hơn Pra sẽ không gia tăng hơn cung lượng tim bởi vì VR trở nên giới hạn khi Pra dưới mức 0. Điều này giải thích tại sao các thuốc có hoạt tính inotrope dương không có hiệu quả trong các trường hợp shock giảm thể tích.
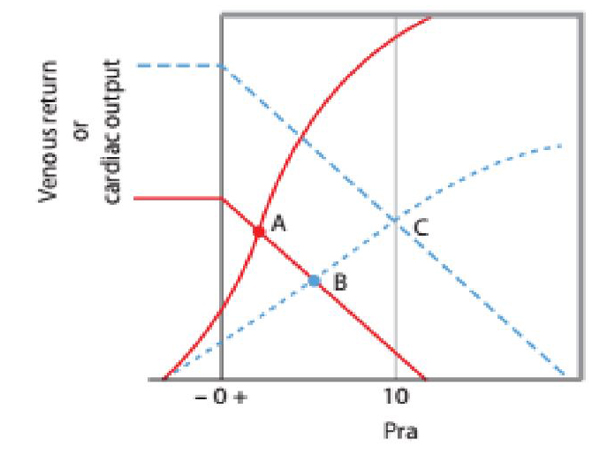
Hình 7. Giảm chức năng tim (đường ngắt quảng BC) làm trạng thái ổn định của VR từ điểm A xuống điểm B bởi vì áp suất nhĩ phải (Pra) gia tăng. Khi đáp ứng bù trừ, các phản xạ baroeceptor và tái hấp thu dịch sẽ gây tăng áp lực trung bình hệ thống đưa đường biểu diễn VR lên một vị trí mới giao với đường cong chức năng tim đã suy tại vị trí C, nơi mà cung lượng tim trở về bình thường tại điểm Pra tăng. Trạng thái ổn định mới có thể tạo ra bởi suy chức năng tâm thu hay tâm trương của thất trái hay thất phải.
Khi chức năng bơm của tim bị suy giảm, như trên đường ngắt quản của hình 7, VR bị giảm từ điểm A đến điểm B với cùng một giá trị Pms khi Pra gia tăng. Bệnh nhân sau đó phải tái hấp thu dịch hay gia tăng các phản xạ tim để gia tăng Pms hướng về một giá trị mới để duy trì một cung lượng tim đầy đủ như trong tình huống suy tim sung huyết. Điều này liên quan tới gia tăng Pra từ điểm B đến điểm C, mà nó sẽ gây tĩnh mạch cổ nổi, gan to, và phù ngoại biên. Lợi tiểu gây giảm thể tích nội mạch sẽ điều chỉnh lại những bất thường này và giảm Pms và VR. Ngược lại, các thuốc inotrope và dãn mạch sẽ giúp cải thiện chức năng tim đã suy bằng cách chuyển đường ngắt quảng lên trên và sang trái, tăng cung lượng tim và giảm Pra hiệu quả hơn bệnh nhân có chức năng tim bình thường.
Kháng trở của hồi lưu tĩnh mạch
Với một mức Pms và Pra nào đó, VR sẽ tăng bằng cách giảm kháng trở hồi lưu – RVR. RVR là trung bình cho tất cả các kháng trở của các khu vực. Kháng trở mỗi khu vực (R) được xác định bởi sức compliance của mạch máu tại nơi đó vào toàn bộ compliance mạch hệ thống (C/CT) và phân suất dẫn lưu từ khu vực mạch máu vào cung lượng tim toàn bộ (F/FT):
RVR = R1(C1/CT)(F1/FT) + R2(C2/CT)(F2/FT) + … + Rn(Cn/CT)(Fn/FT).
Trong hầu hết các trường hợp, RVR duy trì tương đối hằng định, chỉ gia tăng thoáng qua với sự kích thích giao cảm mạnh, thậm chí sau đó có sự tăng kháng trở khu vực được bù trừ lại bởi tái phân phối dòng máu đến mạch ngoại biên có kháng trở và compliance thấp.
Một minh họa cho hiệu ứng này là người ta thực nghiệm bằng cách tạo một nối thông giữa động mạch chủ và tĩnh mạch chủ dưới, như vậy sẽ tăng gấp đôi VR với cùng một Pms và Pra (hình 8). Nếu như xem xét lấy hết phần máu tống ra khỏi thất trái đổ về tim phải trước khi nó tưới máu cho phần thân dưới. Khi một phân suất lớn của cung lượng tim chuyển qua ống nối có một compliance và kháng trở thấp, nhiều máu sẽ được trở về tim hơn do có RVR giảm đi. Việc tạo ra một mô hình như vậy giải thích cho sự thay đổi của huyết động học ở bệnh nhân shock nhiễm trùng, khi cung lượng tim cao được cho có liên quan tăng các dòng máu đến cơ xương, khi một số kích thích chuyển hóa gia tăng phân suất cung lượng tim tưới máu các vùng cơ xương có kháng trở và compliance thấp, do đó RVR thấp và sẽ tăng VR. Một ví dụ khác, hạ oxi máu hệ thống sẽ tăng VR gấp 3 lần. Điều đó đạt được thông qua việc gia tăng Pms do co thắt tĩnh mạch (gây tăng 70%), trong khi tái phân bố cung lượng tim đến các giường mao mạch có giảm compliance và kháng trở chỉ chiếm 30% sự thay đổi này. Các cơ chế này ít có khả năng tiên đoán hơn là việc nhìn thấy nó (tức là chúng ta chỉ nhận biết được hậu quả chứ không thể tiên lượng được quá trình tái phân bố xảy ra để dự phòng trong lâm sàng), vì thế các công việc tương lai sẽ cho chúng ta hiểu biết các ảnh hưởng của tình trạng toan máu, tăng thán khí, và các thuốc giãn mạch trên bệnh nhân hồi sức.
Chú ý trong hình 8, sự gia tăng VR từ điểm A đến điểm B có liên quan đến tăng Pra khi RVR giảm mà không thay đổi cung lượng tim nhiều. Pra không tăng, VR thật sự tăng từ điểm A đến điểm C, khi nối tắc động tĩnh mạch cải thiện chức năng tim từ đường biểu diễn chức năng tim liên tục sang đường ngắt quản như trong hình. Một cách giải thích là việc giảm kháng trở mạch ngoại biên liên quan đến nối thông động tĩnh mạch làm giảm hơn hậu tải của thất trái làm cải thiện chức năng tim.
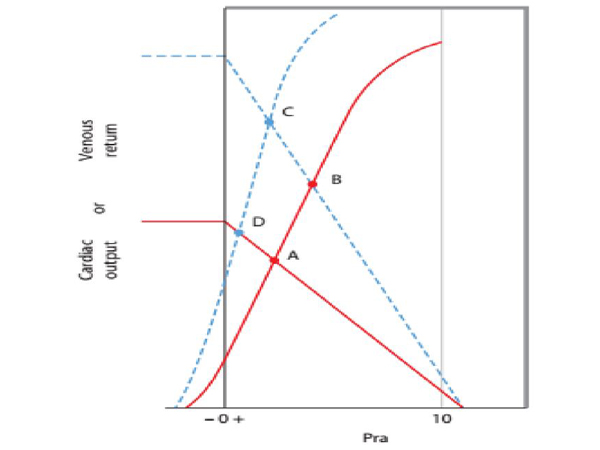
Hình 8. Giảm RVR (đường ngắt quảng BC) làm gia tăng chức năng tim từ A đến B tại cùng một giá trị Pms giống nhau, so sánh với trạng thái có RVR bình thường (đường liên tục AD), chức năng tim không thay đổi (đường liên tục AB). Giản đồ trên miêu tả tác động của mô hình tạo ra một nối thông động tĩnh mạch lớn trên thực nghiệm, với một mong đợi là tạo ra một cung lượng tim (từ A đến C), bởi nối thông làm giảm hậu tải của thất trái và cải thiện chức năng tim (như đường biểu diễn chức năng tim DC). Có thể hình dung được là một thay đổi nhỏ của RVR gây ra tác động lên huyết động bệnh nhân hồi sức (sepsis, giảm oxi máu, toan máu), hay sử dụng các thuốc dãn mạch ở bệnh nhân hồi sức, các trạng thái gây tăng VR sau đó.
Ảnh hưởng các áp suất ngoài tim lên cung lượng tim
Trong các hình ảnh trích dẫn và các thảo luận phía trước, giá trị của Pms và Pra được diễn giải trong điều kiện của áp suất khí quyển. Tuy nhiên, áp suất xuyên thành của nhĩ phải luôn lớn hơn Pra bởi áp lực âm dưới mức áp suất khí quyển (khoảng – 4mmHg) của áp suất màng phổi – Ppl bao xung quanh tim. Xem xét trường hợp được mở ngực hoàn toàn, lúc đó Ppl tăng từ – 4mmHg lên 0 mmHg: thì hồi lưu tĩnh mạch giảm từ điểm A sang điểm B (hình 9) do Pra tăng. Điều này thể hiện bằng đường cong chức năng tim chuyển dịch sang phải bởi sự gia tăng các áp suất bên ngoài tim nhưng nó song song với đường cong chức năng tim bình thường (đường liên tục của điểm A). VR được phục hồi bình thường (từ điểm B đến điểm C) bởi Pms được gia tăng một lượng tương đương với mức gia tăng Ppl và Pra khi mở ngực. Sau đó áp lực xuyên thành của nhĩ phải khi này tương đương như tại điểm A, và Pra sẽ gia tăng từ điểm A đến điểm C tại cùng một mức cung lượng tim.
cung lượng tim.
Hình 9. Giản đồ cho thấy tác động của việc gia tăng áp suất màng phổi lên VR và cung lượng tim. So sánh với trạng thái ổn định bình thường (đường VR và đường chức năng tim liên tục), gia tăng Ppl và áp suất nhĩ phải (Pra) 4mmHg sẽ chuyển đường chức năng tim sang phải (đường chức năng tim ngắt quảng BC) làm cho VR từ A xuống B. Điều đó cho thấy có sự giảm cung lượng tim khi mở ngực để cho áp suất bên ngoài nhĩ phải bằng áp suất khi quyển; sự thay đổi tương tự khi có sự tăng Ppl và Pra trên bệnh nhân được cài đặt PEEP trong thông khi áp lực dương có lồng ngực kín. Trong cả hai trường hợp trên, các phản xạ áp thụ quan của mạch máu và liệu pháp bù dịch làm tăng Pms cho phép xuất hiện một đường VR ngắt quảng giao với đường cong chức năng tim mới tại điểm E, cung lượng tim trở lại bình thường. Một gia tăng lớn mức PEEP làm tăng Ppl và Pra làm thậm chí là nhiều hơn đủ để dịch chuyển đường cong chức năng tim (đường chấm DE) về phía phải nhiều hơn, và để phục hồi lại cung lượng tim (vị trí E) đòi hỏi phải tăng mức Pms để đưa đường cong VR sang một ví trí mới.
Những cơ chế này giải thích cho việc giảm cung lượng tim khi mở ngực, một trạng thái gây thay đổi áp suất trong lồng ngực – các áp suất bên ngoài tim, tương tự việc cài đặt PEEP trong thông khí cơ học. Ppl trong lồng ngực kín sẽ tăng khi thông khí thụ động áp lực dương, do đó, sẽ tăng Pra và giảm VR. Khi cài đặt PEEP là 8mmHg (10 cmH2O), thì Ppl cuối thì thở ra tăng lên phân nửa, từ – 4 mmHg lên 0 mmHg. Theo đó, VR giảm với PEEP từ điểm A đến điểm B như trong hình 9, nhưng không thay đổi chức năng tim và Pms. Cung lượng tim trở lại bình thường bằng cách truyền dịch hay các phản xạ mạch máu nội tại làm tăng Pms một lượng tương đương với mức tăng Ppl hay Pra. Một mức PEEP lớn hơn (20 cmH2O, như trong hình 9) làm giảm VR hơn nữa (từ điểm A xuống điểm D) và đòi hỏi phải gia tăng Pms để trở về mức bình thường (từ điểm D lên điểm E). Trong một nghiên cứu trên loài chó, Pms phải tăng nhiều bằng mức Pra tăng hay mức PEEP thêm vào. Cung lượng tim ít bị ảnh hưởng xấu của PEEP nếu như sự gia tăng áp lực trong lồng ngực được Pms điều chỉnh đủ lớn. Trên bệnh nhân có giảm thể tích tuần hoàn, các phản xạ mạch sẽ duy trì mức VR và Pms bằng cách giảm các thể tích unstress hay compliance mạch máu. Nhưng ở các bệnh nhân có ít các phản xạ mạch máu và dung nạp kém với đặt nội khí quản và cũng như với thông khí áp lực dương nên xem xét truyền thêm dịch để gia tăng thể tích stress mạch máu. Ngược lại, những bệnh nhân đã được đổ dịch tốt hay quá tải dịch có thể dung nạp với một mức PEEP lớn hay sự gia tăng áp lực trong lồng ngực từ việc tăng thể tích thông khí cơ học (thở máy) mà không giảm cung lượng tim bởi vì hoạt động phản xạ mạch trước đó có thể gia tăng Pms với thể tích máu nội mạch đầy đủ tương ứng với mức Ppl tăng lên từ PEEP. Đó là những nhận xét cho phép bác sĩ lâm sàng nhận ra và điều trị tụt huyết áp trên bệnh nhân thở máy; nhưng nội dung này không nên hiểu thành một chỉ định duy trì một thể tích tuần hoàn cao trên bệnh nhân hồi sức có thở máy bởi vì nó thường gây ra phù phổi. Ngoài ra, áp suất bên ngoài tim có thể được gia tăng bởi các bệnh lý khác cùng xuất hiện hay các biến chứng trên bệnh nhân hồi sức; tất cả các biến cố này làm gia tăng áp lực trong buồng tim và gây giảm thể tích hiệu quả của buồng tim; mà trên lâm sàng có thể hiện bằng hội chứng suy chức năng tâm trương (xem bảng 1).
Tiếp cận tình trạng giảm tưới máu
Tình trạng giảm tưới máu, hay shock, luôn hầu như được báo hiệu bởi tình trạng tụt huyết áp hệ thống; đặc điểm lâm sàng thường gặp của giảm tưới máu hệ thống nhiều cơ quan là nhịp tim nhanh, thở nhanh, thiểu niệu trước thận (lượng nước tiểu <20 mL/h, Na+ niệu <20 mEq/L, phân suất bài tiết Na+ <1%, K+ niệu >20 mEq/L, tỷ trọng nước tiểu >1.020), bất thường về tri giác, mức độ thức tỉnh, và toan chuyển hóa. Huyết áp trung bình được xác định bởi cung lượng tim và sức cản ngoại mạch ngoại biên. Một nội dung cơ bản để khởi đầu chẩn đoán và điều trị của bệnh nhân tụt huyết áp được liệt kê trong bảng 2. Hiệu quả của cách tiếp cận này nhắm vào phân loại các dấu hiệu của bệnh nhân nằm 1 trong 3 nguyên nhân thường gặp của shock (septic – shock nhiễm trùng, do tim, hay do giảm thể tích tuần hoàn) và khởi đầu sớm cho điều trị với chẩn đoán ban đầu. Đáp ứng với điều trị can thiệp là một test chính xác đối với chuẩn đoán ban đầu, vì thế đáp ứng huyết động nên được tái đánh giá mỗi 30 phút.Quyết định chẩn đoán được thêm vào bởi tập hợp các dữ kiện từ các tiền sử, bệnh sử y khoa, thăm khám lâm sàng, và các xét nghiệm thường qui để trả lời 3 câu hỏi sau đây.
Septic Shock: Có phải huyết áp giảm là do giảm cung lượng tim hay không?
Nếu KHÔNG, thì SVR phải giảm, bệnh lý gần như luôn gây ra tình trạng giảm kháng lực mạch ngoại biên là sepsis hay nhiễm độc nội sinh vô trùng thường liên quan bệnh suy gan nặng. Như đã trình bày trong cột bên phải của bảng 2, một tình trạng giảm huyết áp kèm theo một giãn cách huyết áp rộng bởi vì nó có SV lớn và có mức huyết áp tâm trương thấp bởi SV được chảy rất nhanh ra ngoại biên thông qua một hệ thống động mạch bị dãn ( xem hình 3). Điều này làm cho chi ấm, da hồng với độ phục hồi màu móng nhanh cùng với tiếng tim rõ, mạnh. Như những các loại shock khác, nhịp tim nhanh là bằng chứng do các phản xạ áp thu quan mạch máu đáp ứng với tụt huyết áp, nhưng co động mạch là đáp ứng với phản xạ giao cảm bị cản trở bởi sự dãn các cơ vòng do các yếu tố dãn mạch phóng thích từ nội mạc mạch máu (hay NO). Kết hợp tình trạng nhịp nhanh và mức giãn cách huyết áp rộng chỉ ra tình trạng tăng cung lượng tim hầu như luôn xảy ra trong giai đoạn sớm trừ khi có giảm thể tích tuần hoàn cùng xuất hiện hay có tình trạng suy chức năng cơ tim trước đó mới làm mất đi trạng thái tăng động tuần hoàn của sepsis.
Điều trị ban đầu được bắt đầu với kháng sinh phổ rộng thích hợp và bao gồm phục hồi thể tích tuần hoàn (thể tích stress) bằng cách đổ dịch để điều trị giảm thể tích liên quan đến sepsis, do giãn các tĩnh mạch gây giảm Pms và VR thấp hơn nhu cầu để duy trì tưới máu đầy đủ cho các cơ quan sống. Mục tiêu cuối cùng của truyền dịch là mơ hồ bởi vì cung lượng tim và mức phân phối oxi (DO2) đã được tăng, và mặc dù cung lượng tim đa phần tăng hơn sau khi truyền dịch, nhưng mức huyết áp tăng ít hơn với mức gia tăng của cung lượng tim. Hơn nữa, nhu cầu một cung lượng tim lớn để đủ để tăng DO2 là một câu hỏi bởi vì toan acid lactic trong septic shock có thể không do chuyển hóa yếm khí gây ra. Theo đó, bệnh nhân septic, những người được tối ưu cung lượng tim lớn nhất không cải thiện được sống còn. Ngược lại, áp suất mạch máu phổi luôn luôn tăng khi truyền dịch, vì thế tăng phù phổi khi quá trình nhiểm khuẩn máu gây gia tăng tính thấm của mạch máu phổi. Xảy ra đồng thời ARDS và septic shock đã tạo ra một tình thế tiến thoái lưỡng nang liên quan đến liệu pháp bù dịch và các vấn đề tim mạch trên những bệnh nhân này. Một cách tiếp cận đảm bảo cho việc hồi sức bệnh nhân septic shock (choáng nhiễm trùng) là đầu tiên đảm bảo một cung lượng tim đủ lớn với áp lực động mạch phổi bít Ppw không vượt quá 15mmHg hoặc CVP từ 8 – 12 mmHg trong trường hợp không có catheter động mạch phổi và thêm dobutamine để tăng cung lượng tim hay huyết áp khi cần thiết. Như đã chú ý ở trên, cung lượng tim tối ưu không có nghĩa là cung lượng tim lớn nhất, và lợi ích từ việc gia tăng cung lượng tim khi đáp ứng với các inotrope cần được cân nhắc lợi ích với nguy cơ loạn nhịp nhanh. Khi trong giai đoạn sớm ARDS không liên quan đến septic shock, chúng ta nên chọn một thể tích tuần hoàn thấp nhất nhưng lại có một cung lượng tim hiệu quả.
Cơ tim trên bệnh nhân sepsic không có chức năng bình thường, nhưng suy chức năng này thường được cho có liên quan đến SV lớn hơn 100ml ở mức LVEDP bình thường. Theo đó, dường như không có khả năng là suy chức năng tâm thu góp phần tạo ra tình trạng shock, nhưng sử dụng dobutamin làm gia tăng cung lượng tim với một LVEDP mức bình thường cao không tăng mức sử dụng O2 hay điều chỉnh mức nhiễm toan acid lactic ở bệnh nhân nhiễm trùng. Thậm chí khi cung lượng tim và DO2 được làm cho đầy đủ bằng cách truyền dịch và sử dụng dobutamin, áp suất tưới máu cho các cơ quan như não và tim vẫn có thể quá thấp ở một số bệnh nhân septic shock. Trong những ca này, sử dụng norepinephrine làm tăng huyết áp và dòng máu đến các tạng, không làm xấu hơn chức năng thận, ngược lại dopamine và epinephrine sẽ gây giảm tưới máu các tạng trong septic shock và các rối loạn nhịp nhanh thông qua tác động β1 của nó. Thở nhanh và suy hô hấp có thể rất trầm trọng, vì thế điều trị ban đầu cần xem xét đặt nội khí quản sớm và thông khí cơ học và điều chỉnh tăng thân nhiệt bằng thuốc hạ sốt, dãn cơ, và làm lạnh. Điều đó ngăn ngừa thảm họa toan hô hấp do kiệt cơ hô hấp, và các biến chứng của đặt nội khí quản cấp cứu và cải thiện oxi hóa cho mô bằng cách giảm nhu cầu O2 trên bệnh nhân bị giới hạn DO2.
Shock tim :
Ngược với septic shock, cung lượng tim thấp được thể hiện bởi huyết áp kẹp cho thấy SV thấp (xem hình 3), dấu hiệu gia tăng SVR (lạnh, tái xanh, chi ẩm, và mức độ hồi phục màu móng giảm), và một tiền sử hay bệnh cảnh có những dấu hiệu gợi ý nguyên nhân tại tim hay mất thể tích tuần hoàn hiệu quả gây tụt huyết áp. Nếu cung lượng tim bị giảm trên bệnh nhân choáng, câu hỏi kế tiếp là: Tim có thật sự khỏe hay không?
| Bảng 2: Tiếp cận ban đầu để đánh giá và điều trị một bệnh nhân Choáng | ||
| Tiêu chí, khám lâm sàng | Cung lượng tim có giảm hay không? | |
| Có | Không | |
| Huyết áp | 90/70. | 90/40. |
| Da niêm | Lạnh ẩm, tái xanh. | Ấm, hồng. |
| CRT | Chậm. | Nhanh. |
| Tiếng tim | Mờ, nhẹ/ | Rõ, mạnh. |
| Bệnh sử/ cận lâm sàng | Triệu chứng của giảm thể tích hay tim mạch. | Tăng, giảm bạch cầu/ nhiệt độ. Ổ nhiễm. Suy giảm miễn dịch. Suy gan nặng. |
| Chẩn đoán | Nhiễm trùng huyết. Nhiễm độc endotoxin. |
|
| Câu hỏi kế tiếp | Tim bệnh nhân có quá tải không? | |
| Có | Không | |
| Bệnh cảnh | Đau thắt ngực, khó thở. | Chảy máu/ mất nước. |
| Dấu hiệu | Tim lớn. Tiếng tim Gallop. Tĩnh mạch cổ nổi. |
Giảm độ căng của mô. Tiêu máu/ ói máu. |
| Cận lâm sàng | ECG. X quang tim phổi. Siêu âm tim. |
Hct. Tăng BUN/ Creatinine. |
| Chẩn đoán | Shock tim | Shock giảm thể tích |
| Có các vấn đề khác hay không? | ||
| Chèn ép tim cấp. Cơn tăng áp phổi cấp. Nhồi máu thất phải. |
Phản vệ. Choáng tủy. Suy thượng thận cấp. Các nguyên nhân chồng lấn lẫn nhau. |
|
Một trái tim có các dấu hiệu của thiếu máu cục bộ cơ tim hay rối loạn nhịp tim, dấu hiệu tim lớn, các tiếng gallop T3, T4, một âm thổi trào ngược mới của suy chức năng valve, tăng áp lực tĩnh mạch cổ hay CVP, các cận lâm sàng cho thấy có thiếu máu cục bộ cơ tim ( \như các dấu hiệu trên ECG, CPK, troponine) hay suy chức năng thất (xquang tim phổi cho thấy tim lớn, dãn rộng các động mạch phổi gốc, hay phù phổi do tim hay siêu âm tim có rối loạn vận động khu trú hay toàn bộ). Nguyên nhân thường gặp nhất của tụt huyết áp với các triệu chứng tim mạch nổi bật là shock tim do thiếu máu cục bộ cơ tim.
Khởi đầu điều trị cho chẩn đoán ban đầu này là thuốc có hoạt tính inotrope dương (dobutamine 3-10 μg/kg/phút) để đánh giá chức năng tống máu của tim bị thiếu máu cục bộ. Điều trị như vậy không trực tiếp chỉ ra sự thiếu hụt mạch vành và có thể gia tăng nhu cầu tiêu thụ oxi cơ tim, đặc biệt nếu nó gây nhịp nhanh. Các chế phẩm notroglycerin dạng ngậm dưới lưỡi, dán da, hay truyền tĩnh mạch giải phóng được tình trạng co thắt mạch vành để gia tăng dòng máu và giảm tiền tải từ đó giảm nhu cầu tiêu thụ oxi cơ tim. Morphine có thể giảm đau, lo lắng, và cả tiền tải nữa. Trong tình huống này, test nước phải rất cẩn thận có thể tăng nguy cơ bởi vì chức năng thất và cung lượng tim giảm lại được gia tăng theo cách can thiệp này thì nguy cơ phù phổi sẽ tăng. Khi dấu hiệu của phù phổi hiện diện trên lâm sàng hay trên hình ảnh Xquang ngực, thì lợi tiểu, morphine, và nitroglycerin sẽ làm giảm tiền tải bởi nó giãn tĩnh mạch, và cải thiện được SV. Tuy nhiên, có khoảng 10% bệnh nhân thiếu máu cục bộ cơ tim có giảm thể tích tuần hoàn. Theo đó, đánh giá lâm sàng huyết động sẽ được hỗ trợ ngay khi có thể với ý nghĩa cần loại trừ ngay tình trạng thiếu dịch tuần hoàn (ví dụ như siêu âm tim, các test đánh giá động thể tích tuần hoàn, catheter tim phải, hay chiến lược thử thách dịch) để có thể tích truyền dịch thích hợp hay giảm thể tích được điều trị. Khi các đo lường này cho thấy đã đủ dịch nhưng tình trạng giảm tưới máu vẫn còn dai dẵng, nên hướng đến sớm giải pháp dãn các động mạch bằng các thuốc giãn động mạch hay sử dụng bóng nội động mạch chủ đối xung để giảm hậu tải thất trái và bảo tồn áp suất tưới máu mạch vành. Các biện pháp can thiệp sau không nên xem như là một biện pháp sau cùng mà cần xem như là những biện pháp sớm khởi đầu để ổn định bệnh nhân shock tim. Tương tự như vậy, nên chọn lọc bệnh nhân đặt nội khí quản sớm và thông khí cơ học cho phép sử dụng an thần hiệu quả và giảm mức tiêu thụ O2 cơ tim, sử dụng PEEP thích hợp để cải thiện oxi hóa máu, không làm giảm VR cũng như hỗ trợ công cho thất trái và giảm được hậu tải.
Shock giảm thể tích:
Sau khi đánh giá lâm sàng không có dấu hiệu gợi ý nguyên nhân tim mạch trên bệnh nhân tụt huyết áp và giảm động tuần hoàn, thì shock giảm thể tích nên được phân biệt với shock tim với những dấu hiệu lâm sàng âm tính và dương tính. Thông thường sẽ quan sát được nguồn chảy máu ngoài (chấn thương nặng, ho máu, ói máu, tiêu máu, hay tiêu phân đen) hoặc xuất huyết nội bằng các thăm khám lâm sàng như hút máu từ sonde dạ dày hay thăm khám trực tràng, gia tăng đề kháng thành bụng, hoặc thăm khám lâm sàng và hình ảnh của khoang ngực, màng phổi, phế nang, khoang sau phúc mạc, hay máu xung quanh động mạch chủ. Mỗi dấu hiệu trên thường liên quan đến dung tích hồng cầu giảm mới. Gỉam thể tích tuần hoàn không có chảy máu thường được nhận ra với tình trạng mất dịch tiêu hóa (ói mữa, tiêu chảy, hút dịch quá mức…), mất dịch qua đường niệu, hay mất dịch qua khoang thứ 3 như trong bỏng nặng.
Thăm khám lâm sàng cho thấy niêm mạc khô, mô mất độ căng thích hợp, và các cận lâm sàng thường qui thường cho thấy tăng nồng độ urea so với mức creatinine tương đối bình thường và tăng dung tích hồng cầu do cô đặc máu.
Khởi đầu điều trị cho bệnh nhân được cho là shock giảm thể tích là cần lập ngay một đường truyền kim 14 ở tĩnh mạch ngoại biên để truyền dịch nhanh với một thể tích máu lớn đã được làm ấm và dịch cho bệnh nhân chảy máu cấp và dịch tinh thể thích hợp cho bệnh nhân bị mất nước. Một catheter tĩnh mạch trung tâm nên được đặt để có một đường truyền chắc chắc và cho phép đo được CVP. Một đáp ứng ngay với việc tăng huyết áp và trương lực mạch sẽ giúp hỗ trợ chẩn đoán thêm chắc chắn hơn, trong khi không có một cải thiện huyết động nào hơn thì phải cần thiết kiểm soát ngay vị trí mất máu còn tiếp diễn hay không và đồng thời tái đánh giá lại chẩn đoán. Đạt được một ổn định nội môi trên bệnh nhân shock mất máu là điều kiện tiên quyết cho việc hồi sức đủ dịch: theo dõi sát tình trạng nội môi và bù dịch nên được tích cực. Các thuốc co mạch như norepinephrine sẽ chỉ được sử dụng trong một thời gian ngắn trong giai đoạn tụt huyết áp để huy động thể tích unstress vào trong hệ tuần hoàn và hỗ trợ co tiểu động mạch cho đến khi thể tích tuần hoàn được hồi phục đầy đủ bởi truyền máu; việc sử dụng kéo dài các thuốc này sẽ làm cho bác sĩ lâm sàng bị rối trong việc xác định mục tiêu hồi sức. Đặt nội khí quản sơm và thông khí cơ học sớm làm giảm công thở cho bệnh nhân và cho phép bù trừ hô hấp cho toan acid lactic trong suốt quá trình hồi sức dịch; làm ấm dịch hồi sức và chườm ấm bệnh nhân với các túi làm ấm để ngăn ngừa các biến chứng hạ thân nhiệt, bao gồm rối loạn đông máu do lạnh và sẽ chảy máu hơn nữa.
Các nguyên nhân khác có thể gây shock:
Mục đích của bảng 2 là đưa ra một công thức để làm công việc chẩn đoán cho những nguyên nhân thường gặp nhất gây choáng đủ để khởi đầu cho việc chẩn đoán và điều trị. Đáp ứng với điều trị ban đầu như là một test chẩn đoán và xác nhận chẩn đoán. Khi những đặc điểm lâm sàng ban đầu hay đáp ứng của bệnh nhân với điều trị cho thấy việc chẩn đoán đã đi đúng hướng, và có được những thông tin về huyết động sớm cũng là cần thiết. Trong giai đoạn tạm thời này, các nguyên nhân khác gây shock có thể nằm ngoài các chiến lược này và nó có thể chồng lấn lẫn nhau hoặc là nguyên nhân đồng thời gây shock mà chúng ta có thể không nhận ra và bỏ sót. Trong phần này sẽ có một cái nhìn lại một số nguyên nhân khác có thể gây ra shock tim (tamponade, suy thất phải cấp) và shock giảm thể tích (shock phản vệ; shock thần kinh; shock thượng thận).
Chèn ép tim cấp
Tràn dịch màng tim nên được nghỉ đến sớm khi có các điều kiện lâm sàng thuận lợi (suy thận, bệnh lý ác tính, đau ngực..), dấu hiệu của thăm khám lâm sàng (tĩnh mạch cổ nổi, huyết áp tâm thu giảm hơn 10mmHg khi hít vào, hay tiếng tim xa xăm), hay thông qua các xét nghiệm thường qui (bóng tim hình bầu rượu trên phim Xquang ngực thẳng, điện thế thấp hay so le điện thế). Siêu âm tim sẽ xác định chẩn đoán và dấu hiệu chèn ép tim khi có tình trạng thất phải hay nhĩ phải bị đè sụp trong thì tâm trương và xấu hơn khi bệnh nhân hít vào, với một thất trái nhỏ một cách tương đối. Tình trạng chèn ép tim đòi hỏi phải dẫn lưu màng tim khẩn cấp hay mở cửa sổ màng tim dẫn lưu. Trong khi quyết định điều trị, phải nhớ rằng truyền dịch để tối ưu thể tích tuần hoàn có thể gây tăng huyết áp nhẹ, trong khi giảm nhẹ thể tích tuần hoàn (lợi tiểu, nitroglycerine, morphine, hay lọc thận ngắt quảng) có thể gây ra một thảm họa về giảm cung lượng tim do giảm trương lực tĩnh mạch do giảm VR cũng như Pms. Thông tim phải cho thấy áp lực nhĩ phải lúc này là 16 -20 mmHg tương đương với áp lực tâm trương động mạch phổi và áp lực phổi bít Ppw; cung lượng tim và Sv giảm. Thông số huyết động như vậy giống như trong shock tim (Ppw và SV thấp). Tuy nhiên, trong những ca chèn ép tim do tràn dịch màng ngoài tim, Ppw gia tăng bởi áp lực màng ngoài tim gia tăng, vì áp lực xuyên thành của thất trái lúc này gần bằng không, và do đó tạo ra một LVEDV thấp sẽ tạo ra SV thấp. Những nguyên nhân khác gây tụt huyết áp với áp suất buồng tim cao nhưng thể tích thất nhỏ bao gồm viêm màng ngoài tim co thắt, tràn khí màng phổi có áp lực, tràn dịch màng phổi lượng nhiều, thông khí áp lực dương với PEEP cao không thích hợp, hay hội chứng tăng áp lực ổ bụng. Trên 33% bệnh nhân có dấu hiệu chèn ép tim cấp nhưng huyết áp tâm thu gia tăng mặc dù cung lượng tim thấp, thường thì các bệnh nhân này có tiền căn tăng huyết áp trước khi rơi vào chèn ép tim.
Điều trị chèn ép tim bao gồm dẫn lưu màng ngoài tim bằng kim hay mở cửa sổ màng ngoài tim. Cẩn thận quan sát sau thủ thuật, có thể xuất hiện phù phổi sau thủ thuật.
Nhồi máu thất phải hay quá tải thất phải
Một bệnh cảnh lâm sàng khác có thể nằm ngoài cách tiếp cận như trong bảng 2 là tụt huyết áp liên quan đến tăng áp phổi cấp hay cơn tăng áp phổi trên nền mãn. Shock sau thuyên tắc phổi cấp thường được xuất hiện trong bệnh cảnh bệnh nhân có nhiều yếu tố thuận lợi (chu phẫu, bất động, tăng đông, hay thuyên tắc phổi trước đó); triệu chứng của khó thở cấp, đau ngực, hay ho máu, thăm khám thực thể có P2 đanh mạch, tác đôi thuận chiều, một giảm oxi máu mới xuất hiện không thể giải thích bởi được bởi các tổn thương trên phim Xquang; hay dấu hiệu căng dãn thất phải cấp trên điện tâm đồ. Siêu âm Doppler không xâm lấn tĩnh mạch sâu 2 chi dưới và chụp mạch cản quang bằng CTScan có thể xác nhận chẩn đoán. Kháng đông hay đặt lưới lọc tĩnh mạch chủ dưới có thể giảm tỷ lệ mắc thuyên tắc huyết khối sau đó, và có thể có thành công với điều trị tiêu sợi huyết (hay ở một số trung tâm có thể thực hiện phẫu thuật lấy huyết khối) ở bệnh nhân shock do thuyên tắc phổi.
Cơn tăng áp phổi cấp trên nền mãn có thể gây shock trên bệnh nhân có tăng áp phổi trước đó, hay thuyên tắc phổi trước đó tái phát, bệnh collagen mạch máu tiến triển, suy hô hấp có giảm oxi máu, hay suy hô hấp mãn (COPD hay xơ phổi) bị thúc đẩy bởi tình trạng co mạch máu do giảm oxi máu. Trong những tình huống này, liệu pháp O2 và các thuốc giãn động mạch phổi kết hợp làm giảm tăng áp phổi và tăng cung lượng tim tuy ít ỏi nhưng có ý nghĩa đáng kể trên những bệnh nhân này.
Thông tim phải chỉ cho thấy một thông tin huyết động duy nhất: áp lực động mạch phổi trung bình rất cao, áp lực động mạch phổi thì tâm trương cao hơn Ppw và giảm cung lượng tim cũng như SV thất phải. Không phải không thường gặp, áp lực Ppw bình thường hay tăng mặc dù LVEDV nhỏ trên siêu âm tim, nhưng sự đẩy lệch vách liên thất từ phải sang trái được cho là nguyên nhân gây “cứng” thất trái, gây suy chức năng tâm trương thất trái. Một biến chứng của liệu pháp dãn động mạch phổi là tụt huyết áp do giãn động mạch hệ thống, dù cung lượng tim phải có tăng. Những hiệu ứng này thúc đẩy tình trạng giảm tưới máu mô, và làm giảm tưới máu vành phải trên thất phải đã dày và dãn trước đó. Một số bằng chứng cho thấy tình trạng shock do tăng áp động mạch phổi được giảm đi khi sử dụng các thuốc đồng vận α (norepinephrine, epinephrine..), do nó gây co mạch hiệu quả nâng cao được huyết áp tâm thu từ đó cải thiện được tưới máu thất phải.
Nhồi máu thất phải gây áp suất động mạch phổi thấp và một áp suất đổ đầy thất trái bình thường bởi vì thất phải dãn, tổn thương không đủ duy trì một cung lượng đủ cho thất trái. Tĩnh mạch cổ nổi, tăng Pra có xu hướng giảm khi truyền dobutamine, có lẽ do tăng sức co bóp của thất trái cải thiện chức năng tâm thu từ đó tương tác cơ học với thất phải. Truyền dịch tích cực sẽ làm cho thất phải suy hơn, và co mạch hệ thống có thể bảo tồn áp lực tưới máu thất phải.
Trong những ca AHRF, tăng áp lực động mạch phổi do nguyên nhân co mạch giảm oxi máu. Co mạch này bị kích thích khi giảm oxi máu tĩnh mạch trộn. Ở nhóm bệnh nhân này, suy chức năng thất phải với tình trạng dãn thất phải và vách liên thất bung sang thất trái (hình 10). Điều trị tương tự như trên nhưng bổ sung điều trị cải thiện thông khí tưới máu, như thở nitric oxide. Một nghiên cứu đa trung tâm cho thấy nitric oxide cải thiện mức độ oxi hóa máu trong giai đoạn sớm nhưng không cải thiện được sống còn.
Shock phản vệ, shock thần kinh, shock do suy thượng thận
Các nguyên nhân gây shock khác có những bệnh cảnh lâm sàng đơn lẻ mà nó thường được chẩn đoán sớm là shock phản vệ và shock thần kinh. Sự nhận biết sớm khi tình trạng shock xuất hiện thông qua các yếu tố khởi phát như dị nguyên hay chấn thương, bác sĩ lâm sàng nên chú ý đến sinh bệnh học của mỗi loại là tình trạng dãn động mạch làm gia tăng rất nhiều thể tích unstress làm cho tình trạng shock giảm thể tích xuất hiện. Theo đó, điều trị chính yếu cho cả hai trường hợp này là truyền đủ dịch, và epinephrine là chất đối kháng phóng thích các hóa chất trung gian trong phản ứng phản vệ, trong khi kiểm tra cẩn thận nguồn chảy máu và tình trạng shock mất máu là một phần trong hồi sức sớm của choáng tủy trên bệnh nhân đa chấn thương. Không phải không thường gặp, bệnh cảnh bệnh nhân shock giảm thể tích không mất máu có liên quan đến tình trạng suy thượng thận cấp. Khi tình trạng này không thể loại trừ được nên thử nồng độ cortisol máu, cung cấp đủ steroid trong tuần hoàn bằng dexamethasone, và tiếp tục test kích thích corticotropin để xác nhận hay loại trừ chẩn đoán. Có một đặc trưng là tình trạng tụt huyết áp và giảm tưới máu mô ở những bệnh nhân này sẽ không đáp ứng với đổ đủ dịch.
Shock do nhiều nguyên nhân
Các chẩn đoán phân biệt và điều trị, tái đánh giá phải luôn nhớ trong đầu, tiếp cận ban đầu bệnh nhân với tình trạng giảm tưới máu sẽ được hoàn thành sớm nhất có thể. Mục tiêu là phân biệt được bệnh nhân shock có nằm trong 3 nguyên nhân shock thường gặp nhất hay không đó là shock tim, shock giảm thể tích, và septic shock đồng thời khởi đầu điều trị thích hợp như là một test chẩn đoán – kháng sinh, các inotrope dương, hay đổ dịch – trong vòng 30 phút. Một khi đáp ứng với điều trị, nó có thể xác nhận chẩn đoán hay là một test thử, như đối với các trường hợp đặt biệt đáp ứng nữa vời với điều trị hay có một nguyên nhân nào khác đồng thời gây ra shock. Khi đó lựa chọn nguyên nhân nào là nguyên nhân chính gây ra tình trạng giảm tưới máu thường đòi hỏi phải xem xét thêm nhiều thông tin khác. Quá trình đó có nhiều phức tạp hơn bởi có nhiều yếu tố đồng thời gây ra shock, ví dụ bệnh nhân septic shock sẽ không có trạng thái tăng động tuần hoàn nếu như có nhồi máu cơ tin đồng thời xuất hiện, bệnh nhân nhồi máu cơ tim có thể có tình trạng giảm thể tích tuần hoàn, hay bệnh nhân septic shock có xuất huyết tiêu hóa kèm theo. Những phân loại shock đó có thể chồng lấn nhau và làm rối loạn hơn thông tim huyết động khi bệnh nhân có chèn ép tim, có thông khí áp lực dương, tràn khí màng phổi, và tăng áp động mạch phổi – tất cả tạo ra thách thức trong chẩn đoán và điều trị shock.
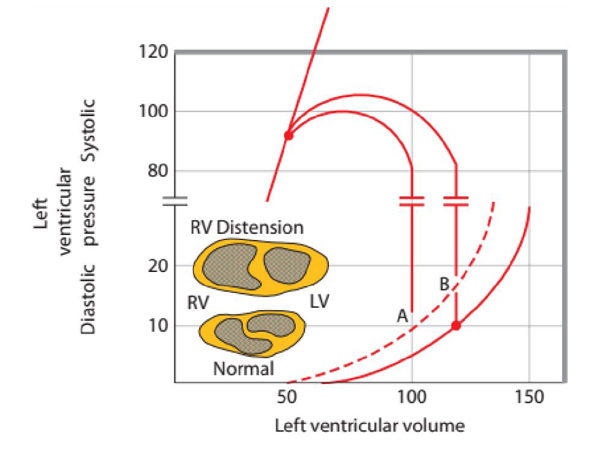
Hình 10. Đường cong V-P trong thì tâm thu và tâm trương của thất trái trước (đường liên tục ) và trong khi bị AHRF (đường ngắt quảng ). Đó là tình trạng suy chức năng tâm trương thất trái do thất phải bị căng dãn quá mức và đẩy lệch vách liên thất sang bên trái đủ để gây tiền tải thất trái và SV bị giảm đi. Các thuốc dãn động mạch phổi như NO có thể có kết quả nhưng ECMO trong các trường hợp này thì cho kết quả tốt hơn.
Tuần hoàn phổi
Áp suất, dòng máu và kháng trở của mạch máu phổi
Cung lượng tim từ tim trái tương đương với VR của tim phải, vì thế toàn bộ cung lượng tim trong mạch máu phổi cũng có dạng động học như tim trái. Thất phải tống máu vào động mạch phổi, vì thế làm tăng áp lực động mạch phổi để đẩy dòng máu đi thông qua các nhánh tiểu động mạch nằm trong nhu mô phổi, nơi có một mạng lưới mạch máu vô cùng nằm ở các vách phế nang hay các mao mạch chảy xuyên qua giữa các khoảng không khí để trao đổi khí. Những mạch máu thành này sẽ tập hợp thành tĩnh mạch phổi và đổ vào nhĩ trái, nơi mà áp suất (Pla) thường được xem là áp suất dòng ra của tuần hoàn phổi. Khi áp suất chênh lệch xuyên tuần hoàn phổi (Ppa – Pla) được chia cho cung lượng của tuần hoàn phổi, thì khi đó kháng trở của tần hoàn phổi được tính ra (mmHg/L/phút) và đôi khi được chuyển sang đơn vị mét (dyn-s/cm5) khi nhân với 80. Bằng phân tích này, gia tăng dòng máu từ một mức này đến một mức khác liên quan đến việc giảm áp suất xuyên tuần hoàn phổi theo mức thay đổi mối liên hệ áp suất – dòng trên đường liên tục trong hình 11B.
Kháng trở dòng máu có thể gia tăng do tình trạng co thắt các tiểu động mạch phổi và các mạch máu phế nang do bởi giảm oxi máu, do bởi đè ép các mao mạch phế nang do tăng áp suất phế nang (Pa), bởi tắc nghẽn một mạch máu lớn do thuyên tắc huyết khối, hoặc bởi tắc nghẽn của nhiều mạch máu song song khi chúng chảy qua nhu mô phổi đủ để cùng một lượng máu nhưng buộc phải chảy qua một hệ thống mạch máu ít hơn. Các tình huống này làm gia tăng kháng trở mạch máu phổi được thể hiện ở điểm A trên đường ngắt quảng trong hình11, nơi mà áp suất khác biệt xuyên phổi (Ppa – Pla ) gia tăng trong cùng một thể tích cung lượng giống nhau. Tăng áp động mạch phổi là một bất thường thường gặp ở bệnh nhân hồi sức các nguyên nhân được liệt kê trong bảng 4 và điều trị của nó được thảo luận trong chuyên đề suy thất phải ở bệnh nhân hồi sức.
Hình 11 mô tả cách thường dùng để đo lường các thông số huyết động với catheter động mạch phổi (PAC) mà nó được đưa vào hệ tĩnh mạch (tĩnh mạch cảnh hay tĩnh mạch dưới đòn) vào trong hệ tuần hoàn trung tâm. Khi cái bóng nhỏ ở đầu catheter được bơm lên, bóng sẽ trôi theo dòng hồi lưu tĩnh mạch vào trong nhĩ phải rồi thất phải, và động mạch phổi cho đến khi nó bít tại một nhánh của động mạch phổi, tắc luôn dòng chảy tại đây. Bởi vì không có dòng chảy, cái lỗ ở đầu catheter mở thông với cột máu được trải dài từ tĩnh mạch đến nhĩ trái.
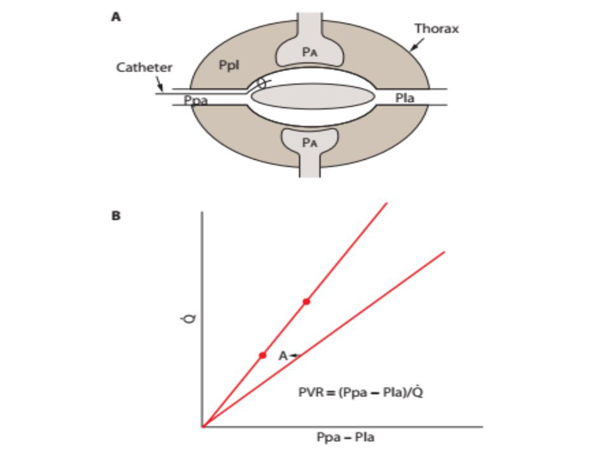
Hình 11. A. Giản đồ của tuần hoàn phổi diễn tả một cách nhìn đơn giản về kháng trở mạch máu phổi (PVR). Máu trong mạch phổi chảy từ động mạch phổi (Ppa) thông qua các nhánh mạch máu đến nhĩ trái (Pla). Tuần hoàn trung tâm được nằm kín trong khoang ngực, mà nó cũng chứa các khoảng thông khí (Pa) tiếp giáp với các vi mạch phế nang. Giữa khoang khí và thành ngực là khoang màng phổi (Ppl), áp suất màng phổi xấp xỉ gần bằng áp suất bên ngoài cách mạch máu bên ngoài phế nang, bao gồm cả tim. Một catheter có bóng chèn ở đầu, khi được bơm lên sẽ làm tắc một nhánh của động mạch phổi đủ để tạo thành một cột máu thông liên tục với nhĩ trái – Pla, từ đó có thể ước lượng áp lực động mạch phổi bít (Ppw), trừ khi áp lực phế nang (Pa) vượt quá Pla, khi đó áp lực bít sẽ vượt quá áp lực nhĩ trái bởi vì Pa tác động trực tiếp lên mạch máu phế nang; trong những trường hợp khác, khi bóng chèn được xả, đầu catheter sẽ đo Ppa, và một cảm biến ở đầu catheter có thể đo lưu lượng dòng máu trong động mạch phổi bằng phương pháp pha loãng nhiệt. B. Trục tung thể hiện cung lượng thất phải, trục hoành thể hiện áp lực xuyên tuần hoàn phổi : Ppa – Pla.
Theo đó, áp lực phổi bít xấp xỉ áp lực nhĩ trái, từ đó ước lượng được LVEDP để đánh giá chức năng thất trái và ước tính được áp suất vi mạch của phổi để giúp điều trị bệnh nhân phù phổi. Khi bóng được xả và dòng máu được tái lập thì áp lực tại đây được xem như là áp lực động mạch phổi. Máu tĩnh mạch trộn lấy từ động mạch phổi cung cấp được nồng độ O2 trong máu tĩnh mạch trộn (CvO2), khi đánh giá đồng thời với độ bão hòa O2 trong máu động mạch (CaO2) và cung lượng tim (Q), sẽ tính toán được mức tiêu thụ O2: VO2 = Q x ([CaO2] − [CvO2]) và mức phân phối O2: DO2 = Q x CaO2. Một dụng cụ cảm biến nhiệt ở đầu catheter có thể tầm soát sự thay đổi nhiệt độ sau khi tiêm nước muối sinh lý lạnh vào trong nhĩ phải cho phép ước tính cung lượng tim từ đường cong pha loãng nhiệt.
Động mạch phổi và nhĩ trái được bao xung quanh bởi áp lực màng phổi – Ppl, vì thế có một giá trị tuyệt đối của Ppa và Pla thay đổi theo nhịp thở. Khi nhịp thở tự phát hít vào gây giảm Ppl, áp suất động mạch phổi cũng như áp lực nhĩ trái sẽ giảm theo, nhưng áp lực đẩy dòng máu xuyên tuần hoàn phổi sẽ không thay đổi (Ppa – Pla), khi áp lực dương bơm trong lúc thở máy làm gia tăng Ppl, Ppa, Pla. Theo đó, rất hữu ích khi ghi các áp lực động mạch phổi cuối thì thở ra trên bệnh nhân thở máy; các giá trị này bị rối loạn khi bệnh nhân có các hoạt động thở mạnh và dữ dội. Khi áp suất phế nang vượt xa áp suất nhĩ trái thì áp lực đẩy máu thật sự là Ppa – Pa. Một tác dụng phụ thường thấy của thông khí áp lực dương với PEEP cao không thích hợp hay Vt cao là sự gia tăng khoảng chết (Vd/Vt) khi dòng máu bị dừng lại khi Pa quá cao; tuy không thường thấy, thông khí phế có thể gia tăng khi Vt được giảm trong những tình huống này, gọi là giảm PaCO2 nghịch thường. Một hậu quả của Pa vượt quá Pla là sẽ thống kê sai áp lực động mạch phổi bít; điều đó có thể nhận ra khi Ppa dao động theo hô hấp và nó thấp hơn áp lực động mạch phổi bít Ppw. Do tác động khá mạnh mẽ của hô hấp lên trên việc đo lường Ppa và Ppw cho nên thật không ngạc nhiên trên thực hành có rất nhiều bác sĩ giải thích sai các thông tin huyết động có được từ PAC. Hơn nữa, PAC thường liên quan đến các biến chứng, và có tranh cãi các thông tin huyết động có được có thể suy luận được từ thăm khám lâm sàng, nó không giúp ích được cho các quyết định lâm sàng và do đó nó không cải thiện được kết quả. Tuy nhiên, các nhà lâm sàng vẫn mắc lỗi trong đánh giá lâm sàng của họ, và cho nên đó là lý do khuyến khích có nhiều công cụ để đánh giá tuần hoàn, bao gồm siêu âm tim, các đánh giá động (độ biến thiên PP, hay độ biến thiên áp lực nhĩ phải), và đôi khi là cần có các thông tin huyết động có được từ PAC, khi mà lâm sàng trở nên không chắc chắn.
Phù phổi
Hình 12 mô tả các yếu tố tuần hoàn quyết địng đến sự di chuyển của dịch phù (Qe) giữa mô kẽ và mạch máu phổi; cân bằng Starling các dòng dịch di chuyển được mô tả trong hình. Áp suất thủy tĩnh trong các vi mạch của phổi (Pmv = 12mmHg nằm lưng chừng giữa áp suất Ppa (bình thường khoảng 15 mmHg) và LVEDP (bình thường khoảng 10 mmHg). Áp suất thủy tĩnh ở những mô kẽ (Pis) là dưới mức áp suất khí quyển (- 4 mmHg), do bởi một phần dịch kẽ được dẫn lưu vào khoang kẽ chung quanh bó mạch-phế quản, nơi có mức áp lực âm hơn, và một phần vì các mạch bạch huyết, các tĩnh mạch van cho phép dòng máu di chuyển một chiều, hoạt động lấy đi dịch từ khoang kẻ mà cấu trúc bên trong ổn định chống lại sự đè sụp. Theo đó, có một áp lực thủy tĩnh dương (Pmv – Pis = 16 mmHg) dẫn lưu dịch phù xuyên qua nội mạch mạch máu đi vào khoang kẽ. Thành mạch máu hiện diện như một hàng rào cho dòng dịch lớn này mà nó được đặc trưng bởi tính thấm với nước (Kf; đơn vị là ml dịch phù/ mmHg/ phút); Kf phụ thuộc vào diện tích bề mặt tiếp xúc (S) và vì thế nó được đặt lên toàn bộ vào hệ mao mạch phế nang, nơi mà diện tích tiếp xúc tập trung vào đó.
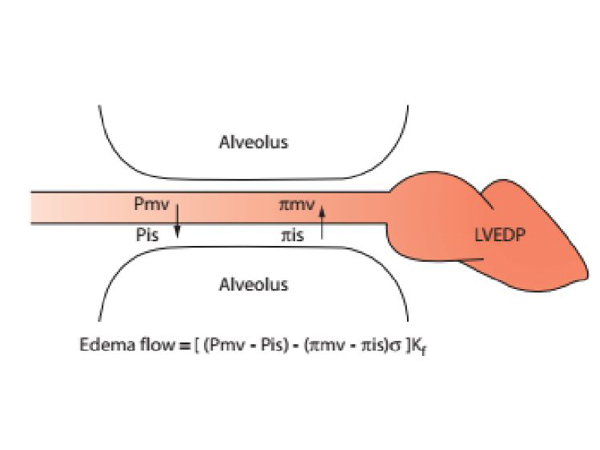
Hình 12. Lược đồ thể hiện các lực Starling kiểm soát các dòng chảy dịch trong nhu nhô phổi từ trong mạch máu đi ra khoảng kẽ.
Màng vi mạch còn có đặc tính bởi tính thấm của nó với protein trong tuần hoàn, chủ yếu là albumine và globulin. Nếu như các protein huyết tương dội lại hoàn toàn khi va thành mạch (σ = 1), tức là không có một protein nào đi qua thành mạch để vào khoang kẻ, nếu màng vi mạch cho protein thấm hoàn toàn (σ = 0), nồng độ protein trong khoang kẽ (Cl), được đo trong bạch mạch của phổi, sẽ tương đương nồng độ protein trog huyết tương (Cp). Cl/Cp = 0,6 là tỷ lệ ổn định bình thường của dịch phù trong khoang kẽ của hầu hết động vật có vú; khi Qe, được ước tính từ lưu lượng dịch trong bạch mạch phổi (Ql), nó sẽ gia tăng khi áp suất thủy tĩnh trong vi mạch tăng, lức này Cl/Cp sẽ giảm xuống và giữ khá hằng định là 0,3. Giá trị hằng định này cho thấy tính thấm của vi mạch trong điều kiện lưu lượng dịch phù tăng cao (σ = 1 − Cl/Cp = 0.7); khi lưu lượng dịch phù giảm đi, nước khuếch tán từ khoang kẽ vào trong máu theo chênh lệch nồng độ nước được tạo bởi Cp > Cl.
Trong phù phổi do tim, Qe sẽ tăng do áp suất thủy tĩnh vi mạch tăng. Một vài yếu tố hoạt động kiểm soát sự tích tụ dịch phù quá mức này: gia tăng dòng bạch mạch, Cl/Cp giảm, và tăng áp suất thủy tĩnh mô kẽ – Pis. Sự gia tăng áp suất thủy tĩnh tại khoang kẽ đẩy dịch phù từ các rãnh mô chảy về khoang kẽ chung quanh các bó mạch-phế quản lớn, nơi mà áp suất thủy tĩnh mô kẽ âm hơn so với áp suất khí quyển (-10 mmHg) bởi vì khi phế nang được giãn nỡ khi thông khí sẽ tạo ra một lực có xu hướng kéo dãn các mạch máu và các cấu trúc quanh mạch máu như các phế quản vốn dĩ tương đối cứng so với nhu mô ngoại biên. Và sự kéo dãn mạch máu và các cấu trúc cạnh mạch máu làm cho áp suất Pis ngày càng âm hơn theo mỗi nhịp thở (nên nhớ các nhịp thở trong giai đoạn phù phổi luôn là những nhịp mạnh mẽ và dồn dập), tạo ra một lực hút hút các dịch phù từ vách phế nang hướng về rốn phổi, nơi mà áp suất thủy tĩnh xung quanh khoang kẽ bó mạch – phế quản âm nhất, và cũng là nơi có khoang chứa lớn nhất có khả năng tích chứa dịch phù, và cũng là nơi mà các ống bạch mạch sắp xếp dày đặc để đẫn lưu dịch phù về hệ tĩnh mạch. Điều này giải thích cho các đường Kerley, phế quản đậm, phù tại rốn phổi lan ra ngoại biên với đặc điểm đám mờ hình cánh bướm kinh điển của phù phổi huyết động trên phim Xquang ngực thẳng.
Trong giai đoạn xuất tiết của ARDS, một thể tích dịch phù không do tim được tích tụ trong phế nang, vì thế tạo ra nhiều shunt hơn trong phù phổi do tim. Có thể được cho là do có sự khác biệt sự phân phối dịch phù xuất hiện trong trường hợp này, thật vậy, phổi bị tổn thương làm tăng Kf và làm giảm σ do tổn thương hàng rào phế nang mao mạch, do đó sẽ gia tăng Qe. Thông thường thì, áp suất thủy tĩnh đẩu dịch phù từ mạch máu vào khoang kẽ bình thường hay giảm, khi Qe tăng với Pmv bình thường sau tổn thương phổi cấp xuất hiện, Cl/Cp không giảm như trong phù phổi do tim nhưng lại tăng nhẹ lên mức 0,8; như vậy cho thấy tính thấm của màng vi mạch tăng lên (σ = 1 – Cl/Cp = 0.2) (không nên lẫn lộn trong khi đọc trị số này, σ càng nhỏ thì tính thấm của thành mạch càng tăng). Theo đó, nồng độ protein trong dịch lụt phế nang gần bằng nồng độ protein trong huyết tương ở ARDS nhưng sẽ thấp hơn trên bệnh nhân phù phổi do tim. Khi màng vi mạch được sữa chữa, dịch phù phế nang được thanh thải rất chậm ở các mô phổi không bị tổn thương bởi các bơm vận chuyển natri; nước sẽ theo sự chênh lệch nồng độ áp suất thẩm thấu mà dịch chuyển qua màng phế nang bình thường, tốc độ thanh thải protein trong dịch phù cũng tăng lên trong giai đoạn hồi phục của ARDS.
PEEP tăng thể tích cuối thì thở ra đễ giảm Pis và tăng thể tích chứa tại các mô liên kết xung quanh bó mạch – phế quản tại rốn phổi; điều đó tái phân bố dịch phù phế nang vào trong các hồ chứa mô kẽ, có liên quan giảm bớt các phế nang bị tràn ngập dịch lụt và từ đó cải thiện được shunt và cải thiện được trao đổi khí, cải thiện được compliance của phổi mà không thay đổi lượng dịch phù. Bởi vì thể tích phổi gia tăng rất nhiều khi PEEP có hiệu quả tái phân bố lại dịch phù, Ppl phải tăng để đẩy thành ngực tương đương với một thể tích lớn hơn. Điều đó gia tăng Pra và giảm VR và giảm huyết áp tâm thu, trừ khi các phản xạ áp cảm thụ quan của bệnh nhân, truyền dịch trong quá trình điều trị, hay có thuốc co mạch duy trì được Pms và cung lượng tim.
Tài liệu tham khảo
1. Principles of Critical Care, 4 edition, 2014.
2. Critical Care Medicine – Principles and Diagnosis and Managemnet in the Adult, 4 edition, 2014.
3. Critical Care Medicine: The Essentials, 4 edition, 2010.
4. Textbook of Critical Care, 7 edition, 2017.
5. Oxford Textbook of Critical Care, second edition, 2016.
6. Oh’s Intensive Care Manual, 7 edition, 2014.
7. The ICU Manual, second edition, 2015.
8. Marino’s The ICU Book, 4 edition, 2014.
9. Evidence – Base Practice of Critical Care, second edition, 2016. 10.Cardiac Intensive Care, second edition, 2010.
Tác giả bài viết:
THS. BS Hồ Hoàng Kim – Khoa HSTC-CĐ – BV Nguyễn Tri Phương
Đăng tải bởi: Heal Central (Health Education Assets Library)





