Lịch sử ra đời nhóm kháng sinh Penicillin
Không còn gì phải nghi ngờ nữa, sự kiện bác sĩ người Scotland Alexander Fleming phát hiện ra Penicillin là một trong những khám phá vĩ đại nhất của y học hiện đại trong thế kỷ XX nói riêng và của lịch sử y học nói chung. Sự kiện này đã mở ra một thời kỳ mới của y học, trong đó loài người chúng ta không còn e sợ các bệnh lý nhiễm khuẩn nữa, những bệnh lý mà trước đó, việc mắc bệnh gần như đồng nghĩa với án tử (hoặc ít nhất là bệnh nhân cũng bị cắt cụt một bộ phận cơ thể nào đó). Sự ra đời của Penicillin cũng mở đường cho một loạt các kháng sinh khác ra đời và phát triển, làm cho cuộc chiến với các vi khuẩn gây bệnh dần nghiêng về phía loài người. Cho đến nay, hàng trăm triệu người trên thế giới đã được cứu sống nhờ kháng sinh.

Trước khi đi vào tìm hiểu sự kiện phát hiện ra Penicillin, chúng ta cũng cần dành vài lời ngắn gọn và súc tích để tri ân đến bác sĩ người Đức Paul Ehrlich, người đã đi tiên phong trong đề xuất việc sử dụng hóa trị liệu (chemotherapy: thuật ngữ này do chính ông tự đề ra), có nghĩa là dùng một loại hợp chất hóa học nào đó để tiêu diệt vi sinh vật mà không làm tổn hại đến cơ thể người bệnh. Ông gọi đó là “viên đạn diệu kỳ” (Magic Bullet). Bản thân ông cũng tìm ra được 2 loại “thuốc” có tác dụng điều trị bệnh giang mai (do xoắn khuẩn giang mai Treponema pallidum gây ra) khá tốt ở thời điểm đó là Arsphenamine (Salvarsan) và Neoarsphenamine (Neosalvarsan) (năm 1910). Hai chất này có cấu trúc hóa học tương tự nhau và đều có chứa nguyên tử arsen trong cấu trúc, có thể gây nhiễm độc cho bệnh nhân, do vậy chúng đã không còn được sử dụng kể từ khi Penicillin ra đời và thay thế chúng, trở thành một loại thuốc hiệu quả trong điều trị giang mai.
Sự phát hiện ra Penicillin thực chất chỉ là một tai nạn, hay nói đúng hơn là một sự tình cờ ngẫu nhiên. A.Fleming, vào năm 1928, đang tiến hành một số nghiên cứu về tụ cầu khuẩn được nuôi cấy trên các đĩa petri tại bệnh viện St.Mary, Luân Đôn. Trước khi bước vào kì nghỉ, ông đã quên (hoặc có thể người kỹ thuật viên của ông đã quên) vệ sinh sạch sẽ các đĩa petri trước khi tạm thời đóng cửa phòng thí nghiệm. Để rồi trở lại sau kì nghỉ, ông quan sát thấy có một hiện tượng lạ: Trên các đĩa petri nuôi cấy tụ cầu khuẩn mà ông đã để quên trước kì nghỉ, có xuất hiện những vòng màu tròn mà trong đó vi khuẩn không thể phát triển được (những vòng tròn đó sau này được gọi là vòng vô khuẩn). Ông nhận thấy trong vòng tròn mà tụ cầu khuẩn không thể phát triển được đó, có một loại vi sinh vật tồn tại và phát triển ở chính giữa. Sau này nó được xác định chính là loài nấm Penicillium notatum. A.Fleming dự đoán rằng, có lẽ loài nấm này đã tiết ra một loại chất hóa học nào đó ức chế sự phát triển của các tụ cầu khuẩn trong đĩa petri đó, ông gọi nó là Penicillin (sau này chúng ta gọi nó là Penicillin G, hay Benzylpenicillin). Phát hiện này sau đó của ông được công bố trên tạp chí The British Journal of Experimental Pathology năm 1929. Ông đã chỉ ra rằng, Penicillin có khả năng ức chế sự phát triển của tụ cầu khuẩn in vitro. Phát hiện này thực ra có thể nói là một thành tựu rất mới và quan trọng thời bấy giờ, và sau này nó sẽ góp phần giúp ông giành được giải thưởng Nobel về Sinh lý và Y khoa năm 1945. Tuy nhiên, ở thời điểm công bố bài báo đó, ông chưa tìm ra cách nào để có thể chiết xuất và tinh chế được Penicillin tinh khiết, vì nó quá kém ổn định. Thành thử ra bài báo không gây được tiếng vang lớn lắm.
Phải mất đến hơn 10 năm sau, Penicillin mới được tinh chế. Nhưng trước đó, chỉ vài năm sau phát hiện ra Penicillin của A.Fleming, vào những năm đầu của thập niên 30, hi vọng của các nhà khoa học về một “viên đạn diệu kỳ” của Paul Ehrlich đã giảm dần (bởi trong vòng khoảng 20 năm kể từ năm 1910 [năm ra đời của Arsphenamine và Neoarsphenamine], người ta không tìm ra một hợp chất hóa học nào có thể ứng dụng trên lâm sàng để điều trị các bệnh lý nhiễm khuẩn, Penicillin thì lúc này vẫn còn chưa tinh chế được). Điều này chỉ thay đổi và mọi người trở nên lạc quan sau sự kiện phát hiện ra Prontosil (thuốc kháng khuẩn Sulfamide đầu tiên) của nhà khoa học người Đức Gerhard Domagk. Ông đã phát hiện ra một điều khá thú vị là thuốc này chỉ có hoạt tính kháng khuẩn in vitro, chứ hoàn toàn không có hoạt tính in vivo. Sau này, nguyên nhân đã được làm sáng tỏ. Lý do là bởi Prontosil thực chất chỉ là tiền thuốc (prodrug), sau khi vào cơ thể, nó được chuyển hóa thành dạng có hoạt tính kháng khuẩn thực sự là Sulfanilamide. Mặc dù Penicillin là kháng sinh đầu tiên được phát hiện ra, nhưng chính Prontosil mới là kháng sinh đầu tiên được tiếp thị trên thị trường. Gerhard Domagk sau đó đã được trao giải thưởng Nobel về Sinh lý và Y khoa năm 1939. Cũng may mắn là nhờ có phát hiện của Gerhard Domagk mà người ta đã không còn hoài nghi về “viên đạn diệu kỳ” của Paul Ehrlich nữa.
Quay trở lại với Penicillin, mãi đến năm 1939, một số nhà khoa học tại đại học Oxford, trong khi đang nghiên cứu về các hợp chất kháng khuẩn mới, đã đọc được bài báo về Penicillin của A.Fleming và bắt đầu chú ý đến nó. Lúc đó, Howard Florey, người sau này cũng sẽ nhận được giải thưởng Nobel cùng với A.Fleming, đang nghiên cứu về hoạt tính kháng khuẩn của lysozyme. Howard Florey, cùng với đồng nghiệp Ernst Chain, đã ngay lập tức nhìn thấy tiềm năng của Penicillin. Họ đã lập tức liên hệ với A.Fleming và cùng với một nhà hóa học trẻ khác trong phòng thí nghiệm của Florey là Norman Heatley, họ tìm cách nuôi cấy nấm và chiết xuất Penicillin với lượng lớn. Sau đó, đến giữa những năm 1940, Sir William Dunn School of Pathology của Oxford đã có đủ lượng Penicillin để tiến hành các thử nghiệm trên chuột. Đây có thể được coi là thử nghiệm tiền lâm sàng đầu tiên của Penicillin. Thử nghiệm được tiến hành như sau: Có tổng cộng 8 con chuột “tham gia” thử nghiệm này. Tất cả chúng đều được tiêm vào cơ thể một lượng liên cầu khuẩn (Streptococcus) nhóm A đủ để có thể gây tử vong nhanh chóng. Sau đó 8 con chuột được chia thành 2 nhóm: Nhóm 1 không được cho sử dụng Penicillin, còn nhóm 2 được cho sử dụng Penicillin, mỗi nhóm gồm 4 con. Kết quả là nhóm chuột không được sử dụng Penicillin đều tử vong, còn nhóm chuột được sử dụng Penicillin đều sống sót. Thí nghiệm này đã bước đầu chứng minh được hiệu quả của Penicillin in vivo.
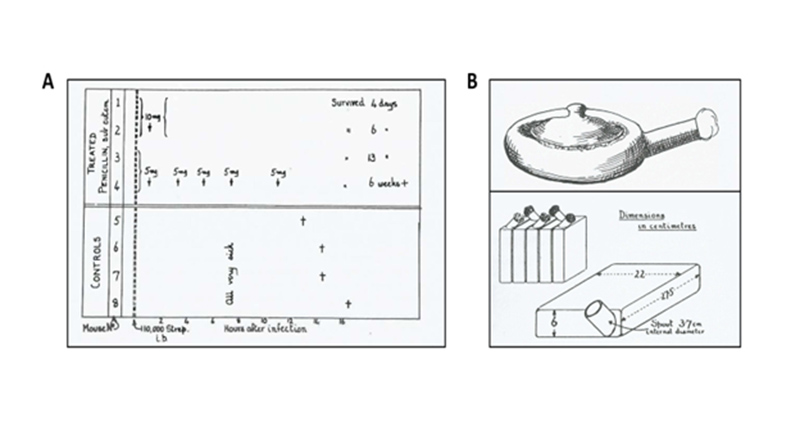
Tuy nhiên thử nghiệm trên chuột thì tiến hành khá dễ, bởi ta chỉ cần một lượng nhỏ Penicillin. Nhưng thử nghiệm trên người thì cần một lượng Penicillin lớn hơn rất nhiều, điều này đã buộc Florey và các cộng sự phải cải tiến các thiết bị lên men của mình cho phù hợp hơn và năng suất hơn (hình trên). Thiết bị đơn giản này được làm từ gốm sứ, bề mặt phải phẳng để có thể chồng lên nhau với số lượng lớn, từ đó tiết kiệm diện tích. Dịch lên men sau đó được lấy ra thông qua các đầu ống. Phương pháp này cho Penicillin với lượng lớn hơn rất nhiều phương pháp nuôi cấy và lên men cũ, nhưng cũng có nhược điểm là ta không thể quan sát được tình trạng phát triển của nấm bên trong thiết bị để có những điều chỉnh phù hợp, cũng như chất lượng dịch lên men giữa các mẻ là không đồng nhất. Dù sao thì công việc sản xuất cũng được tiến hành khá thuận lợi, khi mà chỉ mới đến tháng 2/1941, các nhà khoa học tại đại học Oxford đã có đủ lượng Penicillin mà họ cần để tiến hành thử nghiệm trên người.
Penicillin đã sẵn sàng để được tiến hành thử nghiệm trên người. Tuy nhiên, thử nghiệm đầu tiên có vẻ như không được thành công cho lắm, khi mà một người phụ nữ bị ung thư giai đoạn cuối, sau khi được tiêm Penicillin, đã bị sốt cao. Sau này, chúng ta sẽ biết đây chính là do trong thuốc còn chứa các chất gây sốt (chí nhiệt tố). Sau trường hợp thử nghiệm đầu tiên này, Penicillin được tinh chế kĩ hơn và tinh khiết hơn để đảm bảo đã loại bỏ hoàn toàn chất gây sốt. Trường hợp thử nghiệm lần thứ hai là trên một viên cảnh sát bị nhiễm khuẩn nặng. Việc sử dụng Penicillin đã đem lại đáp ứng lâm sàng tích cực cho bệnh nhân sau 5 ngày điều trị. Tuy nhiên, do nguồn thuốc hạn chế, các nhà khoa học phải tiến hành tinh chế lại Penicillin trong nước tiểu của bệnh nhân để tái sử dụng. Thế nhưng rốt cuộc, họ vẫn không thể cứu sống bệnh nhân này do không thể bù đắp được sự thiếu hụt Penicillin. Tuy rằng thất bại trong việc cứu sống bệnh nhân, Penicillin thực sự đã cho thấy tiềm năng to lớn trong việc điều trị các bệnh lý nhiễm khuẩn, miễn là chúng ta có đủ thuốc.
Sau đó, trong giai đoạn 1941-1942, 170 bệnh nhân đã tham gia các thử nghiệm về Penicillin trên người và kết quả và Penicillin đã chứng minh được hiệu quả tuyệt vời của nó, với các tác dụng phụ không đáng kể.
Sau đó, các nhà khoa học tại đại học Oxford đã nghĩ đến việc sử dụng Penicillin cho những người bị nhiễm trùng do bị thương trong chiến tranh, bao gồm cả binh lính và dân thường. Tuy nhiên, họ không có đủ nguồn lực để làm việc này. Thêm vào đó, do cam kết của Anh trong Chiến tranh Thế giới lần thứ II, các công ty dược phẩm tại Anh cũng không được phép sản xuất Penicillin ở quy mô công nghiệp. Chính điều này đã khiến Florey và Heatley phải tìm đến sự hỗ trợ của chính phủ Hoa Kỳ. Tại đây, họ không chỉ phải tìm cách cải tiến phương pháp tinh chế để cho ra Penicillin sạch hơn, tinh khiết hơn, cùng với tìm cách nâng quy mô sản xuất Penicillin, mà còn phải tìm ra các chủng nấm Penicillium khác cho năng suất sản xuất Penicillin cao hơn chủng P.notatum của A.Fleming ban đầu. Cuối cùng, chủng P.chrysogenum (được tìm thấy trên một quả dưa bị mốc) là chủng được lựa chọn vì khả năng sản xuất Penicillin mạnh hơn chủng ban đầu 6 lần. Có tới 15 công ty dược phẩm, đến từ cả Anh và Hoa Kỳ, cùng tham gia nghiên cứu và sản xuất Penicillin ở quy mô công nghiệp, cũng như chịu trách nhiệm tiến hành các thử nghiệm lâm sàng để chứng minh hiệu quả của thuốc. Thử nghiệm lâm sàng với quy mô lớn đầu tiên về Penicillin được tiến hành tại mặt trận Bắc Phi năm 1942 (vào thời điểm này, lượng Penicillin sản xuất được chỉ đủ để phục vụ cho nhu cầu của không quá 100 người, tuy vậy, rất sớm thôi, đến tháng 9/1943, lượng Penicillin sản xuất được sẽ đáp ứng được nhu cầu của toàn bộ quân đội các nước Đồng minh), tại các bệnh viện của quân đội, nơi mà Penicillin đã cho thấy hiệu quả vượt trội của nó trên các vết thương đã bị nhiễm trùng. Số lượng binh sĩ tử vong trong Chiến tranh Thế giới lần thứ II nhờ đó đã giảm được đi đáng kể (Nếu không có Penicillin, số lượng người chết sau cuộc chiến có lẽ đã nhiều hơn thế). Penicillin cũng giúp được nhiều người tránh khỏi nguy cơ tàn phế (trước khi có Penicillin, hầu như các nhiễm trùng đều được xử lý bằng cách cắt bỏ bộ phận nhiễm trùng). Kể từ sau Chiến tranh Thế giới thứ II, Penicillin bắt đầu được phổ biến đại trà trong dân chúng nhiều nước, với giá thành ngày càng rẻ.
Năm 1945, như một điều tất yếu, A.Fleming được trao giải thưởng Nobel về Sinh lý và Y khoa nhờ có công lao phát hiện ra Penicillin, cùng với 2 người đã góp công lớn trong quá trình chiết xuất và tinh chế Penicillin, đó là Florey và Chain. Nhiều người cho rằng A.Fleming đã may mắn, nhưng chẳng phải có nhiều phát minh khác của loài người cũng xuất phát từ một sự may mắn hay sai lầm ngẫu nhiên hay sao? Như một nhà toán học lừng danh đã từng nói “Chỉ những bộ óc vĩ đại mới có những phát minh tình cờ”. Nếu không phải nhờ óc quan sát và khả năng suy luận của ông, chưa chắc Penicillin đã ra đời và tạo ra một cuộc cách mạng y học lớn đến vậy.
Cũng từ đây, kỷ nguyên kháng sinh đã mở ra, với hàng loạt các kháng sinh khác được ra đời sau đó, cách mạng hóa trong việc điều trị các bệnh lý nhiễm khuẩn. Và A.Fleming cũng chính thức bước vào ngôi đền của những huyền thoại trong lịch sử y khoa thế giới.
Cấu trúc hóa học của nhóm kháng sinh Penicillin
Năm 1943, Chain và Abraham đã đề xuất cấu trúc hóa học của Penicillin có chứa vòng β-lactam. Sau này, nhờ phương pháp tinh thể học tia X, 2 nhà khoa học Barbara Low và Dorothy Hodgkin đã chứng minh được dự đoán của Chain và Abraham là chính xác.
Hiện nay, cái tên Penicillin được sử dụng như là đại diện cho một nhóm kháng sinh có cấu trúc vòng β-lactam tương tự nhau, chỉ khác nhau ở nhóm thế R như hình dưới.
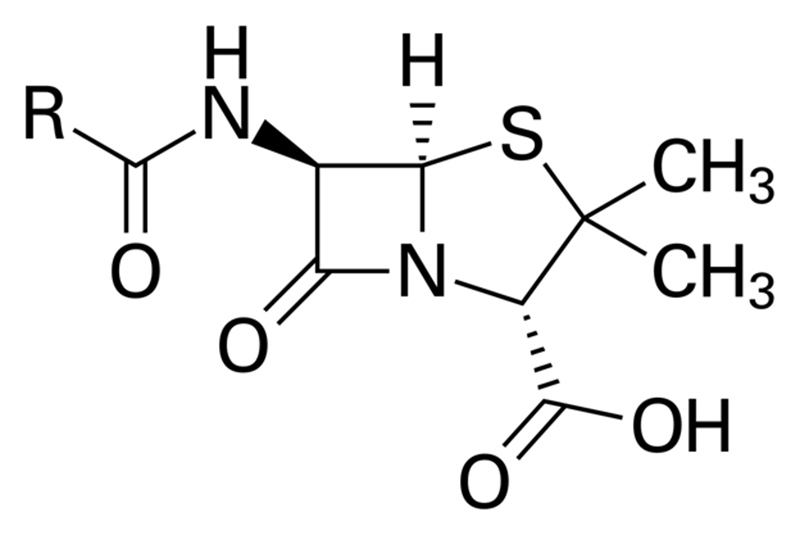
Nhóm thế R này có ảnh hưởng đặc biệt lớn đến phổ kháng khuẩn của kháng sinh cũng như độ bền của nó với enzyme β-lactamase của vi khuẩn và acid trong dịch vị. Do vậy, trong nghiên cứu và phát triển thuốc, người ta thường tập trung chú trọng thay đổi nhóm thế R của kháng sinh bằng bán tổng hợp theo các phương pháp hóa học. Những kháng sinh nhóm Penicillin quan trọng nhất và được sử dụng nhiều nhất trên lâm sàng hiện nay đến chủ yếu từ việc thay đổi phổ kháng khuẩn của kháng sinh. Việc cải thiện độ bền của kháng sinh với enzyme β-lactamase của vi khuẩn hay acid trong dịch vị chỉ là mục tiêu thứ yếu. Lý do là bởi với enzyme β-lactamase của vi khuẩn, chúng ta có thể sử dụng các chất ức chế β-lactamase để bảo vệ phân tử kháng sinh, còn với độ bền trong acid dịch vị, chúng ta có thể thay đổi đường dùng thuốc (tuy vậy đường uống vẫn luôn là đường dùng tiện lợi nhất).
Dược lý học nhóm kháng sinh Penicillin
Cơ chế tác dụng
Penicillin nói riêng cũng như các kháng sinh nhóm β-lactam nói chung đều có cơ chế tiêu diệt vi khuẩn thông qua ức chế tổng hợp thành (vách) tế bào. Penicillin là nhóm kháng sinh diệt khuẩn phụ thuộc thời gian, có nghĩa là, thời gian mà nồng độ thuốc trong máu lớn hơn giá trị MIC (nồng độ ức chế tối thiểu) đóng vai trò quan trọng trong hiệu quả điều trị.

Đích nhắm của các kháng sinh nhóm Penicillin này là thành tế bào, cụ thể hơn là lớp peptidoglycan trên thành tế bào vi khuẩn. Peptidoglycan là một lớp quan trọng chịu trách nhiệm duy trì hình dạng tế bào vi khuẩn cũng như đảm bảo vi khuẩn không bị “nổ tung” vì áp suất thẩm thấu (áp suất thẩm thấu bên trong vi khuẩn cao hơn bên ngoài rất nhiều). Độ dày của lớp peptidoglycan là khác nhau giữa các vi khuẩn gram dương và vi khuẩn gram âm. Nếu như các vi khuẩn gram dương có một lớp peptidoglycan dày, chiếm phần lớn cấu tạo thành tế bào thì vi khuẩn gram âm lại chỉ có một lớp peptidoglycan mỏng, nhưng đi cùng với nó lại là lớp phospholipid kép bao bên ngoài cùng với nhiều thành phần phức tạp khác. Đó có thể là lý do giải thích được tại sao các Penicillin tự nhiên như Penicillin G và Penicillin V chỉ có hoạt tính tốt trên vi khuẩn gram dương, còn trên vi khuẩn gram âm thì chúng lại bị hạn chế hơn nhiều. Có thể chính lớp phospholipid kép bao bên ngoài lớp peptidoglycan của vi khuẩn gram âm là một hàng rào cản trở các phân tử kháng sinh có thể tiếp cận được với đích tác dụng của nó. Các Penicillin bán tổng hợp đã khắc phục được nhược điểm này và mở rộng phổ hơn rất nhiều về phía các vi khuẩn gram âm.
Peptidoglycan là một polymer phức tạp, cấu thành từ các đơn phân (monomer), mỗi monomer lại bao gồm 2 thành phần nhỏ hơn liên kết với nhau, đó là N-acetylglucosamine và N-acetylmuramic acid. Các monomer được liên kết cộng hóa trị với nhau thông qua các cầu nối là các chuỗi peptide ngắn, điều này làm nên cấu trúc không gian 3 chiều phức tạp của peptidoglycan, trong đó nhiều monomer không chỉ được liên kết với nhau theo chiều ngang, mà chúng còn liên kết chéo với nhau theo chiều dọc. Chính điều này đã làm nên sự bền vững của lớp peptidoglycan.
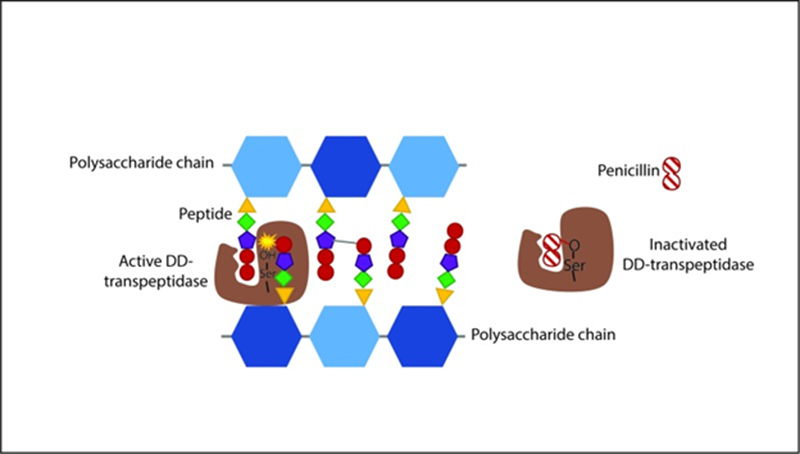
Để có thể tạo nên các liên kết chéo như vậy, vi khuẩn cần đến một loại enzyme đặc hiệu có tên là transpeptidase, sau này còn được gọi với cái tên khác là PBP (Penicillin-Binding Protein: Protein gắn Penicillin). Bản thân các kháng sinh nhóm Penicillin có cấu trúc tương đồng với đầu D-Ala-D-Ala của chuỗi peptide tạo liên kết chéo trong peptidoglycan, điều này dẫn đến chúng ức chế cạnh tranh và không hồi phục transpeptidase, vì đầu D-Ala-D-Ala đó vốn là cơ chất của enzyme. Khi bị ức chế cạnh tranh, enzyme này không thể giúp vi khuẩn tạo ra các liên kết chéo giữa các lớp peptidoglycan, khiến cho lớp peptidoglycan trở nên yếu đuối và chúng dễ dàng bị phá vỡ từ bên trong do áp suất thẩm thấu. Khi lớp peptidoglycan đã vỡ, vi khuẩn bị ly giải.
Cơ chế tác dụng thú vị này làm cho các kháng sinh nhóm Penicillin không ảnh hưởng đến các tế bào của cơ thể bệnh nhân. Bởi các tế bào nhân thực của cơ thể người không có lớp peptidoglycan cũng như các enzyme chịu trách nhiệm tổng hợp peptidoglycan. Về mặt lý thuyết, cơ chế tác dụng của các kháng sinh nhóm này có thể có tác dụng trên tất cả các vi khuẩn thường gặp, trừ vi khuẩn không điển hình. Các vi khuẩn này sẽ đề kháng tự nhiên với kháng sinh nhóm Penicillin nói riêng cũng như các kháng sinh ức chế tổng hợp vách tế bào nói chung vì một lẽ rất hiển nhiên: Chúng không có vách tế bào!
Phổ tác dụng
Chúng ta sẽ phân loại phổ tác dụng của các Penicillin thành các nhóm như sau:
– Penicillin tự nhiên: Đại diện của phân nhóm kháng sinh này là các kháng sinh ra đời đầu tiên, bao gồm Penicillin G và Penicillin V, cùng với các dẫn chất của nó như Benzathine Penicillin G, hay Procain Penicillin G…
Phổ tác dụng của các kháng sinh này chủ yếu bao gồm các vi khuẩn gram dương, bao gồm cầu khuẩn gram dương như tụ cầu (Staphylococcus), liên cầu (Streptococcus), phế cầu (Streptococcus pneumoniae) và trực khuẩn gram dương như trực khuẩn than (Bacillus anthracis) và trực khuẩn bạch hầu (Corynebacterium diphtheriae). Thuốc cũng có phổ tác dụng trên các vi khuẩn gram âm (nhưng hạn chế hơn) như lậu cầu (Neisseria gonorrhoeae) và xoắn khuẩn giang mai (Treponema pallidum). Trên vi khuẩn kị khí, thuốc còn giữ được tác dụng với một số chủng chưa sản xuất β-lactamase như Clostridium perfringens.
Các kháng sinh nhóm này đều không có khả năng chống lại sự phá hủy của enzyme β-lactamase do vi khuẩn tiết ra.
– Penicillin chống tụ cầu: Với các đại diện điển hình cho phân nhóm kháng sinh này là Methicillin, Cloxacillin, Oxacillin, Dicloxacillin, Flucloxacillin và Nafcillin (hiện nay Methicillin không còn được sử dụng nữa do các độc tính của nó trên thận). Đây là nhóm kháng sinh bán tổng hợp từ Penicillin tự nhiên, với nhóm thế R được thay đổi, cồng kềnh hơn và che chắn không gian tốt hơn cho vòng β-lactam, từ đó ngăn cản khả năng enzyme β-lactamase có thể tiếp cận và phá hủy vòng. Các thuốc nhóm này có khả năng chống lại các penicillinase, tuy nhiên không thể chống lại được các β-lactamase mạnh hơn như cephalosporinase hay carbapenemase.
Phổ tác dụng hẹp trên các vi khuẩn gram dương, bao gồm chủ yếu là tụ cầu và liên cầu. Vì có thể chống lại các chủng tụ cầu sinh penicillinase, các kháng sinh nhóm này thường được sử dụng cho các nhiễm khuẩn da và mô mềm.
Với các chủng tụ cầu đã đề kháng với các kháng sinh nhóm này, chúng có một tên gọi chung là tụ cầu kháng Methicillin (bao gồm MRSA – tụ cầu vàng kháng Methicillin [Methicillin-Resistant Staphylococcus aureus] và MRSE – tụ cầu da kháng Methicillin [Methicillin-Resistant Staphylococcus epidermidis]). Cơ chế đề kháng của chúng thường không còn thông qua enzyme phá hủy kháng sinh nữa, mà chúng đã có sự đột biến làm giảm ái lực gắn của Penicillin với PBP2a. Đây là nhóm vi khuẩn cực kỳ khó điều trị và thường gây ra các nhiễm khuẩn bệnh viện nặng. Không chỉ các Penicillin mà tất cả các kháng sinh nhóm β-lactam nói chung đều không mang lại hiệu quả trong việc điều trị nhóm vi khuẩn này (trừ các Cephalosporin thế hệ 5 mới xuất hiện như Ceftaroline hay Ceftolozane, đặc biệt biệt dược Zerbaxa [Ceftolozane + Tazobactam] đã vào thị trường Việt Nam).
– Penicillin phổ rộng: Phân nhóm này lại bao gồm các phân nhóm nhỏ hơn như sau.
+ Aminopenicillin: Hai đại diện cho phân nhóm kháng sinh này bao gồm Amoxicillin và Ampicillin. Với việc có thêm nhóm amino trong nhóm thế R, phổ tác dụng của chúng được mở rộng về phía các vi khuẩn gram âm hơn, bao gồm E.coli, Shigella sp., Salmonella sp., Proteus mirabilis, Klebsiella pneumoniae, Haemophilus influenzae… Tuy vậy, hiệu lực kháng khuẩn trên các vi khuẩn gram dương không bằng các Penicillin tự nhiên. Đây là nhóm kháng sinh bán tổng hợp phổ rộng và không có khả năng đề kháng với β-lactamase. Do vậy, khi sử dụng trên lâm sàng, chúng thường được sử dụng dưới dạng kết hợp với chất ức chế β-lactamase, điển hình là Amoxicillin + Acid clavulanic (Augmentin) và Ampicillin + Sulbactam (Unasyn).
+ Penicillin chống trực khuẩn mủ xanh: Đây là nhóm kháng sinh đặc biệt thường được sử dụng trong nhiễm khuẩn bệnh viện do trực khuẩn mủ xanh (Pseudomonas aeruginosa) gây ra. Phổ tác dụng yếu trên các vi khuẩn gram dương, nhưng lại có tác dụng tốt trên các vi khuẩn gram âm, đặc biệt có hiệu lực vượt trội trên trực khuẩn mủ xanh. Tuy vậy, do không bền với các β-lactamase nên chúng cũng phải được kết hợp với các chất ức chế β-lactamase. Phân nhóm kháng sinh này lại có thể chia nhỏ ra hơn nữa, bao gồm: Các carboxypenicillin như Carbenicillin, Ticarcillin (Ticarcillin + Acid clavulanic [Timentin]); ureidopenicillin như Piperacillin (Piperacillin + Tazobactam [Zosyn]) và các acylampicillin như Azlocillin và Mezlocillin. Tuy nhiên, để điều trị nhiễm khuẩn nặng do trực khuẩn mủ xanh, tại Việt Nam hiện nay các bác sĩ ưa dùng 2 loại Penicillin là Ticarcillin và Piperacillin.
Cơ chế đề kháng
Ngay sau khi nhận giải thưởng Nobel năm 1945, A.Fleming đã cho thấy tầm nhìn vượt thời đại của mình, khi ông đã cảnh báo rằng sự lạm dụng Penicillin nói riêng (cũng như các loại kháng sinh khác nói chung) có thể dẫn đến tình trạng đề kháng kháng sinh của vi khuẩn, gây ra một mối hiểm họa toàn cầu.
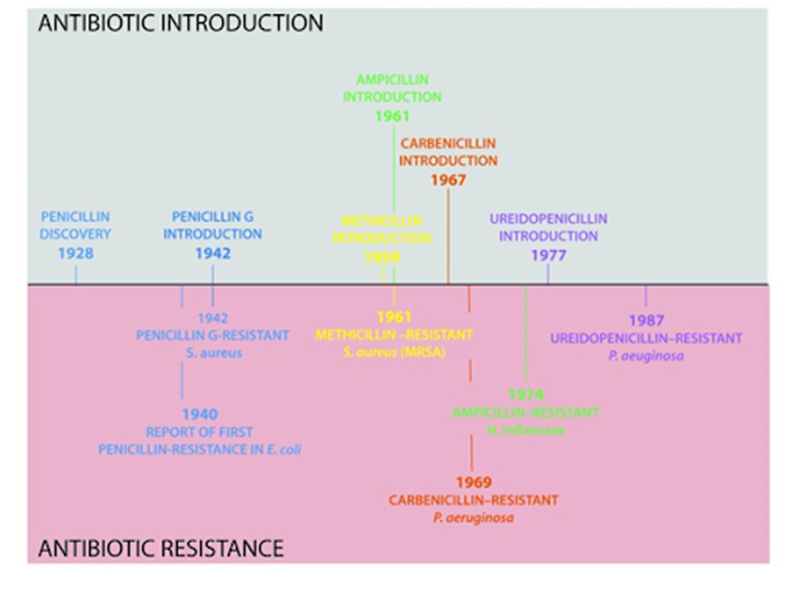
Cơ chế đề kháng với các kháng sinh nhóm Penicillin nói riêng cũng tương tự như các kháng sinh nhóm β-lactam nói chung. Tất cả các cơ chế đề kháng này đều có nguồn gốc từ sự đột biến gen. Sự đột biến này có thể là tự phát sinh dưới áp lực chọn lọc từ việc sử dụng quá nhiều kháng sinh của con người, nhưng cũng có thể là vi khuẩn thu nhận gen đột biến của vi khuẩn khác (việc lấy gen đột biến kháng kháng sinh của vi khuẩn khác có thể thông qua quá trình tiếp hợp [áp dụng cho gen đột biến nằm trên plasmid] nhưng cũng có thể là thông qua thu nạp gen đột biến khi vi khuẩn mang gen đột biến bị ly giải [kiểu đề kháng điển hình của phế cầu]).
Có 4 cơ chế đề kháng kháng sinh nhóm Penicillin đã được phát hiện bao gồm:
– Thay đổi đích tác dụng của thuốc: Đột biến thay đổi cấu trúc của PBP sao cho nó vẫn có tác dụng tốt trong việc hình thành các liên kết chéo giữa các chuỗi peptidoglycan, nhưng ái lực của chúng với Penicillin bị giảm đi. Thông thường, đề kháng kiểu này là do đột biến gen quy định PBP ở ADN trong vùng nhân của vi khuẩn, và một khi cấu trúc PBP đã bị thay đổi, nó sẽ không chỉ đề kháng với các Penicillin, mà nó còn đề kháng với gần như tất cả các kháng sinh nhóm β-lactam, trừ Cephalosporin thế hệ 5. Đây là kiểu đề kháng điển hình của MRSA và MRSE. Trong khi các loại PBP khác bị Penicillin ức chế, PBP2a lại không bị ảnh hưởng bởi kháng sinh và vẫn có thể tiếp tục thực hiện chức năng của nó, nhờ đó mà thành tế bào vi khuẩn vẫn được tổng hợp (cũng có thể hiểu đây là một dạng đề kháng theo kiểu “bypass”, hiểu đơn giản là “đi đường khác”). Cơ chế đề kháng kháng sinh kiểu này cũng chỉ gặp ở các vi khuẩn gram dương.
– Sản xuất enzyme phá hủy kháng sinh: Một số vi khuẩn sản xuất enzyme β-lactamase có khả năng phá hủy cấu trúc vòng β-lactam của Penicillin. Đây là kiểu đề kháng kháng sinh nhóm β-lactam thường gặp nhất, ở mọi loại vi khuẩn từ gram dương cho đến gram âm, từ hiếu khí cho đến kị khí. Enzyme phá hủy được vòng β-lactam của penicillin gọi là Penicillinase, phá hủy được hầu hết các Penicillin trừ nhóm Penicillin chống tụ cầu. Các enzyme β-lactamase mạnh hơn như cephalosporinase, carbapenemase, hay như ESBL (β-lactamase phổ mở rộng [Extended Spectrum Beta-Lactamase]), AmpC β-lactamase hoặc metallo-β-lactamase, đều có khả năng phá hủy vòng β-lactam của Penicillin.
Ở các vi khuẩn gram dương, β-lactamase được sản xuất và tiết ra liên tục vào ngoại bào, trong khi đó, ở các vi khuẩn gram âm, β-lactamase được lưu giữ trong vùng không gian chu chất, bên dưới lớp phospholipid kép bao ngoài lớp peptidoglycan của vi khuẩn. Do đó, cơ chế đề kháng bằng cách sản xuất enzyme phá hủy thuốc này của các vi khuẩn gram âm hiệu quả hơn các vi khuẩn gram dương.
– Giảm tính thấm của kháng sinh với lớp màng ngoài tế bào: Đây là cơ chế chỉ có ở các vi khuẩn gram âm (do các vi khuẩn gram dương không có lớp màng nào bên ngoài lớp peptidoglycan). Sự giảm tính thấm này thường được biểu hiện thông qua các kênh porin (một loại kênh protein xuyên màng tế bào). Bình thường, để vào được bên trong vi khuẩn và ức chế được transpeptidase, các Penicillin cần qua được lớp màng ngoài tế bào thông qua các kênh porin này. Vi khuẩn có thể phát sinh đột biến bằng cách giảm ái lực của các kênh porin này với kháng sinh, giảm số lượng các kênh porin xuyên màng, hay thậm chí cực đoan hơn là xóa sổ toàn bộ các kênh porin xuyên màng. Nếu không thể đi qua được lớp màng ngoài tế bào vi khuẩn gram âm, kháng sinh vô tác dụng.
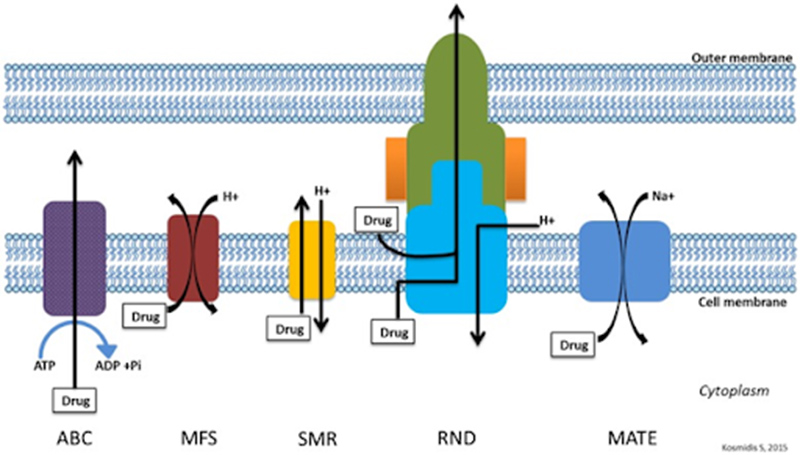
– Phát sinh các bơm tống thuốc (Efflux Pump): Các bơm tống thuốc này có tác dụng đẩy kháng sinh ra khỏi tế bào vi khuẩn trước khi kháng sinh kịp ức chế transpeptidase của vi khuẩn. Kiều đề kháng này cũng chỉ gặp ở các vi khuẩn gram âm chứ không gặp ở các vi khuẩn gram dương (vì ở vi khuẩn gram dương, transpeptidase hoạt động ngay gần bề mặt tế bào và bơm tống thuốc trở nên không có ý nghĩa, vì transpeptidase chắc chắn sẽ gặp phải phân tử kháng sinh). Bơm tống kháng sinh nhóm Penicillin thuộc họ RND (resistance-nodulation-cell division).
Chất ức chế β-lactamase
Các chất ức chế β-lactamase được phát triển vì một lẽ rất hiển nhiên là nhiều vi khuẩn đề kháng với kháng sinh bằng cách tiết ra enzyme β-lactamase. Thêm vào đó, đa phần các kháng sinh nhóm Penicillin tự bản thân nó cũng không bền vững trước các β-lactamase. Việc phối hợp các Penicillin với chất ức chế β-lactamase giúp kháng sinh lấy lại được phổ tác dụng vốn có của nó, mà trước đây đã mất bởi vi khuẩn sản sinh β-lactamase.
Các chất ức chế β-lactamase được biết đến nhiều nhất trên lâm sàng là Acid clavulanic, Sulbactam và Tazobactam. Đây là các chất ức chế β-lactamase cổ điển. Hầu hết các kháng sinh trên thị trường được phối hợp với các chất này. Một số chất ức chế β-lactamase mới hiện đại hơn cũng được phát triển trong thời gian gần đây bao gồm Avibactam, Vaborbactam và Relebactam. Tuy nhiên các chất ức chế β-lactamase này được dùng để phối hợp với các kháng sinh nhóm Cephalosporin và Carbapenem. Còn với các Penicillin, người ta chủ yếu vẫn dùng 3 chất ức chế β-lactamase cổ điển đã nói ở trên.
Lưu ý rằng các chất ức chế β-lactamase không phải là vạn năng, không thể ức chế tất cả các loại β-lactamase của vi khuẩn. Tuy vậy, việc phối hợp này vẫn đem lại cực kỳ nhiều thành công trên lâm sàng.
Dược động học
Hấp thu: Hấp thu của thuốc phụ thuộc rất nhiều vào đường dùng thuốc và mục đích dùng thuốc. Một số kháng sinh được dùng theo đường truyền tĩnh mạch sẽ không có quá trình hấp thu (ví dụ như Ticarcillin, Piperacillin, Ampicillin…), một số kháng sinh được sử dụng theo đường tiêm bắp thì sẽ có hấp thu kém hơn đường tĩnh mạch một chút, nhưng sinh khả dụng vẫn gần như tuyệt đối (gần 100%). Một số kháng sinh được dùng theo đường tiêm bắp với mục đích giải phóng duy trì (như Benzathine Penicillin G) thì sau khi tiêm bắp, thuốc sẽ tủa lại tại vị trí tiêm, sau đó quá trình hòa tan chậm sẽ đưa thuốc vào máu với nồng độ ổn định, đảm bảo nồng độ thuốc trong máu luôn ở trong ngưỡng điều trị. Với các thuốc đường uống, sinh khả dụng biến thiên nhiều hơn. Các Penicillin được sử dụng nhiều theo đường uống là Penicillin V (Phenoxypenicillin), Amoxicillin và Ampicillin. Sinh khả dụng của Penicillin V và Ampicillin là khá thấp (40-50%) và bị ảnh hưởng bởi thức ăn (các kháng sinh này phải sử dụng trước bữa ăn), trong khi sinh khả dụng của Amoxicillin là khoảng hơn 90% và hầu như không bị ảnh hưởng bởi thức ăn. Do vậy, Amoxicillin vẫn luôn là Penicillin được ưu tiên sử dụng theo đường uống.

Phân bố: Các kháng sinh nhóm Penicillin nói chung đều có tính thân nước, do vậy các thuốc thuộc nhóm này sẽ phân bố chủ yếu ở trong máu cũng như các dịch cơ thể thân nước. Các kháng sinh nhóm này nhìn chung khó có thể qua được hàng rào máu não để vào dịch não tủy (trừ trường hợp màng não bị viêm). Cũng có những tài liệu cho thấy các kháng sinh này có khả năng đi qua hàng rào nhau thai và vào được sữa mẹ, nhưng chúng nhìn chung an toàn cho phụ nữ có thai cũng như đang cho con bú.
Chuyển hóa: Hầu như các kháng sinh nhóm này không được chuyển hóa hoặc được chuyển hóa với tỷ lệ nhỏ tại gan.
Thải trừ: Thải trừ dưới dạng nguyên vẹn là chủ yếu, thường qua nước tiểu (một số có thải trừ qua mật là Oxacillin, Cloxacillin và Dicloxacillin). Chỉnh liều ở bệnh nhân suy thận hoặc trẻ sơ sinh thường là cần thiết. Thời gian bán thải nhìn chung ngắn, thường phải sử dụng thuốc 2-4 lần/ngày.
Tác dụng và Chỉ định của nhóm kháng sinh Penicillin
Thuốc có tác dụng diệt khuẩn phụ thuộc thời gian với các chủng vi khuẩn nhạy cảm. Tác dụng diệt khuẩn chỉ đạt ngưỡng tối đa ở một mức liều nào đó và sau đó sẽ không tăng lên cho dù liều có tăng bao nhiêu đi chăng nữa.

Chỉ định: Các kháng sinh nhóm Penicillin được chỉ định cho các nhiễm trùng gây ra bởi các chủng vi khuẩn nhạy cảm. Tuy nhiên, chỉ dựa vào phổ kháng khuẩn thôi là chưa đủ, còn cần phải xem xem liệu loại kháng sinh đó có thể đạt được nồng độ điều trị cần thiết ở vị trí nhiễm khuẩn hay không. Tức là phải cân bằng giữa 2 yếu tố: dược lực học và dược động học.
Penicillin tự nhiên: Các thuốc nhóm này được chỉ định cho bệnh than, bạch hầu, giang mai, lậu (tuy nhiên hiện nay ít dùng đã kháng thuốc nhiều), nhiễm khuẩn da và mô mềm, viêm họng (do liên cầu tan huyết nhóm A), viêm phổi (hiện nay cũng kém hiệu quả do tình trạng kháng thuốc), viêm nội tâm mạc bán cấp do liên cầu (ít dùng). Dạng bào chế Benzathine Penicillin G được chỉ định cho dự phòng thấp tim sau nhiễm liên cầu.
Penicillin chống tụ cầu: Các thuốc nhóm này chủ yếu được chỉ định cho nhiễm khuẩn da và mô mềm do tụ cầu và liên cầu.
Penicillin phổ rộng:
+ Aminopenicillin: Các thuốc này được dùng nhiều trong nhiễm khuẩn hô hấp trên và dưới (bao gồm viêm họng, viêm mũi xoang – tai giữa và viêm phế quản – phổi do các tác nhân Streptococcus pyogenes, S.pneumoniae, H.influenzae và Moraxella catarrhalis), nhiễm trùng đường tiết niệu, đường ruột do E.coli, K.pneumoniae, P.mirabilis, các Enterobacteriaceae khác…, lỵ do Shigella, thương hàn do Salmonella, viêm nội tâm mạc bán cấp (thường kết hợp với một kháng sinh nhóm Aminoside khác, ví dụ như Ampicillin + Gentamicin)… Amoxicillin còn được chỉ định trong viêm loét dạ dày – tá tràng do Helicobacter pylori.
+ Penicillin chống trực khuẩn mủ xanh: Mặc dù có tác dụng trên nhiều vi khuẩn gram âm, nhưng các kháng sinh trong nhóm này chủ yếu được sử dụng để làm kháng sinh dự trữ, đặc biệt là Ticarcillin và Piperacillin, để điều trị các nhiễm trùng bệnh viện nặng do trực khuẩn mủ xanh hoặc một số vi khuẩn gram âm kháng thuốc gây ra như nhiễm trùng vết bỏng, vết mổ, viêm phổi bệnh viện, viêm phổi thở máy, nhiễm khuẩn huyết, nhiễm khuẩn xương khớp, nhiễm khuẩn tiết niệu, nhiễm khuẩn da và mô mềm, nhiễm khuẩn ổ bụng… Trước khi có kết quả kháng sinh đồ, các kháng sinh này có thể được sử dụng trong điều trị theo kinh nghiệm.
Cách dùng – Liều dùng nhóm kháng sinh Penicillin
Với các thuốc sử dụng theo đường uống như Penicillin V, Ampicillin, hay Dicloxacillin, Oxacillin, chúng nên được sử dụng trước bữa ăn 1-2 giờ vì sự hấp thu thuốc bị ảnh hưởng bởi thức ăn. Còn Amoxicillin tuy rằng sinh khả dụng của nó không bị ảnh hưởng bởi thức ăn, nhưng vẫn nên dùng thuốc trước bữa ăn.

Với các thuốc dùng đường tiêm, công việc sử dụng thuốc là của bác sĩ cùng với y tá và điều dưỡng.
Liều dùng mỗi kháng sinh sẽ có những sự khác biệt (Chỉ trình bày liều dùng ở người trưởng thành):
Penicillin tự nhiên:
+ Penicillin G: Thuốc được dùng 4-6 lần/ngày, tổng liều trong 1 ngày còn phụ thuộc vào loại nhiễm trùng. Liều dùng có thể từ rất thấp (2-3 triệu đơn vị/ngày) cho đến rất cao (lên tới 20-30 triệu đơn vị/ngày).
+ Penicillin V: Liều trung bình thường rơi vào ngưỡng 250 mg mỗi 6 giờ hoặc 500 mg mỗi 12 giờ. Trường hợp đặc biệt như Actinomycosis thì tổng liều có thể lên đến 2-4 g/ngày, dùng kéo dài trong vài tháng.
+ Benzathine Penicillin G: Liều dùng 1.2 triệu đơn vị 1 lần duy nhất được chỉ định cho viêm họng do liên cầu tan huyết nhóm A, còn với dự phòng thấp tim sau nhiễm liên cầu, liều dùng là 1.2 triệu đơn vị hàng tháng, hoặc 600,000 đơn vị mỗi 2 tuần. Với giang mai, liều dùng tăng lên 2.4 triệu đơn vị 1 lần duy nhất, đặc biệt, với phụ nữ đang mang thai, liều dùng cần tăng lên 2.4 triệu đơn vị hàng tuần trong 2 tuần, và nếu người bệnh có HIV dương tính, thì liều dùng tiếp tục được tăng lên 2.4 triệu đơn vị hàng tuần trong 3 tuần.
– Penicillin chống tụ cầu:
+ Oxacillin: Liều dùng rất thay đổi, từ mức liều thấp nhất là 250 mg mỗi 4-6 giờ cho đến mức liều cao nhất 2 g mỗi 4-6 giờ, phụ thuộc vào mức độ nặng của nhiễm trùng cũng như vị trí nhiễm trùng.
+ Dicloxacillin: Liều dùng 125-500 mg mỗi 6 giờ.
– Penicillin phổ rộng:
+ Aminopenicillin:
Amoxicillin: Với các nhiễm trùng nhẹ, mức liều có thể chỉ là 500 mg mỗi 12 giờ hoặc 250 mg mỗi 8 giờ, mức nặng hơn có thể tăng liều lên 500 mg mỗi 8 giờ hoặc 875 mg mỗi 12 giờ, nặng hơn nữa có thể dùng 2000 mg mỗi 12 giờ (dạng giải phóng kéo dài). Amoxicillin thường được dùng phối hợp với Acid clavulanic theo các tỷ lệ khác nhau, ví dụ như 250/125 mg, 500/125 mg, 875/125 mg…
Ampicillin: Liều thông thường là 1-2 g mỗi 6 giờ, không quá 12 g/ngày. Ampicillin thường được dùng phối hợp với Sulbactam theo tỷ lệ 1/0.5 g hoặc 2/1 g.
+ Penicillin chống trực khuẩn mủ xanh:
Ticarcillin: Liều thông thường là 3 g mỗi 4-6 giờ (thường phối hợp Ticarcillin với Acid clavulanic theo tỷ lệ 3/0.1 g).
Piperacillin: Liều thông thường là 3-4 g mỗi 6 giờ (thường phối hợp Piperacillin với Tazobactam theo tỷ lệ 3/0.375 g hoặc 4/0.5 g).
Tác dụng không mong muốn của nhóm kháng sinh Penicillin

Dị ứng và quá mẫn: Đây là tác dụng không mong muốn đáng lo ngại nhất của các Penicillin. Các phản ứng dị ứng có thể xuất hiện từ nhẹ (như nổi mẩn, ngứa, phát ban…) đến nặng và rất nặng (phản ứng phản vệ, hội chứng Stevens-Johnson, hội chứng Lyell…), có thể gây tử vong cho người bệnh. Trong các kháng sinh nhóm β-lactam, Penicillin là nhóm có tỷ lệ gây ra các phản ứng dị ứng và quá mẫn nặng cao nhất (Penicillin > Cephalosporin > Carbapenem). Sự dị ứng chéo ít khi xảy ra giữa các nhóm kháng sinh này, tuy nhiên, những kháng sinh tuy khác nhóm nhưng lại mang cùng nhóm thế trong công thức với nhau có nguy cơ gây ra dị ứng chéo cao.
Viêm đại tràng giả mạc do bùng phát Clostridium difficile, có thể gây tử vong nhanh chóng cho bệnh nhân.
Viêm thận kẽ do thuốc (chủ yếu với một số thuốc thuộc nhóm Penicillin chống tụ cầu).
Rối loạn tiêu hóa: Buồn nôn, nôn, tiêu chảy.
Nhiễm nấm Candida miệng.
Chống chỉ định sử dụng kháng sinh Penicillin
Quá mẫn cảm với bất cứ thành phần nào của thuốc.
Người đã từng có tiền sử dị ứng ở mức độ nghiêm trọng với các Penicillin cũng như các kháng sinh nhóm β-lactam khác.
Tương tác thuốc với nhóm kháng sinh Penicillin
Các kháng sinh nhóm Penicillin có tác dụng hiệp đồng tăng cường với các kháng sinh nhóm Aminoside. Đây là một sự phối hợp thuốc kinh điển đã được chứng minh hiệu quả từ lâu. Cơ chế được đề xuất có thể là bởi các kháng sinh nhóm Penicillin ức chế tổng hợp vách tế bào, tạo điều kiện cho các kháng sinh nhóm Aminoside tiếp cận dễ dàng với ribosome 30S (đích tác dụng của các Aminoside) và ức chế chúng. Sự hiệp đồng tăng cường này rất có ý nghĩa và đôi khi nó còn có tác dụng trên cả các chủng vi khuẩn đã đề kháng cả 2 loại kháng sinh.

Các phối hợp kháng sinh khác với Penicillin mang ý nghĩa mở rộng phổ tác dụng nhiều hơn là hiệp đồng tác dụng.
Các kháng sinh nhóm Penicillin có thể làm tăng tác dụng chống đông máu của các thuốc kháng vitamin K (Warfarin): Nguyên nhân là bởi các Penicillin có thể tiêu diệt không chọn lọc các vi khuẩn có trong đường ruột, điều này dẫn đến suy giảm số lượng vi khuẩn cộng sinh trong đường ruột và gián tiếp làm giảm lượng vitamin K mà cơ thể có thể hấp thu được (do một phần lớn vitamin K cung cấp cho cơ thể chúng ta có nguồn gốc từ các vi khuẩn cộng sinh trong ruột). Lượng vitamin K giảm làm máu khó đông hơn, cộng hưởng với tác dụng của thuốc chống đông kháng vitamin K.
Probenecid có thể làm tăng nồng độ các Penicillin trong huyết thanh do cạnh tranh bài tiết ở ống thận. Trước đây, khi kháng sinh còn thiếu hụt nhiều, người ta thường sử dụng phối hợp này. Còn hiện nay, khi lượng kháng sinh đã đủ để đáp ứng nhu cầu của mọi bệnh nhân, Probenecid không còn được phối hợp với các Penicillin nữa.
Lưu ý và thận trọng khi sử dụng thuốc Penicillin
Với những bệnh nhân có tiền sử dị ứng Penicillin ở mức độ nhẹ trước đó, cần thận trọng khi kê đơn lại nhóm kháng sinh này cho bệnh nhân. Tốt nhất nên chuyển sang kháng sinh cùng nhóm là Cephalosporin hoặc chuyển hẳn sang nhóm kháng sinh khác.

Viêm đại tràng giả mạc do C.difficile là một tình trạng nguy hiểm và có thể làm cho bệnh nhân tử vong. Nếu bệnh nhân bị tiêu chảy liên tục và không thể điều trị được theo các phương pháp thông thường, cần nghĩ ngay đến viêm đại tràng giả mạc do C.difficile. Nếu được chẩn đoán xác định, bệnh nhân sẽ được cho sử dụng thuốc Metronidazole, Vancomycin (đường uống) hoặc Fidaxomicin, kết hợp với bù nước và điện giải thích hợp.
Với những bệnh nhân có suy giảm chức năng thận, hiệu chỉnh liều có thể là cần thiết ở những bệnh nhân này. Thêm vào đó, nếu phải dùng các thuốc có khả năng gây viêm thận kẽ, cần chú ý đánh giá chức năng thận thường xuyên.
Sử dụng thuốc Penicillin trên đối tượng đặc biệt

Người già và trẻ em: Vấn đề chủ yếu liên quan đến 2 nhóm đối tượng này là chức năng gan thận không được như người khỏe mạnh, đặc biệt là thận. Người già thì chức năng các cơ quan thường suy giảm do lão hóa và nhiều bệnh lý mắc kèm, còn trẻ em thì thường có chức năng cơ quan chưa hoàn chỉnh (đặc biệt là trẻ sơ sinh và trẻ đẻ non). Cần đánh giá chức năng gan, thận ở những đối tượng này và hiệu chỉnh liều theo cân nặng (với trẻ em), hoặc độ thanh thải creatinine (với người già suy giảm chức năng thận).
Phụ nữ có thai và phụ nữ đang cho con bú: Nhìn chung, các thuốc nhóm này an toàn với cả hai nhóm đối tượng này. Phân loại an toàn cho phụ nữ có thai: B.
Một số nghiên cứu và thử nghiệm lâm sàng về kháng sinh nhóm Penicillin
Một thử nghiệm lâm sàng đối chứng giả dược đã được thực hiện nhằm kiểm tra hiệu quả của việc sử dụng Amoxicillin trong điều trị viêm tai giữa ở trẻ em. Thử nghiệm được đăng tải trên tạp chí NEJM (New England Journal of Medicine) ngày 13/1/2011. Kết quả của thử nghiệm đã cho thấy Amoxicillin vượt trội hơn so với giả dược trong điều trị viêm tai giữa ở trẻ em (những trẻ em trong thử nghiệm có độ tuổi 6-35 tháng tuổi), đồng thời cũng có nhiều tác dụng phụ hơn (điều này có thể chấp nhận được).
Một thử nghiệm lâm sàng ngẫu nhiên khác đã so sánh tỷ lệ tử vong sau 30 ngày của Piperacillin/Tazobactam với Meropenem ở bệnh nhân bị nhiễm trùng máu do E.coli hoặc K.pneumoniae kháng Ceftriaxone. Thử nghiệm đã được đăng tải trên tạp chí JAMA (Journal of the American Medical Association) ngày 11/9/2018. Thử nghiệm này được thực hiện nhằm xác định xem liệu ở những bệnh nhân như vậy, có thể thay thế Meropenem (đại diện cho nhóm kháng sinh Carbapenem) bằng Piperacillin/Tazobactam được hay không (một cách để “tiết kiệm” Carbapenem). Tuy nhiên, kết luận cuối cùng là: Thử nghiệm đã không ủng hộ cho sự thay thế này.
Tài liệu tham khảo
Mariya Lobanovska và Giulia Pilla, Penicillin’s Discovery and Antibiotic Resistance: Lessons for the Future?, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5369031/
Robert Gaynes, The Discovery of Penicillin—New Insights After More Than 75 Years of Clinical Use, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5403050/
Paula A. Tähtinen, M.D., Miia K. Laine, M.D., Pentti Huovinen, M.D., Ph.D., Jari Jalava, Ph.D., Olli Ruuskanen, M.D., Ph.D. và Aino Ruohola, M.D., Ph.D., A Placebo-Controlled Trial of Antimicrobial Treatment for Acute Otitis Media, https://www.nejm.org/doi/full/10.1056/nejmoa1007174
Patrick N A Harris, Paul A Tambyah, David C Lye, Yin Mo, Tau H Lee, Mesut Yilmaz, Thamer H Alenazi, Yaseen Arabi, Marco Falcone, Matteo Bassetti, Elda Righi, Benjamin A Rogers, Souha Kanj, Hasan Bhally, Jon Iredell, Marc Mendelson, Tom H Boyles, David Looke, Spiros Miyakis, Genevieve Walls, Mohammed Al Khamis, Ahmed Zikri, Amy Crowe, Paul Ingram, Nick Daneman, Paul Griffin, Eugene Athan, Penelope Lorenc, Peter Baker, Leah Roberts, Scott A Beatson, Anton Y Peleg, Tiffany Harris-Brown, David L Paterson, MERINO Trial Investigators and the Australasian Society for Infectious Disease Clinical Research Network (ASID-CRN), Effect of Piperacillin-Tazobactam vs Meropenem on 30-Day Mortality for Patients With E coli or Klebsiella pneumoniae Bloodstream Infection and Ceftriaxone Resistance: A Randomized Clinical Trial, https://pubmed.ncbi.nlm.nih.gov/30208454/