Bài viết Mổ lấy thai: Lập kế hoạch trước phẫu thuật và chuẩn bị bệnh nhân của tác giả Vincenzo Berghella, MD được biên dịch bởi Bs Vũ Tài.
1. Giới thiệu
Mổ lấy thai (còn được gọi là sinh mổ) là một trong những phẫu thuật lớn phổ biến nhất được thực hiện trong phòng mổ ở Hoa Kỳ. Các ca sinh mổ chiếm gần một phần ba số ca sinh ở Hoa Kỳ [ 1 ]. Đây cũng là một phẫu thuật phổ biến ở nhiều quốc gia trên toàn thế giới, và tỷ lệ này nhìn chung đang tăng lên [ 2 ]. Lo ngại về tình trạng gia tăng tỷ lể mổ lấy thai đã thúc đẩy các tổ chức y tế đề xuất các biện pháp can thiệp tiềm năng để làm giảm tỷ lệ các phẫu thuật không cần thiết, như chuẩn bị cho việc sinh con tốt hơn, ý kiến thứ hai trước / đánh giá ngang hàng sau khi mổ lấy thai, chăm sóc toàn diện hon bởi nữ hộ sinh trưởng, thực hiện nhiều thử nghiệm chuyển dạ hơn sau mổ lấy thai, hỗ trợ chuyển dạ liên tục, và những thay đổi trong các khuyến khích / không khuyến khích tài chính hiện tại [ 3-6].
Chủ đề này sẽ xem xét việc lập kế hoạch trước phẫu thuật và chuẩn bị bệnh nhân để mổ lấy thai. Kỹ thuật mổ, các vấn đề hậu phẫu, mổ lấy thai lặp lại, mổ lấy thai theo yêu cầu của mẹ và thử nghiệm chuyển dạ sau sinh mổ được thảo luận ở chủ đề riêng:
- (See “Cesarean delivery: Surgical technique”.)
- (See “Cesarean delivery: Postoperative issues”.)
- (See “Repeat cesarean delivery”.)
- (See “Cesarean delivery on maternal request”.)
- (See “Choosing the route of delivery after cesarean birth”.)
2. Chỉ định
Mổ lấy thai được thực hiện khi bác sĩ lâm sàng và / hoặc bệnh nhân tin rằng mổ lấy thai có khả năng mang lại kết cục tốt hon cho mẹ và / hoặc thai nhi so với sinh ngả âm đạo. Do đó, chỉ định mổ lấy thai được chia thành hai nhóm lớn:
- Được chỉ định về mặt y tế / sản khoa, hoặc
- Theo yêu cầu của mẹ
Khoảng 70% các ca sinh mổ ở Hoa Kỳ là mổ lấy thai lần đầu. Ba chỉ định phổ biến nhất đối với mổ lấy thai lần đầu ở Hoa Kỳ chiếm gần 80% trong số các ca sinh này [ 7 ]:
- Không tiến triển trong quá trình chuyển dạ (35%)
- Tình trạng thai nhi không an toàn (24%)
- Ngôi thai bất thường (19%)
Ngoài ra, các chỉ định ít phổ biến hơn đối với mổ lấy thai lần đầu bao gồm, nhưng không giới hạn ở các chỉ định này:
- Nhau thai bất thường (ví dụ: nhau bong non, mạch máu tiền đạo, placenta accreta) •Nhiễm trùng mẹ với nguy cơ lây truyền chu sinh đáng kể khi sinh qua ngả âm đạo •Một số tình trạng dễ chảy máu của thai nhi
- Ngôi dây rốn hoặc sa dây rốn
- Nghi ngờ thai to (thường là 5000 gam ở phụ nữ không bị đái tháo đường, 4500 gam ở phụ nữ bị đái tháo đường)
- Tắc nghẽn cơ học nếu sinh ngả âm đạo (ví dụ, u xơ lớn, gãy xương chậu di lệch nghiêm trọng, thai bị não úng thủy nặng)
- Vỡ tử cung
- Phẫu thuật tử cung trước đó mà đi vào khoang nội mạc tử cung, như cắt bỏ cơ tử cung
Mặc dù không phổ biến, nhưng mổ lấy thai cũng được chỉ định ở những phụ nữ có sự gia tăng nguy cơ bị biến chứng / tổn thương do cổ tử cung mở, thai xuống và sổ hoặc cắt tầng sinh môn. Một số ví dụ bao gồm phụ nữ bị ung thư cổ tử cung xâm lấn, bệnh ruột viêm quanh hậu môn đang hoạt động hoặc tiền sử sửa chữa lỗ rò âm đạo-trực tràng hoặc sa cơ quan vùng chậu. (See “Cervical cancer in pregnancy”and “Fertility, pregnancy, and nursing in inflammatory bowel disease”and “Effect of pregnancy and childbirth on urinary incontinence and pelvic organ prolapse”and “Fecal and anal incontinence associated with pregnancy and childbirth: Counseling, evaluation, and management”.)
Sinh mổ theo yêu cầu của mẹ là không phổ biến và được thảo luận riêng. (See “Cesarean delivery on maternal request”.)
MỔ lấy thai không được chỉ định thường quy cho trẻ nhẹ cân (see “Delivery of the low birth weight singleton fetus”) và hầu hết các dị tật bẩm sinh. (Tham khảo các tổng quan chủ đề về các dị tật riêng biệt.)
3. Chống chỉ định
Không có chống chỉ định tuyệt đối với mổ lấy thai. Ngược lại với các loại phẫu thuật khác, nguy cơ và lợi ích của phẫu thuật được xem xét vì chúng áp dụng cho hai bệnh nhân (mẹ và thai nhi). Tuy nhiên, nhiều thai phụ có khả năng chịu đựng thấp để chấp nhận bất kỳ nguy cơ nào của thai nhi khi sinh ngả âm đạo, bất kể nguy cơ của người mẹ liên quan đến sinh mổ [ 19].
4. Lập kế hoạch trước phẫu thuật
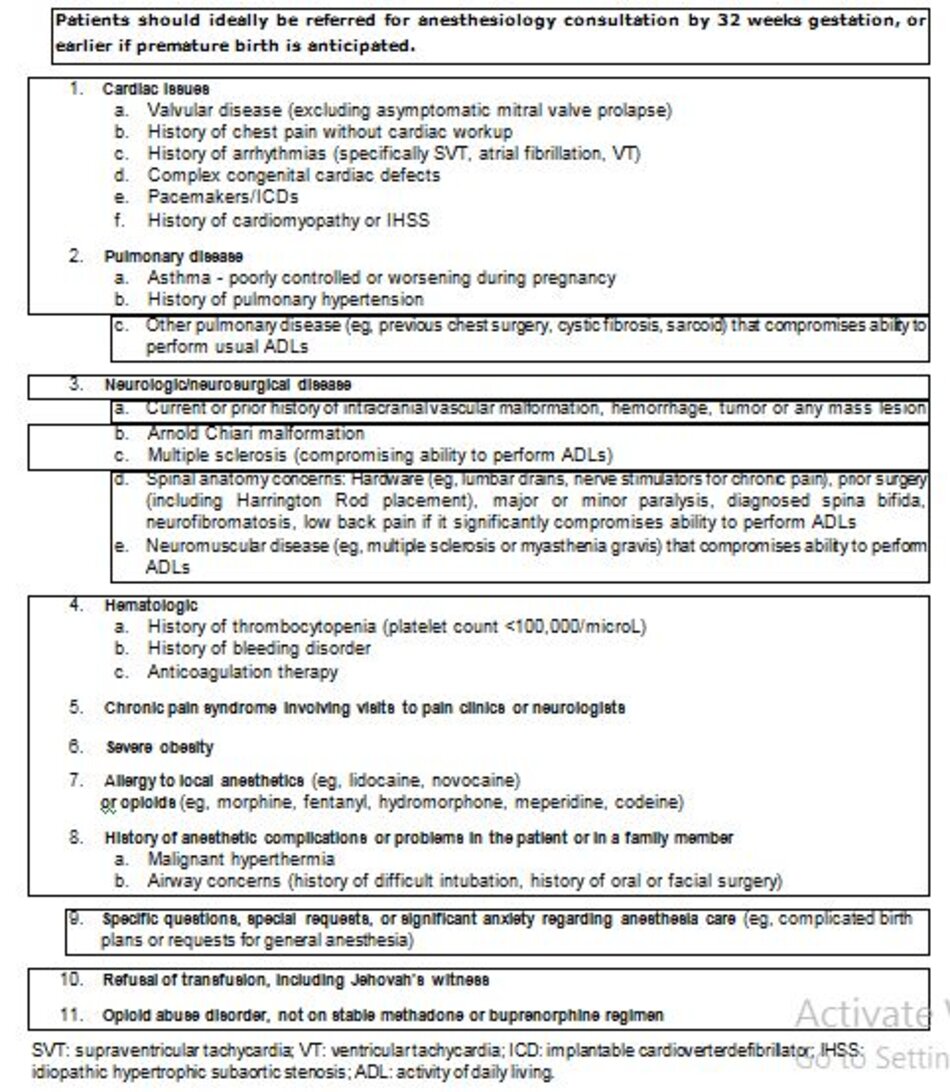
Danh sách kiểm tra – Danh sách kiểm tra có thể hữu ích trong việc lập kế hoạch trước phẫu thuật và có sẵn từ nhiều tổ chức khác nhau, như American College of Obstetricians and Gynecologists (ví dụ: danh sách kiểm tra an toàn cho bệnh nhân để lập kế hoạch trước phẫu thuậtvà lên lịchmổ lấy thai theo kế hoạch) [ 10,11].
Lên lịch mổ
Các phẫu thuật đưọc chỉ định về mặt y tế hoặc sản khoa – Các ca mổ lấy thai được chỉ định về mặt y tế / sản khoa được lên lịch khi có chỉ định lâm sàng. Chỉ định dùng một liệu trình corticosteroid trước sinh trước khi chuyển dạ, nếu thời gian cho phép, được xem xét ở chủ đề riêng. (See “Antenatal corticosteroid therapy for reduction of neonatal respiratory morbidity and mortality from preterm delivery”, section on ‘Gestational age at administration’.))
Khi mổ lấy thai lần đầu được chỉ vì lý do của mẹ hoặc thai nhi, ngoại trừ sinh non không được chỉ định, có sự đồng thuận rằng mổ lấy thai đủ tháng theo kế hoạch nên được lên lịch vào tuần thai thứ 39 hoặc 40 [ 12-14]. Chúng tôi thận trọng đối với việc thực hiện mổ lấy thai sớm (tuần thứ 37 hoặc 38 của thai kỳ) khi các chỉ định y tế / sản khoa để sinh mổ là “tương đối”, như tiền sử biến chứng của thai nhi, mẹ, hoặc sản khoa ở lần mang thai trước đó để không tái diễn.
Ở những thai kỳ có tuổi thai dưới mức tối ưu, việc lên lịch mổ phải dựa vào ước tính tuổi thai lâm sàng tốt nhất [ 15]. Thực hiện chọc ối để đánh giá sự trưởng thành phổi của thai nhi không được khuyến cáo như một phần của quyết định này. (See “Assessment of fetal lung maturity”.)
Cách tiếp cận này dựa trên dữ liệu từ các nghiên cứu quan sát và các thử nghiệm ngẫu nhiên lớn đều cho thấy tỷ lệ bệnh tật đường hô hấp ở trẻ sơ sinh và / hoặc tỷ lệ bệnh tật chung ở trẻ sơ sinh sau sinh mổ theo lịch trình cao hơn so với sinh ngả âm đạo và giảm khi tuổi thai tăng từ 37 đến 40 tuần [ 16 -24]. Một ví dụ về mức độ của những nguy cơ này được lấy từ một thử nghiệm đánh giá các kết cục sơ sinh bất lợi theo tuần tuổi thai đã hoàn thành ở hơn 13.000 ca mổ lấy thai chủ động được thực hiện trước khi bắt đầu chuyển dạ [ 25]. Sinh < 39 tuần tuổi thai có liên quan đến nguy cơ hô hấp và các kết cục sơ sinh bất lợi khác cao hơn có ý nghĩa thống kê so với sinh > 39 tuần tuổi thai:
- Tỷ lệ hội chứng suy hô hấp / thở nhanh thoáng qua theo tuổi thai là 37 tuần (8,2%), 38 tuần (5,5%), 39 tuần (3,4%), 40 tuần (3,0%) và 41 tuần (5,2%)
- Tỷ lệ của bất kỳ kết cục bất lợi / tử vong nào theo tuổi thai là 37 tuần (15,3%), 38 tuần
(11,0%), 39 tuần (8,0%), 40 tuần (7,3%) và 41 tuần (11,3%)
Mổ lấy thai lặp lại theo lịch / kế hoạch – Thời điểm mổ lấy thai lặp lại theo lịch / kế hoạch dựa trên loại vết mổ tử cung trước đó và được xem xét ở chủ đề riêng. (See “Repeat cesarean delivery”, section on ‘Timing’.)
Mổ lấy thai theo yêu cầu của mẹ – Mổ lấy thai theo yêu cầu của mẹ được lên kế hoạch vào tuần thai thứ 39 hoặc 40. (See “Cesarean delivery on maternal request”.)
Mổ lấy thai nhẹ nhàng, tự nhiên hoặc lấy gia đình làm trung tâm – Phương pháp mổ lấy thai tự nhiên, nhẹ nhàng, hoặc lấy gia đình làm trung tâm được phát triển để cải thiện trải nghiệm sinh của phụ nữ sinh mổ không biến chứng, cố gắng tái tạo lại các đặc điểm của quá trình sinh ngả âm đạo càng nhiều càng tốt để làm cho phẫu thuật lấy thai trở nên thân thiện hơn với gia đình. Các thành phần của phương pháp này có thể bao gồm [ 26,27]:
- Phát nhạc nền do mẹ và bố lựa chọn trong khi mổ lấy thai và giảm cường độ ánh sáng khi có thể an toàn. Giảm tiếng ồn từ bên ngoài.
- Sử dụng săng trong suốt hoặc trải săng để cho phép mẹ (và bố) theo dõi quá trình mổ lấy thai.
- Tránh dùng thuốc an thần cho mẹ.
- Cho phép sinh thai bằng cách kết hợp sổ thai từ tử cung với sự hỗ trợ tích cực của bác sĩ để giống với quá trình sổ thai từ âm đạo.
- Giải phóng bàn tay thuận / cánh tay và ngực / bầu vú của mẹ khởi các dây truyền và máy theo dõi, khi có thể để cô ấy có thể bế và cho con bú.
- Thúc đẩy da kề da và cho con bú ngay sau sinh.
Chúng tôi thực hiện mổ lấy thai lấy gia đình làm trung tâm bất cứ khi nào có thể (tức là thường quy trừ khi cần mổ lấy thai cấp cứu). Bệnh nhân trở thành một phần tích cực của quá trình mổ lấy thai bằng cách quan sát trực tiếp quá trình sinh và cắt dây rốn. Trong một thử nghiệm ngẫu nhiên, mổ lấy thai lấy gia đình làm trung tâm thì an toàn cho cả mẹ và trẻ và dẫn đến trải nghiệm sinh con tốt hơn, tỷ lệ bú mẹ cao hơn và cải thiện sự tương tác sớm giữa mẹ và trẻ [ 28].
Mổ lấy thai sau khi khỏi phát chuyển dạ – Mổ lấy thai sau khi khởi phát chuyển dạ đôi khi được phân loại theo mức độ khẩn cấp; ví dụ: (1) đe dọa tính mạng của mẹ hoặc thai nhi ngay lập tức, (2) có dấu hiệu tổn thương thai nhi hoặc mẹ nhưng không đe dọa tính mạng ngay lập tức, hoặc (3) sinh thai là cần thiết, nhưng không có bằng chứng tổn thương mẹ hoặc thai nhi. So với sinh mổ theo kế hoạch, mổ lấy thai sau khi khỏi phát chuyển dạ có liên quan đến sự gia tăng nguy cơ chảy máu sau sinh, các biến chứng gây mê do sử dụng nhanh gây mê toàn thân và vô tình làm tổn thương thai nhi hoặc các tạng ở vùng bùng-chậu.
Mặc dù trước đây, các cơ sở y tế cung cấp dịch vụ sản khoa được yêu cầu có khả năng bắt đầu mổ lấy thai trong vòng 30 phút sau khi quyết định thực hiện sinh mổ, nhưng tiêu chí này dựa trên những hạn chế thực tế mà hầu hết các bệnh viện ở vùng nông thôn gặp phải trong việc tập hợp đội ngũ điều dưỡng, bác sĩ gây mê và bác sĩ phẫu thuật phù họp. Ngưỡng thời gian này không dựa trên bằng chứng, không thể đạt được trên toàn cầu hoặc lý tưởng hóa từ quan điểm giảm tỷ lệ tử vong và bệnh tật chu sinh [ 29-38Ị. Khả năng bắt đầu mổ lấy thai sau khi khởi phát chuyển dạ trong vòng 30 phút sau khi quyết định sinh mổ là một tiêu chuẩn họp lý để theo dõi chất lượng của đơn vị chuyển dạ và sinh nhưng không phải là yêu cầu bắt buộc đối với tất cả các ca mổ lấy thai phải được thực hiện trong vòng 30 phút sau khi quyết định. Trong các nghiên cứu trên người và động vật, tình trạng không có oxy hoàn toàn đột ngột, như xảy ra với đứt hoàn toàn hoặc tắc hoàn toàn dây rốn, có thể cần phải sinh trong vòng năm phút để tránh tổn thương thai nhi do thiếu oxy [ 39-41], mặc dù những người sống sót không hề bị tổn thương đã được báo cáo sau thời gian dài hơn bị thiếu oxy nặng. Hầu hết các thai kỳ có tổn thương thai nhi hoặc mẹ ít nghiêm trọng hơn hoặc phục hồi một phần hoặc hoàn toàn các biểu đồ nhịp tim thai không an toàn sẽ có kết cục tốt mặc dù đã trải qua khoảng thời gian dài hơn trước khi bắt đầu phẫu thuật [ 381.
5. Chuẩn bị mẹ trước phẫu thuật
Làm sạch da – Chúng tôi không yêu cầu bệnh nhân sử dụng bất kỳ sản phẩm cụ thể nào để làm sạch da trước khi phẫu thuật. Các phân tích gộp của các thử nghiệm ngẫu nhiên về việc tắm bồn hoặc dưới vòi hoa sen trước khi phẫu thuật với chlorhexidinehoặc các sản phẩm khác trước một loạt các thủ thuật ngoại khoa không cho thấy giảm tỷ lệ nhiễm trùng vết mổ rõ rệt [ 42-44].
Tư vấn gây mê – Như với bất kỳ thủ thuật ngoại khoa nào, phụ nữ mổ lấy thai nến được tư vấn trước phẫu thuật với đội ngũ gây mê. Những người có nguy cơ liên quan đến thủ thuật trên mức nền nên có một buổi tư vấn trước khi nhập viện, nếu có thể. Các đặc điểm khiến bệnh nhân gia tăng nguy cơ bao gồm, nhung không giới hạn ở nhũng đặc điểm được liệt kê trong bảng (table 1).
Lựa chọn gây tê vùng hay gây mê toàn thân bị ảnh hưởng bởi các yếu tố như mức độ khẩn cấp của thủ thuật, tình trạng sản phụ, sở thích của bác sĩ và bệnh nhân. Các vấn đề liên quan đến gây mê để mổ lấy thai, bao gồm thuốc tiền mê (ví dụ: thuốc kháng acid, thuốc đối kháng thụ thể histamine H2) và chế độ ăn uống, được thảo luận chi tiết ở chủ đề riêng. (See “Anesthesia for cesarean delivery”.)
Xét nghiệm cận lâm sàng – Định lượng huyết sắc tố hoặc hematocrit nền được khuyến cáo cho những bệnh nhân thực hiện một cuộc phẫu thuật lớn, như mổ lấy thai, dự kiến sẽ dẫn đến mất máu đáng kể. Giá trị bình thường thu được trong vòng một tháng sau phẫu thuật có thể không cần phải lặp lại trước phẫu ở những thai kỳ không có biến chứng. (See “Preoperative medical evaluation of the healthy adult patient”.)
Phụ nữ mang thai thường được kiểm tra nhóm máu và kháng thể nhóm máu như một phần của chăm sóc tiền sản thường quy. Mặc dù bỏ qua việc kiểm tra lại nhóm máu và kháng thể trước phẫu thuật có thể là an toàn ở những phụ nữ có nguy cơ thấp chảy máu nặng trong phẫu thuật và những người không có kháng thể hồng cầu đã biết [ 45-49], chúng tôi thực hiện xét nghiệm này thường quy ở mọi phụ nữ trước phẫu thuật, hoặc bệnh nhân ngoại trú trong vòng ba ngày kể từ ngày mổ đã được lên kế hoạch hoặc vào buổi sáng ngày nhập viện. Ngoài ra, bác sĩ phẫu thuật có thể xem xét chỉ định “lấy sẵn máu để trong ống chống đông” ở những bệnh nhân có nguy cơ thấp: Máu được lấy và chống đông, nhưng không thực hiện xét nghiệm nào trừ khi có chỉ định lâm sàng.
Khoảng 2% phụ nữ mổ lấy thai lần đầu được truyền máu [ 47]. Nguy cơ < 1% ở những phụ nữ có nguy cơ chảy máu thấp. Các yếu tố nguy cơ cần truyền máu bao gồm các bất thường nhau thai (ví dụ, nhau tiền đạo, phổ nhau cài răng lược, hoặc nhau bong non), sản giật hoặc huyết, xét nghiệm chức năng gan cao, tiểu cầu thấp), hematocrit trước phẫu thuật < 25%, sử dụng gây mê toàn thân , và tiền sử mổ lấy thai > 5 lần.
5.1 Dự phòng kháng sinh
Phác đồ – Đối với tất cả phụ nữ mổ lấy thai, chúng tôi dùng một liều cefazolinduy nhất trong vòng 60 phút trước khi rạch da và thêm một liều azithromycin 500 mg duy nhất tiêm tĩnh mạch cho nhũng người đang chuyển dạ hoặc vỡ ối.
Liều lượng cefazolincủa chúng tôi như sau:
- Phụ nữ < 120 kg – 2 g tiêm tĩnh mạch
- Phụ nữ > 120 kg – 3 g tiêm tĩnh mạch
Chúng tôi cũng dùng các chế phẩm sát trùng vùng bụng và âm đạo. (See ‘Skin preparation’below and ‘Vaginal preparation’below.)
American College of Obstetricians and Gynecologists (ACOG) cũng khuyến cáo một liều cephalosporin thế hệ 1 duy nhất; tuy nhiên, phác đồ liều của họ thấp hơn ( cefazolin1 g IV đối với phụ nữ < 80 kg, 2 g đối với phụ nữ > 80 kg, và 3 g đối với phụ nữ > 120 kg) Ị 50 Ị.
Bằng chứng – Trong trường hợp không dự phòng kháng sinh, phụ nữ mổ lấy thai có nguy cơ nhiễm trùng cao hơn từ 5 đến 20 lần so với phụ nữ sinh ngả âm đạo [ 51]. Lợi ích của việc dự phòng kháng sinh trước khi mổ lấy thai được minh họa trong một tổng quan hệ thống các thử nghiệm ngẫu nhiên so sánh kết cục của mẹ “có” so với “không” sử dụng kháng sinh dự phòng và nhận thấy rằng dự phòng kháng sinh làm giảm khoảng 60% nguy cơ viêm nội mạc tử cung ở cả mổ lấy thai trước chuyển dạ và sau khi khởi phát chuyển dạ (95 thử nghiệm, n > 15.000 phụ nữ) [ 51]. Các nguy cơ nhiễm trùng vết mổ, nhiễm trùng đường tiết niệu và các biến chúng nhiễm trùng mẹ nghiêm trọng cũng giảm. Trong một tổng quan hệ thống nhỏ hon đánh giá kết cục sơ sinh (12 thử nghiệm, n > 5000 phụ nữ), dự phòng kháng sinh cho mẹ không ảnh hưởng đáng kể đến nguy cơ nhiễm trùng sơ sinh (risk ratio [RR] 0,76, CI 95% 0,51-1,13) hoặc nhiễm khuẩn huyết sơ sinh với vi khuẩn kháng kháng sinh (RR 0,70, CI 95% 0,32-4,14), nhung cần thêm dữ liệu để xác nhận những phát hiện này [ 52 ].
Mặc dù làm giảm nguy cơ tương đối nhiễm trùng ở mẹ có ý nghĩa thống kê và tương tự đối với cả thủ thuật trước khi chuyển dạ và sau khi khởi phát chuyển dạ, nguy cơ tuyệt đối nhiễm trùng ở mẹ là khá thấp trong các trường hợp trước khi chuyển dạ: Ở một nghiên cún quan sát lớn, viêm nội mạc tử cung sau sinh xảy ra ở 2% phụ nữ được dự phòng kháng sinh so với 2,6% không dùng kháng sinh dự phòng; nhiễm trùng vết mổ xảy ra ở 0,52% phụ nữ được dự phòng bằng kháng sinh so với 0,96% không được dự phòng kháng sinh [ 53]. Như vậy, 1000 phụ nữ mổ lấy thai trước khi chuyển dạ sẽ được dùng kháng sinh để ngăn ngừa 6 trường họp viêm nội mạc tử cung và 4,4 trường họp nhiễm trùng vết mổ ở bụng. Nguy cơ nhiễm trùng mẹ thấp trong những trường họp này và sự không chắc chắn về ảnh hưởng lâu dài đến con cái đã thúc đẩy một yêu cầu nghiên cứu thêm về nhũng nguy cơ tiềm ẩn lâu dài khi phơi nhiễm với kháng sinh dự phòng và các chiến lược phân tầng nguy cơ xác định các đối tượng thích họp nhất để dự phòng kháng sinh [ 54]. Cho đến khi có những dữ liệu này, chúng tôi dùng kháng sinh trước tất cả các ca mổ lấy thai, theo hướng dẫn của ACOG [ 50 1.
Liệu pháp kháng sinh nên được dùng trong vòng 60 phút trước khi rạch da để đảm bảo nồng độ thuốc trong mô thỏa đáng [ 50]. Khuyến cáo này được hỗ trợ bởi một phân tích gộp năm 2014 về các thử nghiệm ngẫu nhiên so sánh tỷ lệ nhiễm trùng ở những phụ nữ được chỉ định dùng một liều kháng sinh duy nhất trước khi rạch da so với những người được chỉ định dùng sau khi kẹp rốn [ 52]. Dự phòng trước khi rạch da hiệu quả hơn đáng kể so với việc dùng muộn để phòng ngừa viêm nội mạc tử cung (RR 0,54, CI 95% 0,36-0,79) và không liên quan đến sự gia tăng nhiễm khuẩn huyết sơ sinh đã được chứng minh, các xét nghiệm nhiễm khuẩn huyết hoặc nhập viện vào đơn vị chăm sóc đặc biệt trẻ sơ sinh, mặc dù các thử nghiệm có khả năng hạn chế trong việc phát hiện các ảnh hưởng bất lợi ở trẻ sơ sinh. (See “Antimicrobial prophylaxis for prevention of surgical site infection in adults”, section on ‘Timing’.)
Các thử nghiệm so sánh không cung cấp bằng chứng mạnh để làm căn cứ đưa ra khuyến cáo về loại thuốc và liều lượng tối ưu. Dựa trên ý kiến từ các chuyên gia về bệnh truyền nhiễm, chúng tôi dùng cefazolin, với liều lượng dựa trên cân nặng [ 55]. Liều lượng cao hơn đối với phụ nữ béo phì dựa trên dữ liệu dược động học thay vì tỷ lệ nhiễm trùng vết mổ, và những dữ liệu này không nhất quán [ 56-60]. Cefazolin có thời gian bán thải dài hơn ampicillin(1,8 so với 0,7 đến 1,5 giờ ở người lớn có chức năng thận bình thường [ 61]), đó là một lợi thế ở các ca phẫu thuật dài. Tuy nhiên, ở một tổng quan hệ thống năm 2014 về các thử nghiệm ngẫu nhiên, cefazolin và ampicillin dường như có hiệu quả tương tự để ngăn ngừa nhiễm trùng ở mẹ sau phẫu thuật (viêm nội mạc tử cung, nhiễm trùng vết mổ) sau khi mổ lấy thai [ 62]. Các tổng quan hệ thống khác về các thử nghiệm ngẫu nhiên đã ghi nhận rằng một liều kháng sinh duy nhất có hiệu quả tương đương với nhiều liều [ 63,64].
Dữ liệu gần đây ủng hộ việc sử dụng phối hợp kháng sinh phổ rộng cho những phụ nữ có nguy cơ cao nhiễm trùng sau mổ lấy thai [ 65-67].Ở một thử nghiệm ngẫu nhiên đa trung
tâm có đối chứng – giả dược bao gồm hơn 2000 phụ nữ, sử dụng azithromycin 500 mg tiêm tĩnh mạch trước khi rạch da cùng với cefazolintrước khi phẫu thuật dẫn đến giảm 50% kết cục tổng hợp của viêm nội mạc tử cung, nhiễm trùng vết mổ hoặc nhiễm trùng khác (viêm nội mạc tử cung 3,8 so với 6,1%, nhiễm trùng vết mổ 2,4 so với 6,6%; RR tổng hợp 0,51, CI 95% 0,38-0,68), mà không ảnh hưởng đến tần suất của các kết cục sơ sinh bất lợi [ 66]. Các tác giả cũng nhận thấy rằng dự phòng bổ trợ với azithromycin có hiệu quả về mặt chi phí [ 68]. Lưu ý, chỉ những phụ nữ mổ lấy thai trong khi chuyển dạ hoặc ít nhất bốn giờ sau khi vỡ ối mới được tuyển chọn vào thử nghiệm, vì vậy những dữ liệu này không áp dụng cho các ca mổ lấy thai khác (ví dụ, các ca mổ lấy thai trước khi chuyển dạ với các màng còn nguyên vẹn). Các xét nghiệm đặc hiệu đối với các loài ưreaplasma hoặc Mycoplasmakhông được thực hiện thường quy, do đó không biết liệu sự bao phủ chống lại các loài ưreaplasma và Mycoplasmađược cung cấp bởi phác đồ kháng sinh phổ rộng có làm giảm nhiễm trùng sau phẫu thuật hay không.
Tốt nhất, azithromycin được truyền 60 phút trước khi rạch da, nhưng điều này có thể không khả thi đối với mổ lấy thai sau khi khởi phát chuyển dạ. Ở thử nghiệm này, thuốc dường như có hiệu quả bất kể thời điểm dùng; 83% bệnh nhân nhận azithromycin từ 0 đến 60 phút trước khi rạch da, 5% nhận azithromycin > 60 phút trước khi rạch da, và 12% nhận sau khi rạch da [ 66 ].
Cho đến nay, thử nghiệm này cung cấp bằng chứng tốt nhất về lợi ích của phác đồ phổ rộng và đã khiến chúng tôi bắt đầu sử dụng cefazolinCỘNG azithromycin cho các ca mổ lấy thai sau khi khởi phát chuyển dạ, các ca mổ lấy thai ở phụ nữ bị vỡ ối. Một số bác sĩ lâm sàng cũng sử dụng kết họp này ở những phụ nữ khác có nguy cơ cao bị nhiễm trùng vết mổ sau phẫu thuật. Tuy nhiên, chúng tôi tin rằng một khuyến cáo mạnh ủng hộ việc sử dụng dự phòng kháng sinh phổ rộng thường quy hoặc phổ rộng hon là không có cơ sở tại thời điểm này, do tỷ lệ béo phì cao ở ít nhất một trong số các quần thể thử nghiệm (> 70% [ 66]), thiếu dữ liệu so sánh về hiệu quả của cefazolin liều cao (3 g) trong việc ngăn ngừa nhiễm trùng vết mổ ở phụ nữ béo phì mổ lấy thai, thiếu dữ liệu vi sinh vật trong các thử nghiệm này, lo ngại về việc gây kháng kháng sinh azithromycin, và lo ngại về những ảnh hưởng có thể có đối với việc hình thành hệ vi sinh vật đường ruột bản địa [ 69-72]. ACOG tuyên bố rằng azithromycin có thể được xem xét trong trường họp mổ lấy thai không có kế hoạch r 50 Ị.
Theo truyền thống, điều trị dự phòng sau sinh không được tiếp tục vì các nghiên cứu ở các quần thể phẫu thuật chung cho thấy không có lợi ích từ việc dự phòng kháng sinh sau phẫu thuật. Tuy nhiên, một thử nghiệm ở phụ nữ béo phì mổ lấy thai báo cáo lợi ích của việc dự phòng kháng sinh trong 48 giờ sau mổ lấy thai khi được sử dụng cùng với dự phòng trước phẫu thuật. (See “Cesarean delivery of the obese woman1*, section on ‘Antibiotic prophylaxis’.)
5.2 Các quần thế đặc biệt
Phụ nữ dị ứng vói penicillin – Những phụ nữ này được chia thành hai nhóm: những người có phản ứng nghiêm trọng trước đó và những người có nguy cơ thấp bị phản ứng nghiêm trọng.
- Đối với nhũng phụ nữ có tiền sử dị ứng nghiêm trọng vói penicillin thực hiện mổ lấy thai trước khi chuyển dạ với các màng còn nguyên vẹn, chúng tôi đề nghị liệu pháp kết họp với một liều duy nhất [ 50,55]:
- Clindamycin900 mg tiêm tĩnh mạch CỘNG
- Gentamicin5 mg/kg tiêm tĩnh mạch
Nếu mổ lấy thai được thực hiện sau khi chuyển dạ hoặc sau khi vỡ ối, chúng tôi bổ sung azithromycin 500 mg tiêm tĩnh mạch.
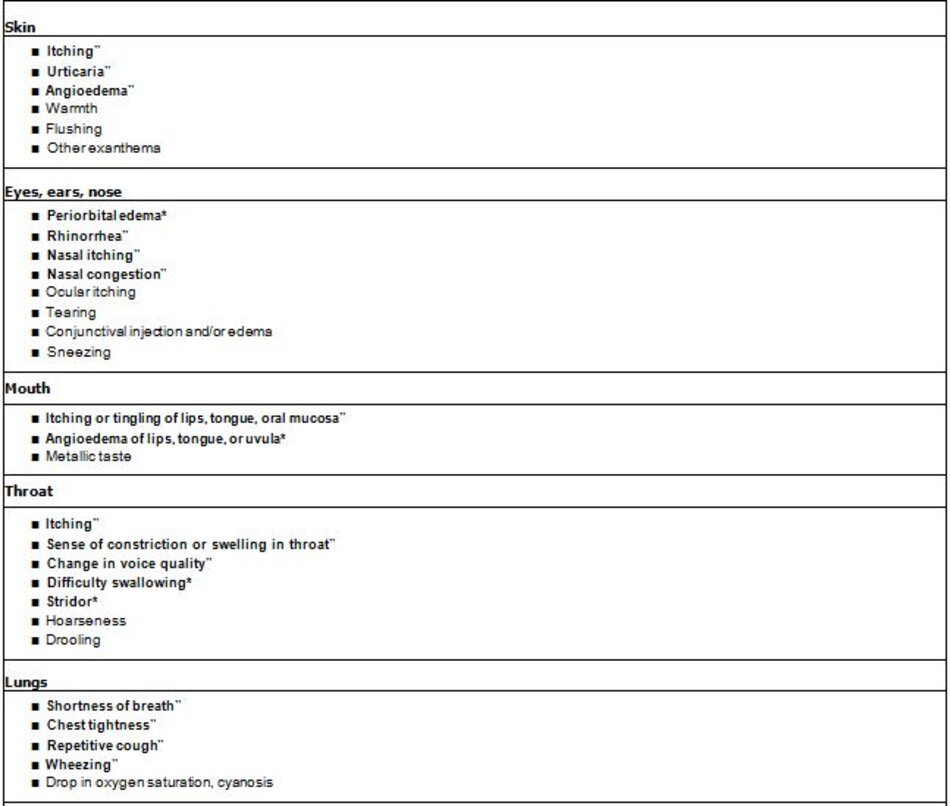
Các dạng dị ứng penicillin nghiêm trọng bao gồm các phản ứng tức thì (tức là phản vệ) ( bàng 2 ), cũng như một số dạng phản ứng chậm (hội chứng Stevens-Johnson [SJS], hoại tử biểu bì nhiễm độc [TEN], phát ban do thuốc với tăng bạch cầu ái toan và nhiều triệu chứng toàn thân [DRESS], tổn thương gan hoặc các cơ quan khác do thuốc và giảm 3 dòng tế bào do thuốc).
Khi gentamicinđược sử dụng để dự phòng kết họp với kháng sinh đường tiêm có hoạt tính chống lại các tác nhân kỵ khí, chúng tôi khuyến nghị dùng gentamicin 4,5 đến 5 mg/kg như một liều duy nhất vì nhiều nghiên cứu ủng hộ tính an toàn và hiệu quả của liều này khi được sử dụng như một liều duy nhất để dự phòng ở bệnh nhân không bị suy thận. Ngoài ra, một thử nghiệm dự phòng kháng sinh trong phẫu thuật đại trực tràng báo cáo rằng liều này có thể hiệu quả hơn nhiều liều tiêu chuẩn 1,5 mg/kg trong các ca phẫu thuật kéo dài [ 731. Tuy nhiên, mổ lấy thai thường mất ít hơn một giờ; do đó, một liều gentamicin thấp hơn có thể là đủ; khồng có thử nghiệm nào so sánh liều lượng ở quần này. Dùng gentamicin liều đơn hàng ngày dường như không liên quan đến độc tính trên thận hoặc thính giác ở trẻ sơ sinh cao hơn so với nhiều liều hàng ngày [ 74 ]
Đối với những phụ nữ có nguy CO’ thấp bị phản ứng dị ứng tức thì nghiêm trọng, có thể dùng cefazolin, như đã mô tả ở trên (see ‘Regimen*above) Nguy cơ bệnh nhân dị úng với penicilin phản ứng với cephalosporin có thể được đánh giá dựa trên kết quả test da penicilin (nếu có), các đặc điểm lâm sàng của phản ứng với penicilin và thời gian trôi qua kể từ lần phản úng cuối cùng với penicilin ( algorithm 1). Nếu mổ lấy thai được thực hiện sau khi khởi phát chuyển dạ hoặc sau khi vỡ ối, chúng tôi thêm azithromycin 500 mg tiêm tĩnh mạch. (See “Allergy evaluation for immediate penicillin allergy: Skin test-based diagnostic strategies and cross-reactivity with other beta-lactam antibiotics”and “Penicillin allergy: Immediate reactions”.)
Người phụ nữ đang dùng kháng sinh – Không có thử nghiệm ngẫu nhiên nào đánh giá hiệu quả của phác đồ kháng sinh trong các tình huống lâm sàng này.
- Phụ nữ đang dùng kháng sinh dự phòng GBS – Khi mổ lấy thai được thực hiện ở phụ nữ đang chuyển dạ hoặc bị vỡ ối đang dùng penicillin Gđể dự phòng Liên cầu khuẩn nhóm B (GBS) cho trẻ sơ sinh chúng tôi không thêm cephalosporin hoặc chuyển sang ampicillinđể dự phòng phẫu thuật, nhưng chúng tôi thêm một liều azithromycin. Ngoài ra, một số bác sĩ lâm sàng thêm một liều kháng sinh phổ hẹp duy nhất (ví dụ: cefazolin) cũng như một liều azithromycin vào phác đồ penicillin G để dự phòng GBS.
- Phụ nữ bị viêm màng đệm-màng ối – Ampicillincộng gentamicinlà một phác đồ phổ biến để điều trị viêm màng đệm-màng ối. Đối với những phụ nữ đang dùng phác đồ này, chúng tôi cũng dùng một liều clindamycin 900 mg hoặc metronidazole500 mg trước khi bắt đầu mổ lấy thai. Chúng tôi không dùng azithromycin đối với những bệnh nhân này.
Sau sinh, có thể là hợp lý-để tiếp tục ampicillinkết họp với gentamicinhoặc chuyển sang ampicilĩin-sulbactamcho đến khi bệnh nhân hết sốt trong ít nhất 24 giờ. Sự đề kháng của Bacteroides với clindamycin ngày càng tăng, do đó, ở những nơi có tỷ lệ kháng thuốc cao, ampicillin-sulbactam được ưu tiên. (Xem “Nhiễm trùng trong buồng trứng (viêm màng đệm lâm sàng hoặc viêm màng mạch ba độ I)”, phần ‘Điều trị sau sinh’.)
Phẫu thuật kéo dài hoặc mất máu quá mức – Nồng độ kháng sinh giảm theo thời gian và với mất máu. Mặc dù bổ sung liều là tiêu chuẩn chăm sóc ở các phẫu thuật khác, nhưng không có dữ liệu cụ thể đối với mổ lấy thai [ 75]. Một liều cefazolinthứ hai có thể là họp lý ở bệnh nhân chảy máu sau sinh > 1500 mL [ 50]. Liều cefazolin thứ hai cũng thích họp đối với trường hợp mổ lấy thai phức tạp hiếm gặp kéo dài hơn 4 giờ vì thời gian bán thải của cefazolin và azithromycintương ứng là khoảng 1,8 và 68,0 giờ.
Hướng dẫn chung của American Society of Health-System Pharmacists, the Infectious Diseases Society of America, the Surgical Infection Society, and the Society for Healthcare Epidemiology of America đề nghị xem xét liều bổ sung trong phẫu thuật ở những bệnh nhân mất máu quá mức (> 1500 mL) hoặc phẫu thuật kéo dài (thời gian phẫu thuật > hai lần thời gian bán hủy của thuốc) [ 55,76].
Sự CU’ trú của Tụ cầu vàng kháng methicillin ỏ’ mũi – Sàng lọc thường quy MRSA không được chỉ định. Quản lý những phụ nữ đã biết đến sự cư trú của chúng (bổ sung một liều vancomycin duy nhất ) được thảo luận ở chủ đề riêng. (See “Intraamniotic infection (clinical chorioamnỉonitis or triple I)”, section on ‘Postpartum treatment’.)
5.3 Dự phòng thuyên tắc huyết khối
Nguy CO’ thuyên tắc huyết khối tĩnh mạch và thuyên tắc phổi – Một nghiên cún sử dụng dữ liệu hành chính từ 1,7 triệu trường hợp mang thai báo cáo rằng tần suất xảy ra biến cố huyết khối (đột quỵ thiếu máu não cục bộ, nhồi máu cơ tim cấp, thuyên tắc huyết khối tĩnh mạch) là 246 trên 100.000 ca mổ lấy thai trong sáu tuần đầu sau sinh [ 77]. Tỷ lệ này cao hơn 20 lần so với tỷ lệ một năm sau đó và cao hơn đáng kể so với tỷ lệ sau sinh ngả âm đạo (165 trên 100.000). So với sinh ngả âm đạo, một phân tích gộp phát hiện tỷ số chênh của thuyên tắc huyết khối tĩnh mạch (VTE) (huyết khối tĩnh mạch sâu và / hoặc thuyên tắc phổi) sau mổ lấy thai chủ động và cấp cứu lần lượt là OR 2,3 và 3,6, và tỷ lệ mắc VTE gộp chung là 260 trên 100.000 ca mổ lấy thai [ 78]. Một nghiên cứu tiến cứu lớn báo cáo tỷ lệ VTE thậm chí còn thấp hơn: 63/100.000 ca mổ lấy thai lặp lại theo kế hoạch và 84/100.000 ca mổ lấy thai cấp cứu [ 79]. Mặc dù thuyên tắc phổi là nguyên nhân phổ biến gây tử vong mẹ [ 80 ] và hơn 80% trường hợp thuyên tắc phổi hậu sản tử vong xảy ra sau mổ lấy thai [ 81], những dữ liệu này gợi ý rằng mức độ nguy cơ tuyệt đối của các biến cố quan trọng trên lâm sàng là nhỏ và tương tự như ở những bệnh nhân phẫu thuật có nguy cơ rất thấp, những người không được khuyến cáo dự phòng huyết khối thường quy (ngoài đi lại sớm). (See “Antimicrobial prophylaxis for prevention of surgical site infection in adults”, section on ‘Role of vancomycin’.)
Cách tiếp cận của chúng tôi – Giá trị của dự phòng huyết khối đối với mổ lấy thai chưa được nghiên cứu trong các thử nghiệm ngẫu nhiên đủ mạnh để đánh giá cả lợi ích và tác hại [ 82,83]. Các hướng dẫn quốc tế về dự phòng huyết khối sau mổ lấy thai khác nhau rõ rệt trong việc lựa chọn bệnh nhân cho liệu pháp này vì cả ngưỡng tối ưu để bắt đầu dự phòng huyết khối bằng thuốc và thời gian điều trị tối ưu đều không rõ ràng [ 84]. Hơn nữa, không có công cụ được phê chuẩn, dễ sử dụng nào để xác định chính xác nguy cơ tuyệt đối của VTE sau sinh ở một bệnh nhân riêng biệt, mặc dù các nghiên cứu thí điểm về các công cụ này đã được báo cáo [ 85,86]. Khó phê chuẩn trên lâm sàng do tỷ lệ mắc VTE tương đối thấp.
Đây là cách tiếp cận của chúng tôi:
- Phụ nữ có nguy cơ thấp – Chúng tôi đồng thuận với khuyến cáo của ACOG r 87 Ị:
- Đeo một máy bơm hơi áp lực cho tất cả các bệnh nhân chưa được nhận dự phòng huyết khối bằng thuốc trước khi mổ lấy thai
- Khuyến khích đi lại sớm sau mổ lấy thai
Chúng tôi tiếp tục dùng máy bơm hơi áp lực cho đến khi bệnh nhân đi lại hoàn toàn [ 88]. Các máy bơm hơi áp lực có thể được loại bỏ trong khi bệnh nhân đang đi lại nhưng nên đeo trở lại khi cô ấy trở lại tư thế ngồi hoặc nằm ngửa. Các nghiên cứu quan sát ở phụ nữ mang thai gợi ý rằng các máy bơm hơi áp lực, cũng như các loại tất áp lực phân đoạn, là an toàn và hiệu quả [ 89,90].
- Phụ nữ có nguy CO’ cao – Phù hợp với các khuyến cáo của ACOG [ 87 Ị:
- Chúng tôi sử dụng cả biện pháp dự phòng huyết khối cơ học và bằng thuốc ở những phụ nữ có nguy cơ cao bị VTE sau mổ lấy thai
- Chúng tôi khuyến khích đi lại sớm sau mổ lấy thai, sớm nhất là tám giờ sau phẫu thuật Tiêu chí lựa chọn phụ nữ có nguy cơ cao đang gặp nhiều thách thức do không có dữ liệu chất lượng cao [ 91]. Chúng tôi xem xét bất kỳ tiêu chí hợp lý nào sau đây để dự phòng cơ học cộng với dự phòng bằng thuốc:
- VTE trước đó .
- Bất kỳ thrombophilia (di truyền hoặc mắc phải).
- Chỉ số khối cơ thể (BMI) >35 kg/m2.
- > 2 yếu tố nguy cơ ít nổi bật hơn đối với VTE – Rất nhiều yếu tố nguy cơ ít nổi bật hơn đối với VTE được mô tả trong y văn (ví dụ: băng huyết hoặc nhiễm trùng sau sinh, các yếu tố y tế hoặc các biến chứng thai kỳ như béo phì, tăng huyết áp, bệnh tự miễn, bệnh tim, bệnh hồng cầu hình liềm, đa thai, tiền sản giật); Các yếu tố nguy cơ theo ACCP và RCOG được mô tả bên dưới [ 92-103] (see ACCP recommendations’below and ‘RCOG recommendations’below). Loại và số lượng các yếu tố nguy cơ ít nồi bật đáp ứng ngưỡng dùng thuốc dự phòng huyết khối được quyết định trên cơ sở từng ca bệnh
Thò’i điếm điều trị dự phòng bằng thuốc – Bắt đầu dự phòng bằng thuốc từ 6 đến 12 giờ sau phẫu thuật, sau khi mối lo ngại về chảy máu đã giảm và được tiếp tục cho đến bệnh nhân đi lại hoàn toàn, ngoại trừ những phụ nữ có các yếu tố nguy cơ đáng kể đối với VTE sau sinh (ví dụ: VTE trước đó, không bị VTE trước đó nhưng có nguy cơ thrombophilia cao): Những phụ nữ này nên được điều trị dự phòng huyết khối trong sáu tuần, và tùy thuộc vào tiền sử bệnh của họ, có thể cần dùng thuốc chống đông vô thời hạn. (See “Use of anticoagulants during pregnancy and postpartum”, section on’Duration of postpartum anticoagulation’and “Rationale and indications for indefinite anticoagulation in patients with venous thromboembolism”and “Antiphospholipid syndrome: Pregnancy implications and management in pregnant women”and “Inherited thrombophilias in pregnancy”.)
Society for Obstetric Anesthesia and Perinatology đề nghị trì hoãn khởi trị chống đông bằng heparin trọng lượng phân tử thấp ít nhất 24 giờ sau khi bắt đầu phong bế thần kinh và 4 giờ sau khi rút ống thông, và sử dụng heparin tiêm tĩnh mạch nếu muốn thuốc chống đông có tác dụng điều trị sớm hơn sau khi sinh [ 104] (see “Neuraxial anesthesia/analgesia techniques in the patient receiving anticoagulant or antiplatelet medication”). Không có dữ liệu từ các thử nghiệm ngẫu nhiên để ủng hộ hoặc bác bở các cách tiếp cận này.
Nên để các máy bơm hơi áp lực tại chỗ cho đến khi bắt đầu điều trị dự phòng bằng thuốc. Chúng tôi thường tiếp tục dùng máy bơm hơi áp lực cho đến khi bệnh nhân được xuất viện vì nó có thể mang lại thêm lợi ích cho bệnh nhân phẫu thuật đang dùng heparin. (See “Prevention of venous thromboembolic disease in adult nonorthopedic surgical patients”.)
Liều lượng heparin – Có thể dùng heparin không phân đoạn hoặc trọng lượng phân tủ’ thấp.
- Đối với phụ nữ có BMI < 40 kg/m2, các lựa chọn bao gồm:
– Enoxaparin40 mg tiêm dưới da hàng ngày (đây là lựa chọn ưu tiên của chúng tôi), hoặc
– Heparin không phân đoạn5000 đơn vị tiêm dưới da mỗi 12 giờ - Đối với phụ nữ béo phì nặng (BMI > 40 kg/m2):
– Chúng tôi uu tiên dùng enoxaparindựa trên cân nặng hơn là dùng liều cố định [ 105-107]: Bắt đầu enoxaparin 0,5 mg/kg tiêm dưới da mỗi 12 giờ, và tăng liều khi cần để đạt được nồng độ anti-factor Xa từ 0,1 đến 0,5 IƯ/mL. Liều duy nhất tối đa không > 100 mg.
– Nếu sử dụng heparin không phân đoạn, chúng tôi đề nghị tiêm dưới da 5000 đơn vị mỗi 8 giờ.
Những bệnh nhân cần dùng thuốc chống đông kéo dài có thể được chuyển sang thuốc Uống (ví dụ: warfarin[có thể dùng cho phụ nữ đang cho con bú] hoặc thuốc chống đông trực tiếp đường uống [không nên dùng nếu đang cho con bú]). (See “Use of anticoagulants during pregnancy and postpartum”,section on ‘Postpartum and breastfeeding*.)
5.4 Khuyến cáo của các hiệp hội khác
Khuyến cáo của ACCP – Đây là bản tóm tắt một phần hướng dẫn cùa ACCPnăm 2012 về liệu pháp chống huyết khối và phỏng ngừa huyết khối trong thai kỳ[ 92 ]:
- Đối với những phụ nữ chỉ có một yếu tố nguy cơ của VTE là mang thai và mổ lấy thai, ACCP chỉ khuyến cáo đi lại sớm sau sinh.
- Đối với những phụ nữ mổ lấy thai có thêm một yếu tố nguy cơ chính của VTE hoặc ít nhất hai yếu tố nguy cơ phụ khác của VTE, ACCP khuyến cáo dự phòng huyết khối bằng thuốc trong thời gian đang nằm viện sau khi sinh. Nếu chống chỉ định dùng thuốc chống đông, khuyến cáo dùng tất áp lực phân đoạn hoặc máy bơm hơi áp lực.
- Đối với những phụ nữ mổ lấy thai có nguy cơ VTE rất cao và có thêm nhiều yếu tố nguy cơ khác của VTE mà vẫn tồn tại dai dẳng trong thời kỳ hậu sản, ACCP khuyến cáo dự phòng bằng thuốc CỘNG tất áp lực phân đoạn và / hoặc máy bơm hơi áp lực trong thời gian đang nằm viện sau khi sinh
- Đối với một số phụ nữ có nguy cơ cao với các yếu tố nguy cơ đáng kể vẫn tồn tại sau khi sinh, ACCP đề nghị kéo dài thời gian dự phòng bằng thuốc lên đến 6 tuần sau sinh sau khi xuất viện.
Năm 2016, một số tác giả của ACCP đã sửa đổi tiêu chí yếu tố nguy cơ ban đầu [ 108] .
Hướng dẫn gần đây nhất của họ về phòng ngừa VTE sau mổ lấy thai tuyên bố:
Nên dự phòng sau mổ lấy thai đối với nhũng phụ nữ có các yếu tố nguy cơ sau:
- Có > 1 các yếu tố nguy cơ sau: VTE trước đó, tiền sử bất động trước khi sinh (nằm liệt giường ít nhất 1 tuần), nhiễm trùng đáng kể sau sinh, băng huyết sau sinh >1000 mL cần mổ lại, tiền sản giật với thai chậm tăng trưởng, các bệnh nội khoa đồng mắc đáng kể (lupus ban đỏ hệ thống, bệnh tim, hoặc bệnh hồng cầu hình liềm), hoặc thrombophilia đã biết.
- Có > 2 các yếu tố nguy cơ sau (hoặc có > 1 trong trường hợp mổ lấy thai cấp cún): băng huyết sau sinh > 1000 mL không cần mồ lại, BMI > 30 kg/m2 , thai chậm tăng trưởng, tiền sản giật, đa thai và sử dụng thuốc lá trong thai kỳ (> 10 điếu/ngày).
Khuyến cáo của RCOG – Royal College of Obstetricians and Gynaecologists(RCOG) tuyên bố rằng “tất cả phụ nữ mổ lấy thai nên được xem xét dự phòng huyết khối với LMWH trong 10 ngày sau khi sinh, ngoại trừ những người mổ lấy thai chủ động nên được xem xét dự phòng huyết khối với LMWH trong 10 ngày sau khi sinh nếu họ có thêm bất kỳ yếu tố nguy cơ nào khác. Nên tiếp tục điều trị dự phòng huyết khối trong sáu tuần ở phụ nữ có nguy cơ cao và trong 10 ngày ở phụ nữ có nguy cơ trung bình “[ 103]. RCOG xem xét các yếu tố nguy cơ sau đối với VTE (tham khảo hướng dẫn của RCOG về mô tả đánh giá nguy cơ chi tiết): VTE trước đó, thrombophilia, một số bệnh nội khoa đồng mắc (ví dụ: ung thư; suy tim; lupus ban đỏ hệ thống hoạt động, bệnh viêm đa khớp hoặc bệnh ruột viêm; hội chứng thận hư ; đái tháo đường type I kèm bệnh thận; bệnh hồng cầu hình liềm; người đang dùng ma túy đường tiêm), >35 tuổi, BMI >30 kg/m2, số lần sinh > 3, giãn tĩnh mạch đại thể (có triệu chứng hoặc trên đầu gối hoặc kèm theo viêm tĩnh mạch, phù / thay đổi da), liệt nửa người, đa thai, tiền sản giật, sinh non, băng huyết sau sinh > 1L / cần truyền máu, nhập viện / bất động > 3 ngày, đang bị nhiễm trùng toàn thân [ 103].
Tuy nhiên, tiêu chí của RCOG về dự phòng huyết khối sau mổ lấy thai sẽ áp dụng cho một nửa số bệnh nhân sinh mổ ở Hoa Kỳ (1,2 triệu một năm), và chỉ tính riêng tiền thuốc có thể lên đến 52 triệu USD cho liệu trình 4 ngày và 130 triệu USD cho liệu trình 10 ngày [ 91].
Chuấn bị cho băng huyết sau sinh – (See “Overview of postpartum hemorrhage”, section on ‘Planning*.)
5.5 Các vấn đề cần xem xét khác
- Chuẩn bị ruột không có lợi và không được khuyến cáo [ 109,110].
- Phẫu thuật ở phụ nữ béo phì nặng có thêm những thách thức được thảo luận ở chủ đề riêng.
(See “Cesarean delivery of the obese woman”.)
6. Đánh giá nhau thai
Theo dõi nhịp tim thai – Đối với nhũng phụ nữ đang chờ mổ lấy thai theo kế hoạch, giá trị của việc theo dôi nhịp tim thai liên tục hoặc ngắt quãng sau khi nhập viện là không rõ ràng [ 111], không có thử nghiệm ngẫu nhiên nào được thực hiện để đánh giá vấn đề này. ít nhất, nhịp tim của thai nhi phải được ghi vào hồ sơ khi nhập viện, tương tự như các dấu hiệu sinh tồn khác. Nếu thai kỳ có nguy cơ cao và đã được làm test thai nhi trước sinh, có thể là hợp lý khi thực hiện test nonstress lúc nhập viện và ngừng theo dõi nếu biểu đồ nhịp tim thai có đáp ứng. Nếu có sự chậm trễ quá mức giữa việc gây mê và chuẩn bị bụng để phẫu thuật, khi đó kiểm tra lại nhịp tim thai trong khoảng thời gian này là thích hợp.
Đối với các bệnh nhân đang chuyển dạ, cần theo dõi nhịp tim thai liên tục sau khi chuyển đến phòng mổ, trong chừng mực có thể. Monitors bên ngoài được lấy bỏ khi bắt đầu chuẩn bị bụng; monitors bên trong được lấy bỏ khi việc chuẩn bị bụng hoàn tất.
Ngôi thai và vị trí bánh nhau – Siêu âm để đánh giá vị trí bánh nhau và ngôi thai, hoặc thủ thuật Leopold để đánh giá ngôi thai, có thể hữu ích trước phẫu thuật, nhưng không bắt buộc. Thông tin này có thể giúp bác sĩ phẫu thuật tránh làm gián đoạn nhau thai khi rạch tử cung và lên kế hoạch sinh thai trong trường hợp không phải ngôi đầu.
7. Chuẩn bị mẹ trong khi phẫu thuật
Đặt ống thông bàng quang – Hầu hết các bác sĩ lâm sàng đặt một ống thông niệu đạo vào đầu ca mổ để duy trì dẫn lưu bàng quang và do đó cải thiện tầm nhìn trong khi phẫu thuật và giảm thiểu tổn thương bàng quang. Óng thông cũng hữu ích để truyền thuốc màu nếu nghi ngờ cắt vào bàng quang và theo dõi lượng nước tiểu. Các tác hại tiềm ẩn bao gồm tăng nguy cơ nhiễm trùng đường tiết niệu, đau niệu đạo, khó đi tiểu sau khi rút ống thông, đi lại muộn và thời gian nằm viện dài hơn [ 112].
Tuy nhiên, không có bằng chứng chất lượng cao nào cho thấy việc đặt ống thông bên trong thường quy là có lợi [ 112,113]. Như một sự thay thế, những bệnh nhân có nguy cơ biến chứng trong phẫu thuật thấp có thể được yêu cầu đi tiểu ngay trước khi vào phòng mổ. Nếu sau đó được yêu cầu, một ống thông bên trong có thể được đặt trong hoặc sau phẫu thuật, và lấy bỏ càng sớm càng tốt [ 114-117].
Loại bó lông – Phân tích gộp các thử nghiệm ngẫu nhiên ở bệnh nhân không mang thai cho thấy không có sự khác biệt về tỷ lệ nhiễm trùng vết mổ (SSI) ở những người được loại bỏ lông trước phẫu thuật so với những người không loại bỏ lông [ 118,119]. Không có thử nghiệm ngẫu nhiên nào được thực hiện để đánh giá can thiệp này đặc biệt trước khi mổ lấy thai.
Nếu cần loại bỏ lông, nên cắt thay vì cạo bởi những bệnh nhân cạo lông có nhiều khả năng bị nhiễm trùng vết mổ hơn. Sử dụng kem làm rụng lông cũng được ưu tiên hơn cạo. Nên thực hiện cắt lông ngay trước khi phẫu thuật. (See “Overview of control measures for prevention of surgical site infection in adults”, section on ‘Hair removal1.)
Chuấn bị da – Chúng tôi chuẩn bị vị trí mổ ở bụng với chlorhexidine-cồn trước khi mổ lấy thai dựa trên dữ liệu từ ba thử nghiệm ngẫu nhiên báo cáo làm giảm nhiễm trùng vết mổ hoặc nuôi cấy vết mổ dương tính với vi khuẩn so với việc chuẩn bị da bằng cồn iodine; hai thử nghiệm ở phụ nữ mổ lấy thai [ 120,121] và thử nghiệm còn lại ở người lớn thực hiện phẫu thuật bị nhiễm bẩn sạch [ 122]. Tuy nhiên, một phân tích gộp năm 2020 về các thử nghiệm ngẫu nhiên đánh giá kỹ thuật chuẩn bị da kết luận rằng nhìn chung không có đủ bằng chúng để xác định kỹ thuật chuẩn bị da nào hiệu quả nhất trong việc ngăn ngừa nhiễm trùng vết mổ sau mổ lấy thai hoặc làm giảm các kết cục không mong muốn khác [ 123], gợi ý chlorhexidine-alcohol hoặc iodine-alcohol đều thích họp. Lưu ý, trong phân tích phụ so sánh chlorhexidine-alcohol với povidone-iodine, chlorhexidine-alcohol có hiệu quả hơn trong việc làm giảm nhiễm trùng vết mổ (risk ratio [RR] 0,72, 95% CI 0,58-0,91, tám thử nghiệm, 4323 phụ nữ), nhưng sự khác biệt là giảm dần khi bốn thử nghiệm có nguy cơ sai lệch cao bị loại bỏ. Hướng dẫn của hiệp hội American College of Obstetricians and Gynecologists (ACOG) và Enhanced Recovery After Surgery (ERAS) về chăm sóc trong phẫu thuật khi mổ lấy thai khuyến cáo sử dụng dung dịch hỗn hợp có chứa cồn như chlorhexidine-alcohol [ 50,124].
Các dung dịch chuẩn bị phẫu thuật có cồn chứa khoảng 70 đến 75% cồn isopropyl và dùng làm nhiên liệu nếu không được cho phép để đủ khô trước khi sử dụng nguồn đánh lửa; cần ít nhất ba phút. Do đó, chuẩn bị bằng xà phòng povidone-iodine hoặc chlorhexidine(ví dụ, Hibiclens) sẽ có lợi khi không thể trì hoãn phẫu thuật, vì những dung dịch này không dễ cháy.
Lợi ích của việc tắm với chế phẩm sát trùng trước khi phẫu thuật để làm giảm nguy cơ nhiễm trùng vết mồ vẫn chưa được chứng minh. Trong một phân tích gộp năm 2006 với sáu thử nghiệm bao gồm 10.000 người tham gia thực hiện phẫu thuật tổng quát, tắm trước khi phẫu thuật với chlorhexidinekhông mang lại lợi ích gì so với việc tắm trước khi phẫu thuật với các sản phẩm khác để làm giảm nhiễm trùng vết mổ [ 125].
Chuẩn bị âm đạo – Đối với phụ nữ đang chuyển dạ và phụ nữ bị vỡ ối, chúng tôi thực hiện chà âm đạo ba lần bằng miếng bọt biển chlorhexidinegluconate 4%, mỗi lần 30 giây để làm giảm nguy cơ nhiễm trùng vết mổ, đặc biệt viêm nội mạc tử cung. Povidone-iodine là một lựa chọn thay thế nhưng kém hiệu quả hơn ở thử nghiệm ngẫu nhiên lớn nhất so sánh hai lựa chọn này [ 126]. Nên tránh cho các chế phẩm có nồng độ cồn cao (chlorhexidine gluconat với 70% cồn dùng để chuẩn bị da) vào trong âm đạo vì cồn gây kích ứng màng nhầy [ 50].
Trong một phân tích gộp năm 2020 về các thử nghiệm ngẫu nhiên giữa làm sạch âm đạo (povidone-iodine hoặc chĩorhexidine) so với giả dược / không can thiệp trước khi mổ lấy thai, làm sạch âm đạo dẫn đến giảm viêm nội mạc tử cung (3,0 so với 7,2%, RR 0,41, CI 95% 0,29-0,58 ), sốt sau phẫu thuật (RR 0,64, CI 95% 0,50-0,82), và nhiễm trùng vết mổ (3,8 so với 6,1%, RR 0,62, CI 95% 0,50-0,77) [ 127]. Trong phân tích phân nhóm, phụ nữ đang chuyển dạ hoặc vỡ ối có sự giảm viêm nội mạc tử cung sau mổ lớn nhất. Không chất làm sạch nào dẫn đến các tác dụng bất lợi.
Một phân tích gộp mạng lưới các thử nghiệm ngẫu nhiên xác nhận rằng tất cả các chế phẩm thuốc sát trùng (povidone-iodine, chlorhexidine, metronidazolegel, cetrimide) đều làm giảm tỷ lệ viêm nội mạc tử cung so với giả dược (5,2 so với 9,1%, odds ratio [OR] 0,48, CI 95% 0,35-0,65); povidone-iodine có khả năng làm giảm nguy cơ viêm nội mạc tử cung, nhiễm trùng vết mổ sau phẫu thuật và sốt cao nhất [ 128]. Tuy nhiên, trong thử nghiệm duy nhất so sánh tỷ lệ nhiễm trùng vết mổ ở những bệnh nhân được chỉ định dùng chlorhexidine so với povidone-iodine trước khi mổ lấy thai, tỷ lệ này thấp hơn ở nhóm chlorhexidine (0,6 so với 2,0%, OR 0,28, CI 95% 0,08-0,98) [ 126Ị, là cơ sở cho sự ưa tiên của chúng tôi đối với chlorhexidine. Tỷ lệ viêm nội mạc tử cung thấp và tương tự ở cả hai nhóm (0,4 và 0,5%).
Băng không dính – VỊ trí mổ được dán bằng băng không dính vì hai thử nghiệm ngẫu nhiên ở bệnh nhân mổ lấy thai báo cáo rằng những miếng băng này dẫn đến tỷ lệ nhiễm trùng vết mổ thấp hon băng có dính [ 129,130].
Đấy lệch tử cung – Tử cung thường bị đẩy lệch sang trái ít nhất 15 độ để giảm chèn ép chủ- cửa (“hội chứng hạ huyết áp khi nằm ngửa”), xảy ra ở tư thế nằm ngửa khi tử cung ngang hoặc trên rốn [ 131-135]. Có thể sử dụng miếng chêm bằng xốp hoặc gỗ, gối hoặc chăn cuộn tròn, hoặc bàn có thể nghiêng, hoặc có thể đẩy lệch tử cung bằng tay. Một tổng quan hệ thống năm 2013 đã không thể xác định phương pháp hoặc tư thế mẹ tối ưu [ 136]. (See “Anesthesia for cesarean delivery”, section on ‘Intraoperative positioning’.)
Quản lý thuốc chu phẫu – Thuốc chu phẫu tương tự như các thủ thuật ngoại khoa khác và được thảo luận ở chủ đề riêng. (See “Perioperative medication management”.)
Nhiệt độ phòng – Nên duy trì nhiệt độ bình thường trong khi gây mê và phẫu thuật. Bệnh nhân đang được gây tê trục thần kinh trở nên hạ thân nhiệt đến một mức tương tự như những bệnh nhân được gây mê toàn thân. (See “Perioperative temperature management”.)
8. Tóm tắt và khuyến cáo
Mổ lấy thai được thực hiện khi bác sĩ lâm sàng và / hoặc bệnh nhân tin rằng mổ lấy thai có khả năng mang lại kết cục tốt hơn cho mẹ và / hoặc thai nhi so với sinh ngả âm đạo Một loạt các tình trạng đáp ứng các tiêu chí này. (See ‘Indications’above.)
Mổ lấy thai lần đầu, đủ tháng theo kế hoạch/ lịch được thực hiện ở tuần thứ 39 hoặc 40 của thai kỳ thay vì tuần thứ 37 hoặc 38. Các ca mồ lấy thai được chỉ định về mặt y tế / sản khoa được thực hiện khi có chỉ định về mặt lâm sàng. (See ‘Scheduling’above.)
Thời điểm mổ lấy thai lặp lại theo lịch / kế hoạch dựa vào loại vết mổ tử cung trước đó và được xem xét ở chủ đề riêng. (See “Repeat cesarean delivery”, section on ‘Timing’.)
Đối với tất cả phụ nữ mổ lấy thai, chúng tôi khuyến cáo dự phòng kháng sinh trước mổ thay vì không dự phòng hoặc dự phòng sau khi kẹp rốn (Grade 1A). Kháng sinh được dùng trước khi rạch da lên đến 60 phút.
- Chúng tôi sử dụng một liều kháng sinh phổ hẹp duy nhất tiêm tĩnh mạch, như cefazolin (2 gam đối với bệnh nhân < 120 kg và 3 gam đối với bệnh nhân > 120 kg). Nhiều liều tốn kém hơn mà không cải thiện kết cục một cách rõ ràng nếu phẫu thuật không kéo dài hoặc mất máu quá mức. Nếu mổ lấy thai sau khi khởi phát chuyển dạ hoặc sau khi vỡ ối, chúng tôi thêm một liều azithromycin500 mg tiêm tĩnh mạch. (See ‘Regimen’above and ‘Prolonged surgery or excessive blood loss’above.)
- Đối với phụ nữ có tiền sử dị ứng nghiêm trọng với penicillin, chúng tôi thay thế clindamycin và gentamicincho cefazolin. Phụ nữ có nguy cơ thấp bị phản ứng dị ứng tức thì nghiêm trọng có thể dùng cefazolin. Nếu mổ lấy thai được thực hiện sau khi khởi phát chuyển dạ hoặc sau khi vỡ ối, chúng tôi thêm một liều azithromycin 500 mg tiêm tĩnh mạch. (See ‘Women with penicillin allergy’above.)
- Đối với phụ nữ đang dùng penicillin Gđể dự phòng nhiễm Liên cầu khuẩn nhóm B (GBS) ở trẻ sơ sinh, chúng tôi không thêm cefazolinhoặc chuyển sang ampicillinđể dự phòng phẫu thuật. Nếu mổ lấy thai được thực hiện sau khi khởi phát chuyển dạ hoặc sau khi vỡ ối, chúng tôi thêm một liều azithromycin500 mg tiêm tĩnh mạch. (See ‘Woman already on antibiotics’above.)
- Đối với phụ nữ đang dùng ampicillinvà gentamicinvì viêm màng đệm- màng ối, chúng tôi thêm một liều clindamycin 900 mg hoặc metronidazole500 mg trước khi rạch da, và tiếp tục ampicillin và gentamicin hoặc chuyển sang ampicillin-sulbactam sau khi sinh cho đến khi bệnh nhân hết sốt trong ít nhất 24 giờ. Sự đề kháng của Bacteroides đối với clindamycin ngày càng tăng; ở những vùng có tỷ lệ kháng thuốc cao, ưu tiên dùng ampicillin-sulbactam. Chúng tôi không dùng azithromycin dự phòng trước khi rạch ra trong trường họp này này. (See ‘Woman already on antibiotics’above.)
Chúng tôi sử dụng chất sát trùng chứa chlorhexidine thay vì chất sát trùng chứa iodine để chuẩn bị da, nhưng cả hai cách tiếp cận này đều họp lý. Các dung dịch chlorhexidine-cồn phải được để khô ít nhất ba phút trước khi sử dụng nguồn đánh lửa, nếu không thì nên sử dụng chế phẩm không dễ cháy (povidone-iodine hoặc xà phòng chlorhexidine). (See ‘Skin preparation’above.)
Đối với phụ nữ đang chuyển dạ và phụ nữ bị vỡ ối, chúng tôi đề nghị làm sạch âm đạo trước khi mổ lấy thai thay vì không làm sạch âm đạo (Grade 2C). Chúng tôi sử dụng chất chà rửa âm đạo chlorhexidinegluconate 4%, nhưng povidone-iodine cũng có thể hợp lý. Làm sạch âm đạo ở những quần thể có nguy cơ cao này làm giảm tần suất viêm nội mạc tử cung sau sinh. (See ‘Vaginal preparation’above.)
Đối với tất cả phụ nữ mổ lấy thai, chúng tôi đề nghị dự phòng huyết khối cơ học (Grade 2C). Đối với những phụ nữ mổ lấy thai có nguy cơ cao bị thuyên tắc huyết khối tĩnh mạch (VTE), chúng tôi đề nghị dự phòng huyết khối cơ học kết hợp với dự phòng huyết khối bằng thuốc (Grade 2C). Dự phòng bằng thuốc được bắt đầu từ 6 đến 12 giờ sau phẫu thuật, sau khi nhũng lo ngại về chảy máu đã giảm. Dự phòng cơ học và bằng thuốc được tiếp tục cho đến khi sản phụ đi lại được hoàn toàn. Phụ nữ có các yếu tố nguy cơ đáng kể đối với VTE vẫn tồn tại sau khi sinh nên được nhận dự phòng huyết khối đủ sáu tuần. (See ‘Thromboembolism prophylaxis’above.)
Trong khi mổ lấy thai, tử cung bị đẩy lệch sang trái ít nhất 15 độ để giảm chèn ép chủ-cửa. (See ‘Uterine displacement’above.)
9. Tham khảo
1. Martin JA, Hamilton BE, Osterman MJK, Driscoll AK. Births: Final Data for 2018. Natl Vital Stat Rep 2019; 68:1.
2. Boerma T, Ronsmans c, Melesse DY, et al. Global epidemiology of use of and disparities in caesarean sections. Lancet 2018; 392:1341.
3. WHO recommendations non-clinical interventions to reduce unnecessary caesarean se
ctions http://apps.who. i nt/i ris/bitstream/ha nd le/10665/275377/9789241550338-eng.pd
4. American College of Obstetricians and Gynecologists (College), Society for Maternal-Fetal Medicine, Caughey AB, et al. Safe prevention of the primary cesarean delivery. Am J Obstet Gynecol 2014:210:179.
5. Gholitabar M, Ullman R, James D, et al. Caesarean section: summary of updated NICE guidance. BMJ 2011; 343:d7108.
6. Visser GHA, Ayres-de-Campos D, Barnea ER, et al. FIGO position paper: how to stop the caesarean section epidemic. Lancet 2018; 392:1286.
7. Boyle A, Reddy UM, Landy HJ, et al. Primary cesarean delivery in the United States.
Obstet Gynecol 2013; 122:33.
8. Walker SP, McCarthy EA, Ugoni A, et al. Cesarean delivery or vaginal birth: a survey of patient and clinician thresholds. Obstet Gynecol 2007; 109:67.
9. Lyerly AD, Mitchell LM, Armstrong EM, et al. Risks, values, and decision making surrounding pregnancy. Obstet Gynecol 2007; 109:979.
10. American College of Obstetricians and Gynecologists. Patient Safety Checklist no. 4: preoperative planned cesarean delivery. Obstet Gynecol 2011; 118:1471.
11. American College of Obstetricians and Gynecologists. Patient Safety Checklist no. 3: scheduling planned cesarean delivery. Obstet Gynecol 2011; 118:1469.
12. Sentilhes L, Vayssière c, Beucher G, et al. Delivery for women with a previous cesarean: guidelines for clinical practice from the French College of Gynecologists and Obstetricians (CNGOF). Eur J Obstet Gynecol Reprod Biol 2013; 170:25.
13. http://www.nice.org.uk/guidance/cg132 (Accessed on October 22, 2014).
14. American College of Obstetricians and Gynecologists. ACQG committee opinion no. 561: Nonmedically indicated early-term deliveries. Obstet Gynecol 2013; 121:911. Reaffirmed 2017.
15. Committee on Obstetric Practice. Committee Opinion No. 688: Management of Suboptimally Dated Pregnancies. Obstet Gynecol 2017; 129:e29. Reaffirmed 2019.
16. Hansen AK, Wisborg K, Uldbjerg N, Henriksen TB. Risk of respiratory morbidity in term infants delivered by elective caesarean section: cohort study. BMJ 2008; 336:85.
17. Zanardo V, Simbi AK, Franzoi M, et al. Neonatal respiratory morbidity risk and mode of delivery at term: influence of timing of elective caesarean delivery, Acta Paediatr 2004; 93:643.
18. Morrison JJ, Rennie JM, Milton PJ. Neonatal respiratory morbidity and mode of delivery at term: influence of timing of elective caesarean section. Br J Obstet Gynaecol 1995; 102:101.
19. Wax JR, Herson V, Carignan E, et al. Contribution of elective delivery to severe respiratory distress at term. Am J Perinatal 2002; 19:81 ■
20. Yee w, Amin H, Wood s. Elective cesarean delivery, neonatal intensive care unit admission, and neonatal respiratory distress. Obstet Gynecol 2008; 111:823.
21. Clark SL, Miller DP, Belfort MA, et al. Neonatal and maternal outcomes associated with elective term delivery. Am J Obstet Gynecol 2009; 200:156.e1.
22. Wilmink FA, Hukkelhoven cw, Lunshof s, et al. Neonatal outcome following elective cesarean section beyond 37 weeks of gestation: a 7-year retrospective analysis of a national registry. Am J Obstet Gynecol 2010; 202:250.e1.
23. Nir V, Nadir E, Feldman M. Late better than early elective term Cesarean section. Acta Paediatr 2012; 101:1054.
24. Glavind J, Kindberg SF, Uldbịerq N, et al. Elective caesarean section at 38 weeks versus
39 weeks: neonatal and maternal outcomes in a randomised controlled trial. BJOG 2013; 120:1123.
25. Tita AT, Landon MB, Spong CY, et al. Timing of elective repeat cesarean delivery at term and neonatal outcomes. N Engl J Med 2009; 360:111.
26. Smith J, Plaat F, Fisk NM. The natural caesarean: a woman-centred technigue. BJQG 2008; 115:1037.
27. Magee SR, Battle c, Morton J, Nothnaqle M. Promotion of family-centered birth with gentle cesarean delivery. J Am Board Fam Med 2014; 27:690.
28. Armbrust R, Hinkson L, von Weizsacker K, Henrich w. The Charite cesarean birth: a family orientated approach of cesarean section. J Matern Fetal Neonatal Med 2016; 29:163.
29. MacKenzie IZ, Cooke I. Prospective 12 month study of 30 minute decision to delivery intervals for “emergency” caesarean section. BMJ 2001; 322:1334.
30. James D, Caesarean section for fetal distress. BMJ 2001; 322:1316,
31. Helmv WH, Jolaoso AS, Ifaturoti 00, et al. The decision-to-delivery interval for emergency caesarean section: is 30 minutes a realistic target? BJOG 2002; 109:505.
32. Tuffnell DJ, Wilkinson K, Beresford N. Interval between decision and delivery by caesarean section-are current standards achievable? Observational case series. BMJ 2001; 322:1330.
33. Chauhan SP, Roach H, Naef RW 2nd, et al. Cesarean section for suspected fetal distress. Does the decision-incision time make a difference? J Reprod Med 1997; 42:347.
34. MacKenzie IZ, Cooke I. What is a reasonable time from decision-to-delivery by caesarean section? Evidence from 415 deliveries. BJOG 2002; 109:498.
35. Thomas J, Paranịothv s, James D, National cross sectional survey to determine whether the decision to delivery interval is critical in emergency caesarean section. BMJ 2004; 328:665.
36. Holcroft CJ, Graham EM, Aina-Mumuney A, et al. Cord gas analysis, decision-to-delivery interval, and the 30-minute rule for emergency cesareans. J Perinatol 2005; 25:229.
37. Bloom SL, Leveno KJ, Spong CY, et al. Decision-to-incision times and maternal and infant outcomes. Obstet Gynecol 2006; 108:6.
38. Tolcher MC, Johnson RL, El-Nashar SA, West CP. Decision-to-incision time and neonatal outcomes: a systematic review and meta-analysis. Obstet Gynecol 2014; 123:536.
39. Stallings SP, Edwards RK, Johnson JW. Correlation of head-to-body delivery intervals in shoulder dystocia and umbilical artery acidosis. Am J Obstet Gynecol 2001; 185:268.
40. Katz VL, Potters DJ, Droeqemueller w. Perimortem cesarean delivery. Obstet Gynecol 1986; 68:571.
41. Myers RE. Two patterns of perinatal brain damage and their conditions of occurrence. Am J Obstet Gynecol 1972; 112:246.
42. Webster J, Osborne s. Preoperative bathing or showering with skin antiseptics to prevent surgical site infection. Cochrane Database Syst Rev 2015; :CD004985.
43. Franco LM, Cota GF, Pinto TS, Ercole FF. Preoperative bathing of the surgical site with chlorhexidine for infection prevention: Systematic review with meta-analysis. Am J Infect Control 2017; 45:343.
44. Chlebicki MP, Safdar N, O’Horo JC, Maki DG. Preoperative chlorhexidine shower or bath for prevention of surgical site infection: a meta-analysis. Am J Infect Control 2013; 41:167.
45. Cousins LM, Teplick FB, Poeltler DM. Pre-cesarean blood bank orders: a safe and less expensive approach. Obstet Gynecol 1996; 87:912.
46. Ransom SB, Fundaro G, Dombrowski MP. Cost-effectiveness of routine blood type and screen testing for cesarean section. J Reprod Med 1999; 44:592.
47. Rouse DJ, MacPherson c, Landon M, et al. Blood transfusion and cesarean delivery. Obstet Gynecol 2006; 108:891.
48. American Society of Anesthesiologists Task Force on Obstetric Anesthesia. Practice guidelines for obstetric anesthesia: an updated report by the American Society of Anesthesiologists Task Force on Obstetric Anesthesia. Anesthesiology 2007; 106:843.
49. Chua SC, Joung SJ, Aziz R. Incidence and risk factors predicting blood transfusion in caesarean section. Aust N z J Obstet Gynaecol 2009; 49:490.
50. Committee on Practice Bulletins-Obstetrics. ACOG Practice Bulletin No. 199: Use of Prophylactic Antibiotics in Labor and Delivery. Obstet Gynecol 2018; 132:e103.
51. Smaill FM, Grivell RM. Antibiotic prophylaxis versus no prophylaxis for preventing infection after cesarean section. Cochrane Database Syst Rev 2014; ;CD007482.
52. Mackeen AD, Packard RE, Ota E, et al. Timing of intravenous prophylactic antibiotics for preventing postpartum infectious morbidity in women undergoing cesarean delivery. Cochrane Database Syst Rev 2014; :CD009516.
53. Dinsmoor MJ, Gilbert s, Landon MB, et al. Perioperative antibiotic prophylaxis for nonlaboring cesarean delivery. Obstet Gynecol 2009; 114:752.
54. Ledger WJ, Blaser MJ. Are we using too many antibiotics during pregnancy? BJOG 2013; 120:1450.
55. Bratzler DW, Dellinger EP, Olsen KM, et al. Clinical practice guidelines for antimicrobial prophylaxis in surgery. Am J Health Syst Pharm 2013; 70:195.
56. Forse RA, Karam B, MacLean LD, Christou NV. Antibiotic prophylaxis for surgery in morbidly obese patients. Surgery 1989; 106:750.
57. Wurtz R, Itokazu G, Rodvoid K. Antimicrobial dosing in obese patients. Clin Infect Dis 1997; 25:112.
58. Swank ML, Wing DA, Nicolau DP, McNulty JA. Increased 3-gram cefazolin dosing for cesarean delivery prophylaxis in obese women. Am J Obstet Gynecol 2015; 213:415.e1.
59. Young OM, Shaik IH, Twedt R, et al. Pharmacokinetics of cefazolin prophylaxis in obese gravidae at time of cesarean delivery. Am J Obstet Gynecol 2015; 213:541 .e1 ■
60. Maggio L, Nicolau DP, DaCosta M, et al. Cefazolin prophylaxis in obese women undergoing cesarean delivery: a randomized controlled trial. Obstet Gynecol 2015; 125:1205.
61. www.drugs.com.
62. Gyte GM, Pou L, Vazguez JC. Different classes of antibiotics given to women routinely for preventing infection at caesarean section. Cochrane Database Syst Rev 2014; :CD008726.
63. Hopkins L, Smaill F. Antibiotic prophylaxis regimens and drugs for cesarean section. Cochrane Database Syst Rev 2000; :CD001136.
64. Pinto-Lopes R, Sousa-Pinto B, Azevedo LF, Single dose versus multiple dose of antibiotic prophylaxis in caesarean section: a systematic review and meta-analysis. BJOG 2017; 124:595.
65. Andrews ww, Hauth JC, Cliver SP, et al. Randomized clinical trial of extended spectrum antibiotic prophylaxis with coverage for Ureaplasma urealyticum to reduce post-cesarean delivery endometritis. Obstet Gynecol 2003; 101:1183,
66. Tita AT, Szychowski JM, Boggess K, et al. Adjunctive Azithromycin Prophylaxis for Cesarean Delivery. N Engl J Med 2016; 375:1231.
67. Farmer N, Hodgetts-Morton V, Morris RK. Are prophylactic adjunctive macrolides efficacious against caesarean section surgical site infection: A systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol 2020; 244:163.
68. Harper LM, Kilgore M, Szychowski JM, et al. Economic Evaluation of Adjunctive Azithromycin Prophylaxis for Cesarean Delivery. Obstet Gynecol 2017; 130:328.
69. Weinstein RA, Boyer KM. Antibiotic Prophylaxis for Cesarean Delivery – When Broader Is Better. N Engl J Med 2016; 375:1284.
70. Ragusa A, Svelato A. Adjunctive Azithromycin Prophylaxis for Cesarean Delivery. N Engl J Med 2017; 376:181.
71. Greig JR, Jones L. Adjunctive Azithromycin Prophylaxis for Cesarean Delivery. N Engl J Med 2017; 376:181.
72. Tita ATN, Boggess K, Saade G. Adjunctive Azithromycin Prophylaxis for Cesarean Delivery. N Engl J Med 2017; 376:182.
73. Zelenitsky SA, Silverman RE, Duckworth H, Harding GK. A prospective, randomized, double-blind studyof single high dose versus multiple standard dose gentamicin both in combination withmetronidazole for colorectal surgicalprophylaxis. J Hosp Infect 2000; 46:135.
74. Rao SC, Srinỉvasịois R, Hagan R, Ahmed M. One dose per day compared to multiple doses per day of gentamicin for treatment of suspected or proven sepsis in neonates. Cochrane Database Syst Rev 2011; :CD005091 ■
75. Fay KE, Yee L. Applying surgical antimicrobial standards in cesarean deliveries. Am J Obstet Gynecol 2018; 218:416.e1.
76. Bratzler DW, Dellinger EP, Olsen KM, et al. Clinical practice guidelines for antimicrobial prophylaxis in surgery. Surg Infect (Larchmt) 2013; 14:73.
77. Kamel H, Navi BB, Sriram N, et al. Risk of a thrombotic event after the 6-week postpartum period. N Engl J Med 2014; 370:1307.
78. Blondon M, Casini A, Hoppe KK, et al. Risks of Venous Thromboembolism After Cesarean Sections: A Meta-Analysis. Chest 2016; 150:572.
79. Landon MB, Hauth JC, Leveno KJ, et al. Maternal and perinatal outcomes associated
with a trial of labor after prior cesarean delivery. N Engl J Med 2004; 351:2581 ■
80. https://www.cdc.gov/mmwr/preview/mmwrhtml/ss5202a1 ,htm#tab3 (Accessed on Febr uary 14,2017).
81. Greer I A. Thrombosis in pregnancy: maternal and fetal issues. Lancet 1999; 353:1258.
82. Bain E, Wilson A, Tooher R, et al. Prophylaxis for venous thromboembolic disease in pregnancy and the early postnatal period. Cochrane Database Syst Rev 2014; :CD001689.
83. Kotaska A. Postpartum venous thromboembolism prophylaxis may cause more harm than benefit: a critical analysis of international guidelines through an evidence-based lens. BJOG 2018; 125:1109.
84. Seeho s, Nassar N. Thromboprophylaxis after caesarean: when even the ‘experts’ disagree. BJOG 2016; 123:2163.
85. O’Shaughnessy F, Donnelly JC, Cooley SM, et al. Thrombocalc: implementation and uptake of personalized postpartum venous thromboembolism risk assessment in a high- throughput obstetric environment. Acta Obstet Gynecol Scand 2017; 96:1382.
86. Taylor GM, McKenzie CA, Mires GJ. Use of a computerised maternity information system to improve clinical effectiveness: thromboprophylaxis at caesarean section. Postgrad Med J 2000; 76:354.
87. ACOG Practice Bulletin No. 196 Summary: Thromboembolism in Pregnancy. Obstet Gynecol 2018; 132:243.
88. Committee on Practice Bulletins-Gynecology, American College of Obstetricians and Gynecologists. ACOG Practice Bulletin No. 84: Prevention of deep vein thrombosis and pulmonary embolism. Obstet Gynecol 2007; 110:429. Reaffirmed 2018.
89. Clark SL, Belfort MA, Dildy GA, et al. Maternal death in the 21st century: causes, prevention, and relationship to cesarean delivery. Am J Obstet Gynecol 2008; 199:36.e1.
90. Clark SL, Christmas JT, Frye DR, et al. Maternal mortality in the United States: predictability and the impact of protocols on fatal postcesarean pulmonary embolism and hypertension-related intracranial hemorrhage. Am J Obstet Gynecol 2014; 211:32.e1.
91. Sibai BM, Rouse DJ. Pharmacologic Thromboprophylaxis in Obstetrics: Broader Use Demands Better Data. Obstet Gynecol 2016; 128:681.
92. Bates SM, Greer IA, Middeldorp s, et al. VTE, thrombophilia, antithrombotic therapy, and pregnancy: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141:e691S.
93. Dargaud Y, Rugeri L, Vergnes MC, et al. A risk score for the management of pregnant women with increased risk of venous thromboembolism: a multicentre prospective study. Br J Haematol 2009; 145:825.
94. Danilenko-Dixon DR, Heit JA, Silverstein MD, et al. Risk factors for deep vein thrombosis and pulmonary embolism during pregnancy or post partum: a population-based, case¬control study. Am J Obstet Gynecol 2001; 184:104.
95. Ettema HB, Kollen BJ, Verheyen cc, Buller HR. Prevention of venous thromboembolism in patients with immobilization of the lower extremities: a meta-analysis of randomized controlled trials. J Thromb Haemost 2008; 6:1093.
96. Jacobsen AF, Skjeldestad FE, Sandset PM. Ante- and postnatal risk factors of venous thrombosis: a hospital-based case-control study. J Thromb Haemost 2008; 6:905.
97. James AH, Jamison MG, Brancazio LR, Myers ER. Venous thromboembolism during pregnancy and the postpartum period: incidence, risk factors, and mortality. Am J Obstet Gynecol 2006; 194:1311.
98. Lindgvist p, Dahlbãck B, Marsál K. Thrombotic risk during pregnancy: a population study. Obstet Gynecol 1999; 94:595.
99. Mackion NS, Greer IA. Venous thromboembolic disease in obstetrics and gynaecology: the Scottish experience. Scott Med J 1996; 41:83,
100. Simpson EL, Lawrenson RA, Nightingale AL, Farmer RD. Venous thromboembolism in pregnancy and the puerperium: incidence and additional risk factors from a London perinatal database. BJOG 2001; 108:56.
101. Blondon M, Perrier A, Nendaz M, et al. Thromboprophylaxis with low-molecular-weight heparin after cesarean delivery. Thromb Haemost 2010; 103:129.
102. Kobayashi T, Nakabayashi M, Ishikawa M, et al. Pulmonary thromboembolism in obstetrics and gynecology increased by 6,5-fold over the past decade in Japan. Circ J 2008; 72:753.
103. Reducing the Risk of Venous Thromboembolism during Pregnancy and the Puerperiu m. Green-top Guideline No. 37a. April 2015 https://www.rcog.org.uk/globalassets/docu ments/guidelines/gtg-37a.pdf (Accessed on October 05, 2016).
104. Leffert L, Butwick A, Carvalho B, et al. The Society for Obstetric Anesthesia and Perinatology Consensus statement on the Anesthetic Management of Pregnant and Postpartum Women Receiving Thromboprophylaxis or Higher Dose Anticoagulants. Anesth Analg 2018; 126:928.
105. Overcash RT, Somers AT, LaCoursiere DY. Enoxaparin dosing after cesarean delivery in morbidly obese women. Obstet Gynecol 2015; 125:1371.
106. He z, Morrissey H, Ball p. Review of current evidence available for guiding optimal Enoxaparin prophylactic dosing strategies in obese patients-Actual Weight-based vs Fixed. Crit Rev Oncol Hematol 2017; 113:191.
107. Haqopian JC, Riney JN, Hollands JM, Deal EN. Assessment of bleeding events associated with short-duration therapeutic enoxaparin use in the morbidly obese. Ann Pharmacother 2013; 47:1641.
108. Bates SM, Middeldorp s, Rodger M, et al. Guidance for the treatment and prevention of obstetric-associated venous thromboembolism. J Thromb Thrombolysis 2016; 41:92.
109. Lurie s, Baider c, Glickman H, et al. Are enemas given before cesarean section useful? A prospective randomized controlled study. Eur J Obstet Gynecol Reprod Biol 2012; 163:27.
110. Wilson RD, Caughey AB, Wood SL, et al. Guidelines for Antenatal and Preoperative care in Cesarean Delivery: Enhanced Recovery After Surgery Society Recommendations (Part 1). Am J Obstet Gynecol 2018; 219:523.e1.
111. Committee on Obstetric Practice. ACOG Committee Opinion No. 382: Fetal Monitoring Prior to Scheduled Cesarean Delivery. Obstet Gynecol 2007; 110:961.
112. Abdel-Aleem H, Aboelnasr MF, Jayousi TM, Habib FA. Indwelling bladder catheterisation as part of intraoperative and postoperative care for caesarean section. Cochrane Database Svst Rev 2014; :CD010322.
113. Li L, Wen J, Wang L, et al. Is routine indwelling catheterisation of the bladder for caesarean section necessary? A systematic review. BJOG 2011; 118:400.
114. Senanavake H. Elective cesarean section without urethral catheterization. J Obstet Gynaecol Res 2005; 31:32.
115. Ghoreishi J. Indwelling urinary catheters in cesarean delivery. Int J Gynaecol Obstet 2003; 83:267.
116. Barnes JS. Is it better to avoid urethral catheterization at hysterectomy and caesarean section? Aust N z J Obstet Gynaecol 1998; 38:315.
117. Nasr AM, EIBigawy AF, Abdelamid AE, et al. Evaluation of the use vs nonuse of urinary catheterization during cesarean delivery: a prospective, multicenter, randomized controlled trial. J Perinatol 2009; 29:416.
118. Tanner J, Norrie p, Melen K. Preoperative hair removal to reduce surgical site infection. Cochrane Database Syst Rev 2011; :CD004122.
119. Lefebvre A, Saliou p, Lucet JC, et al. Preoperative hair removal and surgical site
infections: network meta-analysis of randomized controlled trials. J Hosp Infect 2015; 91:100.
120. Tuuli MG, Liu J, Stout MJ, et al. A Randomized Trial Comparing Skin Antiseptic Agents at Cesarean Delivery. N Engl J Med 2016; 374:647.
121. Kunkle CM, Marchan J, Safadi s, et al. Chlorhexidine gluconate versus povidone iodine at cesarean delivery: a randomized controlled trial. J Matern Fetal Neonatal Med 2015; 28:573.
122. Darouiche RO, Wall MJ Jr, Itani KM, et al. Chlorhexidine-Alcohol versus Povidone-lodine for Surgical-Site Antisepsis. N Engl J Med 2010; 362:18.
123. Hadiati DR, Hakimi M, Nurdiati DS, et al. Skin preparation for preventing infection
following caesarean section. Cochrane Database Syst Rev 2020; 6:CD007462.
124. Caughey AB, Wood SL, Macones GA, et al. Guidelines for intraoperative care in cesarean delivery: Enhanced Recovery After Surgery Society Recommendations (Part 2). Am J Obstet Gynecol 2018:219:533.
125. Webster J, Osborne s. Preoperative bathing or showering with skin antiseptics to prevent surgical site infection. Cochrane Database Syst Rev 2006; :CD004985.
126. Lakhi NA, Tricorico G, Osipova Y, Moretti ML Vaginal cleansing with chlorhexidine gluconateor povidone-iodine prior to cesarean delivery:a randomized comparator- controlled trial. Am J Obstet Gynecol 2019; :2.
127. Haas DM, Morgan s, Contreras K, Kimball s. Vaginal preparation with antiseptic solution before cesarean section for preventing postoperative infections. Cochrane Database Syst Rev 2020; 4:CD007892.
128. Roeckner JT, Sanchez-Ramos L, Mitta M, et al. Povidone-iodine 1% is the most effective vaginal antiseptic for preventing post-cesarean endometritis: a systematic review and network meta-analysis. Am J Obstet Gynecol 2019; 221:261.e1.
129. Cordtz T, Schouenborg L, Laursen K, et al. The effect of incisional plastic drapes and redisinfection of operation site on wound infection following caesarean section. J Hosp Infect 1989; 13:267.
130. Ward HR, Jennings OG, Potgieter p, Lombard CJ. Do plastic adhesive drapes prevent post caesarean wound infection? J Hosp Infect 2001; 47:230.
131. Lee sw, Khaw KS, Ngan Kee WD, et al. Haemodynamic effects from aortocaval compression at different angles of lateral tilt in non-labouring term pregnant women. Br J Anaesth 2012; 109:950.
132. Bamber JH, Dresner M. Aortocaval compression in pregnancy: the effect of changing the degree and direction of lateral tilt on maternal cardiac output. Anesth Analg 2003; 97:256.
133. Kundra p, Velrai J, Amirthalingam u, et al. Effect of positioning from supine and left lateral positions to left lateral tilt on maternal blood flow velocities and waveforms in full¬term parturients. Anaesthesia 2012; 67:889.
134. Kinsella SM, Harvey NL. A comparison of the pelvic angle applied using lateral table tilt or a pelvic wedge at elective caesarean section. Anaesthesia 2012; 67:1327.
135. Calvache JA, Munoz MF, Baron FJ. Hemodynamic effects of a right lumbar-pelvic wedge during spinal anesthesia for cesarean section. Int J Obstet Anesth 2011; 20:307.
136. Cluver c, Novikova N, Hofmeyr GJ, Hall DR. Maternal position during caesarean section for preventing maternal and neonatal complications. Cochrane Database Syst Rev 2013; ;CD007623.