Bài viết Khởi phát chuyển dạ: Tổng quan các hướng dẫn trong khoa sản được biên dịch của Bs. Vũ Tài.
Khởi phát chuyển dạ (IOL) là quá trình kích thích nhân tạo tử cung để bắt đầu chuyển dạ.1 Ngày nay, ở các nước có thu nhập cao, tỷ lệ trẻ sơ sinh được sinh ra sau IOL được ước tính là khoảng 25%, trong khi đó ở các nước có thu nhập thấp và trung bình, tỷ lệ tương ứng thường thấp hơn. 2-6 Tổ chức Y tế Thế giới (WHO) hình dung ra một thế giới mà “mọi thai phụ và trẻ sơ sinh đều được chăm sóc chất lượng trong suốt thời kỳ mang thai, trong và sau khi sinh” .7 Do đó, theo WHO, IOL chỉ nên được thực hiện trong những trường hợp có chỉ định y tế rõ ràng và lợi ích mong đợi lớn hơn tác hại tiềm ẩn.8
Một số hiệp hội y khoa đã công bố các khuyến nghị về các chỉ định lâm sàng và phương pháp IOL.8-13 Tuy nhiên, mặc dù đã có các khuyến nghị chính thức, nhưng ngày càng có nhiều trường hợp khởi phát chuyển dạ không có chỉ định về mặt y tế đang diễn ra, do yêu cầu của người mẹ, để rút ngắn thời gian mang thai hoặc đôi khi vì mục đích chủ động chấm dứt thai kỳ. Không có gì đáng ngạc nhiên khi IOL can thiệp vào quá trình mang thai và chuyển dạ tự nhiên, nó có liên quan đến tỷ lệ một số biến chúng cao hơn như chảy máu, mổ lấy thai, cơn co tử cung mau, hoặc vỡ tử cung và các kết cục chu sinh bất lợi.2,15
Mục đích của tổng quan mô tả này là tóm tắt và so sánh các khuyến nghị từ 4 hiệp hội y khoa quốc gia về IOL liên quan đến các chỉ định và phương pháp lâm sàng được đề xuất.
1. Thu thập bằng chứng
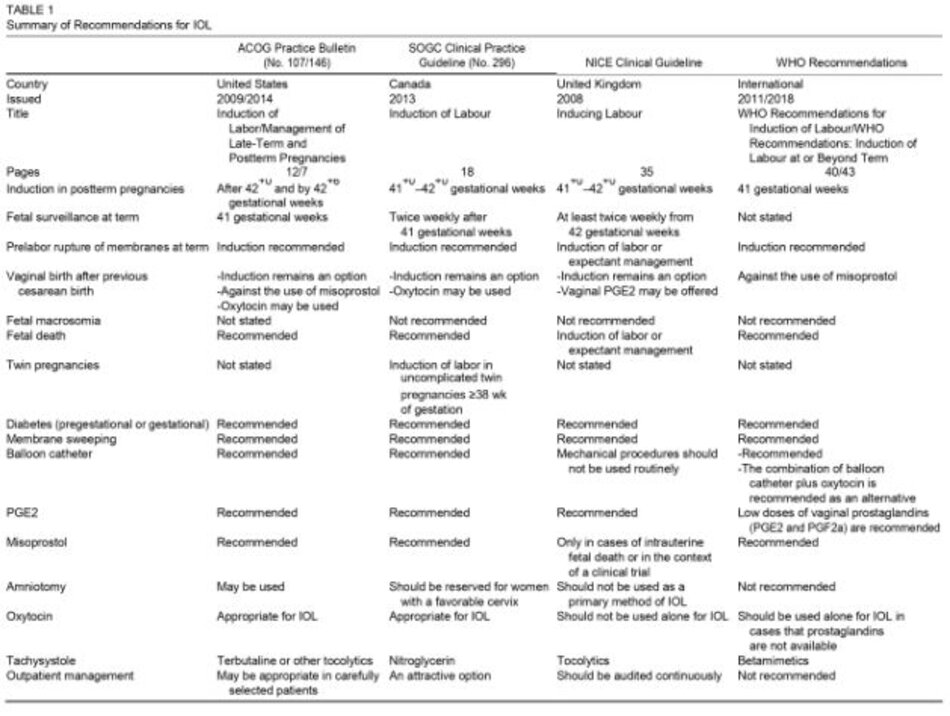
Các hướng dẫn dựa trên bằng chứng được công bố gần đây nhất về IOL được truy xuất và sau đó thực hiện tổng quan mô tả. Cụ thể hơn, 2 thông cáo thực hành của American College of Obstetricians and Gynecologists (ACOG) về IOL (2009 và 2014),12,13cũng như các hướng dẫn tù’Society of Obstetricians and Gynaecologists of Canada (SOGC 2013),11 National Institute for Health and Care Excellence (NICE 2008),9và WHO (2011 và 2018),8,10đã được xem xét. Tổng quan về các khuyến nghị được đưa ra trong các hướng dẫn này được trình bày trong Bảng 1.
2. Chỉ định lâm sàng
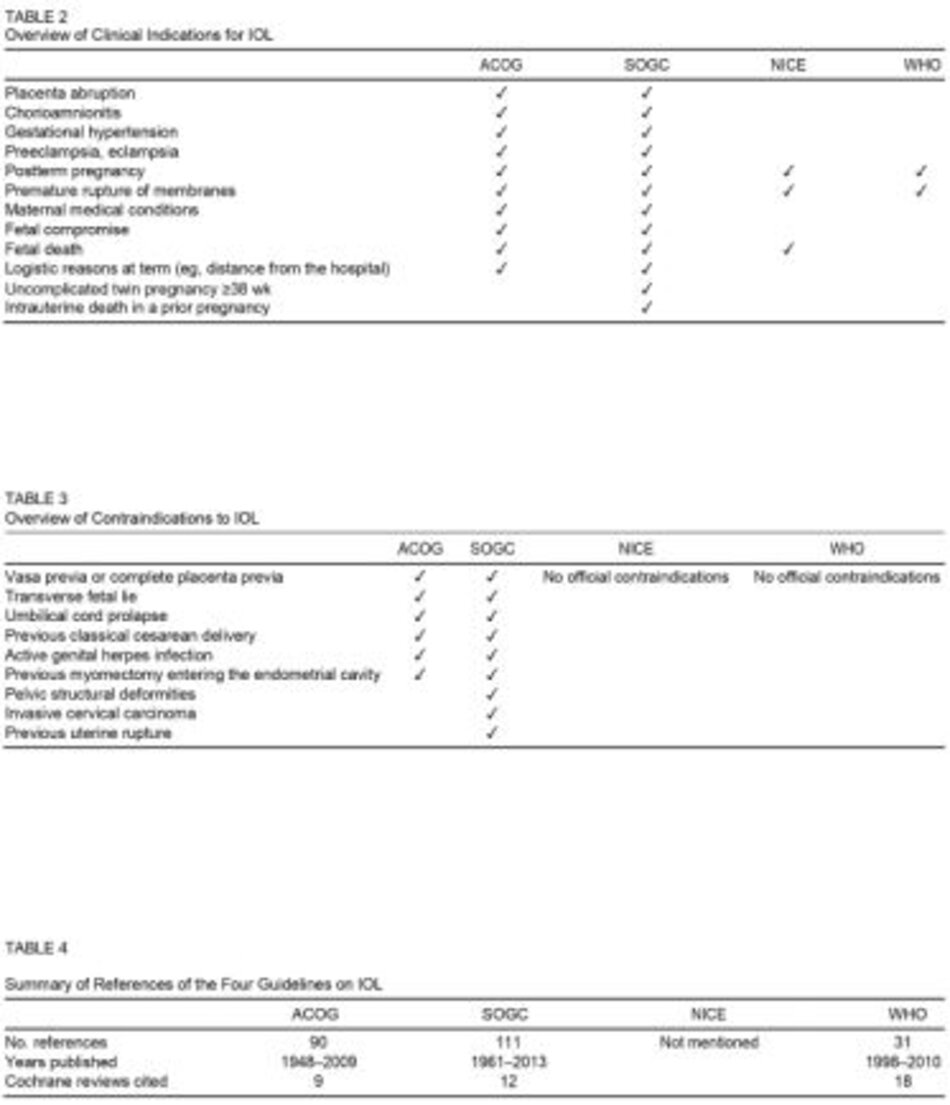
Tóm tắt các chỉ định lâm sàng và chống chỉ định IOL lần lượt được trình bày trong Bảng 2 và 3. Lưu ý, các chỉ định và chống chỉ định của ACOG và SOGC có vẻ rất giống nhau, trong khi NICE và WHO không đề cập các chống chỉ định cụ thể.
2.1 Thai già tháng
Liên quan đến các chỉ định được báo cáo, IOL được khuyến cáo chung để tránh thai kỳ kéo dài. Một số yếu tố nguy cơ đã được xác định đối với thai già tháng bao gồm con so, thai già tháng trước đó, mang thai bé trai và mẹ béo phì.16-20 Chấm dứt thai kỳ sau 42 tuần tuổi thai tương quan với gia tăng tỷ lệ trẻ sơ sinh nhập viện vào đơn vị chăm sóc tích cực, 21 thai to, đẻ khó do vai, 16,22-25 hội chứng thai quá trưởng thành, 26-28 thai chết lưu,29 và tử vong sơ sinh.30 Đối với mẹ, các vết rách tầng sinh môn, nhiễm trùng, băng huyết sau sinh và tỷ lệ sinh mổ31 dường như cũng tăng. Do đó, SOGC và NICE khuyến nghị IOL từ 41+0 đến 42+0 tuần tuổi thai, trong khi đó ACOG khuyến nghị khởi phát sau 42+ 0 và đến 42+ 6 tuần tuổi thai (có thể xem xét IOL từ 41+ 0 đến 42+ 0 tuần tuổi thai) . Ngoài ra, WHO tuyên bố rằng IOL được khuyến nghị cho những thai phụ biết chắc chắn là đã đạt 41 tuần tuổi thai trong các thai kỳ không biến chứng. Đối với từng trường hợp, nên thực hiện siêu âm để xác định ngày sinh chính xác. Năm 2016, WHO đã khuyến nghị sử dụng 1 lần siêu âm thường quy trước 24 tuần tuổi thai.32 Thực hiện khuyến nghị này có thể giúp ước tính tuổi thai chính xác, hỗ trợ thêm trong việc áp dụng các khuyến nghị.
về việc theo dõi thai trong thai già tháng, có một số lựa chọn, bao gồm test nonstress, test stress cơn co, trắc đồ sinh vật lý và trắc đồ sinh vật lý biến đổi.13 Một tổng quan Cochrane về việc theo dõi thai nhi ở gần 3000 thai kỳ nguy cơ cao không phát hiện sự khác biệt nào về tử vong chu sinh hoặc ở điểm Apgar dưới 7 tại thời điểm 5 phút giữa các nhóm test nonstress và trắc đồ sinh vật lý.33 Kết quả, không có đủ bằng chứng để xác định loại hoặc tần suất test tối uư. American College of Obstetricians and Gynecologists tuyên bố rằng có thể chỉ định bắt đầu theo dõi trước sinh lúc thai > 41 tuần tuổi, SOGC khuyến nghị đánh giá tình trạng sức khỏe của thai nhi hai lần mỗi tuần sau 41 tuần tuổi và NICE khuyến nghị nên theo dõi ít nhất hai lần mỗi tuần từ 42 tuần tuổi thai, trong khi WHO không đưa ra khuyến nghị nào về vấn đề này.
2.2 Gia tăng tuổi thai
Một thử nghiệm được công bố gần đây (năm 2018) với hơn 6000 thai phụ kết luận rằng IOL lúc 39 tuần tuổi thai ở nhũng phụ nữ mang thai con so có nguy cơ thấp không dẫn đến tần suất kết cục chu sinh bất lợi gộp chung thấp hơn đáng kể, nhưng tần suất mổ lấy thai thấp hơn đáng kể.34 Dựa trên các phát hiện được cho thấy trong thử nghiệm này, ACOG đã kết luận trong một Tư vấn thực hành rằng thực hiện IOL chủ động cho nhũng phụ nữ mang thai con so có nguy cơ thấp khi thai được 39 tuần tuổi có thể là hợp lý, dựa trên quyết định chung giữa thai phụ và bác sĩ sản khoa của cô ấy, cân nhắc các nguồn sẵn lực sẵn có.35 Bởi vì tất cả các hướng dẫn đều được xuất bản trước thử nghiệm ARRIVE,34 cho đến nay không có bất kỳ khuyến nghị chính thức nào được đưa ra, ngoại trừ từ Tư vấn thực hành ACOG.35 Một phân tích gộp gần đây phát hiện rằng, so với xử trí theo dõi, IOL ở 39 tuần tuổi có liên quan đến tần suất mổ lấy thai thấp hơn đáng kể (26,4% so với 29,1%; relative risk [RR], 0,83; confidence interval 95% [CI], 0,74-0,93) và nhiễm trùng chu sản (2,8% so với 5,2%; RR, 0,53; CI 95%, 0,39-0,72) và tỷ lệ mắc bệnh hô hấp sơ sinh thấp hơn (0,7% so với 1,5%; RR, 0,71; CI 95%, 0,59-0,85), hội chứng hít phân SU (0,7% so với 3,0%; RR, 0,49; 95 % CI, 0,26-0,92) và nhập viện vào đơn vị chăm sóc tích cực trẻ sơ sinh (3,5% so với 5,5%; RR, 0,80; CI 95%, 0,72-0,88) ,36 Ngoài ra, bằng chứng từ phân tích hiệu quả – chi phí cho thấy IOL ở phụ nữ mang thai con so lúc 39 tuần tuổi dẫn đến cải thiện kết cục nhưng gia tăng chi phí.37
Một tổng quan Cochrane thích hợp về 30 thử nghiệm ngẫu nhiên có đối chứng bao gồm 12.479 phụ nữ mang thai đủ tháng hoặc hơn.38 So với xử trí theo dõi, chính sách IOL có liên quan đến tỷ lệ tử vong chu sinh thấp hơn (RR, 0,33; CI 95%, 0,14-0,78) và thai chết lưu thấp hơn (RR, 0,33; CI 95%, 0,11-0,96). Đối với thai phụ trong nhóm khởi phát, tỷ lệ mổ lấy thai thấp hơn so với xử trí theo dõi (RR, 0,92; CI 95%, 0,85-0,99), nhưng tỷ lệ sinh ngả âm đạo vói sự hỗ trợ của dụng cụ tăng nhẹ (RR, 1,07; CI 95%, 0,99 -1.16).
2.3 Tuổi mẹ cao
Không có hướng dẫn nào đề xuất tuổi mẹ cao như một chỉ định để IOL. Trên thực tế, bằng chứng từ một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng thai phụ mang thai con so lớn tuổi (từ 35 tuổi trở lên) IOL ở 39 tuần tuổi thai, so với xử trí theo dõi, không ảnh hưởng đáng kể đến tỷ lệ mổ lấy thai và không có ảnh hưởng bất lợi ngắn hạn nào trên kết cục ở mẹ và trẻ sơ sinh.39
2.4 Vỡ ối non
Một tình trạng lâm sàng quan trọng khác được đề cập trong hướng dẫn là vỡ ối non (PROM). American College of Obstetricians and Gynecologists và NICE khuyến nghị IOL ở 34 tuần tuổi trong các trường hợp PROM thiếu tháng, trong khi SOGC ở 32 tuần tuổi nếu có thể xác nhận sự trưởng thành phổi của thai nhi.9,40 Ngoài ra, ACOG, SOGC và WHO khuyến nghị IOL trong các trường họp PROM đủ tháng và NICE tuyên bố rằng tất cả thai phụ bị PROM đủ tháng nên được lựa chọn IOL với prostaglandin E2 (PGE2) đặt âm đạo hoặc xử trí theo dõi. Một tổng quan Cochrane năm 2017 bao gồm 23 thử nghiệm đánh giá tác động của chấm dứt thai kỳ có kế hoạch (can thiệp ngay hoặc can thiệp trong vòng 24 giờ) khi so sánh với xử trí theo dõi (không can thiệp theo kế hoạch trong vòng 24 giờ) đối với thai phụ bị PROM đủ tháng. Thai phụ chấm dứt thai kỳ sớm theo kế hoạch giúp giảm nguy cơ mắc bệnh tật nhiễm trùng ở mẹ (nhiễm trùng ối và / hoặc viêm nội mạc tử cung) so với thai phụ được xử trí theo dõi sau PROM đủ tháng (RR mean, 0,49; CI 95%, 0,33-0,72) và trẻ sơ sinh của họ ít có khả năng bị hoặc có thể bị nhiễm trùng huyết sơ sinh khởi phát sớm (RR, 0,73; CI 95%, 0,58- 0,92).
2.5 Sinh ngả âm đạo sau mổ lấy thai
Khởi phát chuyển dạ để cố gắng sinh ngả âm đạo sau mổ lấy thai vẫn là một lựa chọn theo ACOG, SOGC và NICE, 42 trong khi WHO không đưa ra khuyến nghị. Trong những trường hợp như vậy, ACOG và WHO khuyến cáo không nên dùng misoprostol, trong khi SOGC tuyên bố rằng không nên dùng prostaglandin.42American College of Obstetricians and Gynecologists tuyên bố rằng rất khó đưa ra khuyến nghị về PGE2, trong khi NICE nói rằng thai phụ mổ lấy thai trước đó có thể thực hiện IOL với PGE2 đặt âm đạo, xem xét hoàn cảnh và mong muốn của thai phụ. Một tổng quan Cochrane kết luận rằng bằng chứng từ các thử nghiệm ngẫu nhiên có đối chứng về các phương pháp IOL cho thai phụ mổ lấy thai trước đó là không đầy đủ và các nghiên cứu hiện có không đủ mạnh để phát hiện những khác biệt có liên quan về mặt lâm sàng đối với nhiều kết cục.43 Đối với oxytocin, cả ACOG và SOGC đều tuyên bố rằng không chống chỉ định và có thể được dùng trong sinh ngả âm đạo sau mổ lấy thai trước đó.42
2.6 Thai chết lưu
Thai chết lưu vẫn là một biến cố bất lợi lớn và nghiên cứu đầu tiên mô tả IOL trong trường hợp này được xuất bản vào năm 1987.44 Cả 4 hiệp hội y khoa đều khuyến nghị lựa chọn IOL trong trường hợp thai chết lưu, trong khi NICE tuyên bố rằng thai phụ cũng có thể được xử trí theo dõi. Phương pháp IOL tối ưu bằng thuốc trong trường hợp thai chết lưu, ACOG khuyến nghị xử trí theo phác đồ sản khoa thông thường (misoprostol, oxytocin), NICE khuyến nghị mifepristone uống, sau đó dùng PGE2 đặt âm đạo hoặc misoprostol đặt âm đạo, và WHO khuyến cáo misoprostol uống hoặc đặt âm đạo. Một tổng quan Cochrane đánh giá dùng prostaglandin (đặc biệt là misoprostol) trong trường họp thai chết lưu.45 So với misoprostol uống, misoprostol đặt âm đạo có liên quan đến nguy cơ không sinh được qua ngả âm đạo trong vòng 24 giờ thấp hơn (RR, 0,37; CI 95%, 0,15 -0,87). Misoprostol đặt dưới lưỡi được phát hiện có hiệu quả hơn misoprostol đặt âm đạo để giảm nguy cơ không sinh được qua ngả âm đạo trong vòng 24 giờ (RR, 0,24; CI 95%, 0,08-0,74). Có một số dữ liệu hạn chế so sánh misoprostol đặt âm đạo với các prostaglandin khác. Khi so sánh misoprostol đặt âm đạo với prostaglandin F2 alpha (PGF2a), thai phụ dùng misoprostol đặt âm đạo cho thấy giảm nguy cơ nạo tử cung phẫu thuật (RR, 0,63; CI 95%, 0,41-0,98).
2.7 Thai to
Liên quan đến thai to, SOGC, NICE và WHO tuyên bố rằng IOL khi đủ tháng không được khuyến nghị cho nhừng trường hợp này, trong khi ACOG không đưa ra khuyến nghị. Một tổng quan Cochrane bao gồm 4 thử nghiệm lâm sàng đánh giá ảnh hưởng của IOL tại thời điểm hoặc ngay trước khi đủ tháng mà nghi ngờ thai to về cách thức sinh và bệnh tật ở mẹ hoặc chu sinh.46 So với xử trí theo dõi, không có ảnh hưởng rõ ràng của IOL đối với nghi ngờ thai to trên nguy cơ mổ lấy thai (RR, 0,91; CI 95%, 0,76-1,09) hoặc sinh bàng dụng cụ (RR, 0,86; CI 95%, 0,65-1,13). Mặt khác, đẻ khó do vai (RR, 0,60; ci 95%, 0,37-0,98) và gãy xương (bất kỳ) (RR, 0,20; CI 95%, 0,05-0,79) đã giảm ở nhóm IOL.
2.8 Đa thai
về song thai, SOGC chỉ khuyến nghị IOL cho những trường họp song thai không biến chứng >38 tuần tuổi, trong khi các hiệp hội khác không đưa ra khuyến cáo. Một tổng quan liên quan của Cochrane bao gồm 2 thử nghiệm ngẫu nhiên có đối chứng so sánh kết cục của mẹ và trẻ sơ sinh trong các trường họp song thai thực hiện chấm dứt thai kỳ chủ động từ 37 tuần tuổi so với xử trí theo dõi.47 Không phát hiện sự khác biệt có ý nghĩa thống kê liên quan đến mổ lấy thai (RR, 1,05 ; CI 95%, 0,83-1,32), tử vong chu sinh hoặc bệnh tật chu sinh nghiêm trọng (RR, 0,34; CI 95%, 0,01 8,35), hoặc tử vong mẹ hoặc bệnh tật nghiêm trọng ở mẹ (RR, 0,29; CI95%, 0,06-1,38).
2.9 Đái tháo đường trong thai kỳ
Đối với đái tháo đường trong thai kỳ, ACOG tuyên bố rằng thời điểm chấm dứt thai kỳ trong các trường hợp đái tháo đường thai kỳ (GDM) được kiểm soát chỉ bằng chế độ ăn uống và tập luyện không được thực hiện trước 39 tuần tuổi thai, trừ khi có chỉ định khác. Ở những thai phụ như vậy, xử trí theo dõi lên đến 406/7 tuần tuổi thai trong bối cảnh xét nghiệm tiền sản được chỉ định nhìn chung là thích hợp.48 Đối với thai phụ bị GDM được kiểm soát tốt bằng thuốc, khuyến cáo chấm dứt thai kỳ từ 390/7 đến 396/7 tuần 48 Đối với thai phụ bị GDM hoặc đái tháo đường tiền thai kỳ, SOGC khuyến cáo khởi phát từ 38 đến 40 tuần tuổi thai, phụ thuộc vào tình trạng kiểm soát đường huyết của họ và các yếu tố bệnh đi kèm khác.49 National Institute for Health and Care Excellence khuyến nghị IOL từ 37 đến 39 tuần tuổi thai đối với thai phụ bị đái tháo đường type 1 hoặc 2 và gợi ý khuyến nghị thai phụ bị GDM không biến chứng nên chấm dứt thai kỳ < 40 + 6 tuần tuổi thai.50 Tổ chức Y tế Thế giới tuyên bố rằng nếu GDM là bất thường duy nhất, không khuyến cáo IOL trước 41 tuần tuổi thai. Một tổng quan Cochrane về một thử nghiệm duy nhất trên 200 thai phụ bị đái tháo đường cần insulin so sánh chính sách IOL chủ động khi thai đủ 38 tuần tuổi với xử trí theo dõi cho đến 42 tuần.51 Nguy cơ mổ lấy thai không có sự khác biệt có ý nghĩa thống kê giữa các nhóm (RR, 0,81; CI 95%, 0,52-1,26). Tuy nhiên, nguy cơ thai to đã giảm ở nhóm khởi phát sớm (RR, 0,56; CI 95%, 0,32-0,98), và 3 trường họp đẻ khó do kẹt vai nhẹ đã được báo cáo ở nhóm xử trí theo dõi. Không có bệnh tật chu sinh nào được báo cáo.
3. Các phương pháp khởi phát
Trước khi bắt đầu IOL, tất cả thai phụ cần được thông báo về các chỉ định của IOL, các phương pháp khởi phát và các nguy cơ đi kèm, bao gồm cả việc khởi phát thất bại và nguy cơ mổ lấy thai đi kèm. 11,12 cần lưu ý rằng, trong các trường hợp IOL, tiến triển của chuyển dạ khác với các trường hợp có khởi phát chuyển dạ tự phát.52 Yếu tố dự đoán tốt nhất để IOL thành công là tình trạng cổ tử cung, được đánh giá bằng điểm Bishop.53Được phát triển lần đầu vào năm 1964, điểm Bishop bao gồm 5 thông số (vị trí ngôi thai, xóa, mở, tư thế, và mật độ cổ tử cung), và mỗi lần đánh giá cổ tủ’ cung có thể có điểm số tối đa là 13.53 Một số tổng quan hệ thống đã chứng minh rằng điểm Bishop dự đoán IOL thành công tốt hơn fibronectin của thai nhi hoặc chiều dài cổ tủ’ cung trên siêu âm và tình trạng mở cổ tủ’ cung là thông số quan trọng nhất của điểm Bishop. 54,55
3.1 Lóc màng ối
Một phương pháp đơn giản được tất cả các hướng dẫn khuyến nghị như một cách để giảm nhu cầu dùng các phương pháp IOL khác là lóc màng ối ,9-12 Cụ thể hơn, NICE khuyến nghị lóc màng ối ở các lần khám tiền sản lúc 40 và 41 tuần đối với phụ nữ mang thai con so và ở lần khám thai lúc 41 tuần đối với phụ nữ mang thai con rạ. Lóc màng ối bao gồm đưa 1 ngón tay qua lỗ trong, sau đó xoay xung quang ngón tay ba lần, điều này gây bong các màng thai khỏi đoạn dưới tử cung.11 Sự can thiệp này gây tăng đáng kể hoạt tính của phospholipase A2 và nồng độ PGF2a, càng ngày càng tăng, theo cách như vậy, khả năng khởi phát chuyển dạ tự phát trong vòng 48 giờ và giảm nhu cầu khởi phát bằng các phương pháp khác.56’57 Một tổng quan Cochrane so sánh lóc màng ối với xử trí theo dõi và phát hiện rằng lóc màng ối có liên quan đến giảm 40% nguy cơ của IOL chính thức (RR, 0,60; CI 95%, 0,51-0,71) ,57 Hơn nữa, nguy cơ không chuyển dạ hoặc không sinh trong vòng 48 giờ cũng thấp hơn 23% (RR, 0,77; CI 95%, 0,70- 0,84). So với xử trí theo dõi, có sự gia tăng nguy cơ chảy máu âm đạo và khó chịu trong khi khám âm đạo khi lóc màng ối.
Lưu ý, liên quan đến kích thích núm vú, quan hệ tình dục, bổ sung thảo dược, châm cứu, vi lượng đồng căn và các phương pháp tương tự khác, không có đủ bằng chứng để khuyến nghị các phương pháp đó cho IOL.
3.2 Phương pháp cơ học
về các phương pháp IOL cơ học, ACOG, SOGC, WHO tuyên bố rằng khuyến nghị IOL bằng một ống thông có bóng, trong khi NICE nói rằng không nên sử dụng thường quy các thủ thuật cơ học. Tổ chức Y tế Thế giới cũng khuyến cáo kết hợp ống thông có bóng với oxytocin như một phương pháp khởi phát thay thế khi không có sẵn prostaglandin hoặc bị chống chỉ định. Lưu ý, một tổng quan hệ thống bao gồm 43 nghiên cứu báo cáo nguy cơ nhiễm trùng mẹ trong khi sinh nhìn chung là gần 10% khi dùng ống thông có bóng để làm chín muồi cổ tử cung.58 Một tổng quan Cochrane so sánh tác dụng của các phương pháp cơ học để làm chín muồi cổ từ cung trong ba tháng cuối thai kỳ hoặc IOL với giả dược / không điều trị, prostaglandin và oxytocin.59Sau khi so sánh các phương pháp cơ học với PGE2 đặt âm đạo, tỷ lệ thai phụ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ không có sự khác biệt đáng kể (RR, 1,72; CI 95%, 0,90- 3,27). Tuy nhiên, đối với phân nhóm phụ nữ mang thai con rạ, nguy cơ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ cao hơn (RR, 4,38; CI 95%, 1,74-10,98), không tăng số ca mổ lấy thai (RR, 1,19; CI 95%, 0,62 -2,29). Các phương pháp cơ học làm giảm nguy cơ các cơn co tử cung mau gây thay đổi nhịp tim thai khi so sánh với prostaglandin đặt âm đạo (PGE2 RR, 0,16 [95% CI, 0,06-0,391;và misoprostol RR, 0,37 [95% CI, 0,25-0,54]). Phương pháp cơ học so với khởi phát bằng oxytocin làm giảm nguy cơ mổ lấy thai (RR, 0,62; CI95%, 0,42-0,90).
3.3 Prostaglandin
Đối với các lựa chọn IOL bằng thuốc, prostaglandin được sử dụng rộng rãi, và đặc biệt, PGE2 được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt để làm chín muồi cổ tử cung.12 Dùng gel PGE2 trong cổ tử cung có 1% nguy cơ gây cơn co tử cung mau với thay đổi nhịp tim thai, trong khi gel PGE2 trong âm đạo và viên đặt âm đạo có liên quan đến 5% nguy cơ.60 62 Các tác dụng bất lợi đối với mẹ khi dùng PGE2 bao gồm sốt, nôn và tiêu chảy nhưng không thường gặp.63 American College of Obstetricians and Gynecologists, SOGC, và NICE tuyên bố rằng PGE2 là thuốc hiệu quả để làm chín muồi cổ tử cung và IOL trong trường hợp cổ tử cung không thuận lợi, trong khi WHO nói rằng nên dùng liều thấp prostaglandin âm đạo (PGE2 và PGF2a). National Institute for Health and Care Excellence cũng tuyên bố rằng 1 chu kỳ dùng viên nén hoặc gel PGE2 âm đạo (1 liều, tiếp theo là liều thứ hai sau 6 giờ nếu chưa chuyển dạ — tối đa 2 liều) hoặc 1 chu kỳ vòng nâng phóng thích PGE2 có kiểm soát trong âm đạo (1 liều trong 24 giờ) là phác đồ thích hợp, ngoài ra dùng vào buổi sáng có liên quan đến sự hài lòng của bà mẹ cao hơn. về việc theo dõi thai nhi sau khi dùng PGE2, cần theo dõi liên tục nhịp tim thai và cơn co tử cung trong ít nhất 30 phút.10-12 Khoảng thời gian tối thiểu giữa các lần dùng prostaglandin và oxytocin, nhà sản xuất tuyên bố rằng sau khi dùng 1,5 mg dinoprostone trong cổ tử cung hoặc 2,5 mg trong âm đạo, nên trì hoãn dùng oxytocin trong 6 đến 12 giờ. Sau khi dùng dinoprostone ở dạng phóng thích kéo dài, nên trì hoãn dùng oxytocin trong 30 đến 60 phút sau khi lấy bỏ.12 Một tổng quan Cochrane cho thấy PGE2 âm đạo so với giả dược hoặc không điều trị làm giảm khả năng không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ. Tuy nhiên, nguy cơ cơn co tủ’ cung mau với thay đổi nhịp tim thai tăng gần gấp 5 lần (4,8% so với 1,0%; RR, 3,16; CI 95%, 1,67-5,98) ,64 Một tổng quan Cochrane khác cho thấy dùng PGE2 so với không điều trị hoặc giả dược có liên quan đến gần một nửa số ca mổ lấy thai (RR, 0,54; CI 95%, 0,29-0,98) ,65 Một tổng quan Cochrane thứ ba so sánh việc dùng PGE2 trong cổ tử cung với giả dược hoặc không điều trị và phát hiện rằng PGE2 làm giảm số lượng thai phụ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ (RR, 0,61; CI 95%, 0,47-0,79) ,66 PGE2 trong cổ tử cung gia tăng nguy cơ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ so với PGE2 âm đạo (RR, 1,26; 95% CI, 1,12-1,41), trong khi không có thay đổi về nguy cơ mổ lấy thai (RR, 1,07; 95% CI, 0,93-1,22). Hơn nữa, nguy cơ cơn co tử cung mau với thay đổi nhịp tim thai (RR, 0,76; CI 95%, 0,39-1,49) và không thay đổi nhịp tim thai (RR, 0,80; CI95%, 0,56-1,15) không khác nhau giữa 2 cách dùng PGE2.
Misoprostol là một chất tương tụ’ PGE1 tổng họp đã được FDA phê duyệt để phòng ngừa và điều trị loét dạ dày.67 Năm 2002, FDA cũng đã phê duyệt việc dùng misoprostol trong thai kỳ để làm chín muồi cổ tử cung và IOL.12 Sự gia tăng nước ối nhuộm phân su đã được báo cáo khi dùng misoprostol, trong khi đó, corn co tử cung mau xảy ra thường xuyên horn với misoprostol âm đạo so với PGE2 âm đạo, PGE2 trong cổ tử cung, hoặc oxytocin.68American College of Obstetricians and Gynecologists, SOGC, and WHO tuyên bố rằng misoprostol có thể được coi là một thuốc an toàn và hiệu quả để IOL; tuy nhiên, NICE tuyên bố rằng misoprostol chỉ nên dùng như một phưorng pháp IOL trong trường hợp thai chết lưu hoặc trong bối cảnh thử nghiệm lâm sàng. American College of Obstetricians and Gynecologists gợi ý rằng liều lượng thích hợp là 25 pg mỗi 3 đến 6 giờ (50 pg mỗi 6 giờ có thể phù hợp trong một số trường họp), SOGC khuyến cáo 50 pg uống với nước hoặc 25 pg đặt âm đạo mỗi 4 giờ, trong khi WHO khuyến cáo 25 mg misoprostol uống mỗi 2 giờ hoặc 25 mg misoprostol đặt âm đạo mỗi 6 giờ để IOL. cần đánh giá tình trạng sức khỏe của thai nhi trước khi dùng misoprostol và theo dõi thai điện tử ít nhất 30 phút sau khi dùng thuốc.11 Không nên bắt đầu dùng oxytocin sớm hon 4 giờ sau liều misoprostol cuối cùng. 11,12 Một phân tích gộp mạng lưới so sánh việc dùng misoprostol, dinoprostone và ống thông có bóng để làm chín muồi cổ tử cung và kết luận rằng không có phương pháp nào vượt trội rõ ràng.69 Một tổng quan Cochrane xác định tác dụng của misoprostol đặt âm đạo để làm chín muồi cổ tử cung hoặc IOL trong ba tháng cuối thai kỳ.68 So với giả dược, misoprostol có liên quan đến việc giảm tỷ lệ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ (RR, 0,51; CI 95%, 0,37-0,71); tuy nhiên, gia tăng cơn co tử cung mau (RR, 3,52; CI 95%, 1,78-6,99). So với PGE2 âm đạo, PGE2 trong cổ tử cung và oxytocin, misoprostol âm đạo có liên quan đến ít dùng thuốc giảm đau ngoài màng cứng hơn, đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ cao hơn, nhưng lại có nhiều cơn co tử cung mau hơn. So với PGE2 âm đạo hoặc trong cổ tử cung, tăng cường chuyển dạ bằng oxytocin ít phổ biến hơn so với misoprostol, nhưng thường gặp nước ối nhuốm phân su hon. Một tổng quan Cochrane khác bao gồm 9 thử nghiệm (1109 phụ nữ) so sánh misoprostol đường uống với giả dược để khởi phát chuyển dạ ở phụ nữ có thai sống.70 Thai phụ dùng misoprostol đường uống có khả năng sinh con qua đường âm đạo trong vòng 24 giờ cao hơn (RR, 0,16; CI 95%, 0,05 -0,49) và số ca mổ lấy thai ít hơn (RR, 0,72; CI 95%, 0,54-0,95). Khi so sánh với misoprostol đặt âm đạo, prostaglandin đặt âm đạo (dinoprostone) hoặc oxytocin tĩnh mạch, misoprostol đường uống không có sự khác biệt về tần suất sinh ngả âm đạo trong vòng 24 giờ hoặc cơn co tử cung mau với thay đổi nhịp tim thai. Năm thử nghiệm (681 phụ nữ) so sánh việc dùng misoprostol đường uống với PGE2 trong cổ tử cung. Misoprostol đường uống có liên quan đến tỷ lệ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ thấp hơn (RR, 0,78; CI 95%, 0,63-0,97) nhưng tỷ lệ cơn co tử cung mau với thay đổi nhịp tim thai cao hơn (RR, 3,57; CI 95%, 1.11-11.54). Một tổng quan Cochrane thứ ba xác định tính hiệu quả và an toàn của misoprostol đặt bên má hoặc ngậm dưới lưỡi để làm chín muồi cổ tử cung và IOL trong ba tháng cuối thai kỳ.71 Đường dùng đặt bên má có liên quan đến xu hướng mổ lấy thai ít hơn so với đường âm đạo (18/73 so với 28/79; RR, 0,70; CI 95%, 0,42-1,15). Không có sự khác biệt đáng kể đối với bất kỳ kết cục nào khác. Khi cùng một liều lượng được dùng dưới lưỡi so với đặt bên má, không có sự khác biệt đáng kể nào được xác định về tỷ lệ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ, tăng cường chuyển dạ bằng oxytocin hoặc mổ lấy thai.
3.4 Bấm ối
Bấm ối là phương pháp IOL bằng ngoại khoa.9 Các nguy cơ tiềm ẩn liên quan đến bấm ối bao gồm sa dây rốn, nhiễm trùng ối, chèn ép dây rốn và vỡ mạch máu tiền đạo.12 Chống chỉ định bấm ối bao gồm nhau tiền đạo, mạch máu tiền đạo và nhiễm trùng đường sinh dục đang hoạt động.11,72 American College of Obstetricians and Gynecologists tuyên bố rằng bấm ối có thể được dùng như một phương pháp IOL, trong khi SOGC nói rằng bấm ấm chỉ nên dành cho những sản phụ có cổ tử cung thuận lợi, hơn nữa nên thận trọng ở trường hợp ngôi chưa cố định và nên dùng oxytocin sớm sau khi bấm ối để khởi phát chuyển dạ. National Institute for Health and Care Excellence tuyên bố rằng bấm ối đơn thuần hoặc với oxytocin không nên được dùng như một phương pháp IOL chính trừ khi có những lý do lâm sàng cụ thể để không dùng PGE2 âm đạo. Cuối cùng, Tổ chức Y tế Thế giới tuyên bố rằng bấm ối đơn thuần không được khuyến cáo để IOL. Một tổng quan Cochrane xác định tác dụng của bấm ối để khởi phát chuyển dạ trong ba tháng cuối thai kỳ ở sản phụ mang thai sống.73 Không có kết luận nào được rút ra khi so sánh giữa bấm ối đơn thuần với không can thiệp và bấm ối đơn thuần với oxytocin đơn thuần. Một tổng quan Cochrane khác đánh giá hiệu quả và độ an toàn của phương pháp bấm ối và oxytocin tĩnh mạch để IOL trong ba tháng cuối thai kỳ.74
3.5 Oxytocin
Năm 1948, Theobald và cộng sự lần đầu tiên mô tả việc dùng oxytocin để IOL. Cơ tử cung bắt đầu đáp ứng với oxytocin sau khi truyền 3 đến 5 phút và đạt được nồng độ oxytocin ổn định trong huyết tương sau 40 phút.76 Các tác dụng bất lợi của oxytocin chủ yếu liên quan đến liều lượng: cơn co tủ’ cung mau, nhịp tim thai bất thường, hạ huyết áp, ngộ độc nước, và hiếm gặp, vỡ tử cung. H’12’77’78 Cả ACOG và SOGC đều tuyên bố rằng cả hai phác đồ oxytocin liều thấp và cao (liều thấp: liều ban đầu 0,5-2 mU / phút, liều tăng dần 1-2 mU / phút, và khoảng cách liều 15^40 phút; liều cao: liều ban đầu 4-6 mU / phút, liều tăng dần 3- 6 mU / phút, và khoảng cách liều 15-40 phút) có thể được xem xét và thích hợp để khởi phát chuyển dạ. National Institute for Health and Care Excellence nói rằng không nên dùng oxytocin tĩnh mạch đơn thuần để IOL; tuy nhiên, WHO khuyến cáo rằng trong những trường họp không có sẵn prostaglandin, nên dùng oxytocin tĩnh mạch đơn thuần để IOL. Sau khi bắt đầu dùng oxytocin, nên theo dõi tốc độ truyền oxytocin, đáp úng của tử cung và nhịp tim thai.10,12 Một tổng quan Cochrane xác định tác dụng của oxytocin đơn thuần để làm chín muồi cổ tử cung và IOL trong ba tháng cuối thai kỳ khi so sánh với các phương pháp IOL khác hoặc giả dược / không điều trị.79 Khởi phát chuyển dạ bằng oxytocin có liên quan đến tỷ lệ không đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ thấp hơn so với xử trí theo dõi (8,4% so với 53,8%; RR, 0,16; CI 95%, 0,10- 0,25). Tuy nhiên, có sự gia tăng đáng kể số sản phụ cần giảm đau ngoài màng cứng (RR, 1,10; CI 95%, 1,04-1,17). So với prostaglandin đặt âm đạo, oxytocin làm tăng tỷ lệ sinh ngả âm đạo không thành công trong vòng 24 giờ trong 2 thử nghiệm báo cáo kết cục này (70% so với 21%; RR, 3,33; CI 95%, 1,61-6,89), nhưng có một sự gia tăng nhỏ số sản phụ cần giảm đau ngoài màng cứng khi dùng oxytocin đơn thuần (RR, 1,09; CI 95%, 1,01-1,17). Khi so sánh oxytocin với các prostaglandin trong cổ tử cung, có sự gia tăng số ca sinh ngả âm đạo không thành công trong vòng 24 giờ (50,4% so với 34,6%; RR, 1,47; CI 95%, 1,10-1,96) và gia tăng số ca mổ lấy thai (19,1% so với 13,7% ; RR, 1,37; CI 95%, 1,08-1,74) ở nhóm oxytocin. Cuối cùng, một phân tích gộp mạng lưới năm 2016 đã kết luận rằng dùng oxytocin tĩnh mạch cộng với bấm ối và dùng misoprostol đặt âm đạo là 2 cách tiếp cận hiệu quả nhất để đạt được mục tiêu sinh ngả âm đạo trong vòng 24 giờ.80
4. Biến chứng
4.1 Cơn co tử cung mau
Prostaglandin và oxytocin có thể dẫn đến tình trạng cơn co tử cung mau có hoặc không có biểu đồ nhịp tim thai bất thường.81-83 Trong những trường hợp này, nếu không đáp ứng với các biện pháp điều chỉnh thông thường (lấy bỏ prostaglandin ra khỏi âm đạo, thay đổi tư thế mẹ, oxy bổ sung, truyền dịch, và giảm hoặc ngừng truyền oxytocin), có thể xem xét mổ lấy thai.83 American College of Obstetricians and Gynecologists tuyên bố rằng có thể xem xét dùng terbutaline hoặc các thuốc giảm co khác, trong khi SOGC tuyên bố rằng có thể dùng nitroglycerin nhưng cần phải nghiên cứu thêm. National Institute for Health and Care Excellence tuyên bố rằng nên xem xét dùng thuốc giảm co nếu xảy ra tình trạng cơn co tử cung mau trong quá trình IOL, trong khi đó WHO khuyến cáo dùng betamimetics. Một tổng quan Cochrane đánh giá tác dụng của liệu pháp giảm co đối với các trường hợp nghi ngờ thai suy trên kết cục của thai nhi, bà mẹ và chu sinh.84 So với không điều trị, có nhiều cải thiện hơn về các bất thường nhịp tim thai với liệu pháp giảm co (RR, 0,26; CI 95%, 0,13 -0,53).
Liệu pháp betamimetic so với magnesium sulfat cho thấy xu hướng làm giảm tình trạng cơn co tử cung mau không có ý nghĩa (RR, 0,07; CI 95%, 0,00-1,10).
4.2 Khởi phát chuyển dạ thất bại
Liên quan đến IOL thất bại, một hội thảo được triệu tập bởi us National Institute of Child Health and Human Development, the Society of Maternal-Fetal Medicine, và ACOG đã đề xuất rằng khởi phát chuyển dạ thất bại nên được xác định theo các tiêu chí sau85: (1) Bấm ối, nếu an toàn và khả thi. Sau khi vỡ ối, khởi phát chuyển dạ có thể được xem là thất bại nếu các cơn co đều đặn và không có sự thay đổi cổ tử cung xảy ra sau ít nhất 12 đến 18 giờ dùng oxytocin. (2) Nếu các màng ối còn nguyên vẹn, khởi phát chuyển dạ có thể được xem là thất bại nếu không tạo ra được các cơn co đều đặn mỗi khoảng 3 phút và không có sự thay đổi cổ tử cung sau ít nhất 24 giờ dùng oxytocin. Thời gian dành cho quá trình làm chín muồi cổ tử cung không được tính vào thời gian khởi phát hoặc chẩn đoán khởi phát chuyển dạ thất bại. Bằng cách cho phép giai đoạn tiềm tàng kéo dài trong 24 giờ hoặc hơn và dùng oxytocin trong 12 đến 18 giờ sau khi vỡ ối, có thể tránh được nhiều ca mổ lấy thai.86 American College of Obstetricians and Gynecologists tuyên bố rằng thời gian tiềm tàng được cho phép ít nhất 12 đến 18 giờ trước khi chẩn đoán khởi phát chuyển dạ thất bại có thể làm giảm nguy cơ mổ lấy thai.87,88Society of Obstetricians and Gynaecologists of Canada tuyên bố rằng các nhân viên y tế cần cân nhắc khi khởi phát chuyển dạ cho sản phụ có cổ tử cung không thuận lợi liên quan đến tỷ lệ thất bại cao hơn ở bệnh nhân mang thai con so và tỷ lệ mổ lấy thai cao hơn cả ở bệnh nhân mang thai con so và con rạ. Theo NICE, nếu khởi phát thất bại, các lựa chọn xử trí tiếp theo bao gồm thử khởi phát chuyển dạ thêm (thời điểm tùy thuộc vào tình trạng lâm sàng và mong muốn của sản phụ) hoặc mổ lấy thai. Tổ chức Y tế Thế giới tuyên bố rằng IOL thất bại không nhất thiết chỉ định mổ lấy thai.
4.3 Quản lý bệnh nhân ngoại trú
về vấn đề quản lý bệnh nhân ngoại trú trong các trường hợp IOL, ACOG tuyên bố rằng khởi phát chuyển dạ ở bệnh nhân ngoại trú có thể thích hợp ở các bệnh nhân được lựa chọn cẩn thận, trong khi SOGC tuyên bố rằng dùng prostaglandin ngoại trú là một lựa chọn hấp dẫn để giảm sử dụng các nguồn lực chăm sóc sức khỏe. National Institute for Health and Care Excellence tuyên bố rằng thực hiện IOL ngoại trú nên được kiểm tra liên tục và WHO tuyên bố rằng không khuyến cáo IOL ngoại trú để cải thiện kết cục sinh. Một tổng quan Cochrane đánh giá ảnh hưởng của IOL đối với kết cục của mẹ và trẻ sơ sinh ở nhũng sản phụ được quản lý ngoại trú so với nội trú.89 PGE2 đặt âm đạo, PGE2 giải phóng có kiểm soát, hoặc ống thông Foley, không có sự khác biệt giữa sản phụ được quản lý ngoại trú so với nội trú với hầu hết các kết cục được xem xét. Một tổng quan Cochrane khác đánh giá các can thiệp bằng thuốc và cơ học để khởi phát chuyển dạ hoặc làm chín muồi cổ tử cung ở những cơ sở ngoại trú.90 Có ít phụ nữ trong nhóm PGE2 đặt âm đạo cần thêm các thuốc để gây chuyển dạ (RR, 0,52; CI 95%, 0,27-0,99). Không có sự khác biệt rõ ràng giữa những sản phụ dùng PGE2 đặt âm đạo, PGE2 trong cổ tử cung, hoặc misoprostol đặt âm đạo và những người không điều trị hoặc giả dược về tỷ lệ cơn co tử cung mau, mổ lấy thai hoặc nhập viện vào đơn vị chăm sóc tích cực sơ sinh. Một tổng quan Cochrane thứ ba trên 2616 phụ nữ kết luận rằng IOL ở cơ sở ngoại trú có vẻ khả thi, nhưng không có đủ bằng chứng để xác định phương pháp khởi phát nào được ưu tiên bởi sản phụ hoặc can thiệp nào hiệu quả và an toàn nhất để sử dụng ở cơ sở ngoại trú.91
5. Tham khảo
Số lượng tài liệu tham khảo cho mỗi hướng dẫn nằm trong khoảng từ 31 (WHO) đến 111 (SOGC) với ngày xuất bản từ năm 1948 đến năm 2013. cần lưu ý rằng các hướng dẫn của NICE, giống như hầu hết các hướng dần từ hiệp hội / tác giả này, không đề cập đến bất kỳ tài liệu tham khảo nào. Các tài liệu tham khảo tù’ tất cả các hướng dẫn, cũng như tất cả các tổng quan Cochrane được trích dẫn, tóm tắt trong Bảng 4.
6. Kết luận
Khởi phát chuyển dạ là một can thiệp sản khoa phổ biến liên quan đến những nguy cơ tiềm ẩn cho mẹ và thai nhi / trẻ sơ sinh và chỉ nên thực hiện khi có chỉ định y tế rõ ràng để chấm dứt thai kỳ. Lưu ý, nhiều chỉ định và chống chỉ định tương tự nhau được xác định giữa ACOG và SOGC để IOL, trong khi NICE và WHO không đề cập đến bất kỳ chống chỉ định nào. Thời điểm IOL ở thai già tháng cũng khác nhau giữa các hướng dẫn, nhưng không nên trước 41 tuần tuổi thai, về phương pháp khởi phát, có sự đồng thuận chung về việc dùng phương pháp lóc màng ối, phương pháp cơ học, prostaglandin và oxytocin, trong khi NICE lập luận chống lại việc dùng misoprostol để IOL. American College of Obstetricians and Gynecologists và SOGC coi bấm ối là một phương pháp IOL, trong khi NICE và WHO không khuyến cáo phương pháp này. Tất cả các hướng dẫn cũng đưa ra các khuyến nghị tương tự nhau liên quan đến việc xử trí tình trạng cơn co tử cung mau bằng các thuốc giảm co trong các trường hợp IOL. Ngoài ra, các hướng dẫn của WHO dường như là dựa trên bằng chứng nhiều nhất, với mọi khuyến nghị đều dựa trên các tổng quan Cochrane, trong khi hướng dẫn của SOGC được xuất bản gần đây nhất. Cuối cùng, mỗi hướng dẫn đều dựa trên các chính sách chăm sóc sức khỏe khác nhau; mỗi cơ sở y tế nên áp dụng các hướng dẫn cụ thể và thông báo cho các bác sĩ lâm sàng về các khuyến nghị địa phương đối với IOL.
Điểm mạnh chính của tổng quan này là tổng hợp các hướng dẫn từ các tổ chức y tế có ảnh hưởng lớn về các chỉ định lâm sàng và các phương pháp thích hợp được khuyến nghị. Mặc dù bài tổng quan chỉ giới hạn ở 4 hướng dẫn bằng tiếng Anh, nhưng nó đã tóm tắt hầu hết các tài liệu y văn hiện có.
Các nhân viên y tế và các nhà hoạch định chính sách cần cập nhật các khuyến nghị để tối ưu hóa chất lượng chăm sóc và thúc đẩy hơn nữa việc áp dụng y học dựa trên bằng chứng.
7. Tham khảo
1. Managing Complication in Pregnancy and Childbirth: A Guide for Midwives and Doctors. 2nd ed. Geneva, Switzerland: World Health Organization; 2017. Available at: http://apps.who.int/ĩris/bitstream/handle/10665/255760/9789241565493-eng.pdf? sequence=1.
2. Caughey AB, Sundaram V, Kaimal AJ, et al. Maternal and neona-tal outcomes of elective induction of labor. Evid Rep Technol As-sess (Full Rep). 2009; 1-257.
3. Declercq ER, Sakala c, Corry MP, et al. Listening to Mothers II: report of the second National U.S. Survey of Women’s Childbear¬ing Experiences: conducted January-February 2006 for Child-birth Connection by Harris Interactive(R) in partnership with Lamaze International. J Perinat Educ. 2007;16:9-14.
4. Martin JA, Hamilton BE, Sutton PD, et al. Births: final data for 2005. Natl Vital stat Rep. 2007;56:1-103.
5. Vogel JP, Souza JP, Gulmezoglu AM. Patterns and Outcomes of Induction of Labour in Africa and Asia: a secondary analysis of the WHO Global Survey on Maternal and Neonatal Health. PLoS One. 2013;8:e65612.
6. Guerra GV, Cecatti JG, Souza JP, et al. Elective induction versus spontaneous labour in Latin America. Bull World Health Organ. 2011;89:657-665.
7. Tunẹalp o, Were WM, MacLennan c, et al. Quality of care for pregnant women and newborns—the WHO vision. BJOG. 2015;122:1045-1049.
8. World Health Organization. WHO Recommendations: Induction of Labour at or Beyond Term. 2018. Available at: https://apps. who.int/iris/bitstream/handle/10665/277233/9789241550413- eng.pdf?ua=1. Accessed August 26, 2019.
9. National Institute for Health and Care Excellence. Inducing La¬bour. Clinical Guideline. Published July 23, 2008. Available at: nice.org.uk/guidance/cg70. Accessed August 26, 2019.
10. World Health Organization. WHO Recommendations for Induc¬tion of Labour. 2011. Available at: http://apps.who.inưiris/bitstream/handle/10665/44531/9789241501156_eng.pdf? sequence=1. Accessed August 26, 2019.
11. Leduc D, Biringer A, Lee L, et al. Induction of labour. J Obstet Gynaecol Can 2013;35:840-857.
12. The American College of Obstetricians and Gynecologists. ACOG Practice Bulletin Number 107. Induction of Labor. August 2009.
13. The American College of Obstetricians and Gynecologists. ACOG Practice Bulletin Number 146. Management of Late- Term and Postterm Pregnancies. August 2014.
14. Mozurkewich E, Chilimigras J, Koepke E, et al. Indications for induc¬tion of labour: a best-evidence review. BJOG. 2009;116:626-636.
15. Guerra GV, Cecatti JG, Souza JP, et al. Factors and outcomes associated with the induction of labour in Latin America. BJOG. 2009;116:1762-1772.
16. Campbell MK, Ostbye T, Irgens LM. Post-term birth: risk factors and outcomes in a 10-year cohort of Norwegian births. Obstet Gynecol. 1997;89:543-548.
17. Mogren I, stenlund H, Hogberg u. Recurrence of prolonged pregnancy. Int J Epidemiol. 1999;28:253-257.
18. Divon MY, Ferber A, Nisell H, et al. Male gender predisposes to prolon¬gation of pregnancy. Am J Obstet Gynecol. 2002;187:1081-1083.
19. Kistka ZA, Palomar L, Boslaugh SE, et al. Risk for postterm de-livery after previous postterm delivery. Am J Obstet Gynecol. 2007:196:241 ,e1-241.e6.
20. stotland NE, Washington AE, Caughey AB. Prepregnancy body mass index and the length of gestation at term. Am J Obstet Gynecol. 2007;197:378 e1-378.e5.
21. Tunon K, Eik-Nes SH, Grottum p. Fetal outcome in pregnancies defined as post-term according to the last menstrual period esti¬mate, but not according to the ultrasound estimate. Ultrasound Obstet Gynecol. 1999;14:12-16.
22. Eden RD, Seifert LS, Winegar A, et al. Perinatal characteristics of uncomplicated postdate pregnancies. Obstet Gynecol. 1987;69(3 pt 1):296-299.
23. McLean FH, Boyd ME, Usher RH, et al. Postterm infants: too big or too small? Am J Obstet Gynecol. 1991;164:619-624.
24. Rand L, Robinson JN, Economy KE, et al. Post-term induction of labor revisited. Obstet Gynecol. 2000;96(5 pt 1):779-783.
25. Alexander JM, McIntire DD, Leveno KJ. Forty weeks and beyond: pregnancy outcomes by week of gestation. Obstet Gynecol. 2000;96:291-294.
26. Vorherr H. Placental insufficiency in relation to postterm preg¬nancy and fetal postmaturity. Evaluation of fetoplacental function; management of the postterm gravida. Am J Obstet Gynecol. 1975;123:67-103.
27. Shime J, Librach CL, Gare DJ, et al. The influence of prolonged pregnancy on infant development at one and two years of age: a pro¬spective controlled study. Am J Obstet Gynecol. 1986;154:341-345.
28. Mannino F. Neonatal complications of postterm gestation. J Reprod Med. 1988;33:271-276.
29. Hilder L, Costeloe K, Thilaganathan B. Prolonged pregnancy: evaluating gestation-specific risks of fetal and infant mortality. Br J Obstet Gynaecol. 1998;105:169-173.
30. Divon MY, Haglund B, Nisell H, et al. Fetal and neonatal mortality in the postterm pregnancy: the impact of gestational age and fetal growth restriction. Am J Obstet Gynecol. 1998;178:726-731.
31. Caughey AB, Musci TJ. Complications of term pregnancies be¬yond 37 weeks of gestation. Obstet Gynecol. 2004;103:57-62.
32. WHO Recommendations on Antenatal Care for a Positive Pregnancy Experience. Geneva, Switzerland: World Health Organization; 2016.
33. Lalor JG, Fawole B, Alfirevic z, et al. Biophysical profile for fetal assessment in high risk pregnancies. Cochrane Database Syst Rev. 2008;CD000038.
34. Grobman WA, Rice MM, Reddy UM, et al. Labor induction versus expectant management in low-risk nulliparous women. N Engl J Med. 2018;379:513-523.
35. Practice Advisory: clinical guidance for integration of the findings of the ARRIVE trial: labor induction versus expectant management in low-risk nulliparous women. Available at: https://www.acog.org/ Clinical-Guidance-and-Publications/Practice-Advisories/Practice- Advisory-Clinical-guidance-for-integration-of-the-findings-of-The- ARRIVE-Trial. Accessed August 26, 2019.
36. Grobman WA, Caughey AB. Elective induction of labor at 39 weeks compared with expectant management: a meta-analysis of cohort studies. Am J Obstet Gynecol. 2019;221:304-310.
37. Hersh AR, Skeith AE, Sargent JA, et al. Induction of labor at 39 weeks of gestation versus expectant management for low- risk nulliparous women: a cost-effectiveness analysis. Am J Obstet Gynecol. 2019;220:590.e1-590.e10.
38. Middleton p, Shepherd E, Crowther CA. Induction of labour for improving birth outcomes for women at or beyond term. Cochrane Database Syst Rev. 2018;5:CD004945.
39. Walker KF, Bugg GJ, Macpherson M, et al. Randomized trial of la-bor induction in women 35 years of age or older. N Engl J Med. 2016;374:813-822.
40. Tsakiridis I, Mamopoulos A, Chalkia-Prapa EM, et al. Preterm premature rupture of membranes: a review of 3 national guide-lines. Obstet Gynecol Surv. 2018;73:368-375.
41. Middleton p, Shepherd E, Flenady V, et al. Planned early birth ver-sus expectant management (waiting) for prelabour rupture of membranes at term (37 weeks or more). Cochrane Database Syst Rev. 2017;1:CD005302.
42. Tsakiridis I, Mamopoulos A, Athanasiadis A, et al. Vaginal birth af-ter previous cesarean birth: a comparison of 3 national guide-lines. Obstet Gynecol Surv. 2018;73:537-543.
43. West HM, Jozwiak M, Dodd JM. Methods of term labour induc-tion for women with a previous caesarean section. Cochrane Da-tabase Syst Rev. 2017;6:CD009792.
44. Mariani Neto c, Leao E, Baretto E, et al. Use of misoprostol for la-bour induction in stillbirths. Rev Paul Med. 1987;105:325-328.
45. Dodd JM, Crowther CA. Misoprostol for induction of labour to ter-minate pregnancy in the second or third trimester for women with a fetal anomaly or after intrauterine fetal death. Cochrane Data-base Syst Rev. 2010;CD004901.
46. Boulvain M, Irion o, Dowswell T, et al. Induction of labour at or near term for suspected fetal macrosomia. Cochrane Database Syst Rev. 2016;CD000938.
47. Dodd JM, Deussen AR, Grivell RM, et al. Elective birth at 37 weeks’ gestation for women with an uncomplicated twin pregnancy. Cochrane Database Syst Rev. 2014;CD003582.
48. Committee on Practice B-O. ACOG Practice Bulletin No. 190: Ges¬tational Diabetes Mellitus. Obstet Gynecol. 2018;131:e49-e64.
49. Berger H, Gagnon R, Sermer M, et al. Diabetes in pregnancy. J Obstet Gynaecol Can. 2016;38:667-679.e1.
50. National Institute for Health and Care Excellence. Diabetes in pregnancy: management from preconception to the postnatal period. NICE guideline. Published February 25, 2015. Available at: nice.org.uk/guidance/ng3. Accessed August 26, 2019.
51. Boulvain M, Stan c, Irion o. Elective delivery in diabetic pregnant women. Cochrane Database Syst Rev. 2001;CD001997.
52. Vahratian A, Zhang J, Troendle JF, et al. Labor progression and risk of cesarean delivery in electively induced nulliparas. Obstet Gynecol. 2005;105:698-704.
53. Bishop EH. Pelvic scoring for elective induction. Obstet Gynecol. 1964;24:266-268.
54. Crane JM. Factors predicting labor induction success: a critical analysis. Clin Obstet Gynecol. 2006;49:573-584.
55. Verhoeven CJ, Opmeer BC, Oei SG, et al. Transvaginal sono¬graphic assessment of cervical length and wedging for predicting outcome of labor induction at term: a systematic review and meta¬analysis. Ultrasound Obstet Gynecol. 2013;42:500-508.
56. McColgin sw, Bennett WA, Roach H, et al. Parturitional factors associated with membrane stripping. Am J Obstet Gynecol. 1993;169:71-77.
57. Boulvain M, Stan c, Irion o. Membrane sweeping for induction of labour. Cochrane Database Syst Rev. 2005;CD000451.
58. Gommers JSM, Diederen M, Wilkinson c, et al. Risk of maternal, fetal and neonatal complications associated with the use of the transcervical balloon catheter in induction of labour: a systematic review. Eur J Obstet Gynecol Reprod Biol. 2017;218:73-84.
59. Jozwiak M, Bloemenkamp KW, Kelly AJ, et al. Mechanical methods for induction of labour. Cochrane Database Syst Rev. 2012;CD001233.
60. Rayburn WF. Prostaglandin E2 gel for cervical ripening and induction of labor: a critical analysis. Am J Obstet Gynecol. 1989;160:529-534.
61. Rayburn WF, Wapner RJ, Barss VA, et al. An intravaginal controlled-release prostaglandin E2 pessary for cervical ripening and initia-tion of labor at term. Obstet Gynecol. 1992;79:374-379.
62. Witter FR, Rocco LE, Johnson TR. A randomized trial of prosta-glandin E2 in a controlled-release vaginal pessary for cervical rip-ening at term. Am J Obstet Gynecol. 1992;166:830-834.
63. Brindley BA, Sokol RJ. Induction and augmentation of labor: basis and methods for current practice. Obstet Gynecol Surv. 1988;43:730-743.
64. Thomas J, Fairclough A, Kavanagh J, et al. Vaginal prostaglandin (PGE2 and PGF2a) for induction of labour at term. Cochrane Da-tabase Syst Rev. 2014;CD003101.
65. French L. Oral prostaglandin E2 for induction of labour. Cochrane Database Syst Rev. 2001;CD003098.
66. Boulvain M, Kelly A, Irion o. Intracervical prostaglandins for induc-tion of labour. Cochrane Database Syst Rev. 2008;CD006971.
67. Eroglu D, Oktem M, Yanik F, et al. Labor induction at term: a com-parison of the effects of 50 microg and 25 microg vaginal miso-prostol. Clin Exp Obstet Gynecol. 2007;34:102-105.
68. Hofmeyr GJ, Gulmezoglu AM, Pileggi c. Vaginal misoprostol for cervical ripening and induction of labour. Cochrane Database Syst Rev. 2010;CD000941.
69. Chen w, Xue J, Peprah MK, et al. A systematic review and net-work meta-analysis comparing the use of Foley catheters, miso-prostol, and dinoprostone for cervical ripening in the induction of labour. BJOG. 2016;123:346-354.
70. Alfirevic z, Aflaifel N, Weeks A. Oral misoprostol for induction of labour. Cochrane Database Syst Rev. 2014;CD001338.
71. Muzonzini G, Hofmeyr GJ. Buccal or sublingual misoprostol for cervical ripening and induction of labour. Cochrane Database Syst Rev. 2004;CD004221.
72. Tsakiridis I, Mamopoulos A, Athanasiadis A, et al. Diagnosis and management of vasa previa: a comparison of 4 national guide-lines. Obstet Gynecol Surv. 2019;74:436-442.
73. Bricker L, Luckas M. Amniotomy alone for induction of labour. Cochrane Database Syst Rev. 2000;CD002862.
74. Howarth GR, Botha DJ. Amniotomy plus intravenous oxytocin for in¬duction of labour. Cochrane Database Syst Rev. 2001;CD003250.
75. Theobald GW, Graham A, Campbell J, et al. The use of post¬pituitary extract in physiological amounts in obstetrics; a prelimi-nary report. Br Med J. 1948;2:123-127.
76. Seitchik J, Amico J, Robinson AG, et al. Oxytocin augmentation of dysfunctional labor. IV. Oxytocin pharmacokinetics. Am J Obstet Gynecol. 1984;150:225-228.
77. Flannelly G, Turner M, Rassmussen M, et al. Rupture of the uterus in Dublin; an update. J Obstet Gynaecol. 1993;13:440-443.
78. Hendricks CH, Brenner WE. Cardiovascular effects of oxytocic drugs used post partum. Am J Obstet Gynecol. 1970;108:751-760.
79. Alfirevic z, Kelly AJ, Dowswell T. Intravenous oxytocin alone for cervical ripening and induction of labour. Cochrane Database Syst Rev. 2009;CD003246.
80. Alfirevic z, Keeney E, Dowswell T, et al. Methods to induce labour: a systematic review, network meta-analysis and cost¬effectiveness analysis. BJOG. 2016;123:1462-1470.
81. Buser D, Mora G, Arias F. A randomized comparison between misoprostol and dinoprostone for cervical ripening and labor induction in patients with unfavorable cervices. Obstet Gynecol. 1997;89:581-585.
82. Sanchez-Ramos L, Peterson DE, Delke I, et al. Labor induction with prostaglandin E1 misoprostol compared with dinoprostone vaginal insert: a randomized trial. Obstet Gynecol. 1998;91:401-405.
83. Macones GA, Hankins GD, Spong CY, et al. The 2008 National In¬stitute of Child Health and Human Development workshop report on electronic fetal monitoring: update on definitions, interpretation, and research guidelines. Obstet Gynecol. 2008;112:661-666.
84. Kulier R, Hofmeyr GJ. Tocolytics for suspected intrapartum fetal distress. Cochrane Database Syst Rev. 2000;CD000035.
85. Spong CY, Berghella V, Wenstrom KD, et al. Preventing the first cesarean delivery: summary of a joint Eunice Kennedy Shriver Na¬tional Institute of Child Health and Human Development, Society for Maternal-Fetal Medicine, and American College of Obstetricians and Gynecologists Workshop. Obstet Gynecol. 2012;120:1181-1193.
86. American College of Obstetricians and Gynecologists; Society for Maternal-Fetal Medicine. Obstetric care consensus no. 1: safe prevention of the primary cesarean delivery. Obstet Gynecol. 2014;123:693-711.
87. Rouse DJ, Owen J, Hauth JC. Criteria for failed labor induction: prospective evaluation of a standardized protocol. Obstet Gynecol. 2000;96(5 Pt 1):671-677.
88. Simon CE, Grobman WA. When has an induction failed? Obstet Gynecol. 2005;105:705-709.
89. Kelly AJ, Alfirevic z, Ghosh A. Outpatient versus inpatient induc-tion of labour for improving birth outcomes. Cochrane Database Syst Rev. 2013;CD007372.
90. Vogel JP, Osoti AO, Kelly AJ, et al. Pharmacological and mechan-ical interventions for labour induction in outpatient settings. Cochrane Database Syst Rev. 2017;9:CD007701.
91. Dowswell T, Kelly AJ, Livio s, et al. Different methods for the in-duction of labour in outpatient settings. Cochrane Database Syst Rev. 2010;CD007701.