Trên thị trường hiện nay có rất nhiều thuốc gerneric có hoạt chất là Ethinylestradiol tuy nhiên lại rất ít thông tin liên quan đến hoạt chất này. Ở bài này HealCentral.org xin được chia sẻ các thông tin như: Cơ chế tác dụng của Ethinylestradiol là gì? Ethinylestradiol có tác dụng gì? Tác dụng phụ của Ethinylestradiol là gì?… Dưới đây là thông tin chi tiết.
Lịch sử nghiên cứu và phát triển
Ethinylestradiol (EE) là estrogen tổng hợp sử dụng đường uống đầu tiên, được mô tả năm 1938 bởi Hans Herloff Inhoffen và Walter Hohlweg của Schering AG tại Berlin. Nó được FDA phê duyệt ngày 25/6/1943 tại Hoa Kỳ, được tiếp thị bởi Schering dưới tên thương mại Estinyl. FDA đã rút lại sự phế duyệt cho Estinyl từ ngày 4/6/2004 theo yêu cầu của Schering, công ty đã ngừng tiếp thị nó.
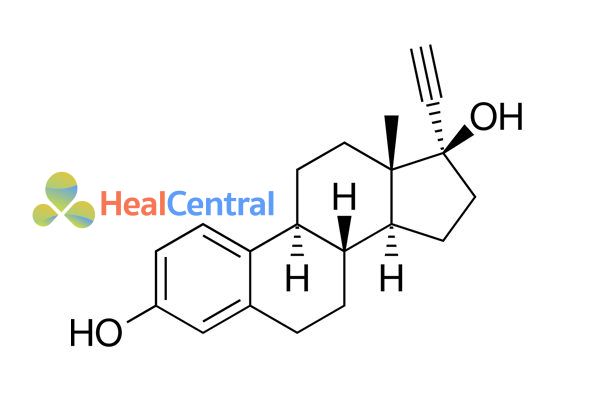
EE lần đầu tiên được sử dụng trong các thuốc tránh thai phối hợp (COC) để thay thế mestranol, và nó đã nhanh chóng thay thế mestranol trong các COC. EE không được sử dụng đơn độc để tránh thai.

Dược lực học
EE liên kết và hoạt hóa cả 2 loại estrogen receptor (ER), là ERα và ERβ. Trong đó, nó có ái lực với thụ thể ERα cao hơn. Các estrogen đối kháng tác dụng của hormon hướng sinh dục thông qua hoạt hóa ERα.
Trong thuốc tránh thai, EE được sử dụng phối hợp với 1 progestin để ức chế sự gia tăng nồng độ các hormon FSH và LH giữa chu kỳ kinh nguyệt, ức chế sự phóng noãn cũng như ức chế trứng rụng.
Cũng như các thuốc tránh thai chỉ chứa progestin, các COC cũng có tác dụng làm teo nội mạc tử cung, tạo môi trường không thuận lợi cho hợp tử làm tổ và đồng thời giảm tiết chất nhầy cổ tử cung, làm chất nhầy ít và quánh hơn, tinh trùng sẽ khó di chuyển đến vị trí của trứng để thụ tinh.
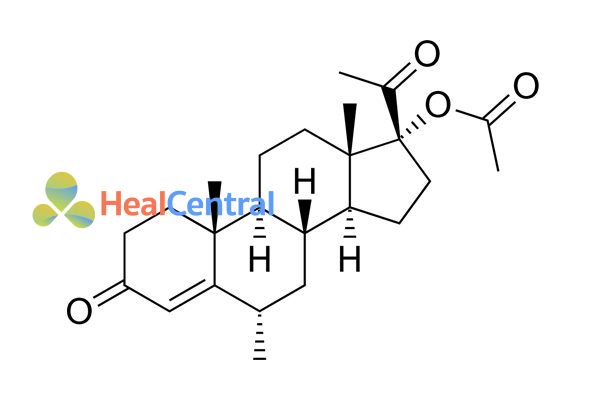
Các thuốc nhóm này có hiệu lực cao hơn thuốc tránh thai chỉ chứa progestin, nhưng đi kèm với đó là nhiều tác dụng phụ hơn (thêm tác dụng phụ do estrogen gây ra) và nhiều nguy cơ, biến chứng liên quan hơn, đồng thời thuốc cũng hạn chế dùng cho phụ nữ đang cho con bú.
Một số thử nghiệm lâm sàng

Kết quả từ 1 nghiên cứu đối chứng ngẫu nhiên, đa trung tâm về khả năng dung nạp dài hạn của ethinylestradiol 20 μg / drospirenone 3 mg trong chế độ điều trị mở rộng linh hoạt.
Các tác giả: Klipping C, Duijkers I, Fortier MP, Marr J, Trummer D và Elliesen J từ Dinox BV, Groningen, Hà Lan.
Nghiên cứu này được thiết kế để đánh giá sự an toàn và dung nạp lâu dài của 1 chế độ điều trị mở rộng linh hoạt mới với ethinylestradiol (EE) 20 μg / drospirenone (DRSP) 3 mg, cho phép quản lí chảy máu trong chu kì (MIB), so với chế độ điều trị mở rộng cố định 28 ngày thông thường.
Thiết kế nghiên cứu: Trong nghiên cứu đa trung tâm, nhãn mở ở pha III này, các phụ nữ (18-35 tuổi) được chọn ngẫu nhiên sử dụng EE/DRSP theo các chế độ sau: linh hoạt (MIB) (sử dụng thuốc chứa hormon hoạt động trong 24-120 ngày, sau đó không dùng thuốc trong 4 ngày), 28 ngày thông thường (sử dụng thuốc chứa hormon hoạt động trong 24 ngày, sau đó không dùng thuốc trong 4 ngày) hoặc kéo dài cố định (sử dụng thuốc chứa hormone hoạt động liên tục trong 120 ngày, sau đó không dùng thuốc 4 ngày) trong pha so sánh 1 năm. Sau đó, họ bước vào pha mở rộng an toàn 1 năm, trong đó phần lớn được nhận chế độ linh hoạt (MIB). Kết quả an toàn / dung nạp được đo trong hơn 2 năm. 1 phân tích riêng về các thông số an toàn xác định (nội mạc tử cung, hormon, lipid, cầm máu và chuyển hóa) đã được tiến hành tại 2 trong số các trung tâm nghiên cứu.
Kết quả: Kết quả được phân tích ở 1067 và 783 phụ nữ trong các pha so sánh và mở rộng an toàn tương ứng. Nhìn chung, 56.3% phụ nữ đã trải qua ít nhất 1 sự kiện bất lợi (AE) trong pha mở rộng an toàn. Các AE nghiêm trọng xảy ra với tỉ lệ 3.0%, 1.4% và 3.3% tương ứng ở các phụ nữ nhận chế độ điều trị linh hoạt (MIB), 28 ngày thông thường và kéo dài cố định. Không có phát hiện bất ngờ về nội mạc tử cung, hormon, lipid, cầm máu hoặc chuyển hóa xảy ra với bất kỳ chế độ nào trong 3 chế độ này.
Kết luận: EE/DRSP trong chế độ kéo dài linh hoạt với quản lí chảy máu trong chu kỳ được dung nạp tốt và khi dùng đến 2 năm, nó có ột hồ sơ an toàn tốt có thể so sánh với các biện pháp tránh thai đường uống sử dụng estrogen / progestogen khác.
Dược động học
Hấp thu: Sinh khả dụng (F) đường uống trung bình là 45%, và có sự biến động cao giữa các cá thể. Với liều 20 μg EE kết hợp với 2 mg norethisterone acetate ở phụ nữ sau mãn kinh, thời gian đạt nồng độ đỉnh trong huyết tương (Tmax) trung bình là 1.5 giờ và nồng độ đỉnh trong huyết tương (Cmax) là 50 pg/mL. Sau liều đầu tiên, nồng độ EE trung bình tăng lên khoảng 50% cho đến khi đạt được trạng thái ổn định. Trạng thái ổn định đạt được sau 1 tuần dùng thuốc hàng ngày. Nhìn chung nồng độ EE cũng biến động cao phụ thuộc vào cá thể nên các thông số trên chỉ mang tính chất tham khảo. Dùng EE với bữa ăn giàu chất béo làm giảm đáng kể Cmax của nó.
Phân bố: Tỉ lệ liên kết protein huyết tương là 97-98% (chủ yếu liên kết với albumin). EE có ái lực thấp với SHBG, không giống estradiol.
Chuyển hóa: Chuyển hóa bước đầu ở ruột và gan. Trong chuyển hóa lần đầu, EE được liên hợp rộng rãi thông qua liên hợp glucuronic và sulfat. Do sự cản trở không gian của nhóm ethinyl ở C17α, EE không bị chuyển hóa bởi 17β-HSD. EE còn được chuyển hóa bằng cách hydroxyl hóa thành catechol estrogen. Chất chuyển hóa là 2-hydroxy-EE, được xúc tác chủ yếu bởi CYP3A4. Hydroxyl hóa EE ở các vị trí C4, C6α và C16β thành 4-, 6α- và 16β-hydroxy-EE cũng đã được báo cáo, nhưng dường như chỉ đóng góp vào chuyển hóa nó ở mức độ thấp. 2- và 4-methoxy-EE cũng được hình thành thông qua sự biến đổi 2- và 4-hydroxy-EE bởi catechol O-methyltransferase. Chất chuyển hóa oxy hóa của EE ức chế không đảo ngược các enzyme cytochrom P450. Và chính điều này cũng làm tăng hiệu lực của EE.
Thải trừ: Có nhiều nguồn báo cáo khác nhau về thời gian bán hủy (t1/2) của EE, trong đó thấp nhất là 7 giờ và dài nhất là 36 giờ. Bài xuất 62% trong phân và 38% trong nước tiểu.
Chỉ định và liều dùng
Tránh thai:
Dùng phối hợp với 1 progestin khác tạo thành COC.
Nên bắt đầu vào chủ nhật hoặc ngày đầu tiên của chu kì kinh nguyệt (thường có chỉ dẫn thứ tự trên vỉ).
Uống 1 viên chứa hormon / ngày trong 21 ngày liên tiếp. Sau đó nghỉ 7 ngày rồi bắt đầu chu kì mới. Hoặc một số nhà sản xuất sẽ có 7 viên giả dược (không chứa hormon) hoặc 7 viên bố sung sắt và vitamin thì bạn sẽ uống 7 viên này trong 7 ngày , mỗi ngày 1 viên, sau đó bắt đầu chu kì mới.
COC không khuyến nghị sử dụng cho phụ nữ đang cho con bú.
Tác dụng phụ
Ta sẽ nói về các tác dụng phụ thường gặp với COC chứa ethinylestradiol.
Phù và tăng cân giả do giữ muối nước.
Buồn nôn và nôn: Nếu nôn trong vòng 2 giờ sau khi uống thuốc, cần uống bố sung 1 liều mới.
Chuột rút chân hay gặp trong thời gian đầu.
Rối loạn kinh nguyệt: Kinh nguyệt không đều, băng huyết, rong kinh, tắt kinh, khí hư… có thể xảy ra nhưng sẽ giảm dần khi dùng thuốc đều đặn.
Đau đầu, chóng mặt, đau ngực, căng tức vú có thể xảy ra trong thời gian đầu dùng thuốc nhưng sẽ nhanh chóng hết đi.
Nám da, mụn trứng cá. Tránh tiếp xúc trực tiếp với ánh sáng mặt trời nhiều nếu có nám da.
Giảm ham muốn tình dục cũng thường xuyên xảy ra.
Huyết khối động hoặc tĩnh mạch có thể xảy ra với nguy cơ cao hơn các thuốc tránh thai chỉ chứa progestin.
Estrogen liều thấp làm tăng nguy cơ phát triển trầm cảm, ý định tự tử.
Tăng tỉ lệ mắc u gan lành tính.
Vàng da ứ mật.
Tăng huyết áp: Thường chỉ tăng huyết áp tâm thu và sẽ trở về bình thường sau khi ngừng thuốc.
Progestin có thể làm tăng tình trạng kháng insulin và gây đái tháo đường
Đồng thời progestin gây tăng LDL-C và giảm HDL-C, tuy nhiên tác dụng phụ này bị giảm bớt bởi estrogen.
Tăng tỉ lệ nhiễm trùng tiết niệu.
Gây thiếu các vitamin C, B6, B12, acid folic, calci, kẽm, mangan. Có thể phải xem xét bổ sung các vitamin và khoáng chất này.
Gây giảm số lượng và chất lượng sữa của bà mẹ đang cho con bú.
Lưu ý và thận trọng
Cảnh báo hộp đen:
Hút thuốc lá làm tăng nguy cơ mắc các biến cố tim mạch nghiêm trọng khi đang dùng COC. Nguy cơ tăng theo tuổi (> 35 tuổi) và lượng thuốc hút trong ngày (≥ 15 điếu/ngày). Phụ nữ đang sử dụng COC không nên hút thuốc.

Thận trọng:
Nếu các tác dụng phụ liên quan đến rối loạn kinh nguyệt, đau đầu, đau vú, buồn nôn, nôn, chuột rút chân không mất đi sau vài tháng sử dụng thuốc đều đặn, cần tham khảo ý kiến bác sĩ để xem xét đổi thuốc hoặc xác định các nguyên nhân khác có thể gây ra các triệu chứng này.
Thận trọng với bệnh nhân suy thận, gan, đái tháo đường, rối loạn lipid máu.
Thận trọng nếu tiền sử gia đình bị ung thư vú, huyết khối tĩnh mạch sâu, thuyên tắc phổi, bệnh van tim do huyết khối, viêm tĩnh mạch huyết khối, huyết khối động mạch, đột quỵ, nhồi máu cơ tim.
Thận trọng với bệnh nhân trầm cảm hoặc có tiền sử trầm cảm.
Thận trọng với bệnh nhân có tiền sử lạc nội mạc tử cung, thay đổi mật độ xương, lupus ban đỏ hệ thống.
Thận trọng với bệnh nhân có các tình trạng có thể nặng hơn do giữ nước (đau nửa đầu, hen phế quản, động kinh).
Ngừng dùng thuốc nếu vàng da, các vấn đề về thị giác (có thể không dung nạp kính áp tròng), bất kỳ dấu hiệu nào của thuyên tắc huyết khối tĩnh mạch, đau nửa đầu mức độ nghiêm trọng khác thường, tăng huyết áp đáng kể, trầm cảm nặng, tăng nguy cơ biến chứng huyết khối sau phẫu thuật.
Ngừng thuốc 4 tuần trước phẫu thuật lớn hoặc bất động kéo dài.
Bệnh nhân có bất kì yếu tố nguy cơ nào của thuyên tắc huyết khối tĩnh mạch không nên sử dụng COC.
Một số nghiên cứu liên kết việc sử dụng thuốc tránh thai với tăng nguy cơ ung thư vú, trong khi các nghiên cứu khác không cho thấy sự thay đổi về nguy cơ.
Tăng nguy cơ ung thư cổ tử cung khi sử dụng thuốc tránh thai, tuy nhiên HPV vẫn là yếu tố nguy cơ chính của ung thư này. Bằng chứng cho thấy việc sử dụng lâu dài các thuốc tránh thai từ 5 năm trở lên có thể liên quan đến tăng nguy cơ.
Tăng nguy cơ ung thư gan khi sử dụng thuốc tránh thai, rủi ro tăng theo với thời gian sử dụng.
Ngừng điều trị bằng COC trước khi bắt đầu điều trị bằng phác đồ phối hợp thuốc ombitasvir / paritaprevir / ritonavir, có hoặc không có dasabuvir. Có thể sử dụng COC khoảng 2 tuần sau khi kết thúc điều trị bằng chế độ thuốc kết hợp trên.
Phụ nữ có thai: Không có thông tin cho thấy lỡ dùng thuốc vào những tháng đầu thai kì có thể gây ra dị tật bẩm sinh. Tuy nhiên, khi phát hiện mang thai, không nên dùng thuốc vì không có lí do gì để dùng thuốc tránh thai trong thai kì.
Phụ nữ đang cho con bú: Estrogen có thể làm giảm chất lượng / số lượng sữa mẹ. Xem xét dùng các biện pháp tránh thai khác khi đang cho con bú. Tối thiểu 6 tuần sau khi sinh mới xem xét sử dụng COC.
Tương tác thuốc
Tương tác thuốc của các COC sẽ là tương tác thuốc của EE và progestin còn lại.
Dùng cùng các kháng sinh: Có thể làm giảm hiệu quả tránh thai do kháng sinh làm thay đổi hệ vi sinh đường ruột, ảnh hưởng đến chu trình gan – ruột của thuốc.

Dùng cùng các thuốc ức chế CYP3A4: Làm tăng nồng độ EE và progestin phối hợp cùng trong huyết tương. Nguy cơ tích lũy thuốc và tăng tác dụng phụ cũng như độc tính của thuốc.
Dùng cùng các thuốc cảm ứng CYP3A4: Làm giảm nồng độ EE và progestin phối hợp cùng trong huyết tương. Nguy cơ giảm tác dụng tránh thai của thuốc.
Chống chỉ định
Quá mẫn cảm với ethinylestradiol hoặc bất cứ thành phần nào của thuốc.
Chống chỉ định của COC:
Phụ nữ nghiện thuốc lá trên 35 tuổi.
Tiền sử hoặc ung thu vú hoạt động.
Bệnh huyết khối động mạch (đột quỵ, nhồi máu cơ tim), viêm tĩnh mạch huyết khối, huyết khối tĩnh mạch sâu, thuyên tắc phổi, bệnh van tim do huyết khối.
Bệnh nhân có yếu tố nguy cơ huyết khối như bất động lâu ngày, phẫu thuật lớn…
Khối u phụ thuộc estrogen. Ung thư nhạy cảm với estrogen hoặc progestin.
Bệnh gan hoạt động, u gan lành hoặc ác tính, vàng da.
Xuất huyết âm đạo bất thường hoặc không được chẩn đoán.
Tăng huyết áp không được kiểm soát.
Đái tháo đường có biến chứng mạch máu.
Đang sử dụng thuốc phối hợp điều trị viêm gan C chứa ombitasvir / paritaprevir / ritonavir, có hoặc không có dasabuvir.
Tài liệu tham khảo:
https://www.ncbi.nlm.nih.gov/pubmed/9853201
https://www.ncbi.nlm.nih.gov/pubmed/7370379
https://www.ncbi.nlm.nih.gov/pubmed/11818367
https://www.ncbi.nlm.nih.gov/pubmed/7856434
https://www.ncbi.nlm.nih.gov/pubmed/14561538
https://www.ncbi.nlm.nih.gov/pubmed/24908814





