Bài viết Đo dung tích cặn chức năng trong điều trị tích cực: Các khía cạnh kỹ thuật và các áp dụng lâm sàng có khả năng của nó được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Measurements of functional residual capacity during intensive care treatment: the technical aspects and its possible clinical applications
Tóm tắt
Đo trực tiếp thể tích phổi, nghĩa là dung tích cặn chức năng (FRC, functional residual capacity) đã được khuyến cáo để theo dõi trong quá trình thông khí cơ học. Chủ yếu là do lý do kỹ thuật, các phép đo FRC đã không trở thành một công cụ giám sát thường xuyên, nhưng các kỹ thuật đầy hứa hẹn sẽ được trình bày. Chúng tôi đã thực hiện tìm kiếm y văn các nghiên cứu với từ khóa “dung tích cặn chức năng” hoặc “thể tích phổi cuối thì thở ra” (EELV, end expiratory lung volume) và tóm tắt sinh lý và sinh lý bệnh học của phép đo FRC ở bệnh nhân thông khí, mô tả các kỹ thuật hiện có để đo lường tại giường và cung cấp tổng quan các câu hỏi lâm sàng có thể được giải quyết bằng cách sử dụng đánh giá FRC.
Việc rửa hoặc xả khí vết (wash-in or wash-out of a tracer gas) trong thủ thuật nhiều nhịp thở có vẻ được áp dụng tốt nhất ở tại giường, và các kỹ thuật đầy hứa hẹn để rửa/xả nitơ hoặc oxy với độ chính xác hợp lý và độ lặp lại nhiều lần đã được trình bày. Các nghiên cứu ở những bệnh nhân thông khí chứng minh rằng FRC có thể dễ dàng được đo ở tại giường trong các môi trường lâm sàng khác nhau, bao gồm tối ưu hóa áp lực dương cuối thì thở ra (PEEP), hút đàm qua nội khí quản, tư thế nằm sấp, và cai thở máy. Mất huy động phế nang (alveolar derecruitment) có thể dễ dàng được theo dõi và cải thiện nhờ vào đo FRC mà không cần thay đổi các cài đặt thông khí dựa vào mức huy động phế nang. FRC có vẻ không nhạy cảm với căng chướng quá mức (overdistension) của phế nang. Bằng chứng cho thấy rằng các phép đo FRC, kết hợp với các thông số khác như oxy hóa động mạch và độ giãn nở hô hấp, có thể cung cấp thông tin quan trọng về tình trạng phổi ở những bệnh nhân bị bệnh nặng. Cần nghiên cứu sâu hơn để xác định vai trò chính xác của FRC trong giám sát và có lẽ hướng dẫn thông khí cơ học.
Giới thiệu
Các thông số được sử dụng để theo dõi trị liệu hô hấp trong điều trị chăm sóc đặc biệt, gồm oxygen hóa, cơ học hô hấp, loại bỏ CO2, hoặc những thông số khác, tất cả đều có những hạn chế trong việc đánh giá phế nang được thông khí. Ví dụ, oxy hóa động mạch bị ảnh hưởng bởi thông khí phế nang, khuếch tán oxy phế nang và tưới máu phổi. [1] Về mặt lý thuyết, việc loại bỏ CO2 có thể là một dấu hiệu nhạy cảm của thông khí phổi ở những đối tượng mà thông khí phút được giữ hằng định, vì có sự liên kết chặt chẽ giữa CO2 thở ra và thông khí phế nang. Nhưng thể tích phút thông khí cũng như sản xuất CO2 là cực kỳ thay đổi ở những bệnh nhân bị bệnh nặng. Do những hạn chế này, đo trực tiếp thể tích phổi thông khí, tức là dung tích cặn chức năng (FRC) đã được khuyến nghị như một thông số giám sát. [2–5]
Mặc dù các phép đo FRC đã được sử dụng cho mục đích nghiên cứu từ những năm 1980 và dường như được sử dụng thường xuyên cho bệnh nhân nhi, [6,7] nhưng cho đến nay, không sử dụng tại giường cho người lớn. Lý do cho điều này có thể chủ yếu là kỹ thuật. Các phép đo FRC ở bệnh nhân đặt nội khí quản là khó khăn về mặt kỹ thuật, thiết bị đo lường cồng kềnh, và tốn công lao động, với sự gián đoạn của thông khí liên tục. [8,9] Ngoài ra, các kỹ thuật dẫn đến tổng sai số hệ thống lên đến 20%. [10]
Với sự ra đời của bộ phận vi xử lý và công nghệ tiên tiến, một số kỹ thuật đo FRC để sử dụng ở những bệnh nhân bị bệnh nặng đã được trình bày trong vài năm qua. Tất cả các phương pháp đều hiển thị lặp lại hợp lý cho các ứng dụng lâm sàng. Hiện tại, một trong những phương pháp này có sẵn trên thị trường (FRC INviewTM, Engstrom Carestation, GE Healthcare, Chalfont St Giles, UK). Vì hầu hết các khía cạnh kỹ thuật dường như đã được giải quyết, các nghiên cứu lâm sàng sâu hơn, nên các phép đo FRC có thể giúp hướng dẫn điều trị hô hấp.
Mục đích của tổng quan này là làm sáng tỏ sinh lý và sinh lý bệnh cơ bản của phép đo thể tích phổi ở bệnh nhân thông khí, cung cấp tổng quan về các kỹ thuật hiện có và giới thiệu các ứng dụng lâm sàng có thể điều trị bằng đường hô hấp.
Sinh lý
FRC được định nghĩa là tổng thể tích phổi cặn (residual volume) và thể tích dự trữ thở ra (expiratory reserve volume). Theo định nghĩa, FRC là lượng khí còn lại trong phổi sau khi thở ra đối với thở bình thường, không nhất thiết phải trong khi nghỉ ngơi. [11] Một số tác giả đề xuất thuật ngữ thể tích phổi cuối thì thở ra (EELV) [12-14] hoặc thể tích khí phổi tiếp cận được (APGV, accessible pulmonary gas volume) [15] đối với thể tích phổi trong điều kiện bất thường như bệnh phổi mãn tính hoặc cấp tính, hoặc thông khí cơ học nhưng không có sự đồng thuận. [11] Cho dù sử dụng thuật ngữ FRC, EELV hoặc APGV, để báo cáo về điều kiện, tức là thông khí với PEEP hoặc tư thế dường như được quan tâm tối đa. Trong phần sau, chúng tôi sử dụng thuật ngữ FRC, vì hầu hết độc giả sẽ quen thuộc với nó.
Các công thức khác nhau để tính giá trị bình thường đã được công bố. [16–19] Có sự gia tăng FRC liên quan đến tuổi do giảm co giãn đàn hồi của nhu mô phổi và sự tăng co giãn đàn hồi của thành ngực [20] và FRC phụ thuộc vào chiều cao cơ thể. Công thức sau đây, được gợi ý bởi Hiệp hội Hô hấp châu Âu, cung cấp một ước tính tốt về FRC ở các đối tượng ngồi khỏe mạnh [16] :
2.34 x heigh (m) + 0.022 x age (years) – 1.23 for men and 2.24 x heigh (m) + 0.001 x age (years) – 1.0 for women
FRC giảm khoảng 25% trong khi thay đổi từ tư thế ngồi sang tư thế nằm ngửa, trong khi tư thế nằm nghiêng cho kết quả trung gian. Khi thay đổi tư thế ở người khỏe mạnh từ nằm ngửa sang tư thế nằm sấp, FRC tăng lên [21] nhưng không phải trong tất cả các nghiên cứu. [22,23] FRC bị giảm trong bệnh phổi hạn chế [24] và béo phì. [25] Trong suy tim mạn tính, FRC giảm trung bình 11% dung tích phổi toàn phần dự đoán. [26–28] Trong bệnh phổi tắc nghẽn và khí phế thũng, FRC có thể tăng rõ rệt do mất tính co giãn của phổi, hoặc do cơ chế động, ví dụ giới hạn lưu lượng thở ra. [11,29,30] FRC giảm khoảng 20% trong khi gây mê, ngoại trừ gây mê với ketamine. [17] Không có sự khác biệt cho dù bệnh nhân thở thông khí cơ học tự phát hoặc kiểm soát được sử dụng. Các cơ chế có thể bao gồm giảm độ đàn hồi thành ngực, tăng áp lực bụng, hình thành xẹp phổi, và bẫy khí do đường thở đóng. [31] Sự giảm này rõ rệt hơn ở bệnh nhân béo phì. [17,32] Giảm FRC có thể được phục hồi một phần bằng cách thông khí bằng PEEP và nâng đầu cao 30 độ. Phẫu thuật ổ bụng và trong lồng ngực có thể làm trầm trọng thêm tình trạng mất FRC.
Sau phẫu thuật, giảm đau và ức chế phản xạ của hoạt động cơ hoành là yếu tố quyết định chính của việc giảm FRC. [31] Mở rộng phổi chủ động sau phẫu thuật chỉ phục hồi một phần những tác dụng này. Không có nhiều dữ liệu điều tra các các yếu tố ảnh hưởng đến FRC ở bệnh nhân thở máy trong khi điều trị chăm sóc tích cực. Về mặt lý thuyết, FRC bị thay đổi bởi vị trí cơ thể, mức độ an thần, tăng áp lực trong ổ bụng, phương thức thông khí và cài đặt của máy thở, tức là mức PEEP và lượng xẹp phổi. Cho đến nay, không có các giá trị bình thường ở bệnh nhân trong khi thở máy và/hoặc suy phổi cấp tính. Do các yếu tố khác nhau đã đề cập ở trên ảnh hưởng đến FRC ở những bệnh nhân được điều trị trong đơn vị chăm sóc đặc biệt, những giá trị này rất khó, mặc dù không thể xác định được. Phân tích xu hướng giả thuyết về giá trị FRC có thể cung cấp nhiều thông tin hơn so với các phép đo tuyệt đối đơn lẻ.
Kỹ thuật đánh giá FRC
Phép đo FRC bắt đầu từ năm 1800, khi H. Davy đo lượng thể tích khí cặn của phổi của mình bằng cách hít một hỗn hợp hydro chứa trong một bộ phận giữ không khí. ngày nay, có bốn phương pháp ước tính FRC: các kỹ thuật chụp ảnh, phép đo thể tích cơ thể, pha loãng bằng khí trơ (ví dụ helium), và rửa hoặc xả (wash-in or wash-out) khí tracer trong kỹ thuật nhiều nhịp thở (multiple breath maneuver).
Kỹ thuật hình ảnh (Imaging techniques)
Chụp cắt lớp vi tính (CT) ngang lập lại hoặc CT xoắn ốc vùng ngực cung cấp biện pháp xác định FRC chính xác và được coi là tiêu chuẩn vàng. [34–36] Thật không may, các phép đo lặp lại không thể thực hiện tại giường và bệnh nhân tiếp xúc với lượng phóng xạ đáng kể. Sử dụng phương pháp chụp cắt lớp điện trở (EIT), các phép đo đầu giường không có bức xạ toàn phần và hơn thế nữa, có thể được sử dụng để phát hiện sự thay đổi thể tích phổi trong quá trình thông khí cơ học ở các mô hình động vật khác nhau và bệnh nhân bị bệnh nặng. [37,38,40–47] Gần đây, các khía cạnh kỹ thuật và ứng dụng lâm sàng của các phép đo EIT đã được xem xét rộng rãi. [1,48–50] Chúng tôi sẽ không thảo luận về các phép đo FRC bằng cách sử dụng CT hoặc EIT trong bài viết này.
Đo thể tích cơ thể (Body plethysmography)
Năm 1956, DuBois [51] và cộng sự đã giới thiệu các phép đo FRC bằng phương pháp đo thể tích cơ thể. Thể tích phổi được đo bằng cách áp dụng luật Boyle, quy định rằng trong điều kiện đẳng nhiệt, tích số của áp suất và thể tích của một thể tích khí cố định là không đổi. Đối với quy trình đo, bệnh nhân ngồi bên trong hộp kín và thở bình thường thông qua một ống ngậm. Mặc dù phương pháp này đã được sử dụng ở những bệnh nhân gây mê, [52] nó là quá cồng kềnh cho các cài đặt chăm sóc đặc biệt.
Phương pháp pha loãng helium (Helium dilution method)
Phương pháp pha loãng là một kỹ thuật thở lại (rebreathing technique) dựa trên sự cân bằng của một khí trong phổi với một lượng khí đã biết có chứa một lượng helium đã biết. Phương pháp này đòi hỏi một hệ thống kín khí để đạt được trạng thái cân bằng của khí tracer, ví dụ như helium. Hệ thống này được trang bị bơm tuần hoàn khí (gas circulation pump), các chất hấp thụ khí cacbonic và nước, cung cấp oxy, và đầu vào và đầu ra khí. [53] Vì máy thở đơn vị chăm sóc đặc biệt thường không sử dụng hệ thống thở lại, kỹ thuật này không thực tế cho đo FRC trong quá trình thông khí cơ học mà không có sự thay đổi đáng kể của máy thở.
Mặc dù có những vấn đề này, kỹ thuật này đã được sửa đổi để thích ứng với thông khí cơ học. [54–56] Phương pháp pha loãng helium kín (closed helium-dilution method) tạo thành một hệ thống bóng trong hộp (balloon-in-box system), cho hệ thống kín trong quá trình đo. Nồng độ helium trong bóng có thể được đo và FRC có thể được tính toán. Hệ thống này đã được sử dụng ở bệnh nhân trong quá trình thông khí có kiểm soát và hỗ trợ [54,56,57] nhưng chưa bao giờ được chấp nhận rộng rãi, có thể do thiết bị phức tạp cần thiết. Một phương pháp pha loãng helium đơn giản đã được sử dụng ở bệnh nhân thở máy nhưng cần phải ngắt kết nối với máy thở. [36,58] Ống nội khí quản của bệnh nhân được kẹp trong khi ngừng cuối kỳ thở ra và sau đó kết nối với một quả bóng chứa đầy thể tích khí đã biết hỗn hợp của helium trong oxy. Sau khi nhả kẹp, 10 thể tích khí lưu thông được bóp bóng thủ công cho bệnh nhân để pha loãng hỗn hợp khí helium với khí chứa trong phổi của bệnh nhân và hỗn hợp khí helium được phân tích. Ngoài việc đòi hỏi một lượng thời gian và công việc đáng kể để thực hiện các phép đo, về mặt lý thuyết, việc ngắt kết nối với máy thở khiến bệnh nhân có nguy cơ bị tái xẹp phế nang và khi bóp bóng thủ công, thông khí có thể làm tăng FRC do huy động các đơn vị phổi.
Phương pháp xả nhiều nhịp thở (Multiple breath wash-out methods)
Sử dụng hệ thống hô hấp mở, FRC có thể được xác định trong quá trình rửa/xả (wash- in/wash-out) khí vết trong phương pháp nhiều nhịp thở. Bất kỳ khí nào không độc và kém hòa tan trong máu và mô [ví dụ, nitơ, lưu huỳnh hexafluoride (SF6), oxy] có thể được sử dụng làm khí tracer. Quy trình rửa trôi thường đạt được trong vòng 3 phút; tuy nhiên, điều này có thể mất nhiều thời gian hơn trong bệnh phổi tắc nghẽn do khí tracer trộn lẫn kém trong đường hô hấp.
Các phép xác định FRC bằng cách sử dụng phương pháp xả nhiều nhịp thở miễn là thể tích khí trong phổi có thể truy cập tự do. Vì điều kiện này không nhất thiết phải đáp ứng cho toàn bộ phổi, do kết quả một phần của không khí bị bẫy, thể tích được xác định bằng các phương pháp này được gọi là ‘thể tích khí phổi tiếp cận được’ thay vì FRC. [15] Do đó, APGV (accessible pulmonary gas volume) có thể nhỏ hơn đáng kể so với FRC được xác định bởi phép đo thể tích cơ thể (body plethysmography), nhưng là thể tích hiệu quả chịu trách nhiệm cho việc trao đổi khí.
SF6 đã được sử dụng làm chất khí tracer để xác định FRC. [34,59–61] Nhưng vì các cảm biến SF6 không có sẵn trên thị trường và SF6 không có sự chấp thuận y tế để sử dụng lâm sàng, chúng tôi sẽ không thảo luận kỹ thuật này nữa. Như một sự thay thế, heptafluoropropane đã được nghiên cứu ở bệnh nhân sơ sinh thở máy.
Nitơ được sử dụng thường xuyên nhất là khí tracer trong nhiều nghiên cứu về nhịp thở. Nó lần đầu tiên được mô tả bởi Darling và cộng sự, [63] sau đó được sửa đổi và sử dụng chủ yếu trong các tình huống nghiên cứu. [8.9,19,57,64,65]
Trong các phép đo, tỷ lệ trong khí hít vào của oxy (FiO2) được thay đổi từ trị số cơ bản ban đầu thành 100% để rửa hết nitơ từ phổi. Sau khi đo, FiO2 được thay đổi trở lại giá trị ban đầu và N2 được vào phổi lại.
Một vấn đề quan trọng với phương pháp này là sự thay đổi đáng kể về độ nhớt của khí (gas viscosity) trong quá trình rửa trôi, ảnh hưởng đến tính chính xác của các phép đo lưu lượng khí. Ngoài ra, máy phân tích luồng bên (side stream analyzers), ví dụ: bằng phép đo phổ khối (mass spectrometry) thông qua phép đo lưu lượng khí mao dẫn và dòng chính (capillary and mainstream gas flow measurement), dẫn đến sự chậm trễ đáng kể giữa hai tín hiệu và cần được đồng bộ hóa. Hơn nữa, độ trễ này phụ thuộc độ nhớt và do đó phải được điều chỉnh liên tục cho độ nhớt tạm thời của hỗn hợp khí. [66,67] Sử dụng hiệu chỉnh độ nhớt khí, thời gian trễ lấy mẫu và nitơ tái hít vào lại, Wrigge và đồng nghiệp [67,68] cho thấy có thể chấp nhận được độ chính xác của phép đo FRC trong quá trình thông khí được điều khiển và hỗ trợ. Tuy nhiên, chủ yếu là do các thiết bị cồng kềnh và sự cần thiết cho một bước thay đổi lớn của FiO2 trong các phép đo để đạt được một sự thay đổi đáng kể nồng độ nitơ trong phổi, không được chấp nhận ở bệnh nhân thông khí với một FiO2 cao, phương pháp này đã không được sử dụng trong các thói quen lâm sàng tại giường.
Để không đo trực tiếp N2, Fretschner và cộng sự [10] giả định rằng ở những bệnh nhân không có khí nào khác ngoài oxy, carbon dioxide và nitơ, N2 có thể được tính là dư lượng bằng cách đo oxy và carbon dioxide. Họ trình bày một kỹ thuật sử dụng một máy phân tích CO2 dòng chính và một máy phân tích O2 dòng bên. Vì hai dạng sóng này là không đồng nhất (inversely congruent), chúng có thể được đồng bộ với một phép đo khí (pneumotachograph measurement) của dòng khí để tích hợp lưu lượng và nồng độ N2. Do quy trình đồng bộ hóa rất nhạy và các lỗi nhỏ trong quá trình đồng bộ hóa có thể dẫn đến tính toán sai tổng của N2, Fretschner và cộng sự [10] đã kết luận rằng chỉ có sai biệt 20% thì phép đo FRC liên tiếp mới có thể phát hiện được bằng kỹ thuật đo này.
Olegard và cộng sự đã trình bày kỹ thuật rửa/xả nitơ cải biên (modified nitrogen wash- out/wash-in technique) mà không cần sử dụng các máy phân tích đặc biệt, chỉ đòi hỏi một sự thay đổi nhỏ của FiO2. Chỉ sử dụng các giá trị bình nguyên (plateau values) của nồng độ khí hít vào và khí lưu thông, sự khác biệt về độ trễ và thời gian đáp ứng trở nên không quan trọng, và không cần đồng bộ hóa liên tục. Việc tính toán chính xác chỉ yêu cầu lưu lượng/thể tích khí lưu thông và nồng độ khí hít vào và khí lưu thông kết nối với nhau đối với mỗi nhịp thở. [70] Hai giả định cơ bản được thực hiện: đầu tiên là không đồng nhất trong phân phối khí phế nang là không đổi trong suốt quá trình đo và thứ hai là sự chuyển hóa tế bào và trao đổi khí giữa máu mao mạch phổi và phế nang là ổn định. Kỹ thuật này ước tính FRC với độ chính xác cao bằng cách sử dụng thay đổi FiO2 chỉ 0,1 (nghĩa là 10%), đã được đánh giá ở bệnh nhân bị tổn thương phổi cấp tính (ALI)/hội chứng suy hô hấp cấp tính (ARDS), [36,70] và gần đây đã được thực hiện trong cơ học thương mại máy thở. Thật không may, phương pháp này không được xác nhận trong quá trình thông khí được hỗ trợ hoặc tự phát.
Sử dụng một cách tiếp cận khác, Eichler và cộng sự [71] cải tiến phương pháp được đề xuất bởi Fretschner và cộng sự [10] Kỹ thuật này được đơn giản hóa bằng cách sử dụng đầu dò lưu lượng khí của máy thở mặc dù có một máy đo thể tích phổi ngoài (external pneumotachograph). Tính toán của họ dựa trên các phép đo của oxy từng nhịp thở và không tính toán nitơ, do đó được gọi là ‘kỹ thuật rửa oxy’ (oxygen wash-out technique). Weismann và cộng sự [66] tiếp tục đơn giản hóa và cải thiện kỹ thuật sử dụng mô hình vật lý/toán học để tính toán thời gian trễ phụ thuộc vào lưu lượng (flow-dependent delay time) của máy phân tích O2 bên trong. Độ chính xác chấp nhận được về mặt lâm sàng đã được chứng minh bằng kỹ thuật này trong quá trình thở tự phát ở người tình nguyện và bệnh nhân [72,73] và trong khi thở máy được hỗ trợ và điều khiển. [74] Tương tự như kỹ thuật được đề xuất bởi Olegard và cộng sự [70] thay đổi bước của FiO2 chỉ 0,1 không bị ảnh hưởng tiêu cực của độ lặp lại. [75] Cho đến nay, phương pháp rửa oxy không có sẵn trên thị trường.
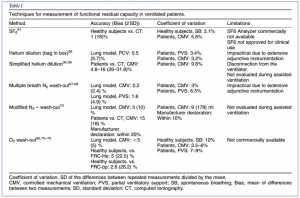
Trong vài năm qua, nhiều kỹ thuật đo lường FRC khác nhau trong quá trình thông khí cơ học đã được phát triển và đánh giá. Tất cả các phương pháp đều cho thấy độ chính xác chấp nhận được về mặt lâm sàng so với các kỹ thuật tiêu chuẩn khác và độ lặp lại tốt của các phép đo liên tiếp. Giá trị độ lặp lại thấp thường được tìm thấy khi đo trong quá trình thông khí hỗ trợ. Do các kiểu thở thay đổi nhanh chóng, các lỗi đo lường có thể tăng lên trong những trường hợp này. Bảng 1 cung cấp tổng quan về các kỹ thuật khác nhau và các hạn chế của chúng.
Theo quan điểm của chúng tôi, kỹ thuật rửa nitơ đã được sửa đổi bởi Olegard và cộng sự. và kỹ thuật rửa oxy phù hợp nhất với kỹ thuật giám sát thông thường tại giường.
Nghiên cứu động vật
Một vài nghiên cứu đã sử dụng phép đo trực tiếp FRC bằng kỹ thuật pha loãng hoặc rửa trong các tình huống thử nghiệm. Chủ yếu, họ nghiên cứu ảnh hưởng của các loại ALI thử nghiệm khác nhau, các loại thủ thuật huy động khác nhau và cài đặt PEEP trên FRC.
Nhất quán, FRC giảm sau khi bị ALI, không phân biệt loại chấn thương. [34,76–79] Thủ thuật huy động phế nang làm tăng FRC trở lại các giá trị cơ bản. [76–78,80] Ngoài ra, thông khí xả áp lực đường thở (airway pressure release ventilation) với nhịp thở tự phát làm tăng FRC. FRC phản ánh sự mất thông khí trong quá trình tiến triển chấn thương phổi tốt hơn so với các thông số đo không xâm lấn khác, [34] nhưng dường như không nhạy cảm với quá căng phế nang (alveolar overdistension). Kết hợp với sự độ giãn nở, FRC đã có thể xác định mức độ tối ưu của PEEP. [79] FRC giảm nhiều hơn sau khi hút đàm nội khí quản mở hơn là hút đàm kín. [43]
Các nghiên cứu cho thấy rằng các phép đo FRC có thể giúp điều tra sự phát triển của ALI/ ARDS, theo giả thuyết của Hedenstierna hơn 15 năm trước. [2] FRC có thể hữu ích trong việc theo dõi sự mất huy động (derecruitment) của phế nang nhưng, nó có vẻ không nhạy cảm với quá căng phế nang. Kết hợp với các thông số khác, ví dụ: sự độ giãn nở của hệ thống hô hấp, FRC cuối cùng có thể xác định được cài đặt PEEP tối ưu.
Ứng dụng lâm sàng
Mặc dù có nhiều nghiên cứu về các phương pháp và phương pháp kỹ thuật của các phép đo FRC ở bệnh nhân người lớn thông khí, [10,36,56,58,66–68,70–75,83–85] chỉ một vài nghiên cứu đã sử dụng phép đo FRC trong điều trị bệnh nhân .
FRC và PEEP
Bikker và cộng sự đã sử dụng kỹ thuật rửa/xả N2 đã được sửa đổi để đo FRC ở 45 bệnh nhân thông khí ở ba mức PEEP, tức là 15, 10 và 5 cmH2O. Họ bao gồm các bệnh nhân có chức năng phổi bình thường, và tổn thương tại phổi và ngoài phổi. FRC thấp hơn rõ rệt ở tất cả các nhóm khi so sánh với các giá trị bình thường ở các đối tượng ngồi. FRC giảm trong khi giảm PEEP, trong khi oxy hóa không bị thay đổi. Họ có thể chứng minh mối tương quan đáng kể giữa sự độ giãn nở và FRC ở nhóm bệnh nhân bị chấn thương phổi ngoài phổi. Để tìm ra PEEP ‘tối ưu’, FRC kết hợp với khoảng chết, sự độ giãn nở và oxy hóa đã được nghiên cứu ở những bệnh nhân gây mê bình thường trong một thủ tục giảm PEEP. Tại PEEP 10 cmH2O, các tác giả tìm thấy các giá trị độ giãn nở cao nhất kết hợp với tỳ lệ khoảng chết thấp nhất, cho thấy số lượng tối đa của lỗ phế nang được mở hiệu quả. FRC và oxy hóa là không nhạy cảm với quá căng phế nang. [86]
FRC và huy động phế nang
Trong 13 bệnh nhân ARDS thông khí với thông khí hỗ trợ áp lực, Patroniti và cs [87] có thể chứng minh rằng FRC được tăng lên bằng cách sử dụng các nhịp thở sâu gián đoạn được cung cấp dưới dạng nhịp thở kiểm soát áp suất mỗi phút. Reutershan et al. [88] đo FRC ở tư thế nằm sấp trên bệnh nhân ARDS. Họ cho thấy rằng việc huy động phế nang gây ra bằng tư thế nằm sấp là một quá trình phụ thuộc vào thời gian cá nhân có thể được theo sau bởi những thay đổi trong FRC. Hơn nữa, người có đáp ứng, được định nghĩa là những người cho thấy tăng 30% oxy hóa, có giá trị cơ bản thấp hơn của FRC. Trong hai nghiên cứu, Dyhr et al. [89,90] đã nghiên cứu ảnh hưởng của các thao tác huy động phế nang sau khi thở với PEEP hoặc ZEEP ở bệnh nhân sau phẫu thuật tim. Một cơ chế huy động là cần thiết để tăng FRC và oxy hóa, nhưng cần phải thông khí với PEEP sau đó để đạt được hiệu quả kéo dài trên FRC và oxy hóa.
FRC và mất huy động phế nang
Trong một nghiên cứu nhỏ với tám bệnh nhân thông khí do ARDS, họ nghiên cứu ảnh hưởng của một cơ chế hút đàm qua nội khí quản mở trên oxy hóa và FRC. Việc hút đàm làm giảm cả hai giá trị, trở về mức cơ sở sau khi huy động, nhưng vẫn thấp với thông khí kèm PEEP đơn thuần. [11] Ảnh hưởng của ba loại thủ thuật hút khác nhau, tức là hút mở, hút kín bằng thông khí kiểm soát áp suất và hút kín với thông khí kiểm soát thể tích, đã được nghiên cứu ở bệnh nhân thở sau phẫu thuật tim. FRC đã được giảm đến 15 phút sau khi hút, bất kể phương pháp được sử dụng và có sự thay đổi lớn giữa các cá nhân của các thay đổi FRC sau khi thủ thuật hút. Độ giãn nở cho thấy tương tự, trong khi oxy hóa chỉ giảm sau khi hút kín với thông khí điều khiển thể tích. [92] Ngoài ra, nó đã chứng minh rằng sự cải thiện oxy hóa của một thủ thuật huy động phế nang liên tiếp sau khi hút mở tương quan cao với giảm FRC do hút. Do đó, giảm FRC có thể giúp xác định những bệnh nhân sẽ được hưởng lợi từ thủ thuật huy động, trong điều kiện cải thiện oxy hóa, ngay cả khi không có dữ liệu khí máu. [93] Trong nghiên cứu nhỏ đầu tiên, thông tin này được sử dụng để hướng dẫn thủ thuật huy động phế nang. Bệnh nhân thở máy sau phẫu thuật tim được chia thành hai nhóm dựa trên đáp ứng FRC tương đối của họ sau khi hút nội khí quản mở, tức là > 94% đường cơ sở hoặc < 94% đường cơ sở. Cả hai nhóm sau đó được chọn ngẫu nhiên để nhận hoặc là một thủ thuật huy động phế nang hoặc không có thủ thuật huy động. Kết quả đầu tiên chỉ ra rằng một chiến lược huy động phế nang đã có thể khôi phục lại FRC giảm sau khi hút và cho thấy cải thiện oxy hóa ngắn hạn. [94] Phù hợp với những dữ liệu này, là một nghiên cứu của Lindgren et al. [44] Họ đã chứng minh rằng hút đàm thông qua nội soi khí phế quản bằng sợi quang học trong khi thông khí liên tục, một biến thể của hút nội khí quản khép kín, có thể dẫn đến giảm rõ rệt trong FRC, oxy hóa, và các thông số hô hấp khác ở một số bệnh nhân. Họ kết luận rằng hút kín có thể có tác dụng tương tự như hút mở, chẳng hạn như sự xẹp phổi và nhu cầu có thể cho huy động sau hút đàm.
FRC và cai máy thở
Một nghiên cứu thí điểm nhỏ đánh giá khả năng sử dụng phép đo FRC trong giai đoạn cai máy thở. Trong quá trình chuyển đổi từ thông khí kiểm soát áp suất với PEEP 10 cmH2O chuyển sang kiểm soát áp suất với PEEP 7 cmH2O và sau đó chuyển sang PSV với CPAP là 7 cmH2O, FRC giảm trong khi oxy hóa chỉ giảm khi chuyển sang PSV. Điều này có thể cho thấy sự mất huy động phế nang với PSV. Cho dù FRC có thể giúp hướng dẫn một giao thức cai máy thở nên được nghiên cứu thêm.
FRC và thông khí bảo vệ phổi
Trong vài năm qua, Gattinoni và Pesenti [96] đã giới thiệu khái niệm về stress và strain phổi. Tóm lại, căng thẳng, ví dụ như barotrauma, được định nghĩa là áp lực xuyên phổi, và strain, ví dụ như volutrauma-biotrauma được định nghĩa là sự thay đổi kích thước của phổi so với trạng thái ban đầu của phổi lúc nghỉ, tức là VT/FRC tại ZEEP. Tỷ lệ giữa stress và strain là độ đàn hồi phổi đặc hiệu (specific lung elastance), được giả định là không đổi hoặc nằm trong giới hạn hẹp trong ARDS. Bằng cách biết VT và FRC, stress và strain có thể được tính toán.
Do đó, FRC có thể là cơ sở để cài đặt thông khí bảo vệ phổi. Tính toán VT lý tưởng như một phần của FRC đo sẽ lý tưởng hơn về tình trạng phổi cá nhân so với tính VT dựa trên chiều cao và giới tính. Stress và strain có thể đại diện cho các thông số tốt hơn để cài đặt thông khí phù hợp với nhu cầu cá nhân và giảm thiểu tổn thương phổi do thở máy hơn là áp lực cao nguyên và VT được chuẩn hóa cho trọng lượng cơ thể lý tưởng. [13]
Tóm lại, các phép đo FRC ở những bệnh nhân thông khí đã được thực hiện trong nhiều môi trường lâm sàng khác nhau, bao gồm tối ưu hóa PEEP, hút đàm qua nội khí quản, tư thế nằm sấp, và cai máy từ thông khí cơ học. Mất huy động phế nang, ví dụ: sau khi hút đàm qua nội khí quản hoặc điều chỉnh mức PEEP xuống thấp, có thể dễ dàng được theo dõi. Những cải thiện trên FRC mà không có sự thay đổi của cài đặt thông khí có thể cho thấy việc huy động phế nang.
Vì FRC có vẻ không nhạy cảm với việc quá căng chướng phế nang của các vùng phổi đã tăng cao, nên tham số này không bao giờ nên được sử dụng một mình cho việc ra quyết định lâm sàng. Sự kết hợp của oxy hóa và/hoặc độ giãn nở cùng với các phép đo FRC có thể cung cấp thông tin có giá trị. FRC có thể là cơ sở để cài đặt thông khí bảo vệ phổi. Cần nghiên cứu sâu hơn để xác định vai trò chính xác của FRC trong giám sát và có lẽ là hướng dẫn cho thông khí cơ học.
Kết luận
Bởi vì các thông số đo thường xuyên để hướng dẫn điều trị hô hấp có những hạn chế của chúng, đo trực tiếp thể tích phổi, tức là FRC đã được khuyến cáo. Các phép đo FRC đã được sử dụng từ những năm 1980 ở những bệnh nhân thông khí. Nhưng các thiết bị cồng kềnh và các lỗi đo lường gộp lại đã cản trở việc sử dụng lâm sàng thông thường của nó. Sau khi một số vấn đề kỹ thuật đã được giải quyết trong vài năm qua, một số kỹ thuật đo thường xuyên FRC của bệnh nhân thông khí ở đầu giường đã được trình bày.
Dữ liệu thực nghiệm và nghiên cứu lâm sàng ở người cho thấy giá trị FRC có thể cung cấp thông tin giá trị trong quá trình thông khí cơ học. Các phép đo FRC có thể giúp theo dõi sự tiến triển của chấn thương phổi, cho thấy sự huy động và mất huy động phế nang, và tối ưu hóa các cài đặt PEEP. Vì FRC có vẻ không nhạy cảm với việc quá căng chướng phế nang, nên không nên sử dụng chỉ số FRC một mình. Ảnh hưởng của các yếu tố khác nhau hiện diện trong quá trình điều trị chăm sóc đặc biệt trên các giá trị FRC, bao gồm tăng áp lực trong ổ bụng, mức độ an thần, và tư thế cơ thể, cần được làm rõ. Các nghiên cứu sâu hơn nên đánh giá vai trò chính xác của phép đo FRC kết hợp với oxy hóa và độ giãn nở hô hấp hoặc các phương thức theo dõi khác như EIT.





