Hội chứng suy hô hấp cấp tính (ARDS) không được xác định ở trẻ sơ sinh, mặc dù đã được công nhận chính thức từ lâu về hội chứng ARDS trong giai đoạn sau của cuộc đời. Chúng tôi mô tả Dự án ARDS sơ sinh: một dự án quốc tế, hợp tác, đa trung tâm và đa ngành nhằm tạo ra một định nghĩa đồng thuận ARDS cho trẻ sơ sinh áp dụng từ thời kỳ chu sinh. Định nghĩa được tạo ra thông qua các cuộc thảo luận giữa năm thành viên chuyên gia của Hiệp hội Chăm sóc Chuyên sâu Trẻ em và Trẻ sơ sinh Châu Âu; bốn chuyên gia của Hiệp hội nghiên cứu nhi khoa châu Âu; hai chuyên gia độc lập từ Hoa Kỳ và hai từ Úc. Tài liệu này cung cấp định nghĩa đồng thuận đầu tiên cho ARDS sơ sinh (được gọi là định nghĩa Montreux). Chúng tôi cũng cung cấp sự đồng thuận của các chuyên gia rằng các cơ chế gây ra ARDS ở người lớn và trẻ lớn, cụ thể là rối loạn chức năng chất hoạt động bề mặt phức tạp, viêm mô phổi, mất thể tích phổi, tăng shunt và tổn thương phế nang lan tỏa cũng xuất hiện trong một số rối loạn hô hấp sơ sinh nặng.
Bài viết được dịch bởi Bác sĩ Đặng Thanh Tuấn – Bệnh viện nhi đồng 1 từ bài báo The Montreux definition of neonatal ARDS: biological and clinical background behind the description of a new entity trên tạp chí The Lancet.
https://drive.google.com/file/d/1mXIX_gs68f5SU8_-ycByYrZcs7TDNI8K/view?fbclid=IwAR2ORr6_SeIrczYEfNwEOh_m62l3koV7_R67sX778rQQQZVUfcfvw-ORpdY
Thông điệp chính
Hội chứng suy hô hấp cấp tính (ARDS) tồn tại ở trẻ sơ sinh và có thể xảy ra độc lập với tuổi thai, một giả thuyết được hỗ trợ bởi các đặc điểm sinh lý và sinh lý bệnh tương tự của ARDS và một số tình trạng hô hấp quan trọng điển hình ở trẻ sơ sinh.
ARDS sơ sinh, tương tự như ARDS ở trẻ lớn và người lớn, được đặc trưng bởi viêm phổi lan rộng và dị hóa chất hoạt động bề mặt dẫn đến rối loạn chức năng phổi. Các cơ chế này có thể xảy ra đồng thời với các cơ chế khác điển hình của tuổi sơ sinh (nghĩa là thiếu hụt định lượng chất hoạt động bề mặt và thiếu hình thành phế nang).
Một định nghĩa cụ thể về ARDS sơ sinh (định nghĩa Montreux) đã được ban hành bởi sự đồng thuận của chuyên gia sau khi sửa đổi tài liệu bởi các chuyên gia về chăm sóc sức khỏe trẻ sơ sinh, nhi khoa và hô hấp người lớn và với sự chứng thực của Hiệp hội Chăm sóc Trẻ sơ sinh Châu Âu và Hiệp hội Châu Âu Nghiên cứu nhi khoa.
Định nghĩa Montreux cho ARDS sơ sinh gần giống với định nghĩa về ARDS ở bệnh nhân ở các độ tuổi khác, nhưng đặc thù của trẻ sơ sinh và đặc điểm của chăm sóc quan trọng ở trẻ sơ sinh cũng được xem xét.
Định nghĩa Montreux có thể được sử dụng cho các mục đích lâm sàng, dịch tễ học và nghiên cứu. Một nghiên cứu đoàn hệ dựa trên mạng, đa quốc tế, tiền cứu, đã được triển khai để mô tả quá trình lâm sàng và kết cục của trẻ sơ sinh với ARDS.
Giới thiệu
Hội chứng suy hô hấp cấp tính (ARDS) không được xác định ở trẻ sơ sinh, mặc dù sự công nhận lâu dài của ARDS trong cuộc sống sau này. Chúng tôi mô tả Dự án ARDS sơ sinh: một dự án quốc tế, hợp tác, đa trung tâm và đa ngành nhằm tạo ra một định nghĩa đồng thuận ARDS cho trẻ sơ sinh áp dụng từ thời kỳ chu sinh. Dự án này là một sáng kiến được Hiệp hội Chăm sóc Trẻ em và Trẻ sơ sinh Châu Âu (ESPNIC) và Hiệp hội Nghiên cứu Nhi khoa Châu Âu (ESPR) tán thành. Ban chỉ đạo Dự án ARDS sơ sinh lần đầu tiên xem xét tài liệu về các đặc điểm sinh học, sinh lý bệnh học và mô học của ARDS ở trẻ sơ sinh so với các nhóm tuổi khác và về các định nghĩa hiện tại về ARDS ở trẻ lớn và người lớn. Định nghĩa đồng thuận sau đó được phát triển từ phân tích tài liệu này. Bài viết này cũng trình bày cơ sở lý luận để ban hành một định nghĩa cụ thể về ARDS ở trẻ sơ sinh.

Tuổi và sự phát triển của định nghĩa ARDS
ARDS ban đầu được báo cáo ở 12 bệnh nhân (bao gồm trẻ 11 tuổi) bởi Ashbaugh và đồng nghiệp1 ở The Lancet vào năm 1967. Họ đã mô tả ARDS là chứng khó thở, thở nhanh, tím tái kháng trị liệu bằng oxy, mất độ giãn nở phổi và thâm nhiễm phế nang lan tỏa, “các khu vực phổi xẹp, phù phế nang và xuất huyết” khi tử thiết. Sự tương đồng về lâm sàng và mô học với hội chứng suy hô hấp (RDS) ở trẻ sơ sinh do thiếu hụt chất hoạt động bề mặt nguyên phát2,3 được nhận ra sớm. Thật vậy, ban đầu từ “A” một trong các từ viết tắt ARDS ban đầu là dành cho người lớn để phân định hai thực thể. Mặc dù cả RDS và ARDS đều có chung đặc điểm lâm sàng, sự khác biệt của hai hội chứng đã được chứng minh dựa trên sự khác biệt về sinh lý bệnh học và bệnh học. Có thể cho rằng sự khác biệt này đã hạn chế nhận thức về ARDS trong y học sơ sinh trong một thời gian dài.
Định nghĩa về ARDS đã phát triển đáng kể từ năm 1967 do kiến thức ngày càng tăng của chúng tôi về sinh học chất hoạt động bề mặt và sinh lý học ARDS. ARDS hiện được gọi là hội chứng suy hô hấp cấp tính chính xác hơn, nhận ra rằng các biểu hiện lâm sàng của ARDS không giới hạn ở các nhóm tuổi cụ thể. Điều trị với áp lực dương cuối thì thở ra đã được tìm thấy là có hiệu quả4 và giảm độ giãn nở hệ hô hấp đã được hiển thị.5 Song song, ARDS được công nhận là một quá trình lan tỏa, thay vì khu trú, trong mô phổi. Khái niệm quan trọng này đã dẫn đến một định nghĩa X quang về ARDS bao gồm thâm nhiễm phế nang không đều hai bên với sự tham gia của một số trường phổi (phổi trắng đặc trưng).6 Sau đó, một ngưỡng áp lực mao mạch phổi được đưa vào để cho phép phân biệt ARDS với suy tim sung huyết.6 Khái niệm rằng ARDS có thể được gây ra bởi một số lượng lớn các tình trạng phổi nguyên phát hoặc thứ phát với một số yếu tố nguy cơ, đã được đưa ra vào năm 1988.7 Điểm số tổn thương phổi do Murray và đồng nghiệp tạo ra đã được sửa đổi bởi Newth và đồng nghiệp8 gần một thập kỷ sau đó và một phiên bản nhi khoa đã được đề xuất. Điểm tổn thương phổi ở trẻ em được xác nhận bên ngoài về cơ bản bao gồm điểm số của Murray và đồng nghiệp7 sử dụng các ngưỡng áp lực dương cuối thì thở ra khác nhau và với độ giãn nở được tính theo cân nặng bệnh nhân. [9], [10].
Định nghĩa của ARDS là một bệnh lý và lâm sàng thực thể đã phát triển thông qua sự đồng thuận của chuyên gia hơn 20 năm. Định nghĩa Hội nghị Đồng thuận Âu-Mỹ năm 1994 đã được sử dụng rộng rãi cho nghiên cứu và chăm sóc lâm sàng.11 Tuy nhiên, định nghĩa Hội nghị Đồng thuận Âu-Mỹ thường bị chỉ trích do: thiếu khung thời gian cấp tính; đánh giá không chính xác về suy giảm oxy; sự vắng mặt của một danh sách cụ thể các yếu tố nguy cơ; và sự cần thiết phải đo áp lực mao mạch phổi xâm lấn. Định nghĩa gần đây của Berlin 12,13 đã giải quyết những hạn chế này và thêm vào đó là ba loại mức độ nặng lâm sàng. Định nghĩa Berlin đã được xác thực trong một số lượng lớn bệnh nhân tham gia vào các thử nghiệm ARDS và cơ sở dữ liệu bệnh viện và chính xác hơn định nghĩa của Hội nghị đồng thuận Âu-Mỹ trong việc dự đoán tỷ lệ tử vong hoặc ngày không thở máy. [12] , [13] Mặc dù độ giãn nở hệ thống hô hấp được đo ở bệnh nhân với ARDS nặng, việc sử dụng nó đã không cải thiện dự đoán tử vong và do đó đã bị loại khỏi định nghĩa cuối cùng của Berlin. [12].
ESPNIC đã tiến hành đa trung tâm quốc tế đầu tiên nghiên cứu để xác nhận định nghĩa Berlin ở trẻ nhũ nhi (lớn hơn một tháng) và trẻ mới biết đi bị ARDS.[14] Các xác nhận nhi khoa khác về định nghĩa Berlin đã làm theo sau đó. [15] , [16]. Sau đó, Hội nghị đồng thuận chấn thương phổi cấp tính ở trẻ em (PALICC), một nhóm các bác sĩ chuyên khoa nhi khoa quốc tế, đã đưa ra định nghĩa cụ thể đầu tiên cho ARDS nhi. [17] Định nghĩa PALICC thể hiện một tiến bộ lớn trong việc xác định ARDS, nhưng không đề cập cụ thể đến đặc thù của tuổi sơ sinh hoặc bao gồm các biểu hiện của ARDS trong giai đoạn chu sinh.
Các định nghĩa PALICC và Berlin có chung các đặc điểm quan trọng nhưng cũng có sự khác biệt có liên quan. [12] ,[13], [17]. PALICC chấp nhận sử dụng các tiêu chí dựa trên độ bão hòa oxy khi áp lực riêng phần của oxy động mạch (PaO2) không có sẵn; PALICC sử dụng chỉ số oxygen hóa và chỉ số bão hòa oxygen hóa thay vì tỷ lệ PaO2 chia cho nồng độ oxy hít vào (FiO2) và cho phép trẻ em mắc bệnh phổi mãn tính hoặc bệnh tim bẩm sinh tím trước đó. Khi đánh giá việc áp dụng các định nghĩa ARDS khác nhau, sử dụng tiêu chí PALICC làm tăng số lượng bệnh nhân được chẩn đoán mắc ARDS ở trẻ em và làm giảm tỷ lệ tử vong chung. Tuy nhiên, ARDS ở trẻ em nặng có liên quan đến tỷ lệ tử vong cao, đặc biệt là nếu rối loạn xuất hiện sau 24 giờ chẩn đoán ban đầu.[18].
Tại sao chúng ta cần một định nghĩa về ARDS sơ sinh?
Tháng đầu tiên của cuộc đời (tức là thời kỳ sơ sinh) là giai đoạn sống duy nhất được đặc trưng bởi nguy cơ tử vong cao.[19] Viện Hàn lâm Nhi khoa Hoa Kỳ khuyến cáo rằng các nguyên nhân gây tử vong sẽ được xác định cụ thể cho tháng đầu tiên của cuộc đời và bao gồm cả chu sinh các sự kiện và mức độ trưởng thành của thai nhi.[20] Định nghĩa PALICC17 đặc biệt loại trừ các nguyên nhân gây thiếu oxy máu cấp tính duy nhất trong giai đoạn chu sinh. RDS chính liên quan đến sinh non rõ ràng khác với ARDS ở trẻ em và cần được loại trừ. Tuy nhiên, không có bằng chứng sinh học hoặc lâm sàng nào cho thấy tổn thương phổi nặng chu sinh, chẳng hạn như hội chứng hít phân su hoặc viêm phổi lan tỏa bẩm sinh, khác với ARDS ở trẻ em. Thay vào đó, bằng chứng mạnh mẽ cho thấy các cơ chế liên quan đến ARDS cũng xảy ra ở một số rối loạn hô hấp nặng ở trẻ sơ sinh.
Việc loại trừ các rối loạn sơ sinh khỏi phổ ARDS làm giảm nhận thức liên ngành. Trên thực tế, các bác sĩ sơ sinh thường không quen thuộc với các tài liệu về ARDS ở người lớn và trẻ em, trong khi đó, các bác sĩ chuyên khoa nhi thường không biết về sự xuất hiện của các rối loạn hô hấp sơ sinh nặng ở trẻ sơ sinh. Việc không nhận ra phổ ARDS phổ biến và thiếu chuyển giao kiến thức liên ngành đã làm giảm các liên kết giữa các trung tâm, phổ biến chăm sóc lâm sàng tối ưu và khả năng nghiên cứu trong ARDS sơ sinh. Hơn nữa, ở một số khu vực địa lý, trẻ sơ sinh bị bệnh nặng có thể được chăm sóc cả ở các đơn vị chăm sóc đặc biệt cho trẻ sơ sinh và trẻ em.[21],[22].
Mặc dù định nghĩa PALICC độc lập với tuổi bệnh nhân,[17] nhưng một số khía cạnh làm giảm sự phù hợp của nó đối với trẻ sơ sinh. Chăm sóc quan trọng sơ sinh có các tính năng kỹ thuật cụ thể liên quan đến kích thước bệnh nhân. Một số công cụ lâm sàng và kỹ thuật theo dõi được sử dụng trong định nghĩa PALICC không được sử dụng phổ biến trong chăm sóc quan trọng ở trẻ sơ sinh, bao gồm ống có bóng chèn và đo khoảng chết hô hấp hoặc độ giãn nở tĩnh, vì các công cụ lâm sàng này không thể thực hiện được hoặc do máy thở sơ sinh không cung cấp một số kỹ thuật (ví dụ, thủ thuật tắc nghẽn cuối thì hít vào và cuối thì thở ra). Các tác động sinh lý không thể đoán trước của quá trình chuyển đổi cuộc sống của thai nhi, chẳng hạn như nồng độ hemoglobin của thai nhi thay đổi, cũng có thể ảnh hưởng đến độ bão hòa oxyhaemoglobin ngoại biên (SpO2), tỷ lệ SpO2-FiO2 và shunt trong phổi.[23],[24] Trong khi PALICC bao gồm thông khí áp lực dương. sử dụng trong chăm sóc quan trọng cho trẻ sơ sinh là không thường xuyên, thiếu bằng chứng,[25] và thường không có sẵn trong nhiều máy thở sơ sinh. Ngược lại, việc sử dụng thông khí dao động tần số cao là phổ biến hơn trong chăm sóc quan trọng ở trẻ sơ sinh và được chứng minh bằng bằng chứng lớn hơn ở trẻ lớn và bệnh nhân người lớn.[26],[27] Hơn nữa, bản chất và hậu quả của suy hô hấp nặng ở trẻ sơ sinh rất phức tạp bởi các yếu tố phát triển điều đó có thể ảnh hưởng đến tiên lượng và dịch tễ học. Trẻ sơ sinh có thể có: các tác nhân duy nhất gây suy hô hấp (ví dụ, hội chứng hít phân su, ngạt chu sinh, viêm ruột hoại tử) có thể khác nhau đối với ARDS và ARDS ở trẻ em; sự khác biệt trong các khía cạnh cụ thể của sinh học phổi phát triển và trưởng thành (giai đoạn phế nang hoặc giai đoạn sớm) và dễ bị loạn sản phế quản phổi, có thể gây ra hậu quả lâu dài khác nhau ở trẻ sơ sinh so với tổn thương phổi ở trẻ lớn và bệnh nhân người lớn; và giảm khả năng phòng vệ miễn dịch tại chỗ và toàn thân, có khả năng gây ra các hình ảnh lâm sàng nặng hơn.
Do đó, chúng tôi lập luận rằng một trường hợp mạnh tồn tại cho một định nghĩa về ARDS cụ thể cho tháng đầu tiên của cuộc đời. Một định nghĩa như vậy sẽ làm tăng nhận thức về suy hô hấp nặng ở trẻ sơ sinh và liên kết chuyên môn hiện có trong cộng đồng chăm sóc quan trọng ở trẻ em và người lớn với thực hành sơ sinh. Định nghĩa này cũng sẽ giúp dự đoán tiên lượng và hướng dẫn các chuyên gia chăm sóc sức khỏe sử dụng liệu pháp nào dựa trên mức độ phù hợp hoặc tỷ lệ nguy cơ lợi ích của họ.[12],[13] Định nghĩa ARDS sơ sinh sẽ thúc đẩy nghiên cứu cơ bản, cải thiện sự hiểu biết về dịch tễ học ARDS trẻ sơ sinh và hướng dẫn chăm sóc đồng dạng cho bệnh nhân mắc ARDS, với các lợi ích sức khỏe cộng đồng tiềm năng.
ARDS sơ sinh có thực sự tồn tại?
Từ chiến lược tìm kiếm của chúng tôi, chúng tôi đã lấy được 32 ấn phẩm sử dụng thuật ngữ ARDS sơ sinh: 23 lâm sàng (chủ yếu là loạt ca bệnh) và chín nghiên cứu mô hình động vật sơ sinh tịnh tiến (xem phụ lục). Lần đầu tiên sử dụng thuật ngữ ARDS sơ sinh vào năm 1989 đã mô tả 11 trẻ sơ sinh mắc ARDS liên quan đến ngạt chu sinh và hít phân su hoặc hít máu.[28] Faix và đồng nghiệp [28] kết luận rằng ARDS có thể và xảy ra ở trẻ sơ sinh. Chúng tôi thấy không có lý do tại sao hội chứng này không thể được áp dụng cho một số bệnh hô hấp sơ sinh cổ điển hơn để tạo ra một tình huống lâm sàng tồi tệ hơn nữa.[17].
Mặc dù các bác sĩ lâm sàng nhận thức được sự tồn tại có thể của ARDS ở trẻ sơ sinh, nhưng nó vẫn không được phân loại là một thực thể. Sự cần thiết phải thiết lập một thực thể để xác định ARDS sơ sinh thừa nhận sự khác biệt quan trọng giữa trẻ sơ sinh và người lớn. Phổi sơ sinh tiếp tục trải qua quá trình phế nang hóa và do đó trẻ sơ sinh có ít phế nang hơn người lớn. Ngưng lại sự phát triển, bao gồm các đặc điểm của loạn sản phế quản phổi, có thể xuất hiện ở phổi của trẻ sơ sinh do những thương tổn và trị liệu trước đó. Thành ngực đàn hồi hơn, sự sắp đặt và cấu trúc của cơ hoành khác với người lớn và cơ hoành đóng góp nhiều hơn vào thông khí khí lưu thông ở trẻ sơ sinh so với người lớn Thông khí khí lưu thông ở trẻ sơ sinh sử dụng thể tích khí lưu thông nhỏ hơn và tần số cao hơn.
Cả miễn dịch bẩm sinh và có được đều phải tuân theo sửa đổi rộng rãi trong cuộc sống của thai nhi và trong thời kỳ chu sinh, [29] và trẻ sơ sinh non tháng đã tăng khả năng nhạy cảm đối với các tác nhân truyền nhiễm. Trẻ sơ sinh cũng có tình trạng bệnh phối hợp hoặc các bệnh lý có sẳn khác nhau.
Đặc điểm cụ thể của trẻ sơ sinh có thể ảnh hưởng đến dịch tễ học, diễn biến lâm sàng và tiên lượng của ARDS sơ sinh. Các tác nhân và đặc điểm của ARDS sơ sinh có thể khác với các lứa tuổi khác, tương tự như sự khác biệt đã được quan sát giữa ARDS ở trẻ em và người lớn đối với các yếu tố gây nhiễm trùng, tỷ lệ mắc và tử vong.[30] Những khác biệt này nhấn mạnh rằng điều trị ARDS ở trẻ sơ sinh có thể là khác nhau và chứng minh thêm sự cần thiết cho một định nghĩa ARDS sơ sinh cụ thể.
Cơ sở sinh học, sinh lý bệnh và mô học cho ARDS sơ sinh ARDS được đặc trưng về mặt sinh học bởi rối loạn chức năng bề mặt định tính hoặc định lượng ảnh hưởng đến cả protein và phospholipids, và viêm mô phổi lan rộng.[31],[32] Những quá trình sinh học này có chung điểm với một số rối loạn hô hấp sơ sinh được đặc trưng bởi sự suy yếu chức năng chất hoạt động bề mặt hoặc lượng chất hoạt động bề mặt, thay vì thiếu hụt chất hoạt động bề mặt. Ví dụ, hội chứng hít phân su, viêm phổi do mật và suy hô hấp sau viêm màng đệm nặng hoặc nhiễm trùng huyết là những ví dụ về rối loạn hô hấp ở trẻ sơ sinh nặng.[33], [34],[35],[36],[37],[38].
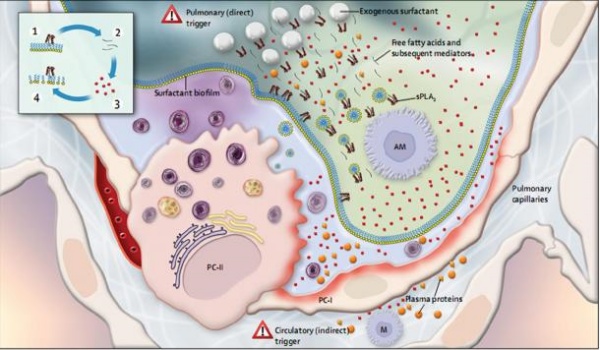
Hình 1: Sinh học của ARDS sơ sinh và tương tác với việc sử dụng chất hoạt động bề mặt ngoại sinh. Một phế nang được mô tả với chất hoạt động bề mặt được tiết ra dưới dạng các thể lamellar và hình thành màng sinh học trên bề mặt phế nang. Các dấu hiệu nguy hiểm đại diện cho các yếu tố kích hoạt ARDS bao gồm các yếu tố kích hoạt trực tiếp (ví dụ viêm phổi và hít phân su hoặc hít sữa) hoặc các yếu tố gián tiếp (ví dụ viêm bào thai, nhiễm trùng huyết và viêm ruột hoại tử). Hình vuông và hình tròn màu đỏ đại diện cho các chất trung gian gây viêm khác nhau, các loại oxy phản ứng và protease được tiết vào khoảng phế nang và mao mạch phổi. Ảnh hưởng của ARDS đối với tổn thương tế bào được thể hiện bằng màu đỏ mờ trên màng của các tế bào phế nang. Các protein huyết tương xuất hiện trong khoảng phế nang có thể làm tổn thương thêm lớp màng chất hoạt động bề mặt và được thể hiện bằng các quả bóng và hình vuông màu cam. Phospholipase A2 tiết được tiết ra bởi các đại thực bào phế nang và được thể hiện với cấu trúc ba chiều thu nhỏ của nó (nhờ MC De Rosa, Phòng thí nghiệm mô hình hóa phân tử, Hội đồng nghiên cứu quốc gia, Rome, Ý) gắn với lớp phospholipid bề mặt. Các axit béo tự do được giải phóng từ quá trình thủy phân phospholipid bề mặt được biểu diễn dưới dạng các vạch ngắn. Hộp tóm tắt chu trình luẩn quẩn [32] được đại diện bởi: (1) quá trình thủy phân phospholipid điều khiển phospholipase; (2) sản xuất axit béo tự do; (3) các chất trung gian gây viêm; (4) tổn thương thêm cho chất hoạt động bề mặt. Chất hoạt động bề mặt ngoại sinh đến phế nang thông qua đường thở được thể hiện bằng các quả bóng màu trắng. Phospholipase A2 cũng có thể thủy phân chất hoạt động bề mặt ngoại sinh, tạo ra axit béo tự do, có thể dẫn đến việc sản xuất các chất trung gian gây viêm hơn nữa. Protein huyết tương và các chất trung gian gây viêm khác cũng làm tổn thương chất hoạt động bề mặt ngoại sinh. Một danh sách đầy đủ các cơ chế bệnh học và tài liệu tham khảo được cung cấp trong phần phụ lục. ARDS = hội chứng suy hô hấp cấp tính. AM = đại thực bào phế nang. M = bạch cầu đơn nhân. PC-I = pneumocyte loại 1. PC-II = pneumocyte loại 2. sPLA2 = phospholipase bài tiết A2. Con số này được điều chỉnh từ Raghavendran và các đồng nghiệp. [41].
| ARDS | Paediatric ARDS | Neonatal ARDS | |||||
| Nhiễm trùng huyết | Viêm phổi* | Hít phân su | Hít sặc† | Xuất huyết phổi | |||
| Crs | Giảm nhiều | Giảm nhiều | Giảm nhiều hoặc ít | Trong giới hạn bình thường hoặc giảm ít‡ | Giảm nhiều | Giảm nhiều | Giảm nhiều |
| Rrs§ | Trong giới hạn bình thường hoặc tăng nhẹ | Trong giới hạn bình thường hoặc tăng nhẹ | Trong giới hạn bình thường hoặc tăng nhẹ | Trong giới hạn bình thường hoặc tăng nhẹ | Thường tăng | Tăng | Trong giới hạn bình thường hoặc tăng |
| Độ lan rộng của tiến trình bệnh lý | Lan tỏa | Lan tỏa | Lan tỏa | Lan tỏa | Lan tỏa | Lan tỏa | Lan tỏa |
| Nguyên nhân¶ | Trực tiếp hoặc gián tiếp | Trực tiếp hoặc gián tiếp | Gián tiếp | Trực tiếp | Trực tiếp | Trực tiếp | Trực tiếp |
Danh sách các tình trạng hô hấp ở trẻ sơ sinh nên được xem là minh họa, bởi vì các rối loạn khác có thể chia sẻ các đặc điểm sinh lý bệnh với ARDS. ARDS = hội chứng suy hô hấp cấp tính. MAS = hội chứng hít phân su. Crs = độ giãn nở hệ hô hấp. Rrs = sức cản hệ hô hấp. * Viêm phổi đề cập đến bất kỳ loại viêm phổi nhiễm trùng hoặc do mật sau khi ứ mật trong thai kỳ. Hít sặc liên quan đến tổn thương phổi liên quan đến việc hít vật chất không phải là phân su (ví dụ: máu mẹ, sữa, dịch tiết dạ dày hoặc mật, và nước trong trường hợp sinh dưới nước). Thay đổi về độ giãn nở có thể thay đổi tùy thuộc vào sự lan rộng của quá trình bệnh lý. §Rrs thường nằm trong phạm vi bình thường hoặc tăng nhẹ ở ARDS và ARDS ở trẻ em, tuy nhiên điều kiện tắc nghẽn tiềm ẩn (ví dụ, loạn sản phế quản phổi) hoặc các bệnh viêm đường thở đồng thời (ví dụ, viêm tiểu phế quản) có thể thay đổi các sức cản này. Hoạt động đề cập đến các yếu tố kích hoạt xảy ra trực tiếp (ví dụ, hội chứng hít ở trẻ sơ sinh và viêm phổi) hoặc gián tiếp trong mô phổi (ví dụ, nhiễm trùng huyết và viêm ruột hoại tử).
Bảng 1: ARDS sơ sinh rối loạn hô hấp có chung sinh lý tương tự với ARDS và ARDS ở trẻ em.
Giống như ARDS, suy giảm thứ phát của chất hoạt động bề mặt nội sinh và tình trạng viêm của phổi trong các rối loạn này giải thích đáp ứng hạn chế và nhất thời đối với việc dùng các chất hoạt động bề mặt ngoại sinh.[39] , [40] Sự suy yếu thứ phát này của chất hoạt động bề mặt có lẽ là do phospholipase A2 tiết ra, gây ra dòng thác viêm và thủy phân phospholipid ở những trẻ bị các bệnh lý sơ sinh và ARDS ở trẻ lớn và người lớn này. 41 Hiện tượng này cũng có thể xảy ra ở trẻ sơ sinh non tháng ngoài sinh lý bệnh đã có từ trước như thiếu phế nang, chức năng hoạt động bề mặt bị suy giảm và thiếu hụt chất hoạt động bề mặt.[37], [38]. Hình 1 minh họa sự tương tác giữa các cơ chế sinh học và chất hoạt động bề mặt trong điều kiện sơ sinh tương tự như ARDS ở trẻ lớn và người lớn. Một danh sách rộng hơn các cơ chế sinh học trong các rối loạn hô hấp sơ sinh này có sẵn trong phần phụ lục.
Bảng 1 tóm tắt các điểm tương đồng sinh lý bệnh giữa các rối loạn hô hấp sơ sinh cụ thể, theo truyền thống được coi là các thực thể riêng biệt, với các yếu tố không liên quan, nhưng mỗi điểm chung có sự tương đồng khi được xem xét trong khuôn khổ sinh lý bệnh của ARDS. Giống như ARDS, những tình trạng này có thể được kích hoạt do tổn thương trực tiếp đến nhu mô phổi (nghĩa là ARDS trực tiếp hoặc nguyên phát) hoặc do quá trình ngoài phổi (ví dụ ARDS gián tiếp hoặc thứ phát), như nhiễm trùng huyết, viêm ruột hoại tử, ngạt chu sinh viêm phổi sau ứ mật sản khoa.[42] Các tầng sinh lý phổ biến của các rối loạn sơ sinh này được tóm tắt trong hình 2.
Nó bao gồm sức căng bề mặt phế nang tăng, làm tăng độ co giãn đàn hồi và giảm độ giãn nở, gây ra tình trạng xẹp phổi không đồng nhất.[31] Quá trình này thường đi kèm với shunt từ phải sang trái và không phù hợp thông khí/tưới máu, làm tăng tình trạng thiếu oxy. Trẻ sơ sinh mắc các rối loạn này cũng có thể có các shunt phức tạp hơn thông qua lỗ bầu dục hoặc ống động mạch, [43] ,[44] và có khả năng tăng sức cản đường thở.[45], [46] Ngoài ra, khung ARDS mang đến tiềm năng hiểu về suy hô hấp cấp tính mãn tính ở trẻ sơ sinh, chẳng hạn như trẻ sơ sinh non tháng mắc chứng loạn sản phế quản tiến triển, ví dụ, hít sặc, viêm phổi hoặc viêm tiểu phế quản. Không giống như RDS ở trẻ sơ sinh, các định nghĩa ARDS cho phép các trạng thái phức tạp, độ giãn nở thấp và sức đề kháng cao xuất hiện đặc trưng ở trẻ sơ sinh mắc ARDS và rối loạn chức năng phế quản phổi. [8] , [45] ,[46] Cuối cùng, phản ứng viêm toàn thân và suy đa cơ quan thứ phát liên quan đến sự cần thiết phải thở máy tích cực [47] thường liên quan đến cả ARDS và rối loạn hô hấp ở trẻ sơ sinh nặng.[48]
Dấu hiệu mô học của giai đoạn cấp tính của ARDS, xảy ra trước sự nổi dậy của xơ hóa lan rộng, là tổn thương phế nang lan tỏa, [1] ,[49] được đặc trưng bởi xuất huyết mô kẽ và phế nang hoặc phù viêm, thâm nhiễm tế bào và xẹp phổi với sự hình thành của màng hyaline. Hít sặc sữa, [52] hoặc hít nước sau khi sinh dưới nước, [53] nhiễm trùng huyết và viêm phổi nhiễm trùng, [54],[55] xuất huyết phổi, 56 ngạt chu sinh phức tạp do suy hô hấp nặng, [57] và viêm phổi do mật.[58]
Sự tương đồng về sinh học, sinh lý bệnh và mô học giữa ARDS và một số rối loạn hô hấp ở trẻ sơ sinh, bao gồm cả những bệnh xảy ra trong thời kỳ chu sinh, cung cấp một lý do mạnh mẽ để xác định các rối loạn này là ARDS sơ sinh.
Các phương pháp được sử dụng trong Dự án ARDS sơ sinh
Một dự án hợp tác đa ngành quốc tế đã bắt đầu vào tháng 1 năm 2014, với mục đích phác thảo và thử nghiệm một định nghĩa cho ARDS sơ sinh. Phương pháp dự án được tóm tắt trong hình 3. Các chuyên gia chăm sóc hô hấp từ các đơn vị chăm sóc đặc biệt cho trẻ sơ sinh và nhi khoa đại diện cho ESPNIC, ESPR và các đồng nghiệp chuyên gia độc lập, đã được liên hệ để thành lập Ban chỉ đạo gồm 12 thành viên. Các chuyên gia đã được lựa chọn sau khi thảo luận trong Hội đồng ESPNIC và ESPR, trên cơ sở nghiên cứu của họ về chăm sóc hô hấp quan trọng ở trẻ em và trẻ sơ sinh trong 10 năm qua. Bởi vì y học hô hấp là một lĩnh vực chăm sóc quan trọng của trẻ sơ sinh, các chuyên gia không được chọn một cách có hệ thống và quy mô của Ban chỉ đạo được quyết định bằng cách lấy mẫu thuận tiện.
Ban chỉ đạo thường xuyên liên lạc thông qua email hoặc thảo luận từ xa được hỗ trợ bởi một ban thư ký hành chính của ESPNIC. Các cuộc gặp mặt trực tiếp cũng được tổ chức cùng với các Hiệp hội học thuật nhi khoa và Viện hàn lâm nhi khoa châu Âu. Dự án ARDS sơ sinh đã nhận được chứng thực ESPNIC và ESPR theo các thủ tục nội bộ phù hợp. Một tác giả, GC, một chuyên gia về chăm sóc quan trọng dành cho người lớn, cũng đã được tư vấn và tham gia các cuộc thảo luận về định nghĩa ARDS, sinh học và sinh lý học, nhưng không tham gia vào các cuộc họp về sự đồng thuận về định nghĩa ARDS sơ sinh.
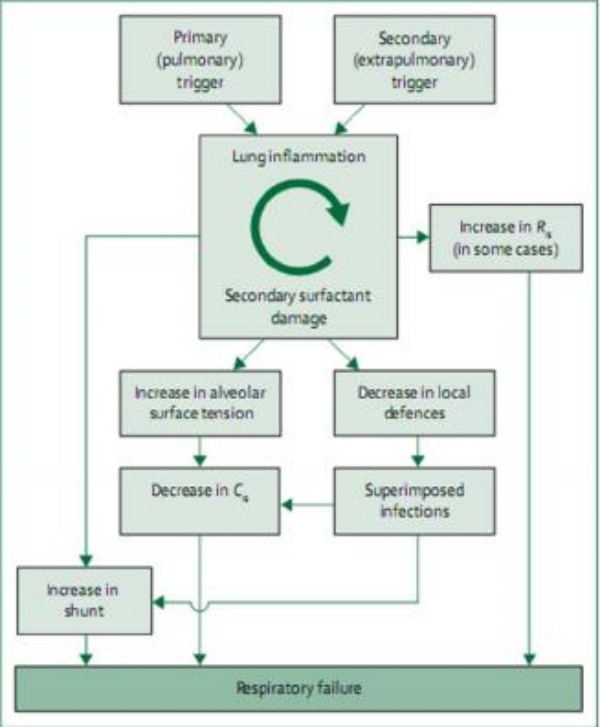
Hình 2: Dòng sinh lý bệnh của ARDS sơ sinh Các yếu tố kích thích phổi điển hình bao gồm nhiễm trùng tại chỗ, viêm phổi do mật, viêm phế quản và hít dịch phân, máu, nước, sữa, mật hoặc dịch tiết dạ dày; các yếu tố kích thích ngoài phổi điển hình bao gồm nhiễm trùng huyết hoặc các tình trạng viêm toàn thân (ví dụ viêm bào thai, viêm màng đệm, viêm ruột hoại tử hoặc ngạt chu sinh). Tất cả các yếu tố kích hoạt chu kỳ tổn thương viêm – chất hoạt động bề mặt (viêm phổi gây ra tổn thương chất hoạt động bề mặt thứ cấp, gây viêm phổi). Shunt từ phải sang trái có thể là trong phổi hoặc ngoài phổi vì sự hiện diện có thể của còn ống động mạch hoặc lỗ bầu dục. Crs = độ giãn nở hệ hô hấp. Rrs = sức cản hệ hô hấp.
Ủy ban đã sử dụng một kỹ thuật đồng thuận dựa trên Quaker, [59] bao gồm các cuộc thảo luận mở với việc lắng nghe và chia sẻ thông tin và câu hỏi tích cực, với các ý tưởng và giải pháp kết quả được quy cho toàn bộ nhóm.[59], [60] Không cần bỏ phiếu cho bất kỳ điểm cụ thể nào, bởi vì, sau các cuộc thảo luận, sự nhất trí đã đạt được trên mọi điểm của định nghĩa. Hơn nữa, các thành viên Ban chỉ đạo đã hợp tác trước các dự án khác hoặc biết nhau, do đó không có ảnh hưởng cá nhân nào rõ ràng. Kỹ thuật Quaker có thể tăng thời gian đạt được sự đồng thuận. Thời gian dành cho giai đoạn này của Dự án ARDS sơ sinh là đủ để cho phép mọi người bày tỏ ý tưởng của mình và trao đổi thông tin đa ngành.
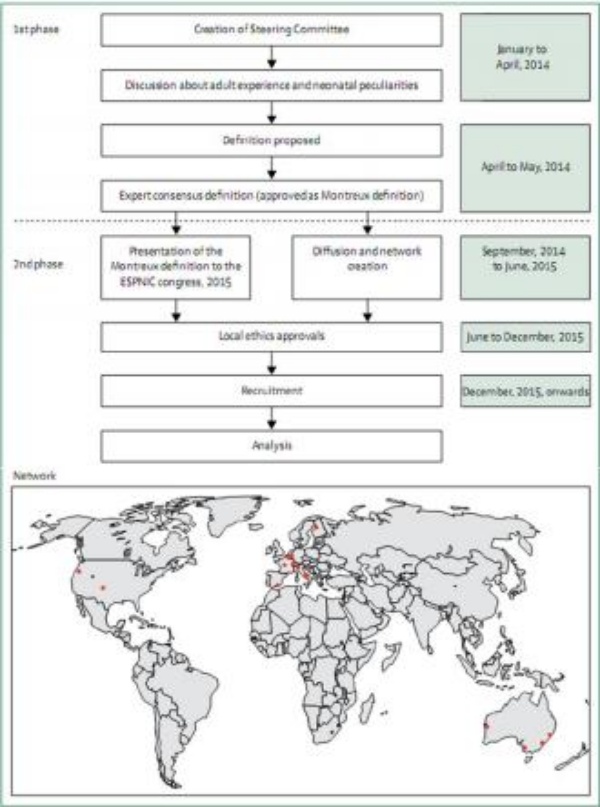
Hình 3: Dự án ARDS sơ sinh: quy trình làm việc và các trung tâm liên quan đến mạng lưới (tính đến tháng 11 năm 2016) Mạng lưới bao gồm hai trung tâm điều phối bao gồm Bệnh viện Đại học Nam Paris (Trung tâm y tế A.Beclere, Paris, Pháp) và Đại học Western Úc (Perth, Úc) và các trung tâm tham gia (phụ lục) theo tháng 11/2016.
Chúng tôi thừa nhận rằng phương pháp này có thể đưa ra một số hạn chế đáng kể, như ảnh hưởng của các ý kiến mạnh mẽ, thiếu ẩn danh hoặc các yếu tố bên ngoài khác nhau so với các kỹ thuật đồng thuận khác. Cách tiếp cận này cũng có thể khiến các thành viên ít chi phối của nhóm đồng ý về các vấn đề hơn là đưa ra một ý kiến khác. Tuy nhiên, chúng tôi tin rằng thời gian thảo luận phần nào làm giảm ảnh hưởng của những hạn chế này đến kết quả và kỹ thuật này là phù hợp nhất cho một cuộc thảo luận nhóm liên ngành.
Theo định nghĩa ARDS gần đây nhất, 12 chúng tôi đã sử dụng một loạt các tiêu chí cơ bản để tạo ra một định nghĩa về ARDS sơ sinh: khởi phát cấp tính; suy giảm oxy với thể tích phổi cuối thì thở ra giảm, cần áp lực dương để huy động phế nang; suy hô hấp không được giải thích đầy đủ bằng phù phổi do suy tim; và thâm nhiễm lan tỏa hai bên với mất thông khí trên X quang phổi.12 Trên cơ sở các tiêu chí này, các rối loạn hô hấp ở trẻ sơ sinh sau đây sẽ đủ điều kiện chẩn đoán ARDS: hít phân su, sữa, mật, máu, hoặc hít nước, xuất huyết phổi và nhiễm trùng hoặc viêm phổi do mật. Chúng tôi cũng xác định các quá trình cấp tính xảy ra trong các hệ thống cơ quan ngoài phổi có thể gây ra suy hô hấp cấp tính thông qua các phản ứng viêm toàn thân và do đó đáp ứng các tiêu chí ARDS, chẳng hạn như nhiễm trùng huyết khởi phát sớm hoặc khởi phát muộn, viêm bào thai, ngạt chu sinh và viêm ruột hoại tử. [61]
Định nghĩa Montreux của ARDS sơ sinh
Ủy ban duy trì tính nhất quán trong các định nghĩa ARDS [12] và ARDS [17] ở trẻ em nếu có thể. Bảng 2 cho thấy định nghĩa Montreux cuối cùng về ARDS sơ sinh, được phê chuẩn bởi sự đồng thuận của Ban chỉ đạo tại một cuộc họp ở Montreux (Thụy Sĩ). Mười điểm sau đây được đề cập trong cuộc họp Ủy ban này cần được nhấn mạnh. Đầu tiên, định nghĩa về ARDS sơ sinh áp dụng cho trẻ sơ sinh từ sơ sinh đến 44 tuần tuổi sau kỳ kinh cuối hoặc đến 4 tuần tuổi sau sinh (đối với trẻ sơ sinh sau 40 tuần, tuổi sau kỳ kinh cuối) để tính đến vai trò của sinh non; Nên chẩn đoán ARDS ở trẻ lớn hơn giới hạn độ tuổi này theo định nghĩa PALICC.[17] Thứ hai, phải đáp ứng tất cả năm tiêu chí được liệt kê trong bảng 2 để chẩn đoán ARDS sơ sinh và thứ ba, với điều kiện là tất cả năm tiêu chí đều được đáp ứng, không có ngưỡng nào cho cân nặng khi sinh hoặc tuổi thai tồn tại. Điểm thứ tư cần nhấn mạnh là ARDS sơ sinh có thể được kích hoạt bởi các điều kiện chu sinh được thảo luận trong Tài liệu này, tuy nhiên, các kích hoạt này không đầy đủ; các điều kiện khác có thể kích hoạt ARDS và được tiết lộ trong giai đoạn thứ hai của Dự án ARDS sơ sinh. Điểm thứ năm là định nghĩa Montreux bao gồm trẻ sơ sinh về bất kỳ loại hỗ trợ hô hấp nào; những trẻ được thông khí xâm lấn và không xâm lấn cũng có thể đủ điều kiện chẩn đoán ARDS.
Ba điều kiện sau đây dành riêng cho trẻ sơ sinh giai đoạn, mỗi giai đoạn có một sinh lý bệnh học khác nhau đối với ARDS, tạo thành các tiêu chí loại trừ để chẩn đoán ARDS sơ sinh và bao gồm điểm thứ sáu được đề cập: (1) bất thường bẩm sinh (ví dụ, CCAM phổi, phổi biệt trí hoặc thoát vị hoành), thường có hình ảnh và đặc điểm lâm sàng dễ nhận biết; (2) các rối loạn di truyền của hệ thống chất hoạt động bề mặt, là những dị thường hiếm gặp và có thể biểu hiện lâm sàng theo cách tương tự như ARDS [62] (trong một số trường hợp, có thể cần phải điều tra di truyền cụ thể để loại trừ các tình trạng này); và (3) RDS và thở nhanh thoáng qua của trẻ sơ sinh, là những thực thể riêng biệt với sinh học riêng của chúng (bảng 2). Các tiêu chí bắt buộc để chẩn đoán RDS là suy hô hấp xuất hiện trong vòng 24 giờ đầu tiên của cuộc đời, với đáp ứng đầy đủ, duy trì và kịp thời cho tuyển dụng chất hoạt động bề mặt hoặc phổi hoặc cả hai; tiêu chí bổ sung không bắt buộc là hình ảnh phổi hỗ trợ chẩn đoán hoặc số lượng thể lamellar ≤30 000/mm3 hoặc cả hai. Tiêu chuẩn bắt buộc để chẩn đoán cơn thở nhanh thoáng qua là suy hô hấp nhẹ (Silverman ≤ 3) xuất hiện trong vòng 24 giờ đầu đời và giải quyết trong 72 giờ đầu đời, chỉ cần điều trị bằng oxy bổ sung hoặc áp lực đường thở dương liên tục qua mũi hoặc cả hai; tiêu chí bổ sung không bắt buộc là hình ảnh phổi hỗ trợ chẩn đoán hoặc số lượng thể lamellar > 30000/mm3 hoặc cả hai. Điểm tiếp theo cần nêu lên là chẩn đoán ARDS sơ sinh đòi hỏi phải có sự lan tỏa, hai bên, mờ đục không đều, thâm nhiễm hoặc làm mờ hoàn toàn phổi, không được giải thích đầy đủ bởi các điều kiện thể hiện tiêu chí loại trừ. Tương tự như ARDS ở trẻ lớn và người lớn, mờ đục hoặc thâm nhiễm không phải liên quan đến cả bốn góc phổi, nhưng các quá trình cục bộ gây ra suy hô hấp thiếu oxy cấp tính, như viêm phổi khu trú hoặc viêm tiểu phế quản, không đủ điều kiện là chụp X quang phổi từ bệnh nhân với ARDS.6 ARDS đáp ứng định nghĩa Montreux, tương tự như quy trình được sử dụng cho định nghĩa Berlin, 12 nằm trong phần phụ lục. Việc sử dụng X quang và CT đã được chứng minh là cải thiện độ chính xác của chẩn đoán ARDS.[63] Hình ảnh cho thấy các kích hoạt phổ biến nhất có thể được thảo luận trong các cuộc họp dự án (phụ lục). X quang được thảo luận trong Ban chỉ đạo và tất cả những người thành viên đều nhất trí về chẩn đoán ARDS. Các kỹ thuật hình ảnh khác, chẳng hạn như quét CT và siêu âm phổi không phải lúc nào cũng có sẵn, do đó hình ảnh sử dụng các kỹ thuật này không được cung cấp. Tuy nhiên, những kỹ thuật hình ảnh này nên được sử dụng trong phòng khám nếu có sẵn và đủ chuyên môn lâm sàng tồn tại cho sự giải thích của họ.
Điểm thứ tám cần nhấn mạnh là để đơn giản hóa việc đánh giá và chẩn đoán ARDS ở lứa tuổi nhi khoa, suy giảm oxy được đánh giá với cùng chỉ số oxygen hóa như trong định nghĩa PALICC. Định nghĩa này quy định ngưỡng chỉ số oxygen hóa là 4,0 – 7,9 đối với ARDS nhẹ, 8,0 – 15,9 đối với ARDS vừa phải và 16,0 hoặc cao hơn đối với ARDS nặng.[17] Đối với trẻ sơ sinh được điều trị bằng hỗ trợ hô hấp không xâm lấn, việc tính toán áp lực đường thở trung bình chính xác là khó khăn. Ước tính áp lực đường thở trung bình được áp dụng chỉ nên được thực hiện khi rò rỉ đường thở đã được giảm thiểu, có thể đạt được bằng cách đóng miệng với áp lực nhẹ lên hàm và sử dụng các giao diện có kích thước phù hợp.[64],[65] Giá trị khí máu từ đường động mạch nên được sử dụng để tính chỉ số oxygen hóa. Tuy nhiên, việc lấy mẫu động mạch có thể khó khăn ở một số trẻ sơ sinh; Áp lực oxy qua da là một phép đo thay thế đáng tin cậy.[66] Vì vậy, các giá trị xuyên da được phép trong tính toán chỉ số oxy khi không có giá trị động mạch, và các giá trị này phải đạt được trong các điều kiện thích hợp theo hướng dẫn thực hành lâm sàng của Hiệp hội Chăm sóc Hô hấp Hoa Kỳ [83] và các khuyến nghị cụ thể của nhà sản xuất.
Điểm thứ chín cần nhấn mạnh là nồng độ SpO2 không được sử dụng để đánh giá oxygen hóa ở trẻ sơ sinh theo định nghĩa Montreux vì sự khác biệt lớn về nồng độ hemoglobin của thai nhi [23],[24] và chính sách truyền máu của các đơn vị chăm sóc đặc biệt ở trẻ sơ sinh,[84] và sự không chắc chắn về SpO2 mục tiêu. [88], [89] Các yếu tố này có thể ảnh hưởng đến đường cong phân ly oxy và đánh giá lâm sàng ở trẻ sơ sinh, do đó không nên sử dụng chỉ số bão hòa oxygen hóa hoặc tỷ lệ SpO2-FiO2.
| Khung thời gian | Khởi phát cấp tính (nghĩa là trong vòng một tuần) từ một thương tổn lâm sàng đã biết hoặc nghi ngờ. |
| Tiêu chí loại trừ | RDS, TTN hoặc dị thường bẩm sinh là nguyên nhân suy hô hấp cấp hiện tại. |
| Hình ảnh phổi | Thâm nhiễm hoặc mờ lan tỏa, 2 bên, và không đều, hoặc mờ hoàn toàn phổi, không được giải thích đầy đủ bởi tràn dịch cục bộ, xẹp phổi, RDS, TTN hoặc dị thường bẩm sinh. |
| Nguồn gốc của phù | Không có bệnh tim bẩm sinh giải thích phù (bao gồm cả ống động mạch với tăng lưu lượng máu phổi nếu không có xuất huyết phổi cấp tính). Siêu âm tim là cần thiết để xác minh nguồn gốc của phù. |
| Giảm oxy thể hiện dưới dạng OI * | ARDS nhẹ: 4≤ OI < 8.
ARDS vừa phải: 8 ≤ OI < 16. ARDS nặng: OI ≥16. |
| ARDS = hội chứng suy hô hấp cấp tính. RDS = hội chứng suy hô hấp. TTN = thở nhanh thoáng qua của trẻ sơ sinh. OI = chỉ số oxygen hóa. * OI có thể được tính bằng cách sử dụng máu động mạch hoặc, nếu các giá trị động mạch không có sẵn, các áp lực oxy qua da, với các thiết bị xuyên da được hiệu chuẩn thích hợp. Trong trường hợp tăng áp phổi tồn tại của còn ống động mạch sơ sinh, nên sử dụng các giá trị PaO2 trước ống. Định nghĩa áp dụng từ khi sinh đến 44 tuần, tuổi sau kỳ kinh cuối hoặc đến 4 tuần tuổi sau sinh (đối với trẻ sơ sinh sau 40 tuần, tuổi sau kỳ kinh cuối). Đối với hội chứng được xác định, tất cả các tiêu chí phải được đáp ứng. OI nên được tính toán với các biện pháp chính xác nhất có sẵn. Hội chứng có thể được chẩn đoán ở bất kỳ tuổi thai hoặc cân nặng khi sinh, với điều kiện là dị tật phổi bẩm sinh, RDS và TTN được loại trừ là rối loạn hô hấp nguyên phát. Tiêu chí chẩn đoán RDS và TTN, tiêu chí loại trừ đối với ARDS sơ sinh và đề xuất cải thiện độ tin cậy của các phép đo khí máu qua da được cung cấp trong định nghĩa Montreux của phần ARDS sơ sinh. | |
Bảng 2: Định nghĩa Montreux của ARDS sơ sinh.
Điểm cuối cùng cần giải quyết là tăng phổi dai dẳng ở trẻ sơ sinh là sự kết hợp tốt của một số rối loạn trong phổ ARDS (ví dụ, hội chứng hít phân su, ngạt chu sinh, nhiễm trùng huyết hoặc viêm phổi bẩm sinh).[90] Tương tự như trẻ em và người lớn ARDS và tăng áp phổi, [91] tăng áp phổi tồn tại có thể làm giảm tình trạng thiếu oxy máu ở trẻ sơ sinh bị ARDS do shunt trong phổi hoặc ngoài phổi. Ở trẻ sơ sinh bị tăng áp phổi tồn tại và còn ống động mạch, PaO2 trước ống nên được sử dụng để tính chỉ số oxygen hóa của chúng. Hướng dẫn của Hiệp hội Chăm sóc Hô hấp Hoa Kỳ xem xét các giá trị PaO2 qua da chính xác hơn nếu các thiết bị được hiệu chuẩn ở 44°C.[83] Điều này có thể ngụ ý một số nguy cơ tổn thương da ở trẻ sơ sinh cực kỳ non tháng và một ứng dụng ngắn (trong 10-15 phút) hoặc hiệu chuẩn nhiệt độ thấp hơn có thể được khuyên. Ngược lại, phải luôn luôn tránh các vùng da bị tổn thương và các yếu tố ảnh hưởng đến độ tin cậy của biện pháp xuyên da.83 Sự hiện diện của cả tăng áp phổi tồn tại và ARDS sơ sinh không làm thay đổi tiêu chí định nghĩa Montreux, nhưng thay vào đó cần điều trị bằng oxit nitric theo thực hành lâm sàng hướng dẫn.[92] Thuốc giãn mạch phổi tiếp theo hoặc hỗ trợ cuộc sống ngoài cơ thể cũng nên được xem xét, khi cần thiết.
Bước tiếp theo
Dự án ARDS sơ sinh được chia thành hai giai đoạn chính (hình 3). Giai đoạn đầu tiên nhằm xem xét các tài liệu có sẵn để tạo ra một định nghĩa về ARDS sơ sinh dựa trên sự đồng thuận của chuyên gia về kiến thức khoa học có sẵn: giai đoạn này đã dẫn đến định nghĩa Montreux. Định nghĩa này hiện đã hoặc đang được trình bày tại ESPNIC, ESPR và các đại hội địa phương để xác định các chuyên gia chăm sóc sức khỏe từ các đơn vị chăm sóc đặc biệt cho trẻ sơ sinh và nhi khoa, những người sẵn sàng tham gia vào giai đoạn thứ hai của dự án. Giai đoạn thứ hai bao gồm một nghiên cứu đoàn hệ tiềm năng, đa trung tâm, dựa trên mạng lưới, trong đó trẻ sơ sinh thực hiện định nghĩa Montreux được đăng ký để: mô tả dịch tễ học, diễn tiến lâm sàng và tiên lượng của trẻ sơ sinh bị ảnh hưởng bởi ARDS sơ sinh; xác định danh sách các yếu tố nguy cơ đối với ARDS sơ sinh, vì nó tồn tại cho người lớn và trẻ lớn hơn mắc ARDS; và hướng dẫn các nghiên cứu trong tương lai. Bởi vì nghiên cứu này là nghiên cứu đầu tiên về một điều kiện mới được xác định, nên không thể tính toán kích thước mẫu chính thức và nó sẽ ghi nhận kích thước mẫu thuận tiện của ít nhất 220 trẻ sơ sinh bị suy hô hấp đáp ứng định nghĩa Montreux của ARDS sơ sinh. Kích thước mẫu thuận tiện này có vẻ phù hợp vì một dân số tương tự đã được đăng ký để xác nhận định nghĩa Berlin ở trẻ sơ sinh. Đến nay, [15] trung tâm đã nhận được sự chấp thuận về đạo đức địa phương bao gồm các đơn vị chăm sóc đặc biệt không liên kết với các thành viên Ban Chỉ đạo. Nghiên cứu được điều phối bởi Bệnh viện Đại học Nam Paris (Paris, Pháp) và Đại học Tây Úc (Perth, Úc) và việc tuyển dụng bắt đầu vào tháng 12 năm 2015. Mặc dù chúng tôi không thể thấy trước bất kỳ sửa đổi cụ thể nào đối với định nghĩa Montreux phát sinh từ nghiên cứu tiền cứu, khi hoàn thành, Ban chỉ đạo sẽ sử dụng các phát hiện để đánh giá lại định nghĩa và, nếu phù hợp, xác định các phân nhóm lâm sàng, dịch tễ và sinh lý bệnh của ARDS sơ sinh.
Kết luận
Với việc phổ biến định nghĩa Montreux về ARDS sơ sinh, chúng tôi hy vọng sẽ tăng sự chú ý lâm sàng đối với thực thể của rối loạn. Định nghĩa Montreux có thể thúc đẩy nghiên cứu ARDS sơ sinh, điều này sẽ tạo điều kiện thuận lợi cho việc điều tra các phương pháp trị liệu mới, chẳng hạn như lớn hơn hoặc nhiều liều chất hoạt động bề mặt ngoại sinh và các chất bảo vệ chống viêm hoặc chất hoạt động bề mặt. [93], [94] Kiến thức sẽ có được trong này khu vực cũng có thể hữu ích trong nghiên cứu và chăm sóc lâm sàng trong ARDS ở trẻ em và người lớn. Hơn nữa, bằng chứng hỗ trợ về tỷ lệ lưu hành và tỷ lệ mắc ARDS sơ sinh sẽ thúc đẩy việc thực hiện các chính sách chăm sóc sức khỏe.
Tài liệu tham khảo















