Bài viết Bệnh cơ tim chu sinh được dịch từ bài gốc Peripartum Cardiomyopathy Bác sĩ Nguyễn Thành Luân – ICU bệnh viện Hoàn Mỹ Cửu Long.
Tóm tắt
Bệnh cơ tim Chu sinh là một bệnh liên quan đến thai kỳ có khả năng đe dọa đến tính mạng, thường phát sinh trong thời kỳ chu sinh và được đánh dấu bằng rối loạn chức năng thất trái và suy tim. Bệnh tương đối hiếm gặp, nhưng tỷ lệ mắc bệnh đang gia tăng. Phụ nữ thường phục hồi chức năng tim, nhưng tỷ lệ mắc bệnh và tử vong về lâu dài không phải ít xảy ra. Việc quản lý bệnh cơ tim chu sinh phần lớn chỉ giới hạn ở các thuốc đối kháng thần kinh-thể dịch tương tự được sử dụng trong các dạng bệnh cơ tim khác, và chưa có phương pháp điều trị đặc hiệu nào được chứng minh. Nghiên cứu trong thập kỷ qua đã gợi ý rằng bệnh cơ tim chu sinh là do rối loạn chức năng mạch máu, được kích hoạt bởi các hormone của thai kỳ muộn ở người mẹ. Gần đây nhất, thông tin cũng chỉ ra rằng nhiều trường hợp bệnh cơ tim chu sinh có nền tảng di truyền. Chúng tôi xem xét ở đây các vấn đề dịch tễ học, biểu hiện lâm sàng và quản lý bệnh cơ tim chu sinh, cũng như hiểu biết hiện tại về sinh lý bệnh của căn bệnh này. (Circulation. 2016; 133: 1397-1409. DOI: 10.1161/ CIRCULATIONAHA.115.020491.)
Key Words: cardiomyopathies ◼ heart failure ◼ pre-eclampsia ◼ pregnancy.
Suy tim liên quan đến mang thai và thời kỳ chu sinh đã được công nhận trong y văn vào đầu những năm 1800 bởi Virchow và những người khác.1,2 Loạt trường hợp lớn đầu tiên được công bố ở New Orleans vào năm 1937, [3,4] nhưng hội chứng vẫn chưa được định nghĩa rõ cho đến khi các ấn phẩm về sinh sản của Demakis và Rahimtoola5 và Demakis và cs6 vào năm 1971. Các tác giả này đã công bố dữ liệu trên 27 bệnh nhân, đặc biệt xác định hội chứng xảy ra trong giai đoạn chu sinh, và lần đầu tiên đưa ra thuật ngữ bệnh cơ tim chu sinh (PPCM). Sự ra đời sau đó của siêu âm tim cho phép mô tả đặc điểm không xâm lấn của hội chứng, và tiêu chí về phân suất tống máu (EF) <45% được giới thiệu vào năm 1999 bởi một hội thảo của NHLBI về PPCM. [7,8]
Mặc dù có những tiến bộ này, PPCM không phải là một thực thể được định nghĩa chính xác. Nhóm làm việc về PPCM của Hiệp hội Tim mạch châu Âu gần đây đã cung cấp một định nghĩa cập nhật về PPCM là bệnh cơ tim với giảm EF, thường <45%, xuất hiện vào cuối thai kỳ hoặc trong những tháng sau khi sinh ở một phụ nữ không có bệnh tim cấu trúc trước đó.[9] Việc không có bệnh tim từ trước thường được phỏng đoán hơn là được biết đến rõ ràng bởi vì hình ảnh tim trước khi có biểu hiện lâm sàng thì hầu như không bao giờ có ở những bệnh nhân trẻ tuổi này. Định nghĩa cũng bao gồm các thực thể như bệnh cơ tim Takotsubo, có khả năng là một quá trình bệnh khác nhau, đôi khi có thể phân biệt bằng các tiêu chí siêu âm tim. [10]
Thời điểm xảy ra PPCM cũng không rõ. Demakis và cs6 ban đầu lưu ý rằng hầu hết các trường hợp xảy ra trong những tuần đầu tiên sau sanh. Bảy mươi lăm trong số 123 bệnh nhân PPCM trong một loạt trường hợp [11] ở Nam California năm 2005 và 35 trong số 100 trường hợp trong một loạt trường hợp [12] năm 2014 ở miền Bắc Hoa Kỳ có biểu hiện trong tuần đầu sau sinh. Thời điểm này khác biệt đáng kể so với thời điểm khởi đầu các thay đổi huyết động lớn của thai kỳ, bao gồm giảm hậu tải, tăng thể tích máu, và tăng cung lượng tim lên tới 40%, tất cả đều xảy ra sớm trong tam cá nguyệt thứ hai.[13] Tuy nhiên, PPCM cũng có thể xuất hiện trước và sau sinh hàng tháng. Một nghiên cứu trên 23 bệnh nhân mắc bệnh cơ tim giãn vô căn (DCM) biểu hiện trước tháng cuối của thai kỳ cho thấy họ không thể phân biệt được về mặt lâm sàng với các bệnh nhân mắc PPCM theo định nghĩa cổ điển.[11] Như là hậu quả của sự không rõ ràng này, không phải tất cả nghiên cứu PPCM đều định nghĩa bệnh lý như nhau, vì thế nên thận trọng hơn khi so sánh kết quả giữa các nghiên cứu.
Bản chất không chính xác của định nghĩa phản ánh sự hiểu biết vẫn chưa hoàn chỉnh của chúng tôi về PPCM. Nguyên nhân gây bệnh vẫn chưa được biết. Nhiều nguyên nhân tiềm năng đã được đề xuất, bao gồm viêm cơ tim do virus, thiếu hụt dinh dưỡng, tự miễn, vi khảm và các căng thẳng huyết động.14 Gần đây, các nghiên cứu đã đề xuất mạnh mẽ vai trò của rối loạn chức năng mạch máu, những ảnh hưởng của nội tiết tố, và di truyền tiềm ẩn. Những dữ liệu mới và đang phát triển này sẽ được thảo luận chi tiết hơn dưới đây.
Dịch tể học
Tỷ lệ mắc PPCM ở Hoa Kỳ dao động từ ≈1 trong 1000 đến 4000 trường hợp sinh còn sống (Hình 115 -18). Phạm vi tỷ lệ mắc dường như phản ánh các nhân khẩu học dân số khác nhau, sự nghiêm ngặt của định nghĩa, và việc đánh giá thấp dẫn đến thiếu nhận thức hoặc chẩn đoán lầm. Một phân tích cơ sở dữ liệu của bệnh nhân nội trú toàn quốc gần đây bao gồm 64 triệu hồ sơ xuất viện từ 1000 bệnh viện ở 47 tiểu bang đã xác định 34 219 trường hợp mắc PPCM, với tỷ lệ mắc 1 trong 968 lần sinh.[18] Hơn một nửa số trường hợp PPCM xảy ra ở miền Nam Hoa Kỳ phản ánh sự khác biệt về chủng tộc (xem bên dưới). Tỷ lệ mắc đang gia tăng, ví dụ, trong nghiên cứu ở trên có từ 8.5 đến 11.8 trên 10.000 lần sinh còn sống từ năm 2004 đến 2011 và trong một nghiên cứu trước đây trên các hồ sơ xuất viện toàn quốc có từ 2.3 đến 4.5 trên 10 000 lần sinh còn sống từ 1990 đến 2002, [15] Sự gia tăng tỷ lệ mắc có thể phản ánh nhận thức và chẩn đoán tăng, tuổi mẹ tăng, thay đổi nhân khẩu học hoặc mang đa thai tăng. Khi tỷ lệ mắc của PPCM tăng lên rõ ràng và khi các phương pháp điều trị các biến chứng khác của thai kỳ được cải thiện, PPCM ngày càng góp phần vào tỷ lệ tử vong. Trong một nghiên cứu dân số về tử vong do tim mạch của mẹ ở California trong giai đoạn 2002-2006, PPCM là nguyên nhân hàng đầu (23%). [19]
Tỷ lệ mắc PPCM bên ngoài Hoa Kỳ ít được ghi nhận. Dữ liệu ở Châu Phi và Châu Á cho thấy tỷ lệ mắc 1 trong 1000 lần sinh sống.[20] Tuy nhiên, có những điểm nóng nổi bật của PPCM, nguyên nhân vẫn chưa rõ ràng. Ở Haiti, tỷ lệ mắc PPCM có thể lên tới 1 trên 300 lần sinh sống,[24] có thể liên quan đến nền tảng chủng tộc, thiếu hụt dinh dưỡng, hoặc tỷ lệ tiền sản giật cao. Ở miền bắc Nigeria, tỷ lệ mắc PPCM được báo cáo là 1 trên 100 lần sinh sống, [25] nguyên nhân ban đầu được cho là việc tắm nước nóng theo phong tục bản địa và lượng muối cao trong chế độ ăn ở giai đoạn chu sinh, mặc dù một nghiên cứu bệnh-chứng gần đây về 39 trường hợp PPCM không ủng hộ kết luận này. [26]
Các tình trạng liên quan
Tuổi
Tỷ lệ mắc PPCM liên quan chặt chẽ với tuổi tác. Mặc dù căn bệnh này có thể tấn công phụ nữ ở mọi lứa tuổi, nhưng >50% trường hợp xảy ra ở phụ nữ >30 tuổi,15,16,18,27 với tỷ số chênh là 10 khi so sánh phụ nữ >40 và <20 tuổi.[18]
Màu da
Tỷ lệ mắc PPCM ở Hoa Kỳ cao hơn đáng kể ở người da đen. Hơn 40% trường hợp trong các nghiên cứu toàn quốc được mô tả ở trên xảy ra ở phụ nữ da đen,[15,18] và một nửa xảy ra ở miền Nam Hoa Kỳ.[18] Một nghiên cứu dân số ở California ghi nhận tỷ lệ mắc PPCM ở người da đen là 1 trong 1421, gấp gần 3 lần ở người da trắng (1 trong 4075).[16] Một nghiên cứu bệnh-chứng đơn trung tâm ở Georgia và Tennessee cho thấy tỷ lệ mắc PPCM cao gấp 16 lần ở phụ nữ da đen so với phụ nữ da trắng.[28] Một nghiên cứu bệnh-chứng trên 52 người da đen và 104 người da trắng PPCM ở Nam California cho thấy bệnh nhân da đen thường trẻ hơn, có tỷ lệ tăng huyết áp cao hơn, xuất hiện muộn hơn, và có tỷ lệ phục hồi EF tâm thất trái (LV) thấp hơn.[29] Trong nghiên cứu dân số toàn bộ 2012 tiểu bang của Bắc Carolina năm 2003, tỷ lệ mắc PPCM ở phụ nữ da đen cao gấp 4 lần phụ nữ da trắng (1:1087 so với 1:4266) và tỷ lệ tử vong khi theo dõi 5 năm cũng cao gấp 4 lần (24% so với 6%).[30] Tóm lại, PPCM tấn công phụ nữ da đen thường xuyên hơn, và những phụ nữ này có kết cục tệ hơn (tiên lượng được mô tả chi tiết hơn dưới đây).
Tiền sản giật và tăng huyết áp
Tiền sản giật và tăng huyết áp có ảnh hưởng mạnh mẽ đến PPCM. Một phân tích gộp gần đây của 22 nghiên cứu trên 979 trường hợp PPCM cho thấy tỷ lệ tiền sản giật chung là 22%, gấp >4 lần tỷ lệ dân số là 3-5%.[31] Bất kỳ rối loạn tăng huyết áp nào (tiền sản giật, tăng huyết áp thai kỳ, hoặc tăng huyết áp mãn tính) hiện diện trong 37% (khoảng, 29-45%) trường hợp. Không có sự khác biệt về địa lý hoặc chủng tộc rõ ràng được phát hiện. Một nghiên cứu gần đây về hồ sơ xuất viện ở 6 tiểu bang đã xác định 535 bệnh nhân mắc PPCM, trong đó 29.3% bị tiền sản giật và 46.9% bị tăng huyết áp (tỷ số chênh, lần lượt là 13.6 và 13.4).[32] Tỷ lệ tiền sản giật trong nhiều nghiên cứu này có thể là bị đánh giá thấp vì tiền sản giật thường không được báo cáo và phân loại sai và vì sự hiện diện của tiền sản giật thường được sử dụng như một tiêu chí loại trừ khỏi chẩn đoán PPCM. PPCM cũng thường liên quan đến sản giật, với tỷ số chênh là 12.9 trong một nghiên cứu dân số ở California trên 1888 bệnh nhân bị sản giật [33] và 27.9 trong nghiên cứu hồ sơ xuất viện của nhiều tiểu bang về các trường hợp PPCM được ghi nhận ở trên.[18]
Điều quan trọng là phải nhận ra rằng tiền sản giật hoặc tăng huyết áp do mang thai cũng có thể kích hoạt phù phổi trong trường hợp không có PPCM. Một báo cáo gần đây đã so sánh trực tiếp 30 trường hợp PPCM với 53 trường hợp suy tim do tăng huyết áp trong thai kỳ tại một trung tâm giới thiệu bệnh ở Nam Phi và thấy rằng suy tim do tăng huyết áp thường xuất hiện trước khi sinh, có liên quan đến phì đại tim và EF bảo tồn, và có tiên lượng tốt hơn.[34] Ngay cả khi không có suy tim về mặt lâm sàng, thì một số nghiên cứu về siêu âm tim cho thấy tiền sản giật gây ra rối loạn chức năng tâm trương, được đo bằng các thông số khác nhau, bao gồm E/E ‘, chỉ số hoạt động của cơ tim, và sức căng cơ tim.[35-37] Rối loạn chức năng tâm trương một phần độc lập với tăng huyết áp và có thể tồn tại kéo dài đến 1 năm sau khi sinh và sau giải quyết tiền sản giật. Do đó, tiền sản giật gây ra độc tính đáng kể cho tim, có thể im lặng trên lâm sàng nhưng cũng có thể xuất hiện dưới dạng phù phổi với EF bảo tồn hoặc là một phần của PPCM. Tuy nhiên, điều quan trọng không kém là nhận ra rằng PPCM không chỉ đơn giản là biểu hiện của tiền sản giật nặng. Hơn 90% phụ nữ bị tiền sản giật, ngay cả khi nghiêm trọng, không phát triển PPCM, và ngược lại, ít nhất 50% phụ nữ mắc PPCM không bị tiền sản giật. Do đó, hai bệnh lý này là các thực thể khác nhau với sự liên kết chồng chéo và mạnh mẽ. Sự liên quan mạnh mẽ này cho thấy PPCM và tiền sản giật có thể chia sẻ các cơ chế sinh lý bệnh, như được thảo luận chi tiết hơn dưới đây. Nói tóm lại, không nên hạ thấp sự nghi ngờ đối với PPCM khi có tiền sản giật. Làm như vậy có thể trì hoãn điều trị thích hợp.
Đa thai
PPCM thường xuất hiện trong những trường hợp đa thai. Trong một phân tích gộp được ghi nhận ở trên, tỷ lệ sinh đôi trung bình trong những trường hợp PPCM qua 16 nghiên cứu là 9%,[31] cao hơn so với tỷ lệ ước tính trung bình là 3%.[38] Một số trường hợp PPCM có sinh ba cũng được báo cáo.[39-41]
Các tình trạng khác có liên quan được báo cáo không nhiều bao gồm làm dụng một số chất, thiếu máu, hen phế quản, dùng các thuốc ức chuyển dạ sớm kéo dài, đái tháo đường, béo phì, và suy dinh dưỡng.
Biểu hiện lâm sàng và Chẩn đoán
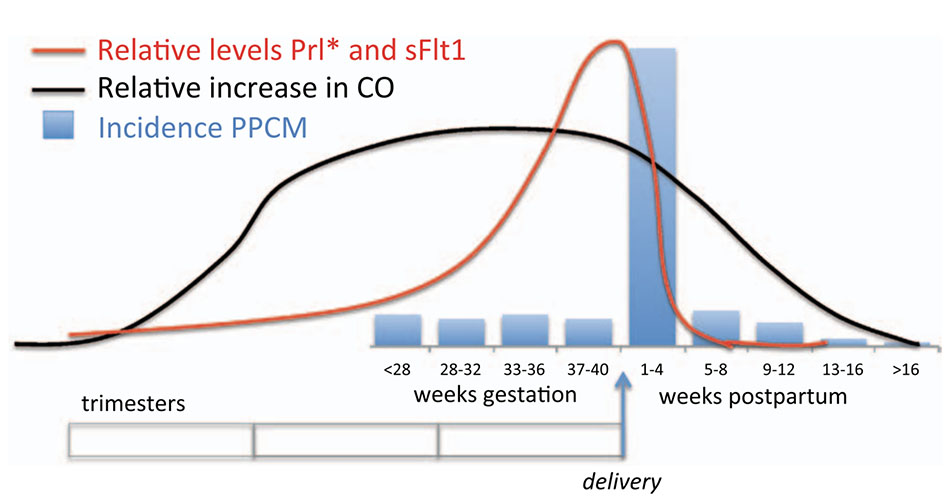
Phần lớn các trường hợp PPCM xuất hiện sau sinh, chủ yếu là trong tuần ngay sau sinh, trong khi một nhóm nhỏ xuất hiện trong tam cá nguyệt thứ hai và thứ ba (Hình 2).[6,11,13,42] Hầu hết phụ nữ có dấu hiệu và triệu chứng suy tim, bao gồm khó thở khi nằn và khó thở kịch phát về đêm. Những triệu chứng này có thể bị nhầm lẫn với những người mang thai bình thường, đặc biệt là thai kỳ muộn, thực tế thường dẫn đến chẩn đoán PPCM bị bỏ lỡ hoặc muộn và ước lượng thấp tỷ lệ mắc bệnh này. Khám thực thể thường phát hiện các dấu hiệu của suy tim, bao gồm nhịp tim nhanh, tăng áp lực tĩnh mạch cảnh, rales phổi và phù ngoại biên. Thỉnh thoảng có các dấu hiệu giãn LV, bao gồm tiếng tim thứ ba và mỏm tim thay đổi vị trí, nhưng thường không được ghi nhận vì PPCM có thể xảy ra ngay cả khi LV không lớn. ECG thường cho thấy nhịp nhanh xoang với những thay đổi không đặc hiệu, và X-quang ngực thường cho thấy bóng tim to và sung huyết tĩnh mạch phổi. Các biểu hiện nguy kịch có thể xảy ra, với suy hô hấp nặng và suy tim có cung lượng thấp cần có sự hỗ trợ về dược lý và cơ học.[43]
Chẩn đoán phân biệt bao gồm các nguyên nhân phổi (ví dụ, viêm phổi do sự dung nạp miễn dịch được kích thích trong quá trình mang thai hoặc thuyên tắc phổi do tăng đông trong giai đoạn chu sinh), phù phổi cấp do dùng thuốc ức chế chuyển dạ sớm kéo dài hoặc tiền sản giật, và nguyên nhân tim bao gồm nhồi máu cơ tim hoặc bệnh cơ tim Takotsubo. Siêu âm tim nói chung là đủ để phân biệt với các nguyên nhân này và thường thấy sự giãn nở LV với các mức độ khác nhau, rối loạn chức năng tâm thu LV, thất phải và hai tâm nhĩ to, hở van hai lá và ba lá, và tăng áp phổi. [8,41]
Dấu ấn sinh học
Hiện tại không có dấu ấn sinh học chuyên biệt nào giúp chẩn đoán PPCM. Nồng độ peptide bài niệu natri và troponin thường không tăng trong hoặc sau khi mang thai và thường tăng trong PPCM. Công trình gần đây (được mô tả chi tiết hơn bên dưới) đã gợi ý rằng microRNAs, cụ thể là miR-146a, có thể đóng vai trò là dấu ấn sinh học mới cho PPCM so với phụ nữ sau sinh không bị ảnh hưởng hoặc phụ nữ mắc DCM vô căn.[44] Tuy nhiên, cần thêm nghiên cứu để xác định liệu nồng độ miR-146a có phân biệt được PPCM với nhồi máu cơ tim chu sinh và các biến cố mạch máu cấp tính khác.
Điều trị và Biến chứng
Dữ liệu hạn chế về tiếp cận điều trị đối với PPCM, và chỉ có 2 thử nghiệm ngẫu nhiên, có đối chứng bao gồm tổng cộng 44 bệnh nhân đã được báo cáo (thảo luận thêm bên dưới).[45-47] Điều trị cho PPCM chủ yếu dựa vào kinh nghiệm lâm sàng và suy luân từ dữ liệu với các dạng suy tim tâm thu khác. Điều trị được chú trọng, như với các dạng suy tâm thu khác, kiểm soát tình trạng thể tích, điều chỉnh các phản ứng thần kinh-thể dịch ác tính, và ngăn ngừa các biến chứng huyết khối và rối loạn nhịp tim. Các thuốc lợi tiểu, bao gồm thuốc lợi tiểu quai và nitrate là những tác nhân được lựa chọn để kiểm soát thể tích, mặc dù cần thận trọng nếu sử dụng trước khi sinh để tránh tụt huyết áp và giảm tưới máu tử cung. Ức chế thần kinh-thể dịch với thuốc ức chế men chuyển angiotensin hoặc thuốc ức chế thụ thể angiotensin có thể được sử dụng sau sinh nhưng chống chỉ định trước khi sinh, trong thời gian đó có thể sử dụng kết hợp nitrate hữu cơ và hydralazine. Chẹn beta nên được xem xét và dường như an toàn trong thai kỳ. Metoprolol tartrate có thể được ưa thích nhờ kinh nghiệm lâm sàng sâu rộng hơn so với các thuốc chẹn beta khác. Ngoài ra, có thể ưu tiên các tác nhân chọn lọc beta 1 trong thời kỳ mang thai để tránh làm tăng hoạt tử cung. Digoxin có thể được sử dụng một cách an toàn trong thai kỳ, nhưng vai trò của nó trong điều trị suy tim tâm thu hiện đang còn bàn cãi.[48,49]
Các nghiên cứu về các điều trị thử nghiệm mới cho đến nay vẫn không rõ ràng hoặc không hiệu quả. Một nghiên cứu không ngẫu nhiên nhỏ năm 1999 trên 6 bệnh nhân được tiêm tĩnh mạch globulin miễn dịch cho thấy sự cải thiện so với 11 đối tượng được điều trị theo truyền thống,[50] nhưng không có nghiên cứu nào được tiến hành thêm. (Một thử nghiệm ngẫu nhiên, có có đối chứng giả dược sau đó đối với immunoglobulin tiêm mạch ở 62 bệnh nhân DCM khởi phát mới gần đây, mặc dù không có ai trong số họ mắc PPCM, không cho thấy sự cải thiện khi điều trị bằng immunoglobulin tiêm mạch.51) Một nghiên cứu khác ở Nam Phi năm 2002 báo cáo cải thiện kết cục ở 30 bệnh nhân được nhận pentoxifylline so với 29 đối tượng được điều trị theo truyền thống,[45] nhưng một lần nữa, không có nghiên cứu nào được thực hiện thêm nữa. Một thử nghiệm ngẫu nhiên, có đối chứng năm 2011 trên 24 phụ nữ PPCM so sánh levosimendan, một chất nhạy cảm với calci được sử dụng trong suy tim mất bù cấp, với giả dược cho thấy không có sự khác biệt về kết cục lâm sàng hoặc siêu âm tim.[52]
Bromocriptine và Ngừng cho con bú
Nghiên cứu về cơ chế gần đây (thảo luận bên dưới) đã đưa hormone prolactin vào nguồn gốc của PPCM và cho rằng ức chế bài tiết prolactin của tuyến yên khi ngừng cho con bú hoặc với bromocriptine, một chất chủ vận thụ thể ergot alkaloid và dopamine có thể có lợi ích.[53] Bromocriptine được FDA Hoa Kỳ chấp thuận để điều trị bệnh Parkinson, hội chứng đa tiết sữa và một số khối u tuyến yên. Nó đã được chứng minh là cải thiện kết cục tim mạch ở bệnh nhân đái tháo đường [54] và có tác dụng kích thích thần kinh-thể dịch và huyết động học có lợi ở bệnh nhân suy tim.[55] Một thử nghiệm ngẫu nhiên, nhãn mở, đơn trung tâm năm 2010 ở 20 phụ nữ châu Phi mới được chẩn đoán PPCM cho thấy sự cải thiện trong phục hồi LV sau 6 tháng (27% so với 58%; P = 0,012) và kết hợp với các kết cục của suy tim. Trong một nghiên cứu quan sát, tiến cứu ở Đức, việc sử dụng bromocriptine thường xuyên gấp đôi ở phụ nữ cho thấy cải thiện siêu âm tim (n = 82) so với những người không (n = 14; P = 0,013).[56] Tuy nhiên, giá trị của những kết quả ban đầu này không nhiều bởi cỡ mẫu nhỏ của các thử nghiệm ngẫu nhiên, có đối chứng, không mù, các kết cục bất lợi thường xuyên gây ngạc nhiên trong nhánh đối chứng của nghiên cứu và nguy cơ tiềm ẩn khi sử dụng bromocriptine trong giai đoạn chu sinh. Bromocriptine được coi là an toàn cho thai nhi vào năm 1982, [57] nhưng năm 1995 Hoa Kỳ đã rút lại chấp thuận cho mục đích ức chế tiết sữa do lo ngại về các biến cố bất lợi của mẹ.[58] Ngoài ra, có thể gây hại cho trẻ sơ sinh bởi việc ức chế tiết sữa phải được xem xét, đặc biệt là ở các nước đang phát triển, nơi thiếu dinh dưỡng và nguồn cung cấp nước không an toàn chiếm phần lớn tỷ lệ tử vong ở trẻ em, cho thấy sự phụ thuộc vào sữa mẹ rất quan trọng.[59] Một nghiên cứu hồi cứu qua Internet ở Hoa Kỳ cho thấy việc cho con bú có liên quan đến kết cục mẹ tốt hơn, thay vì tồi tệ hơn.[60] Tóm lại, việc sử dụng bromocriptine và tự nguyện ngừng cho con bú vẫn còn đang nghiên cứu và việc mang lại lợi ích là không chắc chắn tại thời điểm này. Chúng tôi hy vọng rằng kết quả của một thử nghiệm ngẫu nhiên, có đối chứng đang tiến hành về bromocriptine ở 60 bệnh nhân ở Đức [61] sẽ cung cấp thêm thông tin về tính hiệu quả và độ an toàn của bromocriptine.
Thuyên tắc huyết khối và Kháng đông
PPCM có liên quan đến tỷ lệ thuyên tắc huyết khối cao hơn các dạng bệnh cơ tim khác.[42] Thời kỳ chu sinh có tình trạng tăng đông,[62] là sự thích nghi tiến hóa để giảm thiểu chảy máu sau sinh (trong lịch sử là nguyên nhân phổ biến nhất gây tử vong mẹ). Sự giãn nở tim, tổn thương nội mô và bất động cũng góp phần vào xu hướng tạo cục máu trong PPCM. Trong cơ sở dữ liệu bệnh nhân nội trú toàn quốc được mô tả ở trên, huyết khối tắc mạch là biến chứng nghiêm trọng thường gặp nhất ở mức 6,6%.[18] Nhiều trường hợp cục máu đông ở tâm thất trái và phải đã được báo cáo, [63-67] và biến cố thuyên tắc huyết khối đôi khi có thể tạo thành các biểu hiện triệu chứng của PPCM.[67,68] Một nghiên cứu trên 33 trường hợp PPCM ở Senegal cho thấy huyết khối LV ở 30% bệnh nhân.[69] Trong trường hợp có nguy cơ thuyên tắc huyết khối cao này, nên dùng thuốc kháng đông trong PPCM ít nhất là trong khi mang thai và 2 tháng đầu sau sinh. Heparin và heparin không phân đoạn là an toàn trong thai kỳ, và heparin không phân đoạn được ưu tiên vì thời gian bán hủy ngắn hơn.
Rối loạn nhịp tim và Liệu pháp
Chống loạn nhịp Dữ liệu về tỷ lệ rối loạn nhịp thất trong PPCM còn ít. Đột tử thường được báo cáo là nguyên nhân của tử vong, cho thấy tỷ lệ cao của rối loạn nhịp tim. Ví dụ, trong một nghiên cứu hồi cứu 182 bệnh nhân ở California, 38% trường hợp tử vong được cho là đột tử.[67] Một báo cáo của 19 bệnh nhân ở Senegal đã theo dõi Holter 24 giờ cho thấy nhịp nhanh thất không dai dẳng ở 4 bệnh nhân.[70] Nhịp nhanh thất có thể dai dẳng, đòi hỏi phải cắt đốt.[71] Một phân tích bệnh-chứng hồi cứu ở 19 phụ nữ PPCM đã được đặt máy khử rung tim vĩnh viễn (ICD) để phòng ngừa tiên phát so với 60 phụ nữ nhóm chứng với DCM không do thiếu máu cục bộ cho thấy tỷ lệ 37% của liệu pháp ICU thích hợp trong thời gian theo dõi trung bình 3 năm ở phụ nữ PPCM và xu hướng tăng tỷ lệ mắc cao hơn so với phụ nữ DCM không do thiếu máu cục bộ.[72] Một nghiên cứu đơn trung tâm gần đây ở Đức trên 7 phụ nữ EF giảm nghiêm trọng (trung bình, 18%) đã mang máy chuyển nhịp/máy khử rung tim đã ghi nhận 4 biến cố rung thất với liệu pháp sốc thành công ở 3 phụ nữ trong thời gian theo dõi trung bình 81 ngày.[73] Tuy nhiên, ngược lại, một nghiên cứu hồi cứu lớn hơn về máy chuyển nhịp/máy khử rung tim ở 107 phụ nữ PPCM (EF trung bình là 22%) cho thấy không có cú sốc nào đối với nhịp nhanh thất hoặc rung thất trong 4 tháng.[74] Chỉ có 20% phụ nữ được đặt ICD vĩnh viễn, phần lớn là do rối loạn chức năng tâm thất kéo dài. Do đó, vì tỷ lệ phục hồi cao trong PPCM, nên tránh cấy ghép sớm máy ICD vĩnh viễn, và không có cơ sở dựa trên dữ liệu rõ ràng nào để khuyến cáo đeo máy chuyển nhịp/máy khử rung tim. Tuy nhiên, có thể hợp lý khi xem xét đeo máy chuyển nhịp/máy khử rung tim ở những bệnh nhân có EF <30%, có nguy cơ biến chứng cao, bao gồm tử vong (xem bên dưới), là cầu nối để phục hồi hoặc đặt máy ICD ở những bệnh nhân không phục hồi trên liệu pháp nội khoa tối ưu.
Thiết bị hỗ trợ tim
Bệnh nhân PPCM có thể bị suy giảm nặng chức năng LV và biểu hiện suy sụp nhanh chóng. Thuốc tăng co bóp, bóng nội động mạch chủ, các thiết bị hỗ trợ LV và hai thất, và oxy hóa màng ngoài cơ thể nên được xem xét trong những trường hợp này và đã được sử dụng thành công.[75-79] Điều trị tích cực thường thường xuyên đánh giá dấu hiệu phục hồi của bệnh nhân PPCM. Khi phục hồi không xảy ra, các thiết bị hỗ trợ tim có thể đóng vai trò là cầu nối để ghép tim.
Quản lý Sản khoa
Các trường hợp PPCM xảy ra trong thời kỳ mang thai muộn, mặc dù ít gặp hơn sau sinh, đòi hỏi phải xem xét đặc biệt. Như đã lưu ý ở trên, một số loại thuốc như thuốc ức chế men chuyển angiotensin và thiếu thể tích quá mức cần phải tránh. Không có dữ liệu được công bố để hướng dẫn các quyết định về thời điểm và phương thức cho sinh; đặc biệt, không có dữ liệu nào cho thấy việc sinh sớm hoặc sinh mổ chương trình có thể tốt cho PPCM hoặc cải thiện kết cục của thai nhi. Cân nặng khi sinh trung bình, kích thước và điểm Apgar thấp hơn ở trẻ sơ sinh được sinh ra với phụ nữ PPCM, có vẻ là do tuổi thai sớm hơn khi sinh.17 Thai chết ngay sau sinh là thường gặp hơn (OR, 3.8; P <0,0001 trong nghiên cứu dân số 535 bệnh nhân [32]). Do đó, quyết định quản lý và thời điểm và phương thức sinh nở phải được đưa ra bởi một nhóm các bác sĩ tim mạch và bác sĩ sản khoa. Sinh sớm cần phải được cân nhắc với các rủi ro cho trẻ sơ sinh và thường nên được dành riêng cho các trường hợp sắp xảy ra nguy hiểm cho mẹ hoặc thai nhi.
Tiên lượng
Tiên lượng của PPCM ở Hoa Kỳ đã được cải thiện kể từ khi nó được mô tả vào năm 1971. Nghiên cứu IPAC gần đây đã tuyển chọn 100 phụ nữ từ nhiều trung tâm trên khắp Hoa Kỳ và theo dõi diễn biến lâm sàng trong 12 tháng có đánh giá chăm sóc lâm sàng, bao gồm siêu âm tim lặp lại. Nghiên cứu này cho thấy 71% phụ nữ đã phục hồi LVEF tới >50%, trong khi đó chỉ có 13% có các biến cố lớn hoặc bệnh cơ tim dai dẳng với EF <35%.[80] Phục hồi xảy ra gần như đều đặn trong 6 tháng, sau EF thay đổi ít lại, như được ghi nhận bởi các nghiên cứu trước đó.[11,81] Việc phục hồi LVEF sau 6 tháng đôi khi có thể xảy ra, tuy nhiên, và không nên loại trừ sự phục hồi muộn.
Ghép tim
Mặc dù bệnh nhân PPCM thường có kết cục tốt, nhưng có một tỷ lệ đáng kể cuối cùng cần ghép tim, thường được bắc cầu bằng hỗ trợ tuần hoàn cơ học. Một nghiên cứu trên 99 bệnh nhân PPCM được hỗ trợ tuần hoàn cơ học lâu dài từ năm 2006 đến 2012 đã báo cáo rằng kết cục nhìn chung tốt hơn so với 1159 phụ nữ mắc bệnh cơ tim không phải PPCM nhưng 48% tiếp tục được ghép tim.[82] Chỉ có 4 bệnh nhân được lấy bỏ thiết bị ghép vì phục hồi. Năm phần trăm trường hợp ghép tim ở phụ nữ Hoa Kỳ được thực hiện cho chỉ định PPCM.[83] So với phụ nữ được ghép tim cho các chỉ định khác, tỷ lệ sống ghép kém hơn và tỷ lệ sống điều chỉnh theo tuổi thấp hơn, có lẽ do tuổi trẻ hơn và bị ảnh hưởng miễn dịch cao hơn.[83]
Tỷ lệ tử vong
Bốn phụ nữ (4%) trong nghiên cứu IPAC đã chết. Cơ sở dữ liệu bệnh nhân nội trú quốc gia gần đây cho thấy tỷ lệ tử vong nội viện là 1,3%, [18,32] nhưng nó không bao gồm thông tin sau khi xuất viện. Theo dõi dài hạn ở 100 bệnh nhân ở 2 trung tâm Midwestern academic cho thấy tỷ lệ tử vong là 11% trong thời gian trung bình là 8 năm. Trong một nghiên cứu ở toàn bang Bắc Carolina, tỷ lệ tử vong là 16% sau 7 năm.[30]
Sự khác biệt về chủng tộc và địa lý
Tiên lượng ở Hoa Kỳ xấu hơn đáng kể ở người da đen. Trong một phân tích hồi cứu năm 2013 với 52 bệnh nhân da đen và 104 bệnh nhân da trắng ở 2 trung tâm ở California và Louisiana, bệnh nhân da đen có tỷ lệ phục hồi LV thấp hơn 34% (40% so với 61%; P = 0.02) và tỷ lệ tử vong hoặc ghép tim cao hơn (P = 0.03) mặc dù có EF tương tự (28%) khi vào viện.[29] Trong nghiên cứu IPAC, các bệnh nhân da đen có biểu hiện EF thấp hơn (31% so với 36%; P = 0,008), có EF trung bình thấp hơn ở 1 năm theo dõi (47% so với 56%; P = 0003) và có tỷ lệ phục hồi thấp hơn (được định nghĩa là EF >50%: 59% so với 77%; P = 0.03). Trong một thử nghiệm toàn tiểu bang Bắc Carolina, tỷ lệ tử vong 7 năm ở bệnh nhân da đen là 24% so với 6% ở bệnh nhân da trắng.[30] Nguyên nhân dẫn đến sự khác biệt về kết cục là không chắc chắn và có thể bao gồm sự khác biệt về di truyền (có lẽ liên quan đến tỷ lệ mắc PPCM cao hơn trong dân số này [xem ở trên]) và sự khác biệt về tài nguyên kinh tế xã hội, tiếp cận chăm sóc sức khỏe, chẩn đoán muộn và các biến số môi trường khác. Kết cục ở phụ nữ Hispanic không thấy xấu hơn đáng kể so với người da trắng không gốc Hispanic.[32]
Có Ít dữ liệu về tiên lượng bên ngoài Hoa Kỳ. Một nghiên cứu quốc gia PPCM tiến cứu ở Đức bắt đầu vào năm 2004 cho đến nay đã báo cáo 115 bệnh nhân. Ở thời điểm 6 tháng, 47% bệnh nhân đã hồi phục hoàn toàn, 2% tử vong, và 15% có các biến cố lớn hoặc bệnh cơ tim dai dẳng với EF <35%.[56] Trong một nghiên cứu đơn trung tâm trên 45 bệnh nhân PPCM ở Pakistan, 71% đã hồi phục chức năng LV trong vòng 6 tháng và không có trường hợp tử vong nào được báo cáo, mặc dù 9% phụ nữ trải qua đột quỵ do thuyên tắc huyết khối.[84] Trong một nghiên cứu toàn quốc với 104 bệnh nhân PPCM ở Nhật Bản, 4 người chết (4%), và 63% số người sống sót đã phục hồi LVEF (>50%) sau 6 tháng.[85] Những kết quả này tương tự như kết quả đương đại ở Hoa Kỳ (xem ở trên).
Mặt khác, một nghiên cứu đơn trung tâm gần đây trên 30 bệnh nhân ở Cape Town, Nam Phi, đã báo cáo 5 trường hợp tử vong (17%) trong thời gian theo dõi trung bình là 3.5 năm [34] (chiếm phần lớn các trường hợp tử vong trong một đoàn hệ lớn hơn gồm 152 bệnh nhân có bệnh tim mạch khi mang thai [86]). Trong một nghiên cứu lớn hơn với 176 bệnh nhân ở Soweto, Nam Phi, 13% tử vong và 25% có LVEF <35% dai dẳng sau 6 tháng. [87] Chỉ 21% số người sống sót hồi phục hoàn toàn LVEF (>55%). Phần lớn phụ nữ trong các nghiên cứu này có nguồn gốc châu Phi, có lẽ giải thích một số khác biệt về kết cục. Kết cục kém tương tự đã được báo cáo trong một nghiên cứu 2 trung tâm ở Istanbul, Thổ Nhĩ Kỳ, với 10 trong số 42 bệnh nhân (24%) PPCM tử vong và chỉ có 30% bệnh nhân phục hồi chức năng LV sau 6 tháng.[88] Tóm lại, kết cục vẫn nghèo nàn đối với phụ nữ của một số tổ tiên nhất định và trong các khu vực địa lý nhất định, đặc biệt là châu Phi.
Các yếu tố tiên đoán phục hồi
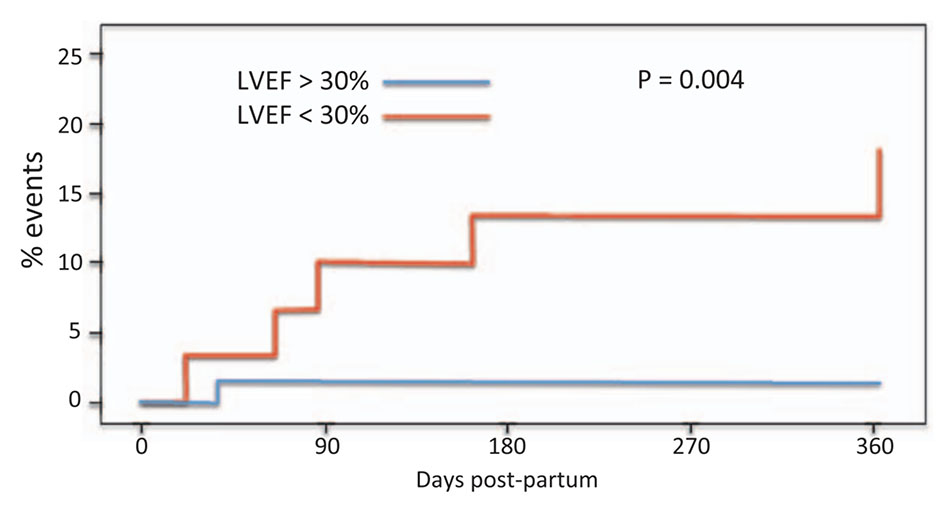
Ngoài nền tảng chủng tộc và độc lập với nó một phần, EF ở thời điểm nhập viện là dự đoán tốt nhất về tỷ lệ phục hồi. Trong nghiên cứu IPAC, chỉ một phần ba trong số 27 phụ nữ có LVEF <30% tại thời điểm nhập viện phục hồi EF đến >50% sau 1 năm. Không ai trong số họ cũng có bằng chứng giãn nở (đường kính cuối tâm trương LV >6.0 cm) phục hồi so với hồi phục ở gần 90% trong số 65 phụ nữ có LVEF >30% (P = 0.003).[80] Các biến cố ( tử vong, thiết bị hỗ trợ LV, hoặc ghép tim) hầu như chỉ xảy ra ở những phụ nữ có LVEF <30% khi nhập viện so với những người có LVEF ≥30% (82% so với 99% sống sót không có biến cố nào; P = 0.004; Hình 3). Trong một nghiên cứu gần đây trên 187 bệnh nhân (hầu hết từ California), EF trung bình là 31% ở những người phục hồi EF đến >50% sau 6 tháng so với 23% ở những người không phục hồi như vậy (P <0,0001).[89] Tương tự, trong một đoàn hệ ở Đức, EF trung bình nhập viện là 28% ở những phụ nữ cải thiện so với 17% ở những người không cải thiện (P <0.0001).[56] Tuy nhiên, điều quan trọng cần lưu ý là giảm EF không phải là một yếu tố tiên đoán đặc hiệu cho việc không phục hồi và do đó không nên là một chỉ định cho cấy thiết bị sớm hoặc ghép tim sớm.[89] Điều thú vị là LVEF khi nhập viện trong nghiên cứu Soweto đã không tiên đoán được kết cục trong đoàn hệ lớn này,[87] khác với các nghiên cứu của Hoa Kỳ. Nồng độ troponin và BNP huyết tương thấp hơn cũng có liên quan đến cải thiện kết cục.[90] Tuy nhiên, giống như LVEF, độ chính xác dự đoán của chúng không đủ để ảnh hưởng đến các quyết định lâm sàng.
Hiện đang có cuộc tranh luận về câu hỏi liệu sự hiện diện của tăng huyết áp hoặc tiền sản giật dự đoán kết cục tốt hơn. Ở những bệnh nhân mà những tình trạng này góp phần vào sự phát triển PPCM, thì việc giải quyết tiền sản giật hoặc tăng huyết áp thai kỳ có thể, ví dụ, tăng tốc độ giải quyết. Phù hợp với quan niệm này, trong đoàn hệ của Đức, 49% phụ nữ cải thiện có tăng huyết áp so với chỉ 7% những người không cải thiện (P = 0.009).[56] Trong nghiên cứu của Soweto, huyết áp có OR 0.97 trên 1 mmHg cho phục hồi kém (P = 0.02).[87] Trong nghiên cứu toàn quốc của Nhật Bản với 102 phụ nữ, trong đó 41% bị tăng huyết áp khi mang thai, sự hiện diện của tăng huyết áp có liên quan độc lập với thời gian nằm viện ngắn hơn và cải thiện EF một cách vừa phải ở 7 tháng theo dõi (59% so với 51%; P <0.05).[85] Mặt khác tiền sản giật hoặc tăng huyết áp không liên quan cải thiện kết cục trong nghiên cứu IPAC.[80] Liệu sự hiện diện của tiền sản giật với PPCM có cải thiện kết cục hay không vẫn không chắc chắn .
Tái phát với Thai kỳ lần sau
Câu hỏi về nguy cơ đối với việc mang thai lần thứ hai thường rất mù mờ ở phụ nữ đã bị PPCM. Một đánh giá toàn diện gần đây các tài liệu về chủ đề này,[91] bao gồm 191 lần mang thai lại, cho thấy nguy cơ tái phát ở bệnh nhân rối loạn chức năng LV kéo dài trước khi mang thai lại cao hơn nhiều so với những người có chức năng LV bình thường: 48% trong nhóm trước (n = 93) có sự suy giảm đáng kể chức năng LV và 16% tử vong, trong khi 27% của nhóm sau cho thấy sự suy giảm và không có trường hợp tử vong nào được báo cáo. Do đó, nguy cơ PPCM xấu đi khi mang thai lại là rất đáng kể. Yếu tố tiên đoán tốt nhất cho sự tái phát và suy giảm chức năng tim là LVEF trước mang thai, nhưng chức năng LV bình thường không đảm bảo lần mang thai tiếp theo không biến chứng. Chứng minh dự trữ tim đầy đủ trên siêu âm tim gắng sức ở bệnh nhân có chức năng LV hồi phục đã được đề xuất để mang lại giá trị tiên lượng bổ sung, nhưng điều này vẫn không chắc chắn.[92] Tuy nhiên, nhiều phụ nữ rất muốn mang thai lần sau. Do đó, quyết định thực hiện là rất khó khăn và có tính cá nhân cao. Không có khuyến cáo vững chắc về chủ đề này có thể được tạo ra trên cơ sở dữ liệu có sẵn. Tuy nhiên, nên chờ đợi bình thường hóa chức năng LV khi không cần thuốc và phụ nữ nên được khuyên rằng họ có nguy cơ tái phát cao ngay cả khi chức năng LV của họ đã hồi phục, việc mang thai lại có thể dẫn đến suy giảm LV nghiêm trọng hoặc biến chứng đe dọa tính mạng, và các kết cục lâu dài hiện chưa được biết.[91] Cách tiếp cận dựa trên một nhóm để ra quyết định, bao gồm các bác sĩ lâm sàng và bệnh nhân được thông tin tốt, rất được ủng hộ. Nếu quyết định tiến hành mang thai được đưa ra, việc theo dõi chặt chẽ các triệu chứng, chức năng LV và BNP được khuyến cáo mạnh mẽ trong và sau khi mang thai.[91]
Điều trị sau Phục hồi
Do thiếu dữ liệu theo dõi lâu dài ở phụ nữ bị PPCM, nên không rõ liệu và khi nào phụ nữ mắc bệnh có thể được xem là đã bình phục hoàn toàn. Đây là một vấn đề quan trọng, ảnh hưởng đến quyết định có nên ngừng sử dụng thuốc dài hạn ở phụ nữ trẻ và khỏe mạnh hay không. Một nghiên cứu trên 15 bệnh nhân đã phục hồi LVEF hoàn toàn đã ngừng sử dụng thuốc ức chế men chuyển angiotensin hoặc thuốc chẹn beta cho thấy không có sự suy giảm chức năng LV trong thời gian theo dõi 2 năm.[81] Dữ liệu MRI tim còn ít, không phát hiện tổn thương cơ tim kéo dài ở phụ nữ PPCM.[93] Tuy nhiên, những người khác đã báo cáo sự suy giảm chức năng LV đã phục hồi ở một số bệnh nhân ít ỏi.[67] Ngoài ra, một nghiên cứu siêu âm tim ban đầu, ở những phụ nữ có chức năng LV hồi phục cho thấy giảm dự trữ co bóp khi đáp ứng với dobutamine,[94] chỉ ra sự hiện diện của rối loạn chức năng dưới lâm sàng kéo dài. Ngoài ra, như đã thảo luận ở trên, những phụ nữ có LVEF hồi phục vẫn có nguy cơ tái phát cao với những lần mang thai tiếp theo. Cùng với nhau, những dữ liệu này cho thấy phục hồi tế bào và cấp độ phân tử có thể thấp hơn đáng kể so với phục hồi trên siêu âm tim. Một cách tiếp cận hợp lý để ngừng sử dụng thuốc ở phụ nữ đã phục hồi hoàn toàn chức năng LV sẽ bao gồm chờ đợi một vài tháng sau khi chức năng LV hồi phục, ngưng một loại thuốc ở một thời điểm, và theo dõi lâm sàng và siêu âm tim chặt chẽ trong quá trình ngừng thuốc bằng cách đánh giá chức năng LV hàng năm.
Sinh bệnh học PPCM
Huyết học và các nguyên nhân được đề xuất khác
PPCM thường được coi là một thử nghiệm căng thẳng huyết động thất bại trong thai kỳ. Thật vậy, mang thai kích hoạt các thay đổi huyết động lớn làm gia tăng đáng kể khối lượng công việc của tim (Hình 2).[13] Thể tích máu và khối lượng hồng cầu tăng, dẫn đến tăng tiền tải. Cung lượng tim tăng từ 20% đến 50%, hậu quả của việc nhịp tim tăng ≈15% đến 30% và tăng thể tích nhát bóp từ 15% đến 25%. Tổng sức cản mạch máu giảm 30%, mặc dù hậu tải tăng trở lại vào cuối thai kỳ. Tất cả những thay đổi này xảy ra giữa tam cá nguyệt thứ nhất và thứ hai, và những bệnh nhân mắc bệnh tim cấu trúc đã biết từ trước thường biểu hiện suy tim lâm sàng tại thời điểm này của thai kỳ.[95] Ngược lại, PPCM xuất hiện chủ yếu trong giai đoạn chu sinh (Hình 2). Việc sinh nở gây ra căng thẳng huyết động học hơn nữa, nhưng các yếu tố điều chỉnh sự căng thẳng đó, bao gồm sinh mổ, dường như không làm thay đổi nguy cơ phát triển PPCM. Do đó, căng thẳng huyết động dường như không phải là nguyên nhân quan trọng góp phần vào PPCM.
Viêm cơ tim thường được đưa ra như một nguyên nhân của PPCM, chủ yếu là do thường gặp nhưng sự quan sát khác nhau về thâm nhiễm viêm trên sinh thiết nội tâm mạc tim phải.[14] Tuy nhiên, thâm nhiễm tương tự thường được tìm thấy trong sinh thiết nội tâm mạc từ các nhóm đối chứng. Ví dụ, trong 1 nghiên cứu, 71% phụ nữ PPCM và 73% đối tượng đối chứng phù hợp có bằng chứng nhiễm trùng coxsackie hoặc echovirus.[96] Tương tự, nghiên cứu PCR trên mẫu sinh thiết nội tâm mạc từ 26 bệnh nhân PPCM phát hiện 30.7% đối tượng tìm thấy bộ gen virus thường liên quan đến viêm cơ tim, bao gồm parvovirus B19, nhưng tỷ lệ bệnh thì giống hệt nhau (30.3%) trong nhóm đối chứng. [97,98] Do đó, độ đặc hiệu của những phát hiện này rất kém và vai trò của viêm cơ tim trong PPCM vẫn chưa chắc chắn. Sinh thiết tim phải không còn được chỉ định trong quá trình chẩn đoán PPCM và hiếm khi được thực hiện. Tương tự, các báo cáo về MRI tim trong giai đoạn cấp của PPCM ở một số ít bệnh nhân đã gợi ý sự hiện diện của viêm ở một số bệnh nhân,[99,100] mặc dù một đánh giá gần đây của 40 bệnh nhân trong nghiên cứu IPAC chỉ cho thấy mô hình gợi ý viêm cơ tim chỉ ở 1 bệnh nhân (dữ liệu chưa được công bố, Erik B. Schelbert, MD, 2016). Do đó, sử dụng MRI trong chẩn đoán PPCM là không chắc chắn tại thời điểm này.
Một số nguyên nhân tiềm năng khác cho PPCM cũng đã được đề xuất, với dữ liệu hỗ trợ hạn chế cho đến nay. Vi khảm, với các tế bào có nguồn gốc từ bào thai có thể tồn tại trong trạng thái mang thai bị ức chế miễn dịch và có thể xuất hiện trong tim mẹ, đã được đề xuất như một tác nhân kích hoạt tự miễn sau sinh.[7] Tuy nhiên, các tế bào vi khảm của thai khu trú ở tim mẹ được cho là để giúp đỡ cơ tim bị tổn thương và là có lợi.[101] Các dạng suy dinh dưỡng khác nhau cũng đã được đề xuất, bao gồm thiếu hụt sắt và selenium, và có thể đại diện cho các tình huống bệnh nặng đặc biệt chỉ có ở các khu vực địa lý. Ví dụ, một nghiên cứu bệnh-chứng gần đây trên 39 bệnh nhân ở Nigeria, trong đó tỷ lệ mắc PPCM cao một cách kỳ là, cho thấy nồng độ selenium huyết thanh trung bình chỉ bằng một nửa so với nhóm chứng (P <0.001),[26] mặc dù quan sát này không thấy ở đâu khác ngoài châu Phi cận Sahara.[102]
Nói tóm lại, cho đến nay, nguyên nhân của PPCM vẫn chưa được làm rõ. Tuy nhiên, nghiên cứu gần đây đã nâng cao đáng kể sự hiểu biết của chúng ta về căn bệnh này. Các kết quả đang bắt đầu làm sáng tỏ 2 khía cạnh mới của PPCM: một là vai trò độc hại quan trọng của các hormone trong thai kỳ muộn đối với hệ thống mạch máu mẹ và sự hiểu biết ngày càng nhiều về nền tảng di truyền của PPCM. Những phát triển gần đây được thảo luận bên dưới.
Giả thuyết nội tiết tố-mạch máu
Prolactin
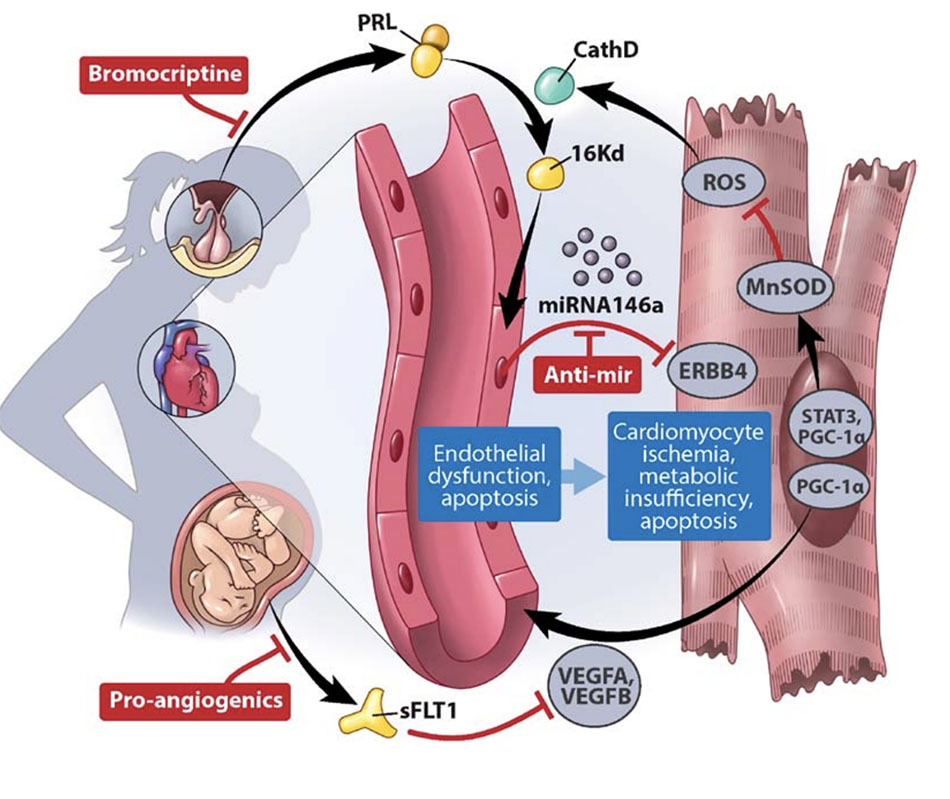
Một bài báo mang tính bước ngoặt năm 2007 lần đầu tiên đưa ra quan niệm rằng PPCM là một bệnh mạch máu được kích hoạt bởi sự thay đổi nội tiết tố của thai kỳ muộn. Mặc dù ý tưởng đã được đề xuất trong quá khứ,[103] nhưng thử nghiệm hỗ trợ cho nó còn thiếu. Các tác giả đã phát triển một mô hình chuột PPCM trong đó yếu tố phiên mã STAT3 đã bị xóa di truyền đặc hiệu trong tế bào cơ tim. Để hỗ trợ cho việc tạo ra mô hình này, biểu hiện của STAT3 đã giảm ở LV từ những bệnh nhân bị suy tim giai đoạn cuối do PPCM gây ra so với các đối tượng đối chứng không suy tim. Mất STAT3 ở tim chuột dẫn đến giảm biểu hiện gen bảo vệ tim chống lại các loại oxy phản ứng, đáng chú ý nhất là manganese superoxide dismutase (MnSOD), trung hòa các superoxide được tạo ra bởi hoạt động ty thể mạnh mẽ trong việc làm tổn thương các tế bào cơ tim. Hậu quả là sự gia tăng các loại oxy phản ứng dẫn đến sự bài tiết, thông qua cơ chế vẫn chưa rõ ràng, của cathepsin D. Peptidase ngoại bào này sau đó cắt prolactin, một loại hormone chuyên biệt cho thai kỳ muộn, thành một đoạn 16-kDa thúc đẩy quá trình chết tế bào theo chu trình trong tế bào nội mô. Kết quả là, chuột STAT3 cho thấy tình trạng suy mạch máu đáng kể trong giai đoạn cuối thai kỳ và hậu quả là DCM do mang thai, đó là PPCM (Hình 4). Khía cạnh hấp dẫn nhất của nghiên cứu này, là bằng chứng về vai trò chính của prolactin, đến từ việc ngăn chặn bài tiết prolactin từ tuyến yên với bromocriptine. Điều trị chuột STAT3 bằng bromocriptine đã đảo ngược hoàn toàn PPCM quan sát được.
Gần đây, cùng một nhóm đã nghiên cứu sâu hơn về cách thức mảnh prolactin 16-kDa kích hoạt tổn thương tế bào nội mô và tế bào cơ tim.[44,104] Họ chỉ ra rằng prolactin 16-kDa tạo ra các tế bào nội mô để đóng gói miR-146a vào exosome, các hạt nhỏ được bọc lipid, sau đó được tiết ra và được hấp thu bởi các tế bào cơ tim. MiR-146a được nội hóa vào tế bào cơ tim sau đó ức chế con đường neuregulin/ErbB, do đó thúc đẩy quá trình chết tế bào theo chu trình của tế bào cơ tim. Đáng chú ý, mức độ lưu hành của miR-146a được tăng lên đáng kể ở phụ nữ PPCM. Hơn nữa, mức độ này giảm đáng kể khi điều trị bằng bromocriptine, chứng minh rằng prolactin điều khiển bài tiết miR-146a. Như đã nêu ở trên, miR-146a có thể hữu ích như một dấu ấn sinh học của PPCM. Ngoài ra, miR-146a có thể trở thành mục tiêu điều trị khả thi vì microRNA có thể bị ức chế lâm sàng một cách hiệu quả và chuyên biệt. Thật vậy, việc điều trị mô hình STAT3 của PPCM bằng LNA (locked nucleic acid) đã được điều chỉnh antisense oligonucleotide để làm im lặng miR-146a đã giải cứu một phần mật độ mao mạch tim và chức năng co bóp. Hơn nữa, LNA- miR-146a không ức chế tiết sữa vì linolenic acid hoạt động ở cuối chu trình hoạt động của prolactin 16-kDa. Do đó, không giống như bromocriptine, liệu pháp với LNA-miR-146a sẽ cho phép tiếp tục nuôi dưỡng trẻ sơ sinh.
Do đó, những dữ liệu này cho thấy một cách thuyết phục rằng, ít nhất là trong mô hình chuột này, một hormone chu sinh (prolactin) cộng với cơ địa chống lại tim (trong trường hợp này, không có STAT3 trong tim) để kích hoạt bệnh mạch máu và hậu quả là PPCM.
Soluble Fms-Like Tyrosine Kinase 1
Một mô hình hormone-mạch máu tương tự gần đây đã được tóm tắt lại trong một mô hình chuột khác của PPCM, trong đó có sự loại bỏ đặc hiệu tim của PGC-1α (proliferator- activated receptor-gamma coactivator-1α), một yếu tố điều hòa phiên mã mạnh mẽ.[105] Giống STAT3, PGC-1α điều khiển biểu hiện của MnSOD, do đó triệt tiêu các gốc oxy phản ứng. Ngoài ra, PCG-1α còn điều khiển biểu hiện của yếu tố tăng trưởng nội mô mạch máu (VEGF), yếu tố tạo mạch được nghiên cứu rộng rãi nhất.106 Việc xóa PGC-1α tim làm thúc đẩy độc tính mạch máu bằng 2 cách: kích hoạt con đường qua trung gian prolactin 16-kDa kháng mạch máu (như trong mô hình STAT3) và mất con đường qua trung gian VEGF (Hình 4). Theo đó, chỉ có sự kết hợp giữa liệu pháp bromocriptine và VEGF mới cứu được PPCM ở những động vật này.
Các quan sát trên đã đặt ra câu hỏi về loại hormone nào trong thai kỳ đang ức chế con đường VEGF và kích hoạt PPCM trong mô hình PGC-1. Trong thời kỳ mang thai muộn ở động vật có vú, nhau thai tiết ra nhiều hormone vào tuần hoàn của mẹ, bao gồm một biến thể hòa tan của thụ thể VEGF 1, soluble Fms-like tyrosine kinase 1 (sFlt1). Hầu hết VEGF tự do trong tuần hoàn mẹ được trung hòa bởi sFlt1 trong giai đoạn thai kỳ muộn.107 Tim và các cơ quan khác tự bảo vệ mình khỏi sự tấn công này một phần do bài tiết VEGF cục bộ, nhưng điều này bị giảm đi và không đủ trong mô hình PGC-1α của PPCM. Sử dụng sFlt1 cho động vật PGC-1α chưa sinh đẻ là đủ để gây ra bệnh cơ tim, ngay cả khi không mang thai, chứng minh rằng sFlt1 là thành phần chính của trạng thái mang thai kích hoạt PPCM ở những động vật này. Do đó, sFlt1 và prolactin là 2 loại hormone có khả năng gây độc mạch máu của thai kỳ muộn có thể kích hoạt PPCM ở vật chủ nhạy cảm.
Sự bài tiết sFlt1 của nhau thai tăng cao rõ rệt trong tiền sản giật [107] và thai đôi.[108] Tim mẹ tiếp xúc với mức sFlt1 cao hơn đáng kể trong những tình trạng này, có thể giải thích mối liên hệ dịch tễ mạnh giữa tiền sản giật, thai đôi và PPCM (đã thảo luận ở trên). Trên thực tế, phụ nữ tiền sản giật nhưng không PPCM vẫn bị rối loạn chức năng tim dưới lâm sàng trên siêu âm tim,[35-37,105] và trong một nghiên cứu nhỏ (n = 20), mức độ rối loạn chức năng tương quan tốt với mức độ lưu hành của sFlt1.[105] Nồng độ sFlt1 gia tăng trong một nhóm phụ nữ PPCM,[105] và trong nghiên cứu IPAC, nồng độ sFlt1 tương quan với suy tim lâm sàng và kết cục bất lợi.108a Một nghiên cứu thí điểm mở nhỏ, không ngẫu nhiên (n = 11) về loại bỏ sFlt1 ngoài cơ thể ở tiền sản giật sinh non sớm cho thấy kết quả đầy hứa hẹn,[109] và một nghiên cứu trường hợp duy nhất về thay huyết tương ở một phụ nữ PPCM nặng cho thấy sự phục hồi nhanh chóng của chức năng tim.[110]
Cùng với nhau, những quan sát này chỉ ra rằng sFlt1, được tiết ra từ nhau thai trong thai kỳ muộn, mang đến một thử thách độc hại cho tim và rằng, trong trường hợp không có phòng vệ thích hợp, PPCM có thể xảy ra. Cùng với mô hình STAT3, các phát hiện hỗ trợ mạnh mẽ cho quan niệm rằng PPCM là một bệnh mạch máu, được kích hoạt bởi môi trường nội tiết tố chu sinh (Hình 4). Khái niệm này có một số đặc tính giải thích cuốn hút. Đầu tiên, nó có thể giải thích tại sao PPCM thường xuất hiện trong giai đoạn chu sinh, khi thay đổi nội tiết tố là lớn nhất, thay vì sớm hơn nhiều trong thai kỳ, khi thay đổi huyết động là lớn nhất (Hình 2). Thứ hai, vai trò của sFlt1 có thể giải thích các quan sát dịch tễ học thiết lập tốt rằng PPCM có liên quan chặt chẽ với tiền sản giật và với đa thai, cả hai đều được đánh dấu bằng sự bài tiết cao sFlt1. Thứ ba, việc loại bỏ môi trường nội tiết tố độc sau khi sinh có thể giải thích sự phục hồi nhanh chóng thường thấy của chức năng tâm thất trong PPCM, thường không thấy trong các nguyên nhân khác của DCM. Giả thuyết nội tiết tố cũng đưa ra các cơ hội chẩn đoán lâm sàng, tiên lượng và điều trị. sFlt1, miR-146a hoặc những yếu tố nội tiết tố chưa được phát hiện có thể trở thành những dấu ấn sinh học hữu ích. Sự ức chế prolactin (ví dụ, với bromocriptine61) hoặc miR-146a (ví dụ, với antagomirs), liệu pháp proangiogenic (ví dụ, với các chất tương tự VEGF), hoặc loại bỏ các hormone độc (ví dụ, với thay huyết tương [109]). Tuy nhiên, những ý tưởng này vẫn đang thử nghiệm ở thời điểm này.
Di truyền
Một câu hỏi xuyên suốt trong cơ chế bệnh sinh của PPCM là biến cố hiếm gặp nào dẫn đến căn bệnh này. Một khả năng là nền tảng di truyền. Lập luận chống lại ý tưởng này, PPCM thường không phải là một bệnh gia đình và phả hệ của bệnh nhân PPCM đã không được báo cáo. Hơn nữa, PPCM thường không tái phát khi mang thai lần thứ hai, cho thấy rằng bất kỳ nguồn gốc di truyền nào, nếu có, là không hoàn toàn quyết định. Một nghiên cứu nhỏ gần đây về siêu âm tim trên chị/em gái của phụ nữ PPCM (n = 17) cho thấy không có bất thường về tim rõ ràng.[111] Tuy nhiên, một số bằng chứng đã ủng hộ quan điểm cho rằng PPCM có thể có thành phần di truyền hoặc gene. Một nghiên cứu kết hợp trên toàn bộ gen ở 79 bệnh nhân đã xác định được đa hình đơn nucleotide gần gen PTHLH có liên quan đến PPCM,[112] và điều thú vị là, PTHLH có thể điều hòa cân bằng nội môi mạch máu.[113] Gia đình PPCM đã được ghi nhận [114-117], 15% bệnh nhân trong đoàn hệ ở Đức có tiền sử gia đình mắc bệnh cơ tim (được định nghĩa một cách lỏng lẻo là PPCM, bệnh cơ tim vô căn [DCM], đột tử hoặc rối loạn nhịp tim ở dòng họ 1 đời).[56] Hai nhóm gần đây đã đánh giá phả hệ hiếm của bệnh nhân bị ảnh hưởng bởi cả PPCM và DCM và đã xác định được các đột biến trong gen mã hóa protein sợi cơ tim, bao gồm TTN, gen mã hóa protein sarcomere titin.[118,119] Liệu các đột biến tương tự có thể được tìm thấy trong PPCM lẻ tẻ vẫn không chắc chắn.
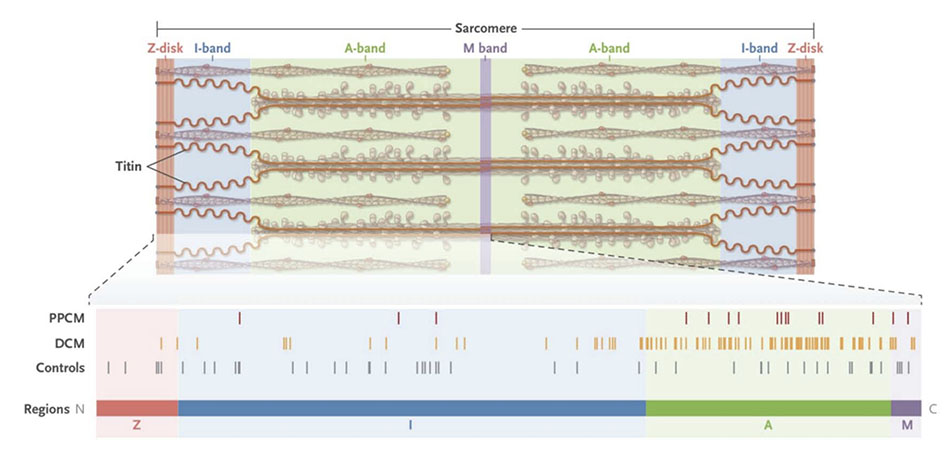
Gần đây nhất, một nghiên cứu di truyền đã được thực hiện với 172 bệnh nhân PPCM không được chọn trước về tiền sử gia đình hoặc các chỉ số khác về nguồn gốc di truyền.120 Trình tự mục tiêu của 43 gen được biết là có liên quan đến DCM cho thấy tỷ lệ mắc 15% ở bệnh nhân PPCM là các đột biến vô nghĩa, lệch khung và ghép nối tác động cao (P = 1.3 × 10−7 so với nhóm chứng). Thật thú vị, tỷ lệ bệnh tương tự như được tìm thấy trong một nhóm lớn các trường hợp DCM (17%; P = 0.81). Đáng chú ý, hai phần ba các đột biến mất đoạn được xác định là ở TTN (tỷ lệ gặp là 10%; P = 2.7 × 10−10 so với 1.4% trong dân số tham chiếu). Đáng chú ý không kém, 14 trong số 17 đột biến mất đoạn TTN này nằm trong dải A của titin (P = 0.0018 so với dân số tham chiếu; Hình 5).[120] Đột biến trong các đối tượng DCM cho thấy thiên hướng tương tự đối với ảnh hưởng đến dải A. [121,122]
Những phát hiện đáng ngạc nhiên này chỉ ra rằng PPCM thường có nguyên nhân di truyền và PPCM có chung nguồn gốc di truyền với DCM gia đình và lẻ tẻ. Các phân tích phân dưới nhóm sau nghiên cứu cũng cho thấy những quan sát thú vị:
- Các đột biến TTN được xác định ở cả phụ nữ da đen và da trắng;
- Trong phân nhóm phụ nữ tham gia đoàn hệ IPAC có đặc điểm lâm sàng tốt (n = 83), sự hiện diện của các đột biến TTN tương quan với EF thấp hơn sau 1 năm theo dõi (P = 0.005); và
- Gánh nặng các đột biến TTN mất đoạn ở những người không bị tăng huyết áp cao hơn gần 10 lần so với những người bị tăng huyết áp (23% so với 2.5%; P = 0.005). Những phát hiện sau nghiên cứu cần xác nhận thêm trước khi khuyến cáo lâm sàng có thể được hình thành.
Những phát hiện di truyền đưa ra một số câu hỏi. PPCM và DCM không giống nhau về mặt lâm sàng. Ví dụ, bệnh nhân DCM phục hồi chức năng LV ít thường xuyên hơn so với bệnh nhân PPCM, và DCM hiếm khi xảy ra ở phụ nữ trẻ. Do đó, vẫn còn bí ẩn về những biến số di truyền hoặc môi trường phân biệt phụ nữ mang đột biến TTN mất đoạn và phát triển PPCM từ những phụ nữ phát triển DCM hoặc từ những người không phát triển DCM. Cần phải làm sáng tỏ sự tương tác cơ học giữa các lần mất đoạn trong TTN và sự tấn công kháng vi mạch máu của thai kỳ muộn.
Kết luận
Những tiến bộ to lớn trong vài năm qua trong hiểu biết của chúng ta về PPCM, cả về mặt lâm sàng và cơ học. Tuy nhiên, tiến bộ này vẫn chưa được chuyển thành lợi ích hữu hình cho bệnh nhân. Không có liệu pháp hiệu quả đặc hiệu cho bệnh đã được chứng minh, và các xét nghiệm chẩn đoán hoặc tiên lượng cụ thể là thiếu. Việc quản lý PPCM vẫn chủ yếu giới hạn ở việc sử dụng thích hợp các thuốc đối kháng thần kinh- thể dịch thường quy được sử dụng trong các dạng DCM khác. Một số phát triển sẽ hỗ trợ đáng kể cho sự tiến bộ trong việc hiểu về PPCM. Đầu tiên, trong bối cảnh bản chất tương đối hiếm của PPCM, sự hợp tác và nghiên cứu đa trung tâm là rất cần thiết. Một cơ quan nghiên cứu tiến cứu trên toàn thế giới bắt đầu vào năm 2012 đang nhắm tới 1000 bệnh nhân và đến nay đã báo cáo 100 bệnh nhân, một nửa từ châu Phi và chỉ một số ít từ Hoa Kỳ.[123] Thứ hai, cần hỗ trợ nghiên cứu thêm. Hiện tại, National Institutes of Health không hỗ trợ một dự án duy nhất nghiên cứu PPCM.[124] Thứ ba, các nhóm vận động bệnh nhân có tổ chức sẽ giúp hỗ trợ và tuyển các đối tượng nghiên cứu; hiện không có nhóm như vậy tồn tại. Sự tiến bộ trong hiểu biết về PPCM đang ở điểm uốn. Với những nỗ lực phối hợp phù hợp, tiến bộ trong vài năm tới sẽ theo cấp số nhân và việc giao cho phòng khám có thể trở thành hiện thực.
Tài liệu tham khảo






















