Bài viết PEEP thấp hơn ARDS Network Protocol kết hợp với tỷ lệ tử vong cao hơn ở ARDS trẻ em được dịch bởi Bác sĩ Đặng Thanh Tuấn từ bài viết gốc: Positive End-Expiratory Pressure Lower Than the ARDS Network Protocol Is Associated with Higher Pediatric Acute Respiratory Distress Syndrome Mortality
Tóm tắt
Cơ sở lý luận: ARDS Network đã sử dụng mô hình PEEP/FiO2 trong nhiều nghiên cứu. Nói chung, các chuyên gia PICU sử dụng PEEP thấp và FiO2 cao hơn so với mô hình này.
Mục tiêu: Để đánh giá xem trẻ em được quản lý với PEEP thấp hơn mức khuyến cáo của mô hình PEEP/FiO2 ARDSNet có tỷ lệ tử vong cao hơn hay không.
Phương pháp: Phân tích hồi cứu đa trung tâm bệnh nhân ARDS Nhi (PARDS), được quản lý không có giao thức PEEP/FiO2 chính thức. Bốn tập dữ liệu riêng biệt được kết hợp để phân tích. Chúng tôi trích xuất các giá trị PEEP/FiO2 phù hợp với thời gian, tính toán sự khác biệt giữa mức PEEP và mức PEEP được đề xuất ARDSNet cho một FiO2 nhất định. Chúng tôi đã phân tích sự khác biệt trung bình trong 24 giờ đầu tiên của chẩn đoán PARDS so với tỷ lệ tử vong do ICU và điều chỉnh cho các biến nhiễu, hiệu chỉnh bổ trợ hoặc các yếu tố có thể ảnh hưởng đến xu hướng sử dụng PEEP thấp hơn.
Các phép đo và kết quả chính: Trong số 1.134 bệnh nhân PARDS, 26,6% được quản lý với PEEP thấp hơn so với FiO2 được đề xuất bởi giao thức ARDSNet. Bệnh nhân được quản lý với PEEP thấp hơn có tỷ lệ tử vong cao hơn so với những bệnh nhân được quản lý với mức PEEP phù hợp với hoặc cao hơn mức khuyến cáo của giao thức (p <0,001). Sau khi điều chỉnh giảm oxy máu, co bóp, bệnh lý kết hợp, mức độ nghiêm trọng của bệnh, cài đặt thông khí, nitric oxide và số liệu, PEEP thấp hơn khuyến cáo của giao thức vẫn độc lập liên quan đến tỷ lệ tử vong cao hơn (OR 2.05 [95% CI 1.32, 3.17]). Kết quả tương tự sau khi điều chỉnh dựa trên khuynh hướng (OR 2.00 [1.24, 3.22]).
Kết luận: Bệnh nhân PARDS được quản lý với PEEP thấp hơn so với FiO2 được khuyến nghị bởi mô hình ARDSNet có tỷ lệ tử vong cao hơn. Các thử nghiệm lâm sàng nhắm mục tiêu quản lý PEEP trong PARDS là cần thiết.
Giới thiệu
Mặc dù đủ PEEP là điều cần thiết để ngăn ngừa atelectrauma ở bệnh nhân có hội chứng suy hô hấp cấp tính (ARDS), dữ liệu quan sát ở cả người lớn và trẻ em làm nổi bật nhiều bệnh nhân ARDS thấp hơn PEEP so với khuyến nghị (1-3). Trong khi các phương pháp chuẩn độ PEEP gây tranh cãi, các nghiên cứu ARDS trước đây đã sử dụng bảng chuẩn độ PEEP/FiO2 được ARDSNetwork (3-5) phổ biến. Bảng này khuyến cáo các kết hợp của PEEP và FiO2, như vậy cả hai đều được lên thang hoặc xuống thang song song với tình trạng thiếu oxy xấu đi hoặc cải thiện. Trong khi các cách tiếp cận khác có thể có lợi, mức độ thiếu oxy là một cân nhắc quan trọng trong quản lý PEEP (4,6,7).
Có sự thay đổi đáng kể trong các kết hợp PEEP/FiO2 được lựa chọn trong quá trình thông khí chăm sóc thông thường, với khuynh hướng tăng FiO2 hơn là tăng PEEP khi có tình trạng thiếu oxy máu (2,8-11). Do đó, trong khi các bảng PEEP/FiO2 là tiêu chuẩn trong các thử nghiệm lâm sàng, thực tế lâm sàng ở nhi khoa có vẻ khá khác biệt. Điều này có thể là do có số liệu hạn chế trực tiếp đánh giá liệu bệnh nhân có được kết hợp với các kết hợp PEEP/FiO2 này có kết quả tốt hơn so với kết hợp được quản lý với các kết hợp khác nhau hay không.
Vấn đề này càng trở nên quan trọng hơn đối với nhi khoa, vì hầu như không có nghiên cứu nào kiểm tra mối quan hệ giữa PEEP và tử vong ở ARDS, mặc dù một số xác nhận khuyến cáo bảng PEEP/FiO2 từ ARDSNet hiếm khi được theo dõi ở trẻ em (8, 9,11-14). Nói chung, BS thường miễn cưỡng tăng PEEP trên 10 cmH2O, đặc biệt đối với trẻ nhỏ (8,11). Thông qua phân tích thứ cấp dữ liệu tổng hợp từ bốn nghiên cứu đã được công bố trước đây với ARDS trẻ em (11,15-18), chúng tôi đã tìm cách xác định xem bệnh nhân được quản lý với mức PEEP thấp hơn mức ARDSNet đề xuất cho một FiO2 đã cho tỷ lệ tử vong cao hơn so với bệnh nhân được quản lý với mức PEEP phù hợp với hoặc cao hơn mức khuyến nghị của bảng ARDSNet.
Phương pháp
Chúng tôi đã kết hợp bốn bộ dữ liệu được công bố trước đó về các trẻ em được thông khí cơ học xâm lấn (IMV, invasively mechanically ventilated) với PARDS (15-18). Hai trong số các bộ dữ liệu được thu thập lại bằng cách xem xét hồ sơ sức khỏe điện tử của Bệnh nhân Nhi khoa chuyên sâu (PICU) đã nhập viện Nhi khoa Los Angeles (CHLA) từ năm 2000 đến 2007 (15) và 2009-2013 (16). Một tập dữ liệu được thu thập nghiên cứu tiền cứu từ những bệnh nhân được nhận vào Bệnh viện Nhi đồng Philadelphia (CHOP) từ năm 2011 đến năm 2016 (17, 18). Tập dữ liệu thứ tư được tập hợp nghiên cứu tiền cứu trên 8 bệnh viện trong Mạng lưới hợp tác nghiên cứu chăm sóc tích cực trẻ em (CPCCRN, Collaborative Pediatric Critical Care Research Network) từ 2011-2012 (11). Chúng tôi đã loại trừ bệnh nhân CHOP và CHLA khỏi tập dữ liệu CPCCRN để ngăn chặn bất kỳ sự trùng lặp tiềm ẩn nào của bệnh nhân.
Đủ điều kiện PARDS
Trong khi các tiêu chí thu nhận cho mỗi nghiên cứu trong bốn nghiên cứu khác nhau một chút, chúng tôi bao gồm những bệnh nhân đã đáp ứng định nghĩa Hội nghị đồng thuận về tổn thương phổi cấp tính (PALICC, Pediatric Acute Lung Injury Consensus Conference) của trẻ trong khi đang điều trị IMV (1). Giảm oxy máu cho định nghĩa PARDS dựa trên chỉ số oxy hóa (OI, Oxygenation Index) ≥ 4 hoặc chỉ số bão hòa oxy (OSI, Oxygen Saturation Index) ≥ 5. Số liệu CHLA từ 2000-2007 và dữ liệu CHOP chỉ bao gồm bệnh nhân dựa trên OI, trong khi số liệu CHLA từ 2009-2013 và CPCCRN dữ liệu bao gồm bệnh nhân sử dụng OSI, khi OI không có sẵn. Tất cả bệnh nhân có một kích hoạt PARDS (tức là viêm phổi, nhiễm trùng huyết) với bệnh nhu mô phổi trên X quang ngực. Bệnh nhân suy hô hấp được cho là chủ yếu do bệnh tim đã được loại trừ. Trong khi yêu cầu đáp ứng các tiêu chí PALICC để đưa vào, vì câu hỏi của chúng tôi tập trung vào PEEP (ảnh hưởng đến áp lực đường thở trung bình, Mean Airway Pressure trong tính toán OI), chúng tôi đã chọn nhóm mức độ thiếu oxy máu dựa trên định nghĩa Berlin (tỷ lệ PaO2/FiO2), tỷ lệ PF được tính toán từ tỷ lệ SpO2/FiO2 sử dụng các phương trình đã công bố trước đó (19) khi không có khí máu động mạch.
Bảng điểm PEEP/FiO2
Chúng tôi trích xuất các giá trị PEEP và FiO2 theo thời gian mỗi 6 giờ trong 24 giờ đầu tiên sau khi chẩn đoán. Các phép đo FiO2 được phân loại thành các khoảng 0,05, dao động từ 0,21 đến 1,0. Đối với mỗi cặp FiO2/PEEP, chúng tôi tính toán mức PEEP được đặt cho một FiO2 đã cho là bao nhiêu từ giao thức ARDSNet “PEEP thấp” được khuyến nghị. Ví dụ, một bệnh nhân FiO2 là 0,6, bảng ARDSNet PEEP/FiO2 đề nghị một PEEP 10 cmH2O. Nếu bệnh nhân thực sự ở mức PEEP là 5 cmH2O, thì điểm khác biệt của PEEP là – 5. Đối với các giá trị FiO2 trong đó có nhiều mức PEEP được ARDSNet cho phép, chúng tôi sử dụng mức gần nhất với PEEP lâm sàng (ví dụ: PEEP lâm sàng = 6 cmH2O, ARDSNet PEEP cho phép 8-10 cmH2O, điểm chênh lệch PEEP = (6-8) = – 2 cmH2O). Sau đó chúng tôi lấy điểm trung bình trong 24 giờ đầu tiên của chẩn đoán PARDS (sử dụng điểm thời gian ban đầu cộng với 4 khối mỗi sáu giờ (nếu có)) để phân tích. Biến tổng hợp được coi là “PEEP thấp” được phân loại cho bệnh nhân có PEEP dưới giao thức cho một FiO2 nhất định và được sử dụng cho phân tích đa biến. Không có bệnh viện nào có giao thức chính thức để quản lý PEEP/FiO2, mặc dù CHOP đã sử dụng một chiến lược trong đó không có khả năng tiêu diệt FiO2 dưới 0,60 sau khi đặt nội khí quản đảm bảo tăng PEEP lên 8-10 cmH2O.
Biến bổ sung
Từ mỗi tập dữ liệu (khi có), chúng tôi trích xuất dữ liệu nhân khẩu học, chẩn đoán, cài đặt máy thở, sử dụng nitric oxide, bệnh lý kết hợp, sử dụng thuốc tăng co bóp/co mạch trong vòng 24 giờ sau khi chẩn đoán PARDS và kết quả. Các biến bổ sung này được đồng nhất giữa các tập dữ liệu để đảm bảo các định nghĩa trường hợp tương tự thông qua thảo luận giữa các nhà điều tra chính của từng nghiên cứu và dựa trên các biểu mẫu báo cáo trường hợp. Phần lớn dữ liệu bổ sung này không có sẵn từ tập dữ liệu CPCCRN, vì vậy những bệnh nhân này đã bị loại trừ khỏi các phân tích đa biến. Tử vong do PICU là kết cục chính.
Các phép đo và phân tích kết cục
Mục tiêu chính là đánh giá xem bệnh nhân có PEEP thấp hơn cho một FiO2 nhất định hơn bảng ARDSNet được đề xuất trong thực tế có tỷ lệ tử vong cao hơn bệnh nhân được quản lý với PEEP phù hợp hoặc cao hơn ARDSNet được đề xuất hay không. Chúng tôi xem xét biến kết hợp này vì trên cơ sở đơn biến, PEEP cao hơn và FiO2 cao hơn có liên quan đến tỷ lệ tử vong (cả hai đều tăng lên trong tình trạng thiếu oxy máu). Biến kết hợp này cho phép chúng tôi kiểm tra tác động tiềm tàng của các chiến lược máy thở ưu tiên một giá trị so với mục tiêu khác để đạt được mục tiêu oxy hóa, vì các biến này được thay đổi ở một mức độ khác nhau bởi các nhà cung cấp ở các trạng thái bệnh nhân tương tự. Mục tiêu thứ hai là xác định mối quan hệ này có nhất quán giữa tất cả các bộ dữ liệu hay không và liệu nó có bị ảnh hưởng bởi các biến có thể ảnh hưởng đến sự lựa chọn của PEEP như giảm oxy máu (tỷ lệ PF), nhân khẩu học và chẩn đoán, nitric oxide hay các yếu tố khác.
Chúng tôi báo cáo tỷ lệ tử vong của PICU như là một hàm của sự chênh lệch PEEP so với bảng ARDSNet. Tiếp theo chúng tôi đã tìm hiểu các yếu tố có thể liên quan đến tỷ lệ tử vong PICU hoặc PEEP thấp hơn so với khuyến cáo của giao thức cho một FiO2 đã cho. Các biến liên tục được phân tích theo tỷ lệ tử vong với Mann Whitney U test, vì dữ liệu thường không được phân phối bình thường. Dữ liệu phân loại được phân tích với một thử nghiệm Chi-squared với điều chỉnh Yates. Tử vong ICU cũng được xem xét như là một hàm của PEEP thấp hơn so với giao thức với phân tích sự sống còn, được phân tầng theo tỷ lệ PF ban đầu. Sau đó chúng tôi đã xây dựng mô hình hồi quy logistic đa biến giữ lại các biến có liên quan đến tử vong PICU hoặc dẫn đến thay đổi lớn hơn 15% trong ước tính tham số cho PEEP thấp hơn giao thức, cũng xem xét các thuật ngữ tương tác nhân (giữ lại các biến với p <0.1). Với sự tương quan cao giữa nhiều biến thông khí và biến oxy hóa, cho các mô hình đa biến, chúng tôi sử dụng tỷ lệ PF (tỷ lệ SF khi không có PaO2) thay vì OI do sự chồng chéo của áp suất đường thở trung bình với PEEP và các thiết lập thông khí khác. Chúng tôi đã chọn các biến khác tương quan chặt chẽ với nhau dựa trên ma trận tương quan (tức là áp suất đẩy và áp suất đỉnh hít vào) giữ lại biến có liên kết đơn biến cao nhất với kết quả, để tránh các vấn đề về đồng tuyến tính. Cuối cùng, điểm số xu hướng được tạo ra để mô hình lâm sàng và mức độ nghiêm trọng của các yếu tố bệnh liên quan đến PEEP thấp hơn giao thức, xem xét tất cả các biến có quan hệ đơn biến (p <0.2), giữ lại các biến duy trì mối quan hệ độc lập với PEEP thấp (p <0.1). Điểm số xu hướng này được sử dụng như điều chỉnh đa biến khi tiếp tục phân tích mối quan hệ độc lập giữa PEEP thấp hơn so với giao thức và tỷ lệ tử vong do PICU. Phân tích được thực hiện bằng cách sử dụng Microsoft Excel (Microsoft Corporation, Redmond, WA), Statistica phiên bản 12 (StatSoft, Tulsa, OK) và Stata version 10 (StatCorp, College Station, TX).
Phân tích độ nhạy
Chúng tôi thực hiện phân tích độ nhạy phân tầng bởi những người có tình trạng thiếu oxy máu kéo dài (PF ≤ 200) lúc 24 giờ. Ngoài ra, do sự khác biệt đáng chú ý giữa CHOP và CHLA datasets, chúng tôi đã thực hiện phân tích phân nhóm trong bộ dữ liệu, và đã phân tích so sánh giữa các tập dữ liệu. Đối với bệnh nhân CHLA, chúng tôi đã kiểm tra xem mối quan hệ này có tương tự như ngày 2 và 3 của thông khí cơ học hay không. Phân tích nhóm phụ bổ sung có thể được tìm thấy trong các tài liệu bổ sung.
Các kết quả
Mô tả của Cohort
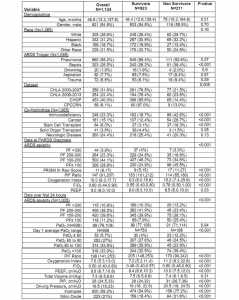
Từ 4 bộ dữ liệu, 1.134 bệnh nhân được thu nhận (358 CHLA 2000-2007, 254 CHLA 2009-2013, 453 CHOP và 69 CPCCRN). Tỷ lệ tử vong chung là 18,6%. Sử dụng phân loại của Berlin: 44 có PF > 300 (3,9%, 15,9% tử vong), 264 có PF 200-300 (23,3%, 13,3% tử vong), 500 có PF 100-200 (44,1%, 14,6% tử vong) và 326 có PF ≤ 100 (28,8%, 29,5% tử vong). Đặc điểm bệnh nhân của nhóm thuần tập được phân tầng theo tỷ lệ tử vong được tóm tắt trong Bảng 1. Phương thức thông khí thông thường là kiểm soát áp suất ở 63% bệnh nhân (> 97% bệnh nhân CHLA) và PRVC ở 36,7% bệnh nhân (93% của bệnh nhân CHOP).
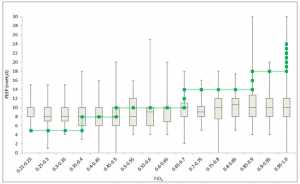
Có sự thay đổi trong các kết hợp PEEP/FiO2 được lựa chọn trong thực tế thực tế (Hình 1). Nói chung, FiO2 được ưu tiên hơn PEEP vì tình trạng thiếu oxy trở nên xấu đi. Nhìn chung, 302 (26,6%) bệnh nhân được quản lý với PEEP thấp hơn khuyến cáo ARDSNet, 351 (31,0%) được quản lý theo giao thức, 394 (34,7%) được quản lý với PEEP cao hơn giao thức và 87 (7,7%) không có dữ liệu PEEP đầy đủ cho ngày 1 của ARDS (5,7% CHOP, 14,5% CHLA 2000-2007, 3,1% CHLA 2009-13, 1,4% CPCCRN).
Chênh lệch PEEP
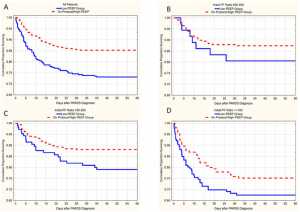
Trên phân tích không điều chỉnh, có một xu hướng phụ thuộc liều mà bệnh nhân được điều trị với PEEP thấp hơn khuyến cáo của giao thức cho một FiO2 nhất định trong 24 giờ đầu tiên chẩn đoán PARDS có tỷ lệ tử vong cao hơn, với tỷ lệ sống cao nhất với mức PEEP 1-4 cmH2O cao hơn sẽ được đề xuất bởi giao thức (Hình 2a). Khi phân tầng theo tỷ lệ PF ban đầu, mẫu này phù hợp, với hiệu ứng lớn nhất được thấy ở những tỷ lệ PF giữa 100 và 200 (Hình 2b-d). Nhìn chung, bệnh nhân được điều trị bằng PEEP thấp hơn khuyến nghị của phác đồ có tỷ lệ tử vong cao hơn (26,5% so với 14,9%, p <0,001). Xu hướng Whilethis là phù hợp trong tất cả các nhóm tỷ lệ PF ban đầu, chỉ có ý nghĩa thống kê ở những người có tỷ lệ PF từ 100 đến 200 (PF <100, 31 so với 26%, p = 0,3; PF 100-200 22,6% so với 11,8%, p = 0,004; PF 200-300 17,1% so với 12,3%, p = 0,4; Hình 3a-d).

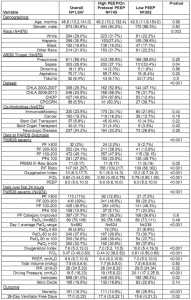
Bởi vì cao hơn FiO2 liên quan đến PEEP có thể phản ánh mức độ nghiêm trọng của bệnh hoặc các yếu tố cụ thể của bệnh nhân, chúng tôi đã tìm cách xác định các biến có thể liên quan đến việc sử dụng PEEP thấp hơn. Đối với phân tích này, chúng tôi đã hạn chế nhóm thuần tập đối với 1.047 bệnh nhân có giá trị PEEP và FiO2 hoàn chỉnh. Các biến được tìm thấy có liên quan đến việc sử dụng PEEP thấp hơn so với khuyến cáo của giao thức cho một FiO2 nhất định (tất cả p <0,05) bao gồm: chủng tộc gốc Tây Ban Nha; tập dữ liệu; nhóm PF 24 giờ thấp hơn tỷ lệ PF ban đầu và PF xấu hơn; OI cao hơn; sử dụng thấp hơn các thuốc tăng co bóp; nhiễm trùng huyết; điểm PRISM III cao hơn; và áp suất đẩy của máy thở (áp suất đỉnh hít vào – PEEP) cao hơn. Tuổi và thể tích khí lưu thông không được kết hợp với PEEP thấp hơn so với giao thức (p> 0.2). Nhóm tỷ lệ PF cải thiện 24 giờ sau khi chẩn đoán PARDS ở 38% bệnh nhân, mặc dù điều này dường như không liên quan đến việc sử dụng PEEP liên quan đến giao thức (Bảng 2).

Mô hình Multivariable và Propensity
Nói chung, nhiều bệnh nhân thiếu oxy có mức độ nghiêm trọng cao hơn của bệnh có nhiều khả năng được quản lý với PEEP thấp hơn so với FiO2 (Bảng 2). Để giải thích các yếu tố này, trước tiên chúng tôi đã xây dựng mô hình hồi quy logistic đa biến về kết quả tử vong của PICU. Sau khi kiểm soát tỷ lệ PF trong 24 giờ đầu tiên, sử dụng inotrope, suy giảm miễn dịch, cấy ghép tế bào gốc, điểm PRISM III, nitric oxide, áp suất đẩy và số liệu, bệnh nhân được quản lý với mức PEEP thấp hơn ARDSNet khuyến nghị cho một FiO2 nhất định có khả năng tử vong (OR 2.05 [1.32, 3.17], Bảng 3). Có hai tương tác cấp số nhân quan trọng được bao gồm (bộ dữ liệu CHOP * Nitric Oxide và Inotrope * Stem Cell Transplant). Sự tương tác giữa dữ liệu CHOP và PEEP liên quan đến giao thức không đáng kể (p = 0,4). Ngoài ra, chúng tôi đã tạo ra một mô hình xu hướng sử dụng PEEP thấp hơn so với khuyến cáo của giao thức. Tương tự, sau khi điều chỉnh xu hướng này để sử dụng PEEP thấp hơn và các biến số khác, chúng tôi nhận thấy PEEP thấp hơn so với FiO2 được đề xuất trong mô hình ARDSNet liên quan độc lập với tỷ lệ tử vong cao hơn (OR 2.0 [1.24, 3.22]) (Bảng bổ sung S1E3).
Phân tích độ nhạy
Khi giới hạn phân tích chỉ những người có tỷ lệ PF ≤ 200 24 giờ sau khi chẩn đoán PARDS, tỷ lệ chênh lệch đa biến tương tự, mặc dù không còn ý nghĩa thống kê (OR 1.64 [0.97, 2.77, p = 0.06]).
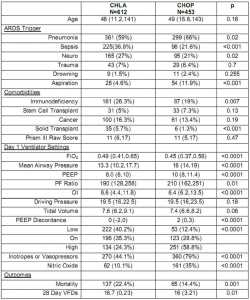
Có sự khác biệt đáng chú ý giữa các bộ dữ liệu, điều này đã thúc đẩy chúng tôi thực hiện phân tích phân nhóm và so sánh trực tiếp các bệnh nhân CHOP và CHLA. CHLA có tỷ lệ bệnh nhân có tỷ lệ PF ban đầu cao hơn <100 (33% CHLA so với 23% CHOP, p <0,001). Tỷ lệ PF được cải thiện ở tỷ lệ phần trăm tương tự của bệnh nhân 24 giờ giữa các bộ dữ liệu (36% CHLA 39% CHOP, p = 0,4). 24 giờ sau khi chẩn đoán PARDS 14,6% bệnh nhân CHLA có PF <100 so với 6,6% ở CHOP (p <0,001). Bệnh nhân tại CHOP có nhiều khả năng dùng thuốc tăng co bóp và co mạch hoặc bị viêm phổi hoặc viêm phổi hít. Bệnh nhân CHLA dễ bị nhiễm trùng huyết, suy giảm miễn dịch và cấy ghép nội tạng (Bảng 4, tất cả p <0,05; Phân lớp theo PF, Bảng S4).
Liên quan đến quản lý máy thở, CHOP sử dụng PEEP cao hơn khi FiO2 nằm trong khoảng 0,21-0,6 so với CHLA (Hình S1a-d). PEEP tại CHOP tuân theo phân phối gần đúng, trong khi PEEP tại CHLA có nhiều biến đổi hơn (Hình 4). CHOP sử dụng PEEP thấp hơn so với giao thức chỉ 12,4% thời gian (79% PF <100, 17,5% PF 100- 200, 2,9% PF 200-300), so với 40% ở CHLA (63% PF <100, 45,1% PF 100-200, 28,4% PF 200-300). Kết quả là, bệnh nhân có tỷ lệ PF> 100 24 giờ sau khi chẩn đoán PARDS tại CHOP là trên áp lực đường thở trung bình cao hơn, PEEP cao hơn, có OI cao hơn, với tỷ lệ PF tương tự hoặc cao hơn. Bệnh nhân CHOP có nhiều khả năng được hít Nitric Oxide (97% PF <100, 51% PF 100-200, 20% PF 200-300) so với bệnh nhân CHLA (26% PF <100, 10% PF 100-200, 5% PF 200-300)) . Áp lực đẩy và thể tích khí lưu thông tương tự giữa CHOP và CHLA (Hình 5, Hình S2, Bảng 4, Bảng S4).
Các chiến lược thông khí phi truyền thống (NCV, Non-Conventional Ventilation) đã được sử dụng ở 24,7% bệnh nhân trong 24 giờ đầu tiên chẩn đoán PARDS tại CHOP, so với 9,6% ở CHLA (p <0,001). OI trung bình lúc bắt đầu NCV là 20 (IQR 15, 28) với PEEP trung bình là 12 (IQR 10, 12) ở CHOP so với chỉ số trung bình là 35 (IQR 18, 48) với PEEP trung vị là 14 (IQR) 10, 15) tại CHLA (cả p = 0,01). Tỷ lệ tử vong tương tự giữa những người đã nhận và không nhận NCV trong 24 giờ đầu tiên ở CHOP (14,3% so với 14,4%, p = 0,99) nhưng những người nhận NCV trong 24 giờ đầu tiên tại CHLA có tỷ lệ tử vong cao hơn nhiều (44% so với 18,9%, p <0,001). Tại CHOP, chế độ NCV đầu tiên là Airway Pressure Release Ventilation ở mức 12.9%, ECMO trong 1.3%, HFOV trong 43% và thông khí vỗ tần số cao (High Frequency Percussive Ventilation) trong 43%. HFOV là chế độ NCV đầu tiên được sử dụng tại CHLA ở tất cả các bệnh nhân.
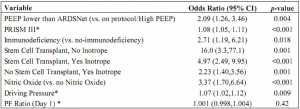
Trên cơ sở đơn biến ở cả hai bệnh viện, PEEP thấp hơn so với giao thức vào ngày thứ 1 có liên quan đến tỷ lệ tử vong cao hơn (Hình S3). Mối quan hệ này được giữ lại trong nhóm CHLA sau khi kiểm soát các yếu tố gây nhiễu tiềm tàng [OR 2.09 (1.26, 3.46), Bảng 5]. Tuy nhiên, sau khi kiểm soát các yếu tố gây nhiễu trong bộ dữ liệu CHOP, PEEP thấp hơn giao thức không liên quan đến tỷ lệ tử vong [OR 0.87 (0.32, 2.35), Bảng 6].

Dữ liệu PEEP ngày 2 và 3 có sẵn từ dữ liệu CHLA và tỷ lệ chênh lệch đa biến tương tự nhau, mặc dù kết quả không có ý nghĩa thống kê, có thể do kích thước mẫu nhỏ hơn (tài liệu bổ sung Bảng S5E6).
Thảo luận
Sử dụng giao thức ARDSNet PEEP/FiO2 như một khuôn khổ để phân tích dữ liệu quan sát từ hơn 1.100 bệnh nhân PARDS, chúng tôi nhận thấy rằng bệnh nhân được quản lý với mức PEEP thấp hơn khuyến cáo của mô hình ARDSNet cho một FiO2 nhất định có tỷ lệ tử vong cao hơn. Điều này phù hợp khi phân tầng theo tỷ lệ PF, và giữ sau khi kiểm soát các biến nhiễu trực tiếp trong mô hình đa biến, cũng như trong điều chỉnh biến đổi dựa trên xu hướng.
Trong khi chúng tôi đã chọn kết hợp các bộ dữ liệu cho phân tích chính bằng cách sử dụng các thuật ngữ tương tác để phân biệt sự khác biệt giữa các tổ chức, sự khác biệt đáng kể về bệnh kết hợp và quản lý máy thở giữa các tập dữ liệu đã khiến chúng tôi thực hiện phân tích phân nhóm theo tổ chức, cụ thể là CHOP và CHLA. Phân tích độ nhạy nhấn mạnh rằng mối quan hệ giữa PEEP thấp hơn so với giao thức và tỷ lệ tử vong có liên quan nhất trong dữ liệu CHLA. Chúng tôi tin rằng đây là vì nhiều lý do:
1. Bệnh nhân CHOP thường được quản lý với PEEP phù hợp với hoặc cao hơn so với khuyến nghị của giao thức. Chỉ có 12% bệnh nhân có mức PEEP thấp hơn so với khuyến nghị của giao thức tại CHOP, so với 40% ở CHLA và 40% trong số liệu CPCCRN. Điều này dẫn đến PEEP và áp suất khí trung bình cao hơn, với tỷ lệ PF tương tự.
2. Việc sử dụng PEEP không thay đổi nhiều ở CHOP như là một chức năng của tình trạng thiếu oxy máu. Tại CHOP, gần như tất cả các bệnh nhân có tỷ lệ PF> 100 đều có PEEP trên giao thức, và gần như tất cả bệnh nhân PF <100 đều có PEEP dưới giao thức. Những điểm cực đoan này (<20% bệnh nhân dưới giao thức khi PF> 100 và 20% trên hoặc cao hơn khi PF <100) gây khó khăn trong việc rút ra kết luận về quản lý PEEP từ dữ liệu CHOP một mình vì sử dụng dữ liệu quan sát để so sánh kết quả của bệnh nhân được quản lý với các kết hợp PEEP/FiO2 khác nhau phụ thuộc vào sự thay đổi mức PEEP đối với một FiO2 đã cho. Sự thay đổi này có mặt trong bộ dữ liệu CHLA và CPCCRN, nhưng không có ở CHOP.
3. Bệnh nhân ở CHOP có khả năng nhận được Nitric Oxide hít nhiều hơn 3 lần so với những người ở CHLA, điều này cũng có thể làm thay đổi mức độ thiếu oxy trong máu.
4. CHOP sử dụng thông khí không thường quy gần gấp 3 lần trong 24 giờ đầu so với CHLA, với chỉ số OI trung bình là 20 khi bắt đầu NCV tại CHOP, so với 35 ở CHLA.
5. CHOP chủ yếu sử dụng Pressure Regulated Volume Control trong khi CHLA sử dụng chủ yếu Pressure Control, mặc dù thể tích khí lưu thông và áp suất đẩy là tương tự giữa các tập dữ liệu.
6. Cuối cùng, CHOP chỉ bao gồm những bệnh nhân thâm nhiễm hai bên trên hình ảnh ngực (CXR), với các bộ dữ liệu khác bao gồm các bệnh nhân mắc bệnh 1 bên hoặc 2 bên. Chúng tôi đã chọn không phân tầng phân tích dựa trên diễn giải CXR vì mỗi tập dữ liệu sử dụng các phương pháp khác nhau để đo bệnh 2 bên so với 1 bên (tức là chuyên gia phóng xạ, BS hồi sức, nhiều học viên và thời gian đọc phim). Các nghiên cứu trong tương lai cần phải tiêu chuẩn hóa các giải thích này trước khi chúng ta hiểu sự liên quan của chúng.
Tỷ lệ tử vong chung thấp hơn CHOP so với CHLA. Một phần của điều này liên quan đến các tiêu chí và phương pháp khác nhau để sàng lọc PARDS, các tác nhân khởi phát PARDS khác nhau, sự khác biệt về bệnh kết hợp giữa các tập dữ liệu và sự khác biệt trong các liệu pháp bổ trợ như oxit nitric hít và các thuốc tăng co bóp và co mạch. Tuy nhiên, các chiến lược thông khí giữa các thể chế tương tự đối với thể tích khí lưu thông và áp lực đẩy, nhưng đặc biệt khác với chiến lược oxy hóa (đặc biệt là PEEP cao hơn ở CHOP đối với những ARDS nhẹ hoặc trung bình và sớm chuyển sang các phương pháp thông khí thay vì PEEP tăng thêm cho ARDS nghiêm trọng). Những dữ liệu nêu bật một thực tế của thực hành và nghiên cứu đa trung tâm, rằng quản lý máy thở là tổ chức và người hành nghề phụ thuộc vào sự thiếu vắng của một giao thức đã thoả thuận. Có rất ít các giao thức nhi khoa đã được phê chuẩn, khiến đây là một lĩnh vực quan trọng để nghiên cứu. Quản lý PEEP tại CHOP ít biến đổi hơn CHLA, với số lượng bệnh nhân thấp hơn đáng kể được điều trị bằng PEEP thấp hơn so với ARDSnet (12% so với 40%). Những phát hiện này có thể góp phần vào sự khác biệt về tỷ lệ tử vong giữa các tập dữ liệu.
Phát hiện của chúng tôi có thể có ý nghĩa quan trọng. Khi dữ liệu của chúng tôi và các nghiên cứu trước đây đã nhấn mạnh (2,8,9,11), có sự miễn cưỡng giữa các chuyên gia tăng cường sức khỏe trẻ em khi tăng PEEP để đáp ứng với tình trạng thiếu oxy, ưu tiên tăng FiO2. Trung bình, PEEP cao khoảng 10 cmH2O, ngay cả với tình trạng thiếu oxy máu nghiêm trọng. Lý do có thể là đa yếu tố, và có thể liên quan đến những lo ngại về mức PEEP cao ở trẻ sơ sinh và trẻ nhũ nhi có độ đàn hồi lồng ngực thấp, mối quan tâm về tương tác tim phổi hoặc niềm tin rằng FiO2 cao không nguy hiểm (20, 21).
Điều thú vị là chúng tôi thấy rằng bệnh nhân bị hyperoxia (tức là PaO2> 100) có tỷ lệ tử vong cao hơn so với những người có PaO2 bình thường hơn (60-100, Bảng 1), mặc dù phát hiện này không giữ trong mô hình đa biến. Tuy nhiên, nó cung cấp bằng chứng gián tiếp về ảnh hưởng xấu của nồng độ oxy cao, đặc biệt nếu nó dẫn đến tăng oxy máu. Mặc dù các nguyên tắc chung về thông khí bảo vệ phổi với việc sử dụng PEEP cao hơn để thúc đẩy việc tuyển dụng phế nang được hỗ trợ trong các chuyên gia về trẻ em, và trên thực tế được đề xuất cụ thể trong các hướng dẫn dựa trên chuyên môn về quản lý PARDS (1,10,22,23) không được thực hiện ở cạnh giường cho hầu hết trẻ em.
Trong thực tế, không có dữ liệu rõ ràng chứng minh rằng mức PEEP quan trọng trong các PARDS. Không có thử nghiệm ngẫu nhiên có đối chứng, và giống như nhiều phần khác của quản lý máy thở trong ARDS, ngoại suy trực tiếp từ người lớn có những hạn chế (3,15,20,24-27). Trong phân tích của chúng tôi, đối với những bệnh nhân có mức độ thiếu oxy tương tự ban đầu, việc quản lý với PEEP được kết hợp với FiO2 có liên quan đến tỷ lệ tử vong thấp hơn so với những người mà FiO2 chủ yếu tăng lên. Điều thú vị là chúng tôi thấy mô hình này rõ ràng nhất ở những người có tình trạng thiếu oxy máu vừa phải (PF 100-200). Trong khi người ta có thể suy đoán về lý do sinh lý cho phát hiện này, nó có thể liên quan đến kích thước mẫu và sự thay đổi trong quản lý PEEP trong phạm vi này. Phạm vi của PEEP (dưới, bằng, và cao hơn so với giao thức) cũng được thể hiện trong phân nhóm này, làm cho nó có thể tìm thấy một mối quan hệ tốt hơn. Một tỷ lệ lớn bệnh nhân bị PF <100 được quản lý với PEEP bên dưới giao thức và nhiều bệnh nhân được chuyển sang phương thức thông khí thay thế, làm cho khó có thể rút ra kết luận trong nhóm này một cách cụ thể.
Tuy nhiên, dữ liệu quan sát của chúng tôi không thể và không bao hàm mối quan hệ nhân quả mà việc quản lý dựa trên bảng ARDSNet PEEP/FiO2 cho PARDS sẽ dẫn đến tỷ lệ tử vong được cải thiện, mặc dù có khả năng sinh học mạnh mẽ cho điều này (6). Hơn nữa, có nhiều lý do để tin rằng bảng ARDSNet PEEP/FiO2 là tối ưu trong PARDS, như một cách tiếp cận cá nhân hơn bằng cách sử dụng áp lực xuyên phổi, độ giãn nở phổi, khoảng chết hoặc các phương pháp khác có lợi thế lý thuyết mạnh (5,6, 28-34). Tuy nhiên, dữ liệu của chúng tôi nhấn mạnh rằng có thể có vấn đề với việc quản lý PEEP chăm sóc thông thường trong PARDS và các thử nghiệm lâm sàng trong lĩnh vực này cần được ưu tiên cho nghiên cứu. Điều này đặc biệt quan trọng trong những phát hiện gần đây từ nghiên cứu huy động phế nang trong ARDS (ART), rằng bệnh nhân ARDS người lớn quản lý với việc huy động phổi và chuẩn độ PEEP dựa trên độ giãn nở hệ thống hô hấp có tỷ lệ tử vong cao hơn so với những người được quản lý bằng giao thức ARDSNet PEEP/FiO2 (35).
Chúng tôi bị hạn chế bởi các dữ liệu có sẵn, và nó có thể là những phát hiện của chúng tôi phản ánh mức độ nghiêm trọng của bệnh nhân của bệnh tật hoặc còn sót lại không được bảo đảm. Do tính chất của mô hình chuẩn độ ARDSNet PEEP/FiO2, bệnh nhân có các giá trị chênh lệch PEEP rất âm phải ở mức cao của FiO2. Thật vậy, tỷ lệ lớn nhất của bệnh nhân được quản lý với PEEP thấp hơn so với lượng FiO2 có tình trạng thiếu oxy máu nghiêm trọng. Để giảm thiểu những mối quan ngại này, chúng tôi đã thực hiện một loạt các phân tích phân tầng cũng như hai phương pháp điều chỉnh và mô hình hóa đa biến. Phát hiện của chúng tôi được tổ chức sau khi điều chỉnh đa biến và khuynh hướng biến đổi kết hợp các chỉ số oxy hóa, nguyên nhân kích hoạt PARDS, bệnh kết hợp, thuốc tăng co bóp và co mạch, mức độ nghiêm trọng của bệnh, các thiết lập thông khí khác và nitric oxide hít. Tuy nhiên, chúng tôi không có dữ liệu về những yếu tố gây nhiễu tiềm tàng khác (tức là các đồng can thiệp khác như thuốc chẹn thần kinh cơ, tư thế nằm sấp, hội chứng rò rỉ khí hoặc tràn khí màng phổi, …), về thâm nhiễm 2 bên và 1 bên. Những hạn chế này có thể chỉ được khắc phục bằng một thử nghiệm đối chứng ngẫu nhiên được thiết kế tốt.
Tóm lại, thông qua phân tích dữ liệu thứ cấp từ hơn 1.100 bệnh nhân PARDS, chúng tôi nhận thấy rằng bệnh nhân được quản lý với mức PEEP thấp hơn khuyến cáo của mô hình ARDSNet PEEP/FiO2 có tỷ lệ tử vong cao hơn, ngay cả sau khi điều chỉnh biến đổi. Các thử nghiệm ngẫu nhiên có đối chứng nhằm quản lý PEEP trong PARDS là cần thiết.





