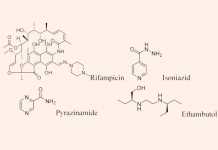
Lịch sử ra đời nhóm kháng sinh Cephalosporin
Các kháng sinh nhóm β-lactam có thể nói là nhóm kháng sinh quan trọng nhất trên lâm sàng hiện nay, bởi hơn 60% (gần 2/3) tổng số kháng sinh được sử dụng trên lâm sàng hiện nay là các kháng sinh thuộc nhóm này. Trong số các β-lactam thì các kháng sinh nhóm Cephalosporin chiếm số lượng lớn nhất và được ứng dụng nhiều nhất, với hơn ½ các β-lactam được sử dụng là các Cephalosporin. Điều này cho thấy tầm quan trọng của các Cephalosporin trong việc điều trị các bệnh lý nhiễm khuẩn hiện nay.

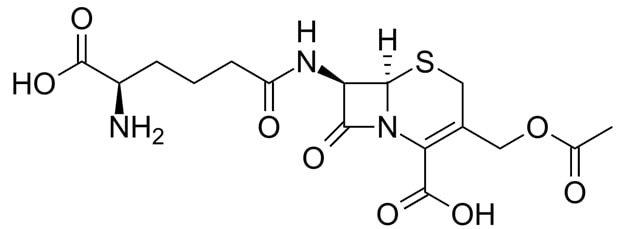
Loại Cephalosporin đầu tiên trên thế giới được tìm ra là Cephalosporin C, được tiết ra từ một loài nấm mốc được tìm thấy trong một cống thoát nước thải tại vùng Su Siccu, cảng Cagliari, đảo Sardinia, một đảo có truyền thống văn hóa lâu đời tại Italia. Nó được nhà khoa học người Italia tên là Giuseppe Brotzu tìm ra đầu tiên từ những năm 1945, có nghĩa là đã từ rất lâu rồi. Ở thời điểm đó, A.Fleming, cha đẻ của Penicillin, mới được trao giải thưởng Nobel về Sinh lý và Y khoa nhờ sự phát hiện ra Penicillin của mình. Đó cũng là năm mà Chiến tranh Thế giới thứ II kết thúc và một kỷ nguyên vàng của kháng sinh sắp sửa chuẩn bị được mở ra. Kỷ nguyên này cũng gắn liền với sự ra đời của rất nhiều Penicillin.
Cephalosporin C được tìm thấy ban đầu có hoạt tính kháng khuẩn rất yếu. Người ta đã nghĩ ra cách biến đổi nó bằng các phản ứng hóa học (bán tổng hợp hóa học), thay thế 2 nhóm thế của nó bằng cách nhóm thế khác để mong muốn tạo ra các loại kháng sinh có hoạt phổ như mong muốn. Từ đó, một lớp các kháng sinh Cephalosporin bán tổng hợp ra đời, phục vụ cho ngày càng nhiều các nhu cầu điều trị khác nhau trên lâm sàng.
Tham khảo thêm: Kháng sinh nhóm Penicillin: Cơ chế tác dụng, Chỉ định, Lưu ý tác dụng phụ
Cấu trúc hóa học
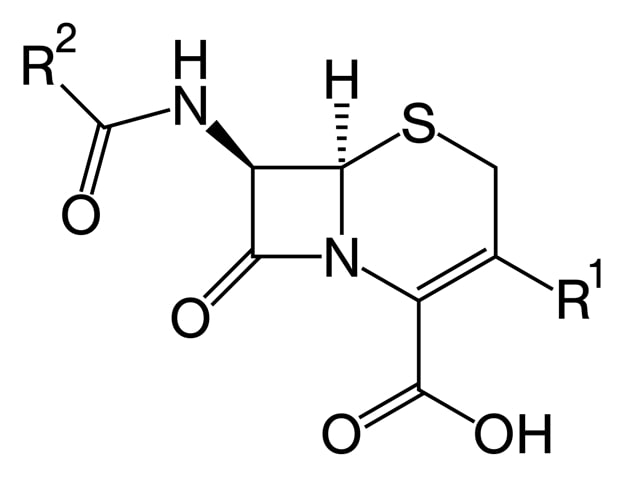
Các Cephalosporin hiện nay đều là các kháng sinh bán tổng hợp, với cấu trúc vòng β-lactam được thể hiện như hình dưới.
So với cấu trúc vòng β-lactam của Penicillin thì cấu trúc vòng của các Cephalosporin ổn định hơn do sức căng của hệ vòng giảm. Từ đó, nhiều kháng sinh nhóm này cũng bền vững hơn trước các β-lactamase so với các Penicillin. Nếu sắp xếp theo thứ tự độ bền vững với enzyme β-lactamase tăng dần, ta có Penicillin < Cephalosporin < Carbapenem.
Các kháng sinh nhóm Cephalosporin đều được đặc trưng bởi 2 nhóm thế R1 và R2 như trên hình vẽ. Không giống như các Penicillin vốn chỉ có 1 nhóm thế, các Cephalosporin có 2 nhóm thế nên số lượng và mức độ đa dạng của các kháng sinh nhóm này cũng cao hơn các Penicillin một cách đáng kể.
Dược lực học của nhóm kháng sinh Cephalosporin
Cơ chế tác dụng
Cơ chế tác dụng diệt khuẩn của các kháng sinh nhóm Cephalosporin nói riêng cũng tương tự như các kháng sinh nhóm β-lactam nói chung. Nhưng trước khi đi vào tìm hiểu cơ chế kháng khuẩn của nó, chúng ta cần ghi nhớ một điều hết sức quan trọng, đó là các kháng sinh nhóm β-lactam (bao gồm cả các Cephalosporin) đều là các kháng sinh diệt khuẩn phụ thuộc vào thời gian. Trái ngược với một số kháng sinh diệt khuẩn phụ thuộc vào nồng độ như các Aminoside (nồng độ càng cao diệt khuẩn càng mạnh), tác dụng diệt khuẩn của các kháng sinh nhóm β-lactam không tăng nhanh theo nồng độ. Tác dụng diệt khuẩn của chúng chỉ đạt được tối đa ở một ngưỡng nồng độ nào đó và ở các nồng độ cao hơn, tác dụng diệt khuẩn không tăng nữa. Yếu tố quyết định đến hiệu quả điều trị của kháng sinh nhóm này là thời gian mà nồng độ thuốc trong máu lớn hơn giá trị MIC (nồng độ ức chế tối thiểu). Việc này đặc biệt có ý nghĩa khi thiết kế chế độ liều cho bệnh nhân. Hiểu rõ PK/PD (dược động học/dược lực học) của thuốc trong thực hành lâm sàng sẽ giúp tối ưu hóa các phác đồ điều trị nhiễm khuẩn, đặc biệt là các nhiễm khuẩn nặng, nhiễm khuẩn bệnh viện và đa kháng. Nếu ứng dụng tốt PK/PD trong chế độ liều cho bệnh nhân, ta vẫn có thể sử dụng một số loại kháng sinh đã bị nhạy cảm trung gian (tức MIC của kháng sinh với vi khuẩn đã tăng lên nhưng chưa đến mức đề kháng [nhiều bệnh viện hiện nay xếp nhạy cảm trung gian đồng nghĩa với đề kháng]) để điều trị một số loại nhiễm khuẩn nặng.
Cơ chế tác dụng của các kháng sinh nhóm β-lactam nói chung cũng như các kháng sinh Cephalosporin nói riêng là ức chế tổng hợp vách tế bào (cell wall) của vi khuẩn. Vách tế bào giống như một bức tường vững chãi để bảo vệ vi khuẩn khỏi các tác nhân bên ngoài có hại với nó cũng như bảo vệ vi khuẩn khỏi bị vỡ do áp suất thẩm thấu nội bào vô cùng cao. Như vậy, việc ức chế tổng hợp vách tế bào của các Cephalosporin chắc chắn sẽ làm cho vi khuẩn chết. Do các Cephalosporin chỉ ức chế tổng hợp vách tế bào vi khuẩn nên chúng chỉ có tác dụng trên các vi khuẩn đang phát triển. Những vi khuẩn nào đã phát triển xong, lớp thành tế bào đã hoàn thiện rồi thì kháng sinh không thể tiêu diệt được chúng.
Vậy các Cephalosporin ức chế tổng hợp vách tế bào của vi khuẩn như thế nào? Kháng sinh này tác động vào một polymer nằm trên vách tế bào vi khuẩn có tên gọi là peptidoglycan. Đây là một polymer liên kết chéo, có cấu trúc mạng lưới phức tạp và rất bền vững. Chính lớp peptidoglycan này làm nên sự chắc chắn của vách tế bào. Tuy vậy, cấu trúc peptidoglycan này ở mỗi loại vi khuẩn lại có sự khác biệt nhất định. Ở vi khuẩn gram dương, lớp peptidoglycan rất dày và là thành phần gần như duy nhất của vách tế bào. Trong khi đó, ở các vi khuẩn gram âm, lớp peptidoglycan này lại rất mỏng, nhưng bù lại, cấu trúc vách tế bào vi khuẩn gram âm lại phức tạp hơn nhiều với thêm một lớp phospholipid kép bên ngoài vách tế bào (còn gọi là lớp màng ngoài “outer membrane”). Trong rất nhiều trường hợp, lớp màng ngoài này chính là một hàng rào tự nhiên cản trở sự xâm nhập của các kháng sinh nhóm Cephalosporin. Chỉ khi đi qua được lớp màng ngoài này, các Cephalosporin mới thể hiện được tác dụng của chúng.
Vậy các kháng sinh nhóm Cephalosporin ức chế tổng hợp lớp peptidoglycan này như thế nào? Chúng ta cần hiểu rõ hơn về cấu tạo của nó cũng như cách vi khuẩn tổng hợp peptidoglycan. Như đã nói ở trên, peptidoglycan là một polymer, đã là một polymer thì phải được cấu tạo từ các monomer. Các monomer cấu thành nên lớp peptidoglycan gồm 2 thành phần: N-acetylmuramic acid và N-acetylglucosamine. Ngoài ra, để tạo nên các liên kết chéo đặc trưng trong lớp peptidoglycan, mỗi monomer không thể thiếu những cầu nối là các chuỗi peptide ngắn, gọi là pentapeptide (gồm 5 amino acid liên kết với nhau), được gắn vào phần N-acetylmuramic acid. Việc các monomer này được liên kết theo chiều ngang với nhau thì rất đơn giản, thông qua phản ứng ngưng tụ giữa một đầu N-acetylglucosamine của monomer này với một đầu N-acetylmuramic acid của một monomer khác. Tuy vậy, mấu chốt trong cơ chế tác dụng của các kháng sinh nhóm Cephalosporin lại nằm ở bước cuối cùng trong tổng hợp lớp peptidoglycan của vi khuẩn, bước hình thành liên kết chéo giữa các monomer. Để hình thành liên kết chéo giữa các monomer với nhau, các vi khuẩn cần có một enzyme có tên gọi là transpeptidase, hay còn có tên gọi khác là PBP (“Penicillin-Binding Protein”: Protein gắn Penicillin). Enzyme này chịu trách nhiệm cho sự kết nối 2 chuỗi peptide ở 2 monomer chéo nhau, thông qua phản ứng cắt đi một amino acid ở phía đầu chuỗi là D-Ala. Cơ chất của enzyme trong phản ứng này chính là đầu D-Ala-D-Ala của chuỗi peptide. Các kháng sinh nhóm Cephalosporin của chúng ta ức chế tổng hợp lớp peptidoglycan thông qua ức chế enzyme transpeptidase này. Cụ thể, các kháng sinh nhóm Cephalosporin nói riêng cũng như các kháng sinh nhóm β-lactam nói chung, đều có cấu trúc hóa học tương đồng với đầu D-Ala-D-Ala của chuỗi peptide đó. Kết quả là, các phân tử kháng sinh có thể trở thành một “cơ chất thứ hai” cạnh tranh với D-Ala-D-Ala là cơ chất thứ nhất của enzyme đó. Các phân tử kháng sinh hình thành liên kết cộng hóa trị bền vững với amino acid Serine trong trung tâm hoạt động của enzyme, làm bất hoạt enzyme. Khi đã bị bất hoạt, điều này đồng nghĩa với sự tổng hợp lớp peptidoglycan bị ức chế. Các liên kết chéo giữa các monomer không được hình thành làm vách tế bào vi khuẩn trở nên yếu ớt và dễ dàng bị phá hủy từ chính áp suất thẩm thấu bên trong.
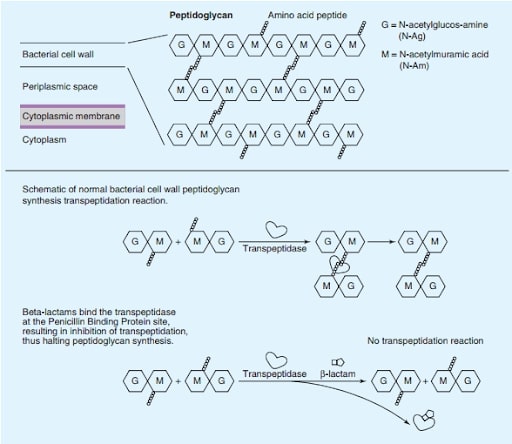
Với cơ chế tác dụng đặc thù như thế này, các kháng sinh nhóm Cephalosporin có thể tác động trên rất nhiều chủng vi khuẩn khác nhau, kể cả gram dương hay gram âm, hiếu khí hay kị khí. Một số chủng vi khuẩn đặc biệt sau không nằm trong phổ tác dụng của các Cephalosporin:
– Vi khuẩn không điển hình: Các vi khuẩn này còn có tên gọi khác là vi khuẩn nội bào. Các vi khuẩn này không có vách tế bào, vậy nên các kháng sinh nhóm Cephalosporin không thể tiêu diệt chúng được.Đại diện cho nhóm các vi khuẩn này bao gồm Chlamydia, Mycoplasma (thường gây viêm phổi không điển hình) và Rickettsia (thường gây bệnh sốt mò).
– Clostridium difficile: Đây là vi khuẩn gây viêm đại tràng giả mạc, thường gặp trong sử dụng kháng sinh điều trị một bệnh nhiễm khuẩn khác. Chỉ có các thuốc sau mới được sử dụng để điều trị viêm đại tràng giả mạc do C.difficile: Vancomycin (bình thường thuốc được dùng theo đường truyền tĩnh mạch, nhưng với bệnh lý này cần dùng thuốc theo đường uống), Metronidazole hoặc Fidaxomicin.
– Tụ cầu vàng kháng Methicillin (Methicillin-Resistant Staphylococcus aureus, gọi tắt là MRSA) hoặc tụ cầu da kháng Methicillin (Methicillin-Resistant Staphylococcus epidermidis, gọi tắt là MRSE): Các kháng sinh nhóm Cephalosporin thế hệ từ I đến IV không thể tiêu diệt các chủng vi khuẩn này, nhưng với sự ra đời của các Cephalosporin thế hệ V gần đây, chúng ta đã có thêm một lựa chọn điều trị tốt cho MRSA và MRSE.
Do tế bào người không có vách tế bào cũng như lớp peptidoglycan, chúng sẽ không bị ảnh hưởng bởi cơ chế tác dụng này của kháng sinh.
Phổ tác dụng
Phổ tác dụng của các Cephalosporin khá phức tạp, nhưng chúng ta có thể dễ dàng ghi nhớ nó nhờ phân loại chúng thành các nhóm:
– Cephalosporin thế hệ I: Đây là nhóm các Cephalosporin có phổ tác dụng ưu thế trên vi khuẩn gram dương hơn là gram âm. Chúng có tác dụng tốt trên tụ cầu (nhạy cảm Methicillin), liên cầu, phế cầu (chưa kháng Penicillin). Với các vi khuẩn gram âm, chúng có thể có hoạt tính trên E.coli, Proteus mirabilis và Klebsiella pneumoniae. Tác dụng hạn chế trên vi khuẩn kị khí, chúng có thể có tác dụng trên các chủng Peptococci và Peptostreptococci, nhưng không có tác dụng trên các chủng Bacteroides và Clostridium.
Các kháng sinh nhóm này nhìn chung không bền với β-lactamase.
Hai đại diện của phân nhóm Cephalosporin thế hệ I nổi bật nhất bao gồm Cephalexin (dùng đường uống) và Cefazolin (dùng đường tiêm).
– Cephalosporin thế hệ II: Thế hệ này có phổ kháng khuẩn trên các vi khuẩn gram dương hẹp hơn một chút nhưng phổ kháng khuẩn trên các vi khuẩn gram âm rộng hơn so với thế hệ I. Thậm chí một số kháng sinh còn có tác dụng tốt trên vi khuẩn kị khí.
Các thuốc trong phân nhóm này có thể chia ra thành 2 phân nhóm nhỏ hơn nữa: Cephalosporin thế hệ II thực sự và các Cephamycin. Đại diện nổi bật cho các kháng sinh Cephalosporin thế hệ II thực sự là Cefuroxime, Cefaclor và Cefprozil. Các kháng sinh này có phổ tác dụng tốt trên Haemophilus influenzae (kể cả các chủng đã kháng Cephalosporin thế hệ I). Đại diện nổi bật cho các kháng sinh Cephamycin là Cefoxitin và Cefotetan. Hai kháng sinh này có tác dụng trên các chủng vi khuẩn kỵ khí Bacteroides và Serratia rất tốt.
Các Cephalosporin thế hệ II đã có độ bền với enzyme β-lactamase cao hơn thế hệ I.
– Cephalosporin thế hệ III: Đây là phân nhóm chứa nhiều kháng sinh nhất trong số các phân nhóm Cephalosporin. Các đại diện nổi bật nhất của phân nhóm này bao gồm các kháng sinh dùng đường tiêm Ceftriaxone và Cefotaxime, các kháng sinh dùng đường uống Cefixime, Cefdinir và Cefpodoxime, các kháng sinh chống trực khuẩn mủ xanh Ceftazidime và Cefoperazone.
So với các Cephalosporin thế hệ II, các kháng sinh thuộc thế hệ III tiếp tục có phổ tác dụng trên vi khuẩn gram dương thu hẹp (nhưng vẫn có tác dụng tốt trên phế cầu và tụ cầu nhạy cảm Methicillin) và phổ trên vi khuẩn gram âm mở rộng, ví dụ như S.marcescens, Providencia và Citrobacter, một số kháng sinh còn có tác dụng trên cả trực khuẩn mủ xanh (Pseudomonas aeruginosa).
Độ bền vững với enzyme β-lactamase của thế hệ III này cao hơn thế hệ II. Nếu như enzyme β-lactamase của vi khuẩn có khả năng phá hủy vòng β-lactam của các kháng sinh từ Cephalosporin thế hệ III trở lên, chúng được coi là ESBL (Extended Spectrum Beta-Lactamase: β-lactamase hoạt phổ rộng).
– Cephalosporin thế hệ IV: Thuốc được dùng phổ biến ở Việt Nam là Cefepime, ngoài ra còn có Cefpirome. Phổ tác dụng của chúng trên vi khuẩn gram dương tương tự như thế hệ III (phổ hẹp, có tác dụng tốt trên các chủng phế cầu kháng Penicillin và tụ cầu nhạy cảm Methicillin), phổ trên vi khuẩn gram âm tiếp tục được mở rộng, ngoài có tác dụng trên các vi khuẩn giống kháng sinh thế hệ III như H.influenzae, lậu cầu (Neisseria gonorrhoeae), trực khuẩn mủ xanh, chúng còn có tác dụng trên các vi khuẩn thuộc chi Enterobacter của họ Enterobacteriaceae.
Độ bền với enzyme β-lactamase của các kháng sinh thế hệ IV tiếp tục được tăng cường, nhưng chúng vẫn bị phá hủy bởi ESBL.
– Cephalosporin thế hệ V: Đây là một phân loại chưa hẳn là chính thức bởi vì nhiều nhà khoa học còn chưa công nhận nó. Nhưng đứng về mặt lâm sàng, chúng xứng đáng được xếp vào thế hệ V. Các kháng sinh thế hệ thứ 5 này có phổ tác dụng trên các vi khuẩn gram âm không tốt lắm, khi mà không có tác dụng trên trực khuẩn mủ xanh (trừ Ceftolozane/Tazobactam), nhưng bù lại, chúng có tác dụng tốt trên các vi khuẩn kị khí như các Cephamycin (Cephalosporin thế hệ II), và đặc biệt, chúng là các kháng sinh β-lactam duy nhất có phổ bao phủ được MRSA và MRSE. Công thức phân tử của các kháng sinh thế hệ này được thiết kế để làm tăng ái lực gắn của thuốc với PBP2a của vi khuẩn.
Các đại diện nổi bật của kháng sinh thế hệ này bao gồm Ceftaroline, Ceftolozane (kết hợp với Tazobactam) và Ceftobiprole. Ceftolozane/Tazobactam đã có mặt tại thị trường Việt Nam dưới tên thương mại Zerbaxa.
Các kháng sinh này cũng bền với enzyme β-lactamase tương tự thế hệ IV, nhưng bị thủy phân bởi ESBL hoặc AmpC β-lactamase.
– Siderophore Cephalosporin: Phần này được dành riêng cho một kháng sinh nhóm Cephalosporin nhưng chưa rõ phải phân loại nó vào thế hệ nào. Đó là Siderophore Cephalosporin, với đại diện là Cefiderocol. Bản thân từ Siderophore có nghĩa là chất vận chuyển sắt. Vậy tại sao Cefiderocol lại có tên gọi lạ như vậy?
Để tìm hiểu điều này, chúng ta cần biết rằng với vi khuẩn gram âm, vách tế bào của nó có cấu tạo rất đặc biệt: Bên ngoài lớp peptidoglycan mỏng là một lớp màng ngoài cấu tạo từ phospholipid kép. Đây là một lớp hàng rào tự nhiên cản trở sự xâm nhập của các kháng sinh nói chung cũng như kháng sinh nhóm Cephalosporin nói riêng. Để có thể vượt qua được lớp màng ngoài vốn kị nước (các kháng sinh Cephalosporin là các phân tử ưa nước), phân tử kháng sinh cần đi qua các kênh porin để vào bên trong tế bào. Các kênh porin này có bản chất là các protein. Chúng chịu trách nhiệm cho các quá trình hấp thu các chất thiết yếu của vi khuẩn. Thông thường, các kháng sinh của chúng ta sẽ di chuyển qua các kênh porin này theo cơ chế khuếch tán thụ động. Để có thể khuếch tán thụ động qua kênh porin cần có cấu trúc cũng như độ phân cực thích hợp, và đó là lý do vì sao các Cephalosporin thế hệ III và IV lại có tác dụng tốt trên các vi khuẩn gram âm hơn các Cephalosporin thế hệ I và II, đó là bởi khả năng đi qua các kênh porin của vi khuẩn tốt hơn (tất nhiên còn có cả nguyên nhân do độ bền với enzyme β-lactamase của các kháng sinh thế hệ III và IV tốt hơn). Nhưng vi khuẩn có thể phát sinh đột biến đề kháng thuốc bằng cách làm giảm số lượng các kênh porin, từ đó làm giảm lượng kháng sinh có thể vào trong tế bào, hoặc làm giảm ái lực của các kênh porin này với kháng sinh của chúng ta, từ đó lượng kháng sinh vào trong tế bào vi khuẩn cũng giảm đáng kể.
Cefiderocol là một kháng sinh đặc biệt hơn các Cephalosporin khác bởi 2 lẽ: Thứ nhất, nó là một kiểu kháng sinh “lai tạp” giữa Ceftazidime và Cefepime. Điều này làm độ bền của phân tử kháng sinh với enzyme β-lactamase cực kỳ cao, mà hoạt phổ của nó trên các vi khuẩn gram âm, trong đó có trực khuẩn mủ xanh, cũng cực kỳ tốt. Tuy nhiên, điều thứ hai mới thực sự là thú vị. Bạn đọc có thể thấy ngay sự thú vị của nó nhờ chữ “Siderophore” (chất vận chuyển sắt) đã được nói ở trên. Trong cấu trúc của kháng sinh, các nhà tổng hợp hóa dược đã thiết kế thêm cho nó một nhóm catechol (tức 2 nhóm –OH phenol ở vị trí liền kề nhau [vị trí ortho] trên nhân phenyl thơm). Cấu trúc này giúp kháng sinh có khả năng tạo thành phức chelate với ion sắt. Mà ion sắt lại là một yếu tố cần thiết, cực kỳ quan trọng cho sự phát triển của vi khuẩn. Cho dù vi khuẩn đó có là vi khuẩn gì đi chăng nữa thì nó vẫn cần sắt, và để có sắt thì nó cần có một cơ chế vận chuyển chủ động sắt vào bên trong tế bào. Và đây chính là mấu chốt của vấn đề: Phức hợp giữa Cefiderocol và ion sắt đã được chính vi khuẩn vận chuyển chủ động vào bên trong tế bào (trái ngược hẳn với các kháng sinh khác được khuếch tán thụ động). Khi đã vào bên trong tế bào rồi, phân tử Cefiderocol tách khỏi sắt và thực hiện chức năng ức chế PBP của vi khuẩn như bình thường. Có thể ví việc khiến cho vi khuẩn tự chủ động vận chuyển phân tử kháng sinh vào bên trong tế bào giống như là “con ngựa thành Troy” vậy.
Cefiderocol có tác dụng tốt trên nhiều vi khuẩn gram âm khác nhau như E.coli, Klebsiella, Haemophilus, Enterobacter, Proteus, Salmonella, Pseudomonas, Acinetobacter… Tác dụng trên các vi khuẩn kị khí cũng như các vi khuẩn gram dương kém hơn.
Cơ chế đề kháng
Với sự sử dụng kháng sinh một cách lạm dụng và bừa bãi như hiện nay, tình trạng kháng kháng sinh ở vi khuẩn đang ngày càng đáng báo động. Tình trạng bán thuốc kháng sinh mà không cần kê đơn ở các nhà thuốc, quầy thuốc là vô cùng phổ biến, không chỉ ở những nước đang phát triển như Việt Nam, mà nó còn phổ biến cả ở những nước phát triển như Hoa Kỳ.
Cơ chế đề kháng với kháng sinh nhóm Cephalosporin của vi khuẩn cũng tương tự như các cơ chế đề kháng với các kháng sinh nhóm β-lactam nói chung. Có tổng cộng tất cả 4 cơ chế đề kháng đã được phát hiện, bao gồm:
– Thay đổi đích tác dụng của kháng sinh: Đây là cơ chế đề kháng đặc biệt phổ biến ở các vi khuẩn gram dương, đồng thời cũng là cơ chế tồn tại với mọi loại kháng sinh, không riêng gì các β-lactam. Các vi khuẩn dưới áp lực của việc sử dụng kháng sinh nhiều, một số lượng nhỏ sẽ phát sinh đột biến thay đổi cấu trúc của PBP, làm giảm ái lực gắn của PBP với phân tử kháng sinh, nhưng đồng thời vẫn đảm bảo có tác dụng hình thành các liên kết chéo trong peptidoglycan tốt. Với cơ chế đề kháng này, vi khuẩn có thể đề kháng với mọi loại kháng sinh trong nhóm β-lactam. Việc điều trị các vi khuẩn này thường gặp nhiều khó khăn bởi rất khó có thể lựa chọn thuốc điều trị.
– Tổng hợp enzyme phá hủy phân tử kháng sinh: Enzyme phá hủy phân tử kháng sinh β-lactam có tên gọi chung là các β-lactamase. Chúng phá vỡ cấu trúc vòng β-lactam, đây là cấu trúc đóng vai trò quan trọng trong hoạt tính của kháng sinh. Bản thân β-lactamase cũng có nhiều loại, bao gồm các penicillinase, cephalosporinase, ESBL, carbapenamase, AmpC β-lactamase, metallo-β-lactamase. Chú ý là các loại có thể có sự giao thoa với nhau chứ không hoàn toàn tách rời nhau. Thông thường, các Cephalosporin từ thế hệ II trở đi khá bền với các penicillinase, nhưng không bền với các β-lactamase khác. Các β-lactamase có khả năng phá hủy cấu trúc vòng β-lactam của Cephalosporin thế hệ III trở lên được gọi là ESBL. ESBL được tiết ra bởi ngày càng nhiều chủng vi khuẩn, khi đã tiết ra được ESBL thì khả năng thất bại trong điều trị nhiễm khuẩn sẽ tăng lên nhiều lần. Nhiều chủng vi khuẩn có khả năng tiết ra ESBL thường là các vi khuẩn gram âm, ví dụ như Acinetobacter baumannii, Pseudomonas aeruginosa, E.coli, Proteus, Klebsiella pneumoniae…
– Hình thành các bơm tống kháng sinh (Efflux Pump): Đây là cơ chế đề kháng đặc trưng xuất hiện ở các vi khuẩn gram âm. Khi phân tử kháng sinh đã qua được các kênh porin và đi vào bên trong tế bào vi khuẩn, bơm tống kháng sinh sẽ có nhiệm vụ đẩy phân tử kháng sinh ra khỏi tế bào, không cho nó kịp tiếp cập và ức chế các PBP của vi khuẩn.
Bơm tống kháng sinh không xuất hiện ở các vi khuẩn gram dương bởi lớp peptidoglycan của chúng nằm ngay bên ngoài tế bào, các PBP cũng hoạt động ngay gần bề mặt tế bào, việc sử dụng bơm tống kháng sinh sẽ không có ý nghĩa.
– Giảm tính thấm của kháng sinh với màng tế bào vi khuẩn: Cơ chế này cũng chỉ xuất hiện ở các vi khuẩn gram âm, đặc biệt nổi tiếng ở trực khuẩn mủ xanh. Vi khuẩn được chọn lọc các đột biến làm giảm số lượng các kênh porin cũng như giảm ái lực của các kênh này với phân tử kháng sinh, từ đó làm hạn chế số phân tử kháng sinh có thể đi vào bên trong tế bào. Cá biệt, nhiều trường hợp quan sát thấy vi khuẩn xóa bỏ hoàn toàn các kênh porin này.
Cơ chế đề kháng kiểu này không xuất hiện ở các vi khuẩn gram dương vì chúng không có kênh porin như vi khuẩn gram âm.
Chất ức chế β-lactamase
Các chất ức chế β-lactamase được phát triển nhằm mục đích ức chế tác dụng của enzyme β-lactamase của vi khuẩn. Chúng sẽ đóng vai trò như là chất “hi sinh” bảo vệ cho vòng β-lactam của kháng sinh.
Các chất ức chế β-lactamase cổ điển bao gồm Acid clavulanic, Sulbactam và Tazobactam. Các chất ức chế β-lactamase mới hơn, mới được phát triển trong thời gian gần đây có thể kể đến Avibactam, Vaborbactam và Relebactam. Mỗi chất ức chế β-lactamase khác nhau sẽ có hiệu lực chống β-lactamase khác nhau. Nhiều loại β-lactamase mạnh đến mức không có chất ức chế β-lactamase nào có thể ức chế được nó.
Tuy rằng số lượng các chất ức chế β-lactamase không phải là ít, nhưng số lượng các Cephalosporin được phối hợp với chất ức chế β-lactamase trên lâm sàng lại không nhiều. Mặc dù sự phối hợp này trên lý thuyết có thể giúp kháng sinh lấy lại được phổ tác dụng mà nó vốn dĩ có trên một số vi khuẩn sinh β-lactamase, nhưng vấn đề lâm sàng lại không đơn giản như vậy. Hiệu quả điều trị thực tế mới là vấn đề mà các nhà lâm sàng cũng như các bác sĩ quan tâm, và cho dù sự phối hợp về mặt lý thuyết có hay, có tuyệt vời đến đâu, mà những thử nghiệm lâm sàng lại không chứng minh được tác dụng của nó, thì mọi thứ đều vô ích. Chính vì vậy, cho đến hiện nay, mới chỉ có 2 kháng sinh nhóm Cephalosporin được phối hợp với chất ức chế β-lactamase trên lâm sàng, đó là Ceftazidime được phối hợp với Avibactam (biệt dược Avycaz) và Ceftolozane phối hợp với Tazobactam (biệt dược Zerbaxa).
Dược động học
Dược động học của các kháng sinh nhóm Cephalosporin nhìn chung có nhiều điểm tương đồng với các kháng sinh nhóm Penicillin cũng như các kháng sinh β-lactam khác.
Hấp thu
Với các thuốc dùng theo đường tiêm truyền tĩnh mạch, không có quá trình hấp thu. Với các thuốc dùng theo đường tiêm bắp, tốc độ hấp thu cũng khá nhanh và sinh khả dụng gần bằng 100%. Với các thuốc dùng đường uống, nhìn chung các kháng sinh nhóm Cephalosporin có sinh khả dụng tương đối tốt và ổn định, bền trong acid dịch vị, thông thường sự hấp thu không bị ảnh hưởng bởi thức ăn.
Phân bố
Các kháng sinh nhóm Cephalosporin có tính thân nước nên có khả năng phân bố tốt vào các mô và dịch cơ thể. Các kháng sinh nhóm Cephalosporin từ thế hệ 2 trở đi có thể đi qua hàng rào máu não khá tốt, nhiều kháng sinh có thể được dùng trong điều trị viêm màng não. Khả năng đi qua nhau thai cũng như vào sữa mẹ khá hạn chế, đây là nhóm kháng sinh được đánh giá là an toàn cho phụ nữ mang thai và đang cho con bú.
Chuyển hóa
Hầu như các kháng sinh nhóm này cũng không bị chuyển hóa. Tuy vậy, vẫn sẽ có những trường hợp đặc biệt được chuyển hóa, thường là qua gan.
Thải trừ
Đường thải trừ chủ yếu của các kháng sinh này là dưới dạng không đổi qua nước tiểu, trừ một số ít thải trừ chủ yếu qua mật (như Cefoperazone). Thời gian bán thải của các thuốc rất thay đổi nhưng nhì chung thường cao hơn so với các Penicillin, tần suất dùng thuốc thường là 1-3 lần/ngày, đôi khi là 4 lần/ngày. Các kháng sinh thải trừ chủ yếu qua thận cần hiệu chỉnh liều trong suy giảm chức năng thận. Một số lại cần chỉnh liều theo chức năng gan.
Tác dụng và chỉ định của kháng sinh nhóm Cephalosporin

Các kháng sinh nhóm Cephalosporin, như đã nói ở trên, có tác dụng tiêu diệt các chủng vi khuẩn nhạy cảm và tác dụng diệt khuẩn của nó phụ thuộc thời gian.
Chỉ định các mỗi kháng sinh cũng khác nhau, thường được phân theo các thế hệ:
– Cephalosporin thế hệ I: Các kháng sinh nhóm này thường được sử dụng cho các nhiễm trùng da và mô mềm (ưu tiên hơn so với các Penicillin chống tụ cầu) do tụ cầu nhạy cảm Methicillin (MSSA: Methicillin-Susceptible Staphylococcus aureus hoặc MSSE: Methicillin-Susceptible Staphylococcus epidermidis) và liên cầu (Streptococcus). Cefazolin là kháng sinh được sử dụng nhiều nhất trong dự phòng nhiễm trùng vết mổ. Các chỉ định khác của phân nhóm kháng sinh này bao gồm: Dự phòng viêm nội tâm mạc, nhiễm trùng tiết niệu dưới không biến chứng, nhiễm trùng túi mật, nhiễm trùng ổ bụng không biến chứng, nhiễm trùng khớp giả…
– Cephalosporin thế hệ II: Các Cephamycin, đặc biệt là Cefoxitin, được sử dụng nhiều trong dự phòng nhiễm trùng vết mổ có nguy cơ nhiễm vi khuẩn kỵ khí, nhiễm trùng các khu vực có liên quan đến vi khuẩn kị khí như bệnh viêm vùng chậu, nhiễm trùng ổ bụng không biến chứng, viêm cổ tử cung, viêm âm đạo… Các Cephalosporin thế hệ 2 thực sự đã có thể được sử dụng cho nhiễm trùng hô hấp trên và dưới, nhiễm trùng tiết niệu dưới không biến chứng, bệnh Lyme…
– Cephalosporin thế hệ III: Các Cephalosporin thế hệ 3 được chỉ định cho viêm màng não nhiễm khuẩn (Ceftriaxone và Cefotaxime), nhiễm trùng hô hấp trên và dưới, viêm phúc mạc, nhiễm trùng sau làm thủ thuật đường tiết niệu, bệnh lậu (Ceftriaxone + Azithromycin), viêm niêm mạc trực tràng, nhiễm trùng tiết niệu trên và dưới không biến chứng, viêm phổi bệnh viện và viêm phổi thở máy do trực khuẩn mủ xanh (Ceftazidime), tả, dịch hạch, lỵ, thương hàn, nhiễm trùng da và mô mềm, viêm nội tâm mạc bán cấp nhiễm khuẩn…
– Cephalosporin thế hệ IV: Các thuốc nhóm này được chỉ định cho các bệnh lý nhiễm khuẩn nặng, bao gồm sốt giảm bạch cầu hạt, viêm phổi bệnh viện, viêm phổi thở máy, viêm phổi cộng đồng phân lập được trực khuẩn mủ xanh, viêm màng não nhiễm khuẩn, nhiễm trùng ổ bụng biến chứng, nhiễm trùng đường tiết niệu có biến chứng, nhiễm trùng đường mật, nhiễm trùng huyết…
– Cephalosporin thế hệ V: Các kháng sinh thuộc phân nhóm này được chỉ định cho nhiễm khuẩn tiết niệu có biến chứng, nhiễm khuẩn ổ bụng có biến chứng, viêm phổi cộng đồng, viêm phổi bệnh viện hoặc viêm phổi thở máy…
Zerbaxa (Ceftolozane/Tazobactam) đã được Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Hoa Kỳ phê duyệt cho chỉ định nhiễm trùng tiết niệu có biến chứng, nhiễm trùng ổ bụng có biến chứng và mới gần đây là viêm phổi bệnh viện và viêm phổi thở máy. Hai chỉ định đầu là nhiễm trùng tiết niệu có biến chứng và nhiễm trùng ổ bụng có biến chứng đã được phê duyệt tại Việt Nam, còn chỉ định thứ ba (viêm phổi bệnh viện và viêm phổi thở máy) đang chờ để được phê duyệt (tính đến tháng 8/2020).
– Siderophore Cephalosporin: Cefiderocol được chỉ định cho nhiễm trùng tiết niệu có biến chứng.
Hướng dẫn sử dụng kháng sinh nhóm Cephalosporin

Cách dùng
Cách dùng nhìn chung không có gì đặc biệt. Đa phần các kháng sinh nhóm Cephalosporin nếu có thể dùng đường uống thì có thể uống trước hoặc sau ăn đều được.
Liều dùng
Cephalosporin thế hệ I:
Cephalexin: Liều dùng thường được áp dụng trên lâm sàng là 250 mg mỗi 6 giờ hoặc 500 mg mỗi 12 giờ. Tổng liều 1 ngày thường dao động từ 1-4 g.
Cefazolin: Mức liều có thể dao động từ 250-500 mg mỗi 8 hoặc 12 giờ với nhiễm khuẩn mức độ nhẹ và trung bình, lên đến 1-2 g mỗi 8 giờ với nhiễm khuẩn mức độ nặng hơn. Nếu sử dụng với mục đích dự phòng nhiễm trùng vết mổ trước phẫu thuật, cần kết thúc truyền kháng sinh trong vòng 60 phút trước khi rạch da. Nếu cuộc mổ kéo dài, cần lặp lại liều mỗi 2 giờ.
Cephalosporin thế hệ II:
+ Cefuroxime: Liều dùng thường được áp dụng trên lâm sàng là 250-500 mg mỗi 12 giờ, nếu nhiễm trùng mức độ nặng hơn có thể tăng lên đến 500-750 mg mỗi 8 giờ. Nếu nhiễm trùng nặng hơn nữa, liều dùng có thể tăng lên đến 1.5 g mỗi 8 giờ, và nếu nhiễm trùng đe dọa tính mạng thì mức liều có thể lên đến 1.5 g mỗi 6h, và các trường hợp như thế này kháng sinh thường được dùng theo đường tiêm (tiêm bắp hoặc tiêm dưới da).
Cephalosporin thế hệ III:
+ Cefixime: Liều dùng thường được áp dụng trên lâm sàng là 400 mg/ngày dùng 1 lần/ngày hoặc 2 lần/ngày với mỗi lần cách nhau 12 giờ.
+ Cefpodoxime: Liều dùng thường được áp dụng trên lâm sàng là 100, 200 hoặc 400 mg mỗi 12 giờ, áp dụng tùy vào vị trí nhiễm trùng.
+ Cefdinir: Liều dùng thường được áp dụng trên lâm sàng là 300 mg mỗi 12 giờ hoặc 600 mg mỗi 24 giờ.
+ Ceftriaxone: Với một số nhiễm trùng nặng, tổng liều hàng ngày của thuốc có thể là 1,2 hoặc 4 g/ngày, dùng 1 lần/ngày hoặc chia ra mỗi 12 giờ. Cá biệt với một số trường hợp như lậu không biến chứng hoặc bệnh viêm vùng chậu, liều dùng chỉ là 250 mg 1 lần duy nhất. Thuốc có thể dùng đường tiêm tĩnh mạch hoặc tiêm bắp.
+ Cefotaxime: Với lậu, liều thường dùng là 0.5-1 g 1 lần duy nhất. Với các tình trạng nhiễm khuẩn khác, mức liều phụ thuộc vào tình trạng nghiêm trọng của bệnh: 1 g mỗi 12 giờ nếu nhiễm trùng nhẹ, 1-2 g mỗi 8 giờ với nhiễm trùng từ trung bình đến nặng, nếu nghiêm trọng hơn thì 2 g mỗi 6-8 giờ và nếu nhiễm trùng đe dọa tính mạng thì dùng 2 g mỗi 4 giờ, liều tối đa 12 g/ngày.
+ Ceftazidime: Liều dùng thường được áp dụng trên lâm sàng là 0.5-1 g mỗi 8 hoặc 12 giờ với nhiễm trùng nhẹ (cá biệt: 250 mg mỗi 12 giờ cho nhiễm trùng tiết niệu không biến chứng), với nhiễm trùng nặng hơn là 2 g mỗi 8 giờ, liều tối đa 6 g/ngày.
Cephalosporin thế hệ IV:
+ Cefepime: Liều dùng thường được áp dụng trên lâm sàng là 1-2 g mỗi 8 hoặc 12 giờ.
– Cephalosporin thế hệ V:
+ Ceftaroline: Liều dùng thường được áp dụng trên lâm sàng là 600 mg mỗi 12 giờ.
+ Ceftolozane: Liều dùng thường được áp dụng trên lâm sàng là 1-2 g mỗi 8 giờ (kết hợp với Tazobactam 0.5-1g tương ứng).
Siderophore Cephalosporin:
+ Cefiderocol: 2 g mỗi 8 giờ.
Tác dụng không mong muốn của kháng sinh nhóm Cephalosporin
Phản ứng dị ứng và quá mẫn: Đây là tác dụng không mong muốn của các kháng sinh nhóm β-lactam nói chung, bao gồm cả các kháng sinh nhóm Cephalosporin. Nguyên nhân là bởi các phân tử kháng sinh khi vào máu, chúng có thể chuyển từ bán kháng nguyên sang kháng nguyên hoàn chỉnh thông qua liên kết với protein huyết tương, từ đó kích hoạt các đáp ứng của hệ miễn dịch. Các phản ứng dị ứng nếu nhẹ thì chỉ là nổi mẩn đỏ, ngứa, khó chịu ở da, phát ban…, nhưng nếu nặng có thể gây ra phản ứng phản vệ, hội chứng Stevens-Johnson, hoại tử thượng bì nhiễm độc (hội chứng TEN hay hội chứng Lyell)…, các tình trạng này cần được cấp cứu nội khoa và chăm sóc tích cực, nếu không sẽ có thể gây tử vong.

Về khả năng dị ứng chéo giữa các kháng sinh nhóm Penicillin và Cephalosporin, thì khả năng này là rất thấp, nhưng vẫn có thể xảy ra. Khả năng dị ứng chéo tăng cao khi nhóm thế ở vị trí R2 trong cấu trúc hóa học của Cephalosporin giống hoặc gần giống với nhóm thế R trong cấu trúc hóa học của Penicillin. Nhóm thế R1 trong cấu trúc hóa học của Cephalosporin ít liên quan đến nguy cơ dị ứng chéo hơn. Để biết vị trí cụ thể của các nhóm thế R1 và R2, xem lại hình ở phần 1.2.
Viêm đại tràng giả mạc do bùng phát C.difficile: C.difficile là một vi khuẩn kỵ khí gram dương, kí sinh bình thường ở đại tràng của người khỏe mạnh. Khi sử dụng kháng sinh, đặc biệt là các kháng sinh phổ rộng nhưng không có phổ tác dụng trên C.difficile, các vi khuẩn trong lòng đại tràng bị tiêu diệt nhiều, nhưng C.difficile không bị tiêu diệt, điều này dẫn đến nguy cơ bùng phát sự phát triển của loại vi khuẩn này. Tình trạng này nếu không được điều trị kịp thời có thể dẫn đến tử vong.
Rối loạn tiêu hóa: Buồn nôn và nôn, đau bụng, tiêu chảy (có thể là dấu hiệu của viêm đại tràng giả mạc do C.difficile).
Tưa lưỡi: Đây là biểu hiện cho sự phát triển quá mức của nấm trong miệng. Bội nhiễm nấm còn có thể xảy ra ở các vị trí khác ngoài lưỡi như âm đạo…
Một số thuốc gây giảm nhẹ chức năng thận.
Các kháng sinh Cephalosporin có chứa nhóm methyl thiotetrazole trong cấu trúc có độc tính với hệ tạo máu, nó gây ra giảm prothrombin máu. Ngoài ra, các Cephalosporin này còn ức chế enzyme aldehyde dehydrogenase, điều này gây ra ức chế sự giáng hóa acetaldehyde (một sản phẩm chuyển hóa có độc tính từ ethanol) thành acid acetic (không có độc tính). Acetaldehyde bị tích tụ gây ra các phản ứng giống như phản ứng cai rượu, gọi là phản ứng Disulfiram.
Một số thuốc có thể gây đau tại chỗ tiêm, hoặc đau đầu, chóng mặt.
Chống chỉ định
Quá mẫn cảm với bất cứ thành phần nào của thuốc.
Bệnh nhân có tiền sử dị ứng ở mức độ nghiệm trọng khi sử dụng kháng sinh nhóm Cephalosporin.
Tương tác thuốc với kháng sinh nhóm Cephalosporin
Tác dụng hiệp đồng tăng mức khi phối hợp với các kháng sinh nhóm Aminoside: Đây là một phối hợp kinh điển và hiệu quả trên lâm sàng của nó đã được chứng minh từ lâu. Phối hợp này thường xuyên được sử dụng trên lâm sàng trong các trường hợp điều trị kháng sinh theo kinh nghiệm cũng như điều trị kháng sinh trong trường hợp đã có kết quả kháng sinh đồ. Ưu điểm của sự kết hợp này là tác dụng diệt khuẩn của 2 loại kháng sinh kết hợp lớn hơn tổng tác dụng diệt khuẩn của từng kháng sinh thành phần (có nghĩa là “1 + 1 > 2”). Phối hợp này thậm chí có thể đem lại hiệu quả trong một số trường hợp vi khuẩn cần điều trị đã kháng cả 2 loại kháng sinh được phối hợp (theo kết quả kháng sinh đồ).

Cơ chế đứng đằng sau giải thích cho sự hiệp đồng tăng mức này có thể được giải thích như sau: Cephalosporin là kháng sinh ức chế tổng hợp vách tế bào, còn Aminoside là kháng sinh ức chế trực tiếp tiểu đơn vị ribosome 30S không hồi phục. Khi được sử dụng phối hợp với nhau, các Cephalosporin ức chế tổng hợp vách tế bào, tạo điều kiện cho các Aminoside đi vào trong tế bào dễ dàng hơn và tiêu diệt vi khuẩn từ bên trong. Phối hợp này phổ biến trên lâm sàng đến nỗi chế độ liều của sự phối hợp này được nghiên cứu rất kỹ. Dựa vào PK/PD, ta có thể thiết kế được chế độ liều phù hợp cho bệnh nhân. Các kháng sinh nhóm Cephalosporin là kháng sinh diệt khuẩn phụ thuộc thời gian nên thường được sử dụng nhiều lần trong ngày (thường là 2-4 lần, một số chỉ sử dụng 1 lần/ngày do thời gian bán thải [t1/2] dài). Các Aminoside là kháng sinh diệt khuẩn phụ thuộc nồng độ nên chúng thường sẽ được sử dụng theo chế độ liều 1 lần/ngày vào một thời điểm nhất định. Tất nhiên cũng sẽ có những trường hợp ngoại lệ (ví dụ: viêm nội tâm mạc bán cấp) nhưng nhìn chung là như vậy. Các kháng sinh Aminoside phát huy tác dụng càng tốt khi ổ nhiễm khuẩn càng có nhiều vi khuẩn, trong khi các Cephalosporin lại phát huy tác dụng tốt nhất khi ổ nhiễm khuẩn có ít vi khuẩn. Trong phối hợp này, các kháng sinh nhóm Aminoside chịu trách nhiệm làm giảm nhanh số lượng vi khuẩn, tạo điều kiện cho các kháng sinh nhóm Cephalosporin “dọn dẹp” nốt số vi khuẩn còn lại tại vị trí nhiễm khuẩn. Các kháng sinh nhóm Aminoside còn có tác dụng hậu kháng sinh (PAE: Post-Antibiotic Effect) kéo dài, có nghĩa là sau thời gian sau khi nồng độ kháng sinh trong máu xuống dưới ngưỡng MIC mà vi khuẩn vẫn bị ức chế kéo dài. Việc sử dụng kháng sinh nhóm Aminoside 1 lần/ngày cũng làm giảm đáng kể độc tính trên thận.
Một số phối hợp khác như các kháng sinh nhóm Cephalosporin kết hợp với các kháng sinh nhóm Macrolide, Quinolone, 5-nitroimidazole như Metronidazole, Lipopeptide như Colistin hoặc Glycopeptide như Vancomycin thường mang tính chất mở rộng phổ là chính, còn tác dụng hiệp đồng của chúng trên lâm sàng không thực sự rõ ràng.
Tăng tác dụng chống đông máu của các thuốc chống đông kháng vitamin K (Warfarin): Nguyên nhân chính của sự tương tác thuốc này là do các kháng sinh nhóm Cephalosporin, đặc biệt là các kháng sinh phổ rộng, có khả năng tiêu diệt luôn cả nhiều vi khuẩn có ích trong hệ khuẩn chí đường ruột, do tác dụng diệt khuẩn không chọn lọc của nó. Các vi khuẩn cộng sinh trong đường ruột của người cung cấp một lượng đáng kể vitamin K cho cơ thể. Vitamin K lại là một yếu tố quan trọng tham gia vào quá trình đông máu nội sinh. Vậy nên, khi nhiều vi khuẩn trong đường ruột bị tiêu diệt nhiều, lượng vitamin K được hấp thu vào cơ thể giảm và có thể gây rối loạn đông máu. Khi dùng cùng với các thuốc chống đông kháng vitamin K như Warfarin, tác dụng chống đông máu được tăng cường.
Lưu ý và thận trọng khi sử dụng thuốc
Với các bệnh nhân có tiền sử dị ứng với Penicillin mức độ nghiêm trọng (như phản ứng phản vệ), vẫn có thể sử dụng các kháng sinh nhóm Cephalosporin nhưng cần tránh các kháng sinh có nhóm thế giống nhau bởi nguy cơ dị ứng chéo trong các trường hợp này là rất cao. Và kể cả khi kháng sinh nhóm Cephalosporin được sử dụng có nhóm thế khác với Penicillin mà bệnh nhân bị dị ứng, vẫn cần theo dõi thận trọng các dấu hiệu của phản ứng dị ứng trên bệnh nhân này.

Nếu trong quá trình điều trị, bệnh nhân bị tiêu chảy nặng, liên tục và các thuốc thông thường không cầm được, cần nghĩ ngay đến viêm đại tràng giả mạc do C.difficile. Đây là một tình trạng nghiêm trọng và có thể dẫn đến tử vong. Điều trị tình trạng này bằng các kháng sinh: Metronidazole, Vancomycin đường uống hoặc Fidaxomicin. Ở Việt Nam, Metronidazole được ưu tiên đầu tiên. Lý do là bởi Fidaxomicin không có ở nhiều bệnh viện, còn sử dụng Vancomycin gây ra những lo ngại về tình trạng phát triển vi khuẩn đề kháng Vancomycin. Ngoài ra, Metronidazole còn là kháng sinh rẻ tiền và phổ biến nhất. Chú ý bổ sung đủ nước và điện giải cho bệnh nhân.
Với một số kháng sinh có độc tính trên thận, cần theo dõi chức năng thận định kỳ thường xuyên và có những điều chỉnh phù hợp.
Sử dụng thuốc trên đối tượng đặc biệt
Phụ nữ có thai và đang cho con bú: Nhìn chung các kháng sinh nhóm Cephalosporin an toàn với phụ nữ có thai và đang cho con bú. Phân loại an toàn trong thai kỳ: B.
Người già và trẻ em: Có thể cần hiệu chỉnh liều ở người già và trẻ em do ở người già, chức năng gan thận thường suy giảm do lão hóa và các bệnh lý mắc kèm, còn ở trẻ em, chức năng gan thận thường chưa hoàn thiện.
Một số nghiên cứu và thử nghiệm lâm sàng
– Thử nghiệm REPROVE: So sánh Ceftazidime/Avibactam với Meropenem trong điều trị viêm phổi bệnh viện và viêm phổi thở máy. Kết thúc thử nghiệm, kết luận được đưa ra là Ceftazidime/Avibactam cung cấp một lựa chọn điều trị mới cho viêm phổi bệnh viện hoặc viêm phổi thở máy do vi khuẩn gram âm gây ra, kể cả các chủng đã không còn nhạy cảm với Ceftazidime.
– Thử nghiệm đối chứng ngẫu nhiên xem xét hiệu quả của Piperacillin/Tazobactam, Cefepime và Ertapenem trong điều trị nhiễm trùng tiết niệu do E.coli sinh ESBL. Kết luận từ thử nghiệm: Piperacillin/Tazobactam cho hiệu quả điều trị tốt nếu vi khuẩn còn nhạy cảm in vitro, và Cefepime thì không nên được sử dụng cho nhiễm trùng tiết niệu gây ra bởi chủng E.coli này.
Tài liệu tham khảo
Janet Y. Wu, Pavithra Srinivas và Jason M. Pogue, Cefiderocol: A Novel Agent for the Management of Multidrug-Resistant Gram-Negative Organisms, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7054475/
Saira B. Chaudhry, Michael P. Veve và Jamie L. Wagner, Cephalosporins: A Focus on Side Chains and β-Lactam Cross-Reactivity, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6789778/
Antoni Torres, Doug Rank, David Melnick, Ludmyla Rekeda, Xiang Chen, Todd Riccobene, Ian A Critchley, Hassan D Lakkis, Dianna Taylor và Angela K Talley, Randomized Trial of Ceftazidime-Avibactam vs Meropenem for Treatment of Hospital-Acquired and Ventilator-Associated Bacterial Pneumonia (REPROVE): Analyses per US FDA–Specified End Points, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6483139/
Yu Bin Seo, Jacob Lee, Young Keun Kim, Seung Soon Lee, Jeong-A Lee, Hyo Youl Kim, Young Uh, Han-Sung Kim, Wonkeun Song, Randomized controlled trial of piperacillin-tazobactam, cefepime and ertapenem for the treatment of urinary tract infection caused by extended-spectrum beta-lactamase-producing Escherichia coli, https://pubmed.ncbi.nlm.nih.gov/28592240/