Biên dịch Bác sĩ Phạm Hoàng Thiên
Shock chủ đề thường gặp nhất của cấp cứu và ICU, việc chẩn đoán và xử trí nó còn rất nhiều điều chưa rõ ràng, thường gây khó khăn trong việc đưa ra quyết định lâm sàng.
Hôm nay, mình viết một bài về một loại sốc thường gặp: SỐC NHIỄM TRÙNG.
Và bài này cũng chỉ nhắm đến một số mục tiêu nhất định, chủ yếu là về thuốc vận mạch và những điều cần biết khi dùng nó mà thôi, những vấn đề khác nằm ở một bài khác nhé!
Chúng ta sẽ trình bày dưới dạng 1 case lâm sàng về sốc nhiễm trùng và cách tiếp cận điều trị. Ở mỗi giai đoạn, chúng ta sẽ dừng lại để phân tích, đưa ra lý do và chứng cứ đằng sau mỗi quyết định lâm sàng. Mình khuyến khích các bạn hãy tự trả lời mỗi câu hỏi trước khi đọc đáp án.
Nào, đến với bệnh nhân thôi: Một bệnh nhân nam 67 tuổi, vào viện vì choáng váng, gần ngất. Người nhà nói ông than là cảm thấy lâng lâng 2 ngày nay, không thấy bất thường gì khác.
- Tiền sử: tăng huyết áp kiểm soát không tốt, tăng lipid máu và phì đại tiền liệt tuyến.
- Tình trạng lúc nhập cấp cứu: Mạch 122; nhiệt 38,8; HA 75/45; nhịp thở 32; Sp02 93%. Lơ mơ, tiếp xúc chậm, định hướng chậm với thời gian, địa điểm và người.
- Niêm mạc khô, không thấy thương tổn. Tim đều, không âm thổi. Phổi trong, không ran. Bụng mềm, ấn đau vùng hạ vị, phản ứng dội âm tính. Thăm trực tràng phân vàng. Cứng cổ âm tính. Đáp ứng đúng với kích thích đau, không thấy yếu liệt. Đường huyết bình thường, ECG nhịp nhanh xoang. Siêu âm nhanh tại cấp cứu cho thấy IVC xẹp và thay đổi > 50% theo nhịp thở, không dịch ở rãnh Morrison, đường kính ĐMC bụng 2,7 cm, thất T giảm co bóp mức độ trung bình, thất P khó thấy. Tờ kết quả siêu âm tim gần đây bình thường.
Chẩn đoán
Chẩn đoán phân biệt của bệnh nhân này là toàn bộ nguyên nhân gây sốc, hiện tại không thấy phù hợp với sốc phản vệ, sốc thần kinh, hay sốc mất máu. Chức năng thất T của BN hiện giảm, trong khi lần gần đây bình thường, có thể là sốc tim, sốc nhiễm khuẩn và sốc phản vệ.
Bonus: biến chứng bệnh lý cơ tim xảy ra trong hơn 50% tất cả case sốc nhiễm khuẩn.
Chẩn đoán ban đầu: sốc nhiễm trùng nghi từ đường tiết niệu.
Xử trí
Xử trí: cấy máu, và kháng sinh phổ rộng. Ringer lactat 30 ml/kg. Công thức máu cho thấy tăng bạch cầu 22k, tiểu cầu 110.
Các xét nghiệm đáng chú ý khác: creatinine 2,2 mmol/L với BUN 43 mg/dL, bicarbonate 15 mEq / L và khoảng trống anion là 20.
X quang phổi không có gì bất thường.
Xét nghiệm nước tiểu: dương tính với ketone, leukocyte esterase và nitrit. Tế bào bạch cầu tăng rất cao.
Siêu âm không thấy thận ứ nước hay dịch quanh thận.
Chẩn đoán hàng đầu: sốc nhiễm trùng nghi từ đường tiết niệu. Sau khi bù dịch 30 ml/kg, huyết áp là 75/45 và refill vẫn chậm >3s.
Thảo luận việc sử dụng thuốc vận mạch và mục tiêu MAP
Bạn đưa ra quyết định bắt đầu thuốc vận mạch để duy trì tưới máu nội tạng. Hãy thảo luận các câu hỏi sau:
3. Khi nào thì bạn sẽ bắt đầu thuốc vận mạch ở một bệnh nhân bị tụt huyết áp kéo dài?
4. Mục tiêu MAP của bạn nói chung và cụ thể ở bệnh nhân này là bao nhiêu?
5. Bạn lựa chọn thuốc vận mạch nào vào lúc này? và tại sao?
6. Bạn sẽ trì hoãn việc bắt đầu sử dụng vận mạch để đặt catheter tĩnh mạch trung tâm?
7. Có phải bệnh nhân này cần đặt đường động mạch để theo dõi huyết áp?
Lưu ý: việc bù dịch ở BN này là cần thiết, và đúng theo khuyến cáo 30ml/kg, tuy nhiên, các bằng chứng cho đến hiện tại, thì liều 30ml/kg có chuẩn hay không thì còn phải xem lại, tốt nhất là hãy dựa vào huyết động, đánh giá đáp ứng bù dịch trên từng bệnh nhân cụ thể, nhưng đó lại là một chủ đề khác.
Và việc chẩn đoán ở BN này là cũng đã được xác định, nên không nhắc đến nhiều, việc chủ yếu là thảo luận các câu hỏi từ 3 đến 7. Nếu chủ đề này được quan tâm, mình sẽ up câu trả lời và tiếp tục với các câu hỏi khác.
THẢO LUẬN:
The Surviving Sepsis Campaign (SSC) đã ban hành các khuyến cáo liên quan đến thuốc vận mạch trong sốc nhiễm trùng [1]. Việc lựa chọn norepinephrine hay dopamine là thuốc vận mạch đầu tiên đã từng là một vấn đề được tranh luận không ngừng. Tuy nhiên, norepinephrine đã trở thành tiêu chuẩn thực hành – là thuốc vận mạch hàng đầu để điều trị sốc nhiễm trùng. Khi so sánh với dopamine, norepinephrine đã chứng minh là làm tăng khả năng đạt được MAP mục tiêu [4]. Sự vượt trội của norepinephrine chủ yếu là do tác dụng phụ tương đối ít của nó mà không làm giảm hiệu quả khi so sánh với các thuốc vận mạch khác. Norepinephrine thường không làm nhịp tim nhanh đáng kể vì tác dụng co tĩnh mạch của nó và kích thích liên quan đến các baroreceptor ở tâm nhĩ phải trung hòa sự kích thích chronotropic beta-1. Khi so sánh với dopamine, norepinephrine có tỷ lệ gây ra các biến cố rối loạn nhịp tim thấp hơn [5, 6]. Trong một phân tích tổng hợp, dopamine có thể làm tăng nguy cơ tử vong tương đối khi so sánh với norepinephrine [7]. Thông tin này đã đẩy norepinephrine lên hàng đầu với tư cách là thuốc vận mạch được ưa thích. Dopamine đã được chuyển thành một loại thuốc vận mạch với một vai trò thích hợp sẽ được thảo luận sau.
Mặc dù không có thử nghiệm đối đầu nào cho thấy norepinephrine vượt trội hơn epinephrine trong điều trị sốc nhiễm trùng, nhưng nói chung, norepinephrine được coi là có tác dụng phụ ít hơn. Epinephrine có liên quan đến nhịp tim nhanh, tăng nhu cầu insulin thoáng qua và làm tăng nồng độ axit lactic như được trình bày trong Hình 11.1 [8]. Epinephrine, cùng với vasopressin liều thấp, được coi là thuốc lựa chọn tiếp theo ở bệnh nhân sốc nhiễm trùng không đáp ứng với norepinephrine.
Các nghiên cứu về sốc nhiễm trùng đã cho thấy nồng độ thấp của vasopressin trong tuần hoàn, một phát hiện bất ngờ là mức độ tăng lên được cho rằng sẽ dự đoán được hạ huyết áp, một kích thích để giải phóng vasopressin [9, 24].
Lập luận này về sự thiếu hụt tương đối vasopressin đã được một số nơi đưa ra để hỗ trợ việc sử dụng vasopressin liều thấp (lên đến 0,03 chỉ 0,04 đơn vị mỗi phút) như một liệu pháp thay thế sinh lý trong sốc nhiễm trùng. Việc sử dụng liều cao hơn vasopressin làm tăng nguy cơ tim mạch, thiếu máu ngón tay – ngón chân và thiếu máu nội tạng [10]. Thử nghiệm VANISH đã sử dụng vasopressin liều trung bình (lên đến 0,06 U / phút) để điều trị sốc nhiễm trùng. Điểm cuối của nghiên cứu này là tỷ lệ suy thận trong sốc nhiễm trùng. Mặc dù không có sự khác biệt trong suy thận đã được chứng minh khi sử dụng liều vasopressin cao hơn, nhưng nhóm sử dụng vasopressin có nguy cơ tác dụng phụ tăng 2,5% (xem thảo luận chi tiết hơn về vasopressin để theo dõi) [11].
Thời điểm bắt đầu thuốc vận mạch không được đề cập trong hướng dẫn của SSC. Các trung tâm sepsis CMS (CMS: The Centers for Medicare and Medicaid Services) đã đưa việc phải sử dụng thuốc vận mạch nhằm đạt được MAP từ 65 mmHg trở lên trong vòng 6 giờ đầu tiên sau khi đã bolus 30 ml/kg thành một tiêu chuẩn chẩn đoán sốc nhiễm trùng. Các lý thuyết cổ điển về việc “làm đầy bể chứa” (bù đủ dịch) bằng cách hồi sức dịch trước khi bắt đầu dùng thuốc vận mạch thường là phương pháp tiếp cận lâm sàng. Nhưng điều này đặt ra một câu hỏi: một bệnh nhân nên duy trì hạ huyết áp trong bao lâu trước khi bắt đầu sử dụng thuốc vận mạch? Các nghiên cứu gần đây đã xem xét việc bắt đầu dùng thuốc vận mạch sớm so với trì hoãn mà không có câu trả lời rõ ràng cho câu hỏi này. Trong một đánh giá hồi cứu, Bai và cộng sự cho thấy sự gia tăng tỷ lệ sống sót khi dùng norepinephrine sớm. Nghiên cứu này ghi nhận tỷ lệ tử vong tăng 5,3% với mỗi giờ chậm trễ trong việc bắt đầu sử dụng thuốc vận mạch [12]. Beck và cộng sự chỉ có thể chỉ ra mối tương quan yếu giữa việc trì hoãn sử dụng thuốc vận mạch và tỉ lệ tử vong tại bệnh viện. Các tác giả của nghiên cứu lưu ý thấy hiệu ứng này được điều khiển bởi những bệnh nhân có độ trễ lớn hơn 1h [13]. Cuối cùng, một bài đánh giá hồi cứu thứ ba của Waechter và cộng sự đã tìm thấy tỷ lệ tử vong thấp nhất khi thuốc vận mạch được khởi động trong vòng 1-6 giờ sau khi khởi phát sốc và đã bù hơn 1 lít dịch đường IV [14]. Nếu không có các thử nghiệm ngẫu nhiên rõ ràng, không thể đưa ra một khuyến cáo dứt khoát về thời gian sử dụng thuốc vận mạch. Tuy nhiên, mức độ nghiêm trọng và thời gian hạ huyết áp được cho là sẽ gây ra tổn thương cơ quan đích. Do đó, cách tiếp cận hợp lý là bắt đầu dùng thuốc vận mạch trong vòng 1-6 giờ đầu tiên của hồi sức để đạt đƣợc MAP thích hợp và tƣới máu đầy đủ. Ở những bệnh nhân bị tụt huyết áp nặng hoặc có các triệu chứng nặng của hạ huyết áp, quyết định bắt đầu vận mạch sớm hơn và song song với hồi sức dịch ban đầu có vẻ phù hợp.
Quyết định tiếp theo sau khi bắt đầu sử dụng thuốc vận mạch là mục tiêu mà MAP nên chọn. Hạ huyết áp kéo dài (MAP < 60-65 mmHg) có liên quan đến kết cục tồi tệ hơn bao gồm cả tăng nguy cơ tử vong [15]. Năm 2014, Asfar và cộng sự đã thực hiện một thử nghiệm ngẫu nhiên có kiểm soát và đối chứng so sánh nhóm có mục tiêu MAP thấp (65- 70 mmHg) với nhóm có mục tiêu MAP cao (80-85 mmHg). Không có sự khác biệt về tỷ lệ tử vong trong 30 hoặc 90 ngày. Nhóm mục tiêu thấp biểu hiện ít rối loạn nhịp tim hơn (chủ yếu là rung nhĩ). Ở những bệnh nhân có tiền sử tăng huyết áp mãn tính, mục tiêu MAP cao hơn đã làm giảm tỷ lệ tăng creatinine và tỷ lệ điều trị chạy thận từ ngày 1 đến ngày 7. Nhìn chung, không có sự khác biệt trong các tác dụng phụ nghiêm trọng giữa hai nhóm [16]. Tài liệu này có thể được phân tích theo những cách khác nhau. Một mục tiêu MAP cao hơn có thể được coi là an toàn và hữu ích ở những bệnh nhân bị tăng huyết áp mãn tính với hy vọng giảm suy thận (theo phân tích dưới phân nhóm). Một quan điểm khác là sẽ coi mục tiêu MAP cao hơn bằng với mục tiêu MAP thấp hơn với nguy cơ rối loạn nhịp tim cao hơn (theo phân tích chính). Các hướng dẫn gần đây nhất của SSC đề xuất mục tiêu MAP là 65 mmHg [1]. Mục tiêu MAP là 65 mmHg nên được xem xét ở phần lớn bệnh nhân nhưng cần tùy chỉnh cho từng cá nhân dựa trên tình trạng tưới máu cơ quan đích và các tác dụng phụ được quan sát.
Sau khi chọn thuốc vận mạch ban đầu và MAP mục tiêu, chúng ta chuyển sang quyết định làm thế nào để cung cấp thuốc vận mạch. Đặt catheter tĩnh mạch trung tâm (CVC) là cần thiết để bắt đầu điều trị? Đường tĩnh mạch ngoại vi (PIV) an toàn đến mức nào? Lý thuyết cổ điển đã cho rằng đặt một CVC là cần thiết để cung cấp thuốc vận mạch. Thực hành chung này đã được thúc đẩy bởi nhiều báo cáo trường hợp về tình trạng thoát mạch của thuốc vận mạch và gây tổn thương mô. Tuy nhiên, các nghiên cứu gần đây đã đưa giáo lý kinh điển này thành một câu hỏi. Năm 2013 Ricard và cộng sự đã làm nghiên cứu với bệnh nhân được chọn ngẫu nhiên để đặt CVC hoặc PIV khi bắt đầu hồi sức dịch và sử dụng vận mạch đồng thời. Các tác giả của nghiên cứu này đã kết luận CVC vượt trội hơn so với PIV, cụ thể là ít biến chứng nghiêm trọng hơn, bao gồm tỷ lệ thoát mạch là 14% ở những bệnh nhân được dùng thuốc vận mạch qua PIV. Tuy nhiên, phần lớn các biến chứng được liệt kê là ban đỏ và khó khăn khi lập hoặc duy trì vị trí của PIV. Vị trí tĩnh mạch ngoại biên và kết quả lâm sàng liên quan đến tổn thương mô không được báo cáo. Đáng chú ý, khoảng một nửa của nhóm lấy đường PIV trong nghiên cứu này đã được chuyển sang CVC [17]. Năm 2015, Cardenas-Garcia và cộng sự đã công bố dữ liệu của một nghiên cứu với khoảng thời gian 20 tháng, trong đó thuốc vận mạch được truyền qua PIV. Trong nghiên này, các tác giả đã ghi nhận chỉ có 2% bệnh nhân sử dụng PIV bị thoát mạch và không có tổn thương mô sau khi điều trị theo phác đồ bao gồm kiểm tra vị trí đặt PIV sau mỗi 2 giờ và điều trị bằng phentolamine và nitroglycerine nếu phát hiện tình trạng thoát mạch. Có 13% bệnh nhân cần chuyển sang đặt CVC. Nghiên cứu này không có nhóm chỉ sử dụng CVC để đối chứng ngẫu nhiên [18].
Tình trạng thoát mạch của thuốc vận mạch là một nguy cơ thực sự. Nhưng mức độ nghiêm trọng và tần suất của rủi ro đó không hoàn toàn rõ ràng. Một bài đánh giá có hệ thống của Loubani và cộng sự năm 2015 đã cho thấy 83,5% của tất cả các trường hợp thoát mạch đã xảy ra ở những vị trí PIV ở xa so với hố khuỷu và hố khoeo. Thời gian trung bình của việc sử dụng thuốc vận mạch đƣờng ngoại biên trƣớc khi tổn thƣơng mô tại chỗ là 24 giờ [19]. Do đó, có một cách tiếp cận hợp lý để bắt đầu thuốc vận mạch thông qua đường PIV mà không trì hoãn điều trị. Dựa vào các tài liệu trên, một đƣờng truyền PIV đƣợc đặt tốt ở vị trí từ hố khuỷu trở lên đƣợc ƣu tiên. Đường truyền này phải được kiểm tra tối thiểu sau mỗi 2 giờ và đƣợc sử dụng dƣới 24 giờ. Điều này có thể hạn chế nhu cầu đặt CVC nếu thuốc vận mạch có thể được cai nhanh chóng bằng cách hồi sức thêm. Chúng tôi không khuyến cáo bạn áp dụng rộng rãi việc sử dụng PIV để truyền thuốc vận mạch.
Ở một bệnh nhân cần dùng thuốc vận mạch vì sốc, nên đặt một đường động mạch khi có thể. Hiện tại không có các thử nghiệm ngẫu nhiên lớn so sánh việc theo dõi huyết áp không xâm lấn và xâm lấn. Tuy nhiên, các nghiên cứu nhỏ hơn đã chỉ ra sự không đáng tin cậy của theo dõi huyết áp không xâm lấn trong sốc [20, 21]. Việc đặt và duy trì các đường động mạch đã được chứng minh là có tỷ lệ biến chứng dưới 1% [22]. Nguy cơ biến chứng rất thấp và sự không đáng tin cậy của theo dõi huyết áp không xâm lấn dẫn đến khuyến cáo sử dụng đường động mạch. Việc đánh giá thấp MAP sẽ dẫn đến việc sử dụng quá mức cần thiết hoặc quá liều các thuốc vận mạch.
Bây giờ chúng ta trở lại với bệnh nhân của mình nào: Kháng sinh và hồi sức dịch đường tĩnh mạch đã được hoàn thành. Norepinephrine đã được bắt đầu, nhưng tình trạng bệnh nhân vẫn tiếp tục xấu đi. Ông ta vẫn còn bị sốc với liều norepinephrine 50 ug/phút và MAP là 55 mmHg.
Thảo luận về liều tối đa thuốc vận mạch và lựa chọn thứ hai
8. Vậy, liều tối đa của thuốc vận mạch hàng đầu là bao nhiêu trước khi thêm một thuốc thứ hai để tham gia hoặc thuốc có khả năng thay thế norepinephrine dựa trên đáp ứng của bệnh nhân?
9. Loại thuốc vận mạch thứ hai chúng ta lựa chọn ở bệnh nhân này là gì? Và sẽ dùng liều như thế nào?
THẢO LUẬN
Như đã thảo luận trước đó, norepinephrine được khuyến cáo là thuốc vận mạch hàng đầu trong sốc nhiễm trùng chủ yếu dựa trên các tác dụng phụ tương đối lành tính của nó. Không có một liều lượng tối đa rõ ràng được khuyến cáo trước khi bắt đầu dùng thuốc vận mạch thứ hai. Ngưỡng để thêm thuốc vận mạch thứ hai thay đổi tùy theo quốc gia (liều cao hơn được sử dụng trong một số quốc gia châu Âu khi so với Mỹ) và theo sở thích cá nhân. Các báo cáo trường hợp lưu ý nguy cơ thiếu máu cục bộ tứ chi khi liều vượt quá 1,2 ug/kg/phút [23]. Tuy nhiên, logic đằng sau sự mối liên quan giữa ngưỡng liều đối với thiếu máu cục bộ tứ chi dường như còn thiếu sót khi mà norepinephrine liều cao hơn đang được sử dụng để điều trị sốc “giãn mạch” kháng trị (refractory “vasodilatory” shock). Lý do thích hợp cho việc sử dụng liều cao hơn là tình trạng giãn mạch dai dẳng, và trong trường hợp có sự giãn mạch mạnh hơn dẫn đến phải dùng liều cao hơn, thì mối liên quan với thiếu máu mô do liều dùng của thuốc vận mạch trở nên kém đi. Trên thực tế, chúng tôi thích sử dụng thuật ngữ “đáp ứng kém” với norepinephrine khi dùng liều cao và ngày càng cao hơn mà không đạt được MAP mục tiêu. Chúng tôi tin rằng thuật ngữ này được ưa thích hơn so thuật ngữ thường được sử dụng là “maxed out” (liều dùng tối đa mà khi vượt liều này cũng không cải thiện bất cứ điều gì) của norepinephrine. Một thử nghiệm ngẫu nhiên có đối chứng đã sử dụng liều norepinephrine 0,5 ug/kg/phút như một điểm cắt (cut-off) cho sốc giãn mạch “kháng catecholamine” [10]. Dường như không có giới hạn rõ ràng đối với norepinephrine. Các tác giả của guidelines SSC đã chọn chuẩn độ đến 35-90 ug/phút làm điểm cắt [1]. Giới hạn của liều dùng phải tính đến khả năng dung nạp của từng cá nhân và đáp ứng với việc tăng thêm liều norepinephrine. Liều lượng tối đa nên thấp hơn liều làm xuất hiện của các tác dụng phụ như rối loạn nhịp tim.
Khi thêm một tác nhân thứ hai, thường là quyết định giữa vasopressin liều thấp và epinephrine. Liên quan đến sốc nhiễm trùng, cả hai đều nằm trong các khuyến cáo của SSC nhằm duy trì một MAP phù hợp.
Mặc dù vasopressin liều thấp không được khuyến cáo là thuốc khởi đầu trong điều trị sốc nhiễm trùng, nhưng nó có thể được thêm vào cùng norepinephrine khi dùng norepinephrine không đạt được MAP mục tiêu hoặc được dùng như là một tác nhân thêm vào môt khi đạt được MAP mục tiêu với norepinephrine đơn độc (vì tính logic: sự thay thế sinh lý).
Trong khi norepinephrine là thuốc vận mạch hàng đầu được khuyến cáo, cả epinephrine và vasopressin đều có những đặc tính độc đáo làm cho chúng trở nên hữu ích như các thuốc hàng hai (second-line).
Vasopressin là một hormone vận mạch nội sinh gây ra co mạch bằng cách tác động lên thụ thể V1 của cơ trơn. Nó là một thuốc vận mạch thuần túy, không ảnh hưởng lên tim ngoại trừ kích thích gián tiếp các baroreceptor tâm nhĩ phải. Ở trạng thái sinh lý bình thường, nồng độ vasopressin thấp. Thử nghiệm VASST năm 2008 đã so sánh norepinephrine với norepinephrine kèm vasopressin (0,01-0,03 U/phút). Nghiên cứu này cho thấy không có sự khác biệt về tỷ lệ tử vong. Nó đã chứng minh một hiệu ứng “catecholamine-sparing” của vasopressin trong đó liều norepinephrine cần thiết sử dụng thấp hơn. Một phân nhóm trước đó trong nghiên cứu này với sốc ít nghiêm trọng hơn có tỷ lệ tử vong thấp hơn (nguy cơ tử vong tương đối trong 28 ngày là 0,74 (KTC 95%, 0,55-1,01; p = 0,05). Nhóm này được xác định bằng nhu cầu norepinephrine < 15 ug/phút một cách ngẫu nhiên [25]. Một số nghiên cứu trước đó đã cho thấy giảm nhu cầu norepinephrine và cải thiện cung lượng tim với sự bắt đầu của vasopressin trong sốc kháng catecholamine [26, 27]. Những nghiên cứu này bao gồm liều cao hơn khuyến cáo bởi SSC. Ở liều cao hơn xuất hiện nguy cơ cao hơn về các biến cố tim mạch, thiếu máu chi và nội tạng [10]. Do đó, liều < 0,03 U/phút (một số cho rằng 0,04 U / phút) được khuyến cáo, và liều cao hơn chỉ được sử dụng trong liệu pháp cứu cánh (các tác nhân thay thế khác đã không đạt được mục tiêu MAP).
Epinephrine là thuốc vận mạch catecholamine hoạt động trên cả thụ thể alpha và beta. Điều này dẫn đến một MAP cao hơn do tăng trương lực mạch máu và tăng cung lượng tim. Như đã lưu ý trước đó, các tác dụng phụ chính của epinephrine bao gồm sự gia tăng lactate huyết thanh và nhịp tim nhanh làm cho nó trở thành thuốc hàng thứ 2 sau norepinephrine [8]. Tuy nhiên, những tác dụng này chưa được chứng minh là làm thay đổi kết cục lâm sàng của bệnh nhân. Năm 2008, Myburgh và cộng sự đã thực hiện một thử nghiệm tiến cứu ngẫu nhiên, mù đôi có đối chứng so sánh việc sử dụng epinephrine với norepinephrine ở bệnh nhân sốc [8]. Không có sự khác biệt về tỷ lệ tử vong giữa hai nhóm ở 28 và 90 ngày. Cụ thể trong một phân nhóm bệnh nhân được chẩn đoán nhiễm trùng huyết, không có sự khác biệt về thời gian để đạt được mục tiêu MAP (> 70 mmHg) hoặc tử vong. Mặc dù không có sự khác biệt về kết cục chính hay phụ, nhưng nghiên cứu này đã được sử dụng để ủng hộ norepinephrine là tác nhân đầu tiên do hiệu quả tương đương và giảm tác dụng phụ (Fig. 11.1).
Lợi ích về mặt lý thuyết của epinephrine so với các thuốc vận mạch khác trong sốc dựa trên hoạt động của thụ thể beta. Mặc dù norepinephrine dự kiến sẽ làm tăng cung lượng tim trong sốc nhiễm trùng, epinephrine là một thuốc tăng co bóp mạnh hơn và sẽ tạo ra một sự gia tăng lớn hơn về cung lượng tim ở bệnh nhân mắc bệnh cơ tim do sepsis gây ra. Năm 2007, Annane và cộng sự đã công bố một nghiên cứu tiến cứu, đa trung tâm, ngẫu nhiên, mù đôi ở 330 bệnh nhân bị sốc nhiễm trùng. Nghiên cứu này đã so sánh epinephrine với norepinephrine cộng với dobutamine. Không có sự khác biệt đáng kể về tỷ lệ tử vong sau 28 ngày giữa hai nhóm. Nhóm epinephrine đã cho thấy pH động mạch thấp hơn vào ngày 1-4 và tăng lactate động mạch vào ngày 1. Những phát hiện này đã được đưa ra giả thuyết là do sự kích thích beta-2 của bơm NA + K ATPase ở cơ xương hơn là rối loạn oxy mô. [28]. Các giá trị xét nghiệm thoáng qua này không có tác động rõ ràng đến kết cục lâm sàng. Trong vòng 4 ngày, không có sự khác biệt về tỷ lệ tử vong, rối loạn chức năng cơ quan đích hay sự ổn định của huyết động. SSC khuyến cáo nên cân nhắc sử dụng dobutamine ở những bệnh nhân được cho là đã bù đầy đủ thể tích nội mạch, đã đạt được MAP mục tiêu, nhưng vẫn tiếp tục giảm tưới máu mô với các dấu hiệu lâm sàng của cung lượng tim thấp (xem thảo luận để theo dõi ).
và khả năng dung nạp
Quyết định bổ sung thêm thuốc vận mạch vào norepinephrine phải dựa trên hiệu quả và khả năng dung nạp ở từng cá thể bệnh. Tại thời điểm này, không có thử nghiệm ngẫu nhiên nào so sánh vasopressin với epinephrine ở những bệnh nhân hiện đang sử dụng norepinephrine. Do đó, cả hai lựa chọn vẫn là một lựa chọn khả thi. Vasopressin dường như làm giảm nhu cầu norepinephrine và có thể đặc biệt hữu ích ở những bệnh nhân không dung nạp được liều cao catecholamine. Epinephrine có thể hữu ích nhất ở những bệnh nhân cần hỗ trợ co bóp (inotropic) và nhịp tim (chronotropic). Điều này đặc biệt hữu ích ở những bệnh nhân có biểu hiện giảm cung lượng tim và sẽ không chịu được tác dụng giãn mạch của một thuốc tăng co bóp như dobutamine.
Chúng ta trở lại với case lâm sàng: Vasopressin được bắt đầu với liều 0,03 U/phút. Bệnh nhân có sự cải thiện ban đầu về huyết áp nhưng một lần nữa tiếp tục mất bù với MAP liên tục dưới 65 mmHg. Epinephrine được thêm vào như là một thuốc vận mạch thứ ba. Huyết áp bệnh nhân cải thiện. Y tá gọi bạn để đánh giá bệnh nhân. Monitor hiển thị một phức bộ hẹp, nhịp không đều một cách không đều: với nhịp thất là 132. Khi nhịp bất thường này xuất hiện, thì MAP giảm từ 70 đến 50 mmHg.
Thảo luận việc thay đổi chế độ thuốc vận mạch trong Shock nhiễm trùng
10. Bạn sẽ thay đổi chế độ thuốc vận mạch của mình?
THẢO LUẬN:
- Phenylephrine, mặc dù không được khuyến cáo cho điều trị theo kinh nghiệm, đã được sử dụng trong bối cảnh biến đổi sinh lý nghiêm trọng – loạn nhịp nhanh do thuốc vận mạch. Phenylephrine là một chất chủ vận alpha-1 chọn lọc không có tác động lên thụ thể beta. Nó là một thuốc co mạch thuần túy – không có kích thích tim. Do đó, nó không gây ra nhịp tim nhanh. Là một thuốc co mạch thuần túy, nó sẽ được kì vọng sẽ làm giảm thể tích nhát bóp (stroke volume) và cung lượng tim, với ít tác dụng phụ hơn. Hiện dữ liệu so sánh phenylephrine với các thuốc vận mạch khác còn hạn chế.
- Morelli và cộng sự. đã thực hiện một thử nghiệm tiến cứu, ngẫu nhiên có đối chứng so sánh phenylephrine với norepinephrine như là một thuốc vận mạch hàng đầu trong sốc nhiễm trùng. Trong nghiên cứu này, phenylephrine có tác dụng tương tự trên các thông số tim phổi. Tuy nhiên, phenylephrine ít hiệu quả hơn trong điều trị hạ huyết áp vì cần liều cao hơn để duy trì mục tiêu MAP [29]. Nghiên cứu này có hạn chế ở chỗ nó chỉ tiến hành trên 32 bệnh nhân và các phép đo thông số tim phổi chỉ được đo ở 12 giờ thông qua đặt catheter vào buồng tim phải. SSC đã khuyến cáo hạn chế sử dụng phenylephrine trong sốc nhiễm trùng (không như điều trị theo kinh nghiệm nhưng cân nhắc trong sốc nhiễm trùng cung lượng tim cao hoặc khi có rối loạn nhịp nhanh do norepinephrine hay epinephrine) [1]. Dựa trên dược lý thì phenylephrine có thể có vai trò nào đó trong nhóm bệnh nhân này, nhưng không có dữ liệu xác nhận.
Thảo luân về vai trò của Dopamine trong điều trị Shock nhiễm trùng
11. Không phải vì nó liên quan đến bệnh nhân của chúng tôi mà là đối với nhóm bệnh nhân sốc nhiễm trùng, dopamine đóng vai trò gì? Và một inotrope thuần túy như dobutamine thì như thế nào?
THẢO LUẬN
Dopamine có vai trò hạn chế trong điều trị sốc nhiễm trùng. Nó có tác dụng đối với cả thụ thể alpha và beta tương tự norepinephrine và epinephrine. Nó có hoạt động trên cả thụ thể dopamin – có thể làm thay đổi tưới máu thận và lách. Như đã thảo luận trước đó, nó đã được thay thế bởi norepinephrine như là thuốc vận mạch hàng đầu cho phần lớn nhóm bệnh nhân này. Sau đó, nó đã trở thành một thuốc vận mạch có khả năng thích hợp cho bệnh nhân bị sốc nhiễm trùng có nhịp chậm xoang và nguy cơ rối loạn nhịp tim thấp. Không có thử nghiệm ngẫu nhiên có đối chứng sử dụng dopamine trong nhóm bệnh nhân này. Ý kiến này dựa trên dược lý đã biết hơn là kết quả nghiên cứu. Dopamine liều thấp không có lợi cho bệnh nhân có nguy cơ bị suy thận. Trong một nghiên cứu đa trung tâm, ngẫu nhiên, mù đôi, có đối chứng giả dược, Bellomo và cộng sự cho thấy không có sự khác biệt đáng kể về tỉ lệ sống còn, creatinine đỉnh hoặc nhu cầu điều trị thay thế thận ở bệnh nhân dùng dopamine liều thấp so với giả dược [30].
Do đó, việc sử dụng dopamine nên được dành riêng cho một nhóm bệnh nhân cụ thể hoặc một phần của liệu pháp cứu cánh.
Ở những bệnh nhân tiếp tục bị giảm tưới máu mặc dù đã cải thiện tình trạng tiền tải và MAP, thuốc hỗ trợ co bóp cơ tim (inotrope) có thể được xem xét. Khuyến nghị này dựa trên dữ liệu hạn chế. Như đã thảo luận trước đó, các thử nghiệm ngẫu nhiên có đối chứng so sánh dobutamine + norepinephrine với epinephrine đơn thuần không cho thấy sự khác biệt về tỷ lệ tử vong [28]. Các khuyến cáo trước đây về việc sử dụng dobutamine trong hồi sức sớm của sốc nhiễm trùng được dựa trên thử nghiệm liệu pháp điều trị theo mục tiêu sớm của Rivers và cộng sự [31]. Dobutamine đã được thêm vào khi có ScV02 < 70% dai dẳng mặc dù đã điều trị bằng thuốc vận mạch, truyền dịch IV và có sự hiện diện của hematocrit thích hợp. Các khuyến cáo hiện tại ủng hộ việc xem xét thêm dobutamine sau khi hồi sức như đã thảo luận ở trên.
Bệnh nhân được tiếp tục dùng norepinephrine và vasopressin liều thấp. Với sự xuất hiện của rối loạn nhịp nhanh, epinephrine đã được ngưng và bắt đầu dùng phenylephrine cùng với việc loại bỏ đợt rối loạn nhịp nhanh của anh ta. Lặp lại xét nghiệm cho thấy lactate là 2,4 mmol/L và cải thiện creatinine với lượng nước tiểu thích hợp 0,75 cc/kg/giờ (mục tiêu 0,5-1,0 cc/kg). Cùng với việc tiếp tục liệu pháp kháng sinh, hỗ trợ thuốc vận mạch được điều chỉnh giảm dần trong vài ngày với sự cải thiện huyết động. Mặc dù không dựa trên bằng chứng, nhưng chúng tôi rút phenylephrine trước, sau đó là vasopressin, và mới đến norepinephrine. Một số sẽ đảo ngược trình tự cho hai thuốc vận mạch sau.
Những mục tiêu trong tương lai
Tương lai của điều trị sốc bao gồm phát hiện sớm các rối loạn chức năng của cơ quan đích, theo dõi hiệu suất tim mạch và hỗ trợ về thuốc và máy móc. Khi các thiết bị không xâm lấn mới hơn được phát triển, độ tin cậy của những công cụ này sẽ cần được đánh giá. Trong khi điều trị bằng thuốc thường bao gồm norepinephrine là thuốc vận mạch được lựa chọn, thì tài liệu so sánh điều trị phối hợp thuốc vận mạch còn hạn chế. Phác đồ điều trị cá nhân hóa và những lựa chọn trong việc dùng thuốc và dịch truyền có thể sẽ được điều chỉnh cho mỗi bệnh nhân dựa trên sinh lý và đáp ứng với điều trị.
Angiotensin II (ATII) gần đây đã được thêm vào danh sách thuốc vận mạch được FDA phê chuẩn trong điều trị sốc phân bố. ATII là một hormone tự nhiên, tương tác với hệ renin-angiotensin-aldosterone system (RAAS) gây ra cả co thắt tĩnh mạch và động mạch. Nó là một thuốc vận mạch thuần túy. Gần đây, thử nghiệm ngẫu nhiên ATHOS-3 trên 321 bệnh nhân bị sốc phân bố được điều trị ATII so với giả dược [32]. Trước khi được chọn, bệnh nhân đã cần phải dùng 0,2 μg/kg/phút norepinephrine hoặc một thuốc vận mạch khác với liều tương đương. Kết cục chính là đáp ứng của MAP – được xác định là tăng MAP 10 mmHg hoặc ít nhất 75 mmHg sau 3 giờ. 69,9% nhóm ATII so với 23,4% của nhóm chứng đạt được kết cục chính này (Fig. 11.2). Mặc dù các kết cục phụ đã cho thấy giảm tỷ lệ tử vong do mọi nguyên nhân vào ngày 7 và 28, nhưng những kết quả này không đạt được ý nghĩa thống kê [31]. Mặc dù các tác giả đã báo cáo sự cải thiện trong đánh giá suy cơ quan tim mạch (SOFA) ở thời điểm 48 giờ mà không có sự khác biệt trong tổng SOFA, nhưng điều này hơi gây hiểu lầm vì sự cải thiện này đạt được chỉ bằng cách cho thuốc vận mạch ở nhóm điều trị tích cực và một giả dược cho nhóm chứng.
Các chỉ trích của nghiên cứu này bao gồm mục tiêu MAP cao hơn so với khuyến cáo cho nhóm bệnh này, tình trạng dịch không rõ ràng của nhóm nghiên cứu, thông tin hạn chế về các marker của tưới máu cơ quan đích như lactate máu và lượng nước tiểu bài tiết, và bỏ qua đánh giá cung lượng tim. Sau cùng, điều quan trọng là phải tránh sử dụng thuốc vận mạch thuần túy này ở những bệnh nhân có cung lượng tim thấp vì thử nghiệm ngẫu nhiên có đối chứng nghiên cứu một thuốc vận mạch thuần túy trong sốc nhiễm trùng này có liên quan đến kết cục tồi tệ hơn ở phân nhóm bệnh nhân có cung lượng tim thấp (được tính trực tiếp trong nghiên cứu này) [33].
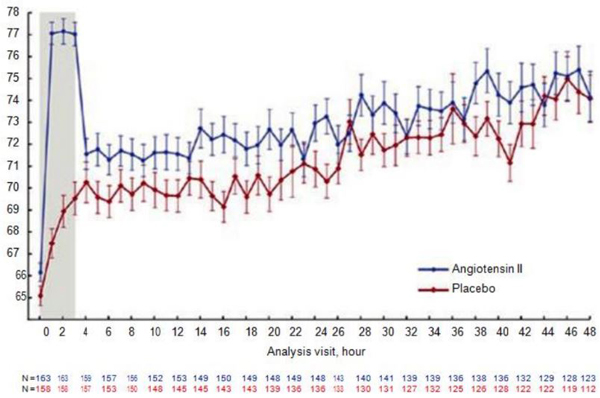
dùng vận mạch.
(Reprinted/adapted with permission from New England Journal of Medicine Khanna et al. [32]).
Mục tiêu tổng hợp chính của thử nghiệm ATHOS-3 tập trung vào việc đạt được mục tiêu MAP hơn là tỷ lệ tử vong của bệnh nhân. Số đối tượng nghiên cứu nhỏ cũng giới hạn dữ liệu an toàn được cung cấp. Đặc biệt, nguy cơ huyết khối được báo cáo bởi FDA không được biểu lộ rõ ràng trong thử nghiệm này nhưng được ghi rõ ràng trên nhãn của FDA – khuyến cáo sử dụng thuốc dự phòng cho cục máu đông. Sẽ cần nhiều nghiên cứu hơn để đánh giá lợi ích tử vong hoặc giới hạn của tác dụng phụ khi sử dụng thuốc vận mạch mới này. Có một thuốc vận mạch bổ sung hoạt động theo một cơ chế khác sẽ hy vọng mang lại lợi thế trong những nhóm bệnh nhân được chọn lọc.
Một phác đồ (dạng flow diagram) gần đây cũng đã được xuất bản khi các tác giả khuyến cáo về phân cấp và liều lượng thuốc vận mạch sử dụng khi mức độ nghiêm trọng của sốc nhiễm trùng gia tăng (Fig. 11.3) [2].
![Figure 11.3 Một ví dụ về phác đồ sử dụng thuốc vận mạch. (Reprinted/ adapted with permission from Springer; Dellinger et al. [2])](https://www.healcentral.org/wp-content/uploads/2020/06/thuoc_van_mach_6.1.jpg)
Những điểm chính
1. Norepinephrine là thuốc vận mạch hàng đầu trong sốc nhiễm trùng.
2. Vasopressin liều thấp và/hoặc epinephrine có thể được thêm vào như thuốc hàng thứ 2.
3. Dopamine và phenylephrine là thuốc vận mạch thích hợp trong những tình huống chọn lọc.
4. MAP mục tiêu ≥65 được khuyến cáo những phải được điều chỉnh tùy theo từng cá thể bệnh.
5. Vận mạch nên được bắt đầu sớm sau khi hồi sức dịch khi MAP vẫn còn thấp.
6. Một đường truyền tĩnh mạch ngoại biên nằm trên hố khuỷu có lẽ là an toàn cho hồi sức ban đầu.
7. Nên lựa chọn thuốc vận mạch dựa trên đáp ứng của từng bệnh nhân đối với điều trị và các tác dụng phụ.
Tài liệu tham khảo
\1.\ Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis cam-paign: international guidelines for the management of sepsis and septic shock: 2016. Crit Care Med. 2017;45:486–552.
\2.\ Dellinger RP, Schorr CA, Levy MM. Users’ guide to the 2016 sur-viving sepsis guidelines. Crit Care Med. 2017;45(3):381–5. https:// doi.org/10.1097/CCM.0000000000002257.
\ 3.\ Vieillard-Baron A, Caille V, Charron C, et al. Actual incidence of global left ventricular hypokinesia in adult septic shock. Crit Care Med. 2008;36:1701–6.
\ 4.\ Martin C, Papazian L, Perrin G, et al. Norepinephrine or dopa-mine for the treatment of hyperdynamic septic shock? Chest. 1993;103(6):1826–31.
\ 5.\ De Backer D, Biston P, Devriendt J, et al. Comparison of dopa-mine and norepinephrine in the treatment of shock. N Engl J Med. 2010;362(9):779–89.
\ 6.\ Avni T, Lador A, Lev S, et al. Vasopressors for the treatment of septic shock: systematic review and meta-analysis. PLoS One. 2015;10:e0129305.
\ 7.\ De Backer D, Aldecoa C, Njimi H, et al. Dopamine versus nor-epinephrine in the treatment of septic shock: a meta-analysis. Crit Care Med. 2012;40:725–30.
\ 8.\ Myburgh JA, Higgins A, Jovanovska A, et al. CAT study inves-tigators: a comparison of epinephrine and norepinephrine in critically ill patients. Intensive Care Med. 2008;34:2226–34.
\ 9.\ Landry DW, Levin HR, Gallant EM, et al. Vasopressin deficiency contributes to the vasodilation of septic shock. Circulation. 1997;95:1122–5.
\10.\ Dünser MW, Mayr AJ, Tür A, et al. Ischemic skin lesions as a com-plication of continuous vasopressin infusion in catecholamine– resistant vasodilatory shock: incidence and risk factors. Crit Care Med. 2003;31:1394–8.
\11.\ Gordon AC, Mason AJ, Thirunavukkarasu N, et al. VANISH investigators: effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: the VANISH ran-domized clinical trial. JAMA. 2016;316:509–18.
\12.\Bai X, Yu W, Ji W, Lin Z, Tan S, Duan K, et al. Early versus delayed administration of norepinephrine in patients with septic shock. Crit Care. 2014;18:532. https://doi.org/10.1186/ s13054-014-0532-y.
\13.\Beck V, Chateau D, et al. Timing of vasopressor initiation and mortality in septic shock: a cohort study. Crit Care. 2014; 18:R97.
14\.\ Waechter J, Kumar A. Lapinsky et al. Interaction between fluids and vasoactive agents on mortality in septic shock: a multicenter, observational study. Crit Care Med. 2014;42(10):2158–68.
\15.\ Dünser MW, Takala J, Ulmer H, Mayr VD, Luckner G, Jochberger S, et al. Arterial blood pressure during early sepsis and outcome. Intensive Care Med. 2009;35:1225– 33.
\16.\ Asfar P, Meziani F, Hamel JF, et al. High versus low blood– pressure target in patients with septic shock. N Engl J Med. 2014;370:1583–93.
\17.\ Ricard JD, Salomon L, Boyer A, et al. Central or peripheral catheters for initial venous access of ICU patients: a randomized controlled trial. Crit Care Med. 2013;41(9):2108–15.
\18.\ Cardenas-Garcia J, Schaub KF, et al. Safety of peripheral intra-venous administration of vasoactive medication. J Hosp Med. 2015;10:581–5.
\19.\ Loubani OM, Green RS. A systematic review of extravasation and local tissue injury from administration of vasopressors through peripheral intravenous catheters and central venous catheters. J Crit Care. 2015;30(3):653.e9–17.
20\.\ Lakhal K, et al. Noninvasive monitoring of blood pressure in the critically ill: reliability according to the cuff site (arm, thigh, or ankle). Crit Care Med. 2012;40:1207–13.
\21.\ Ribezzo S, Spina E, Di BS, Sanson G. Noninvasive techniques for blood pressure measurement are not a reliable alternative to direct measurement: a randomized crossover trial in ICU. Sci World J. 2014;2014:353628.
\22.\ Scheer B, Perel A, Pfeiffer UJ. Clinical review: complications and risk factors of peripheral arterial catheters used for haemo-dynamic monitoring in anaesthesia and intensive care medicine. Crit Care. 2002;6:199–204.
\23.\ Daroca-Perez R, Carrascosa M. Digital necrosis: a poten-tial risk of high-dose norepinephrine. Ther Adv Drug Saf. 2017;8(8):259–61.
\24.\ Sharshar T, Blanchard A, Paillard M, et al. Circulating vasopres-sin levels in septic shock. Crit Care Med. 2003;31:1752–8.
\25.\ Russell JA, Walley KR, Singer J, et al. Vasopressin versus norepi-nephrine infusion in patients with septic shock. N Engl J Med. 2008;358:877–87.
\26.\ Dünser MW, Mayr AJ, Ulmer H, et al. Arginine vasopressin in advanced vasodilatory shock: a prospective, randomized, con-trolled study. Circulation. 2003;107:2313–9.
\27.\ Patel BM, Chittock DR, Russell JA, et al. Beneficial effects of short-term vasopressin infusion during severe septic shock. Anesthesiology. 2002;96:576–82.
\28.\ Annane D, Vignon P, Renault A, et al. CATS Study Group: norepinephrine plus dobutamine versus epinephrine alone for management of septic shock A randomised trial. Lancet. 2007;370:676–84.
\29.\ Morelli A, Ertman C, Rehberg S, et al. Phenylephrine versus norepinephrine for initial hemodynamic support of patients with septic shock: a randomized controlled trial. Crit Care. 2008;12:R43.
\30.\ Bellomo R, Chapman M, Finfer S, et al. Low-dose dopamine in patients with early renal dysfunction: a placebo-controlled ran-domised trial. Lancet. 2000;356:2139–43.
\31.\ Rivers E, Nguyen B, Havstad S, et al. Early goal-directed therapy in the treatment of severe sepsis and septic shock. The New England Journal of Medicine 2001;345(19):1368–77.
\32.\Khanna A, Shane EW, Wang XS. Angiotensin II for treatment of vasodilatory shock. N Engl J Med. 2017;377:419–30. https://doi. org/10.1056/NEJMoa1704154.
\33.\López A, Lorente JA, Steingrub J, et al. Multiple-center, ran-domized, placebo- controlled, double-blind study of the nitric oxide synthase inhibitor 546C88: effect on survival in patients with septic shock. Crit Care Med. 2004;32:21–30.





